文档内容
专练 22 化学工艺流程
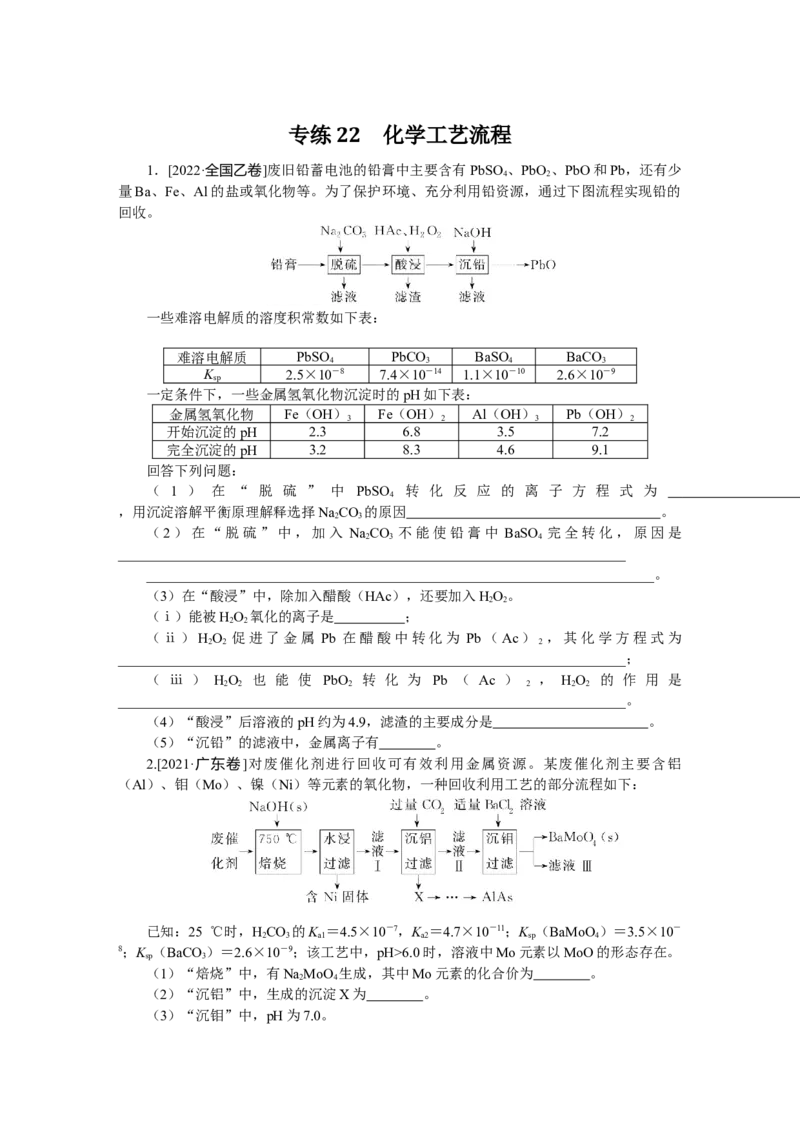
1.[2022·全国乙卷]废旧铅蓄电池的铅膏中主要含有PbSO 、PbO 、PbO和Pb,还有少
4 2
量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的
回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 PbSO PbCO BaSO BaCO
4 3 4 3
K 2.5×10-8 7.4×10-14 1.1×10-10 2.6×10-9
sp
一定条件下,一些金属氢氧化物沉淀时的pH如下表:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH) Pb(OH)
3 2 3 2
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
( 1 ) 在 “ 脱 硫 ” 中 PbSO 转 化 反 应 的 离 子 方 程 式 为
4
,用沉淀溶解平衡原理解释选择NaCO 的原因 。
2 3
(2)在“脱硫”中,加入 NaCO 不能使铅膏中 BaSO 完全转化,原因是
2 3 4
________________________________________________________________________
________________________________________________________________________。
(3)在“酸浸”中,除加入醋酸(HAc),还要加入HO。
2 2
(ⅰ)能被HO 氧化的离子是 ;
2 2
(ⅱ)HO 促进了金属 Pb 在醋酸中转化为 Pb(Ac) ,其化学方程式为
2 2 2
________________________________________________________________________;
( ⅲ ) HO 也 能 使 PbO 转 化 为 Pb ( Ac ) , HO 的 作 用 是
2 2 2 2 2 2
________________________________________________________________________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是 。
(5)“沉铅”的滤液中,金属离子有 。
2.[2021·广东卷]对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝
(Al)、钼(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25 ℃时,HCO 的K =4.5×10-7,K =4.7×10-11;K (BaMoO)=3.5×10-
2 3 a1 a2 sp 4
8;K (BaCO )=2.6×10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO的形态存在。
sp 3
(1)“焙烧”中,有NaMoO 生成,其中Mo元素的化合价为 。
2 4
(2)“沉铝”中,生成的沉淀X为 。
(3)“沉钼”中,pH为7.0。①生成BaMoO 的离子方程式为 。
4
②若条件控制不当,BaCO 也会沉淀。为避免BaMoO 中混入BaCO 沉淀,溶液中c∶c
3 4 3
= (列出算式)时,应停止加入BaCl 溶液。
2
(4)①滤液Ⅲ中,主要存在的钠盐有NaCl和Y,Y为 。
②往滤液Ⅲ中添加适量NaCl固体后,通入足量 (填化学式)气体,再通
入足量CO,可析出Y。
2
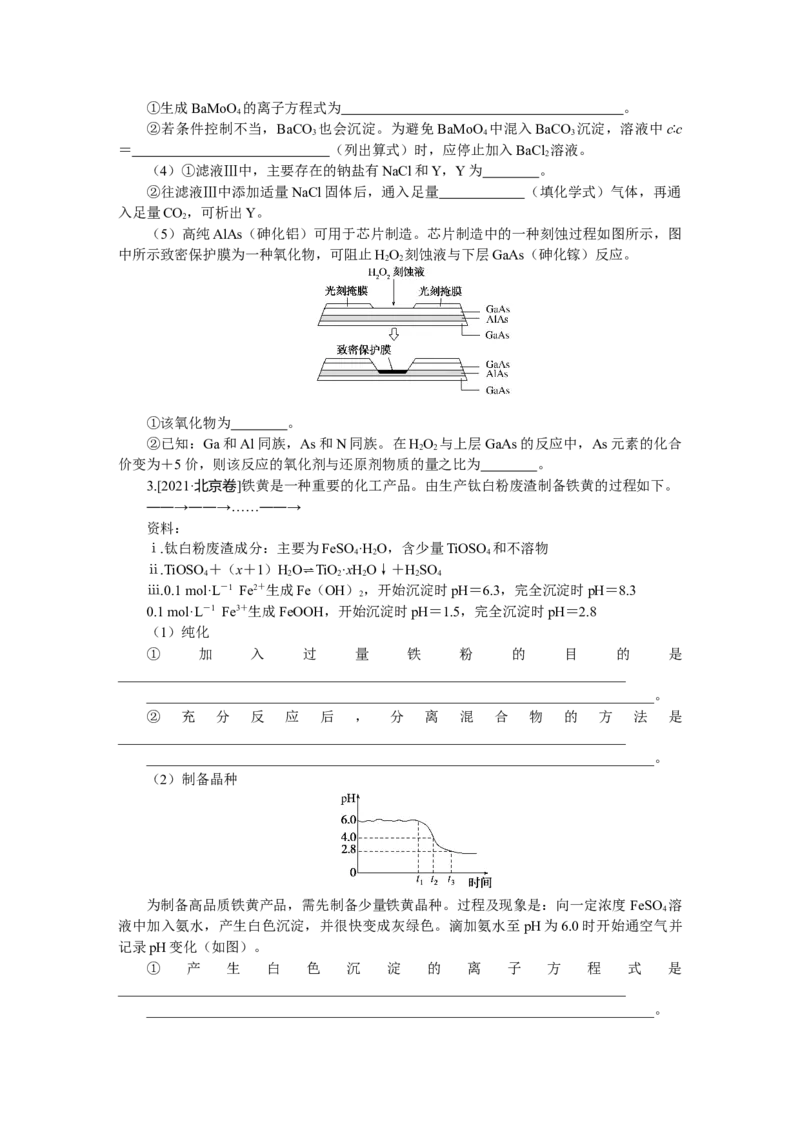
(5)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图
中所示致密保护膜为一种氧化物,可阻止HO 刻蚀液与下层GaAs(砷化镓)反应。
2 2
①该氧化物为 。
②已知:Ga和Al同族,As和N同族。在HO 与上层GaAs的反应中,As元素的化合
2 2
价变为+5价,则该反应的氧化剂与还原剂物质的量之比为 。
3.[2021·北京卷]铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
――→――→……――→
资料:
ⅰ.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ⅱ.TiOSO
4
+(x+1)H
2
O⇌TiO
2
·xH
2
O↓+H
2
SO
4
ⅲ.0.1 mol·L-1 Fe2+生成Fe(OH),开始沉淀时pH=6.3,完全沉淀时pH=8.3
2
0.1 mol·L-1 Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
① 加 入 过 量 铁 粉 的 目 的 是
________________________________________________________________________
________________________________________________________________________。
② 充 分 反 应 后 , 分 离 混 合 物 的 方 法 是
________________________________________________________________________
________________________________________________________________________。
(2)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度 FeSO 溶
4
液中加入氨水,产生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并
记录pH变化(如图)。
① 产 生 白 色 沉 淀 的 离 子 方 程 式 是
________________________________________________________________________
________________________________________________________________________。②产生白色沉淀后的 pH 低于资料ⅲ中的 6.3。原因是:沉淀生成后 c(Fe2+)
0.1 mol·L-1(填“>”“=”或“<”)。
③0~t 时段,pH 几乎不变;t ~t 时段,pH 明显降低。结合方程式解释原因:
1 1 2
________________________________________________________________________
________________________________________________________________________。
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)
3
仍降低,但c(Fe3+)增加,且c(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明
原因:________________________________________________________________________。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
――→――→――→滴定
资料:Fe3++3C O===Fe(C O),
2 2 4
Fe(C O)不与稀碱液反应
2 4
NaC O 过量,会使测定结果 (填“偏大”“偏小”或“不受影响”)。
2 2 4
4.[2021·山东卷]工业上以铬铁矿(FeCr O ,含Al、Si氧化物等杂质)为主要原料制备
2 4
红矾钠(NaCr O·2H O)的工艺流程如下。回答下列问题:
2 2 7 2
(1)焙烧的目的是将FeCr O 转化为NaCrO,并将Al、Si氧化物转化为可溶性钠盐。
2 4 2 4
焙 烧 时 气 体 与 矿 料 逆 流 而 行 , 目 的 是
________________________________________________________________________
________________________________________________________________________。
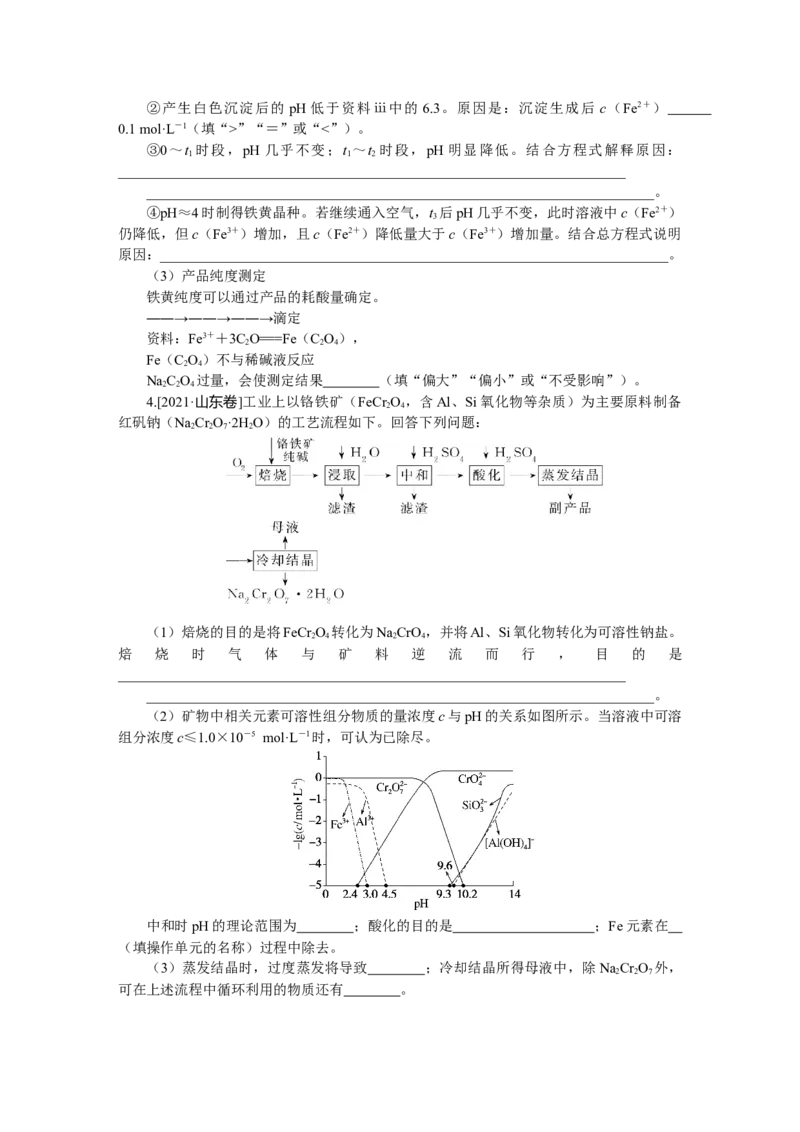
(2)矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶
组分浓度c≤1.0×10-5 mol·L-1时,可认为已除尽。
中和时pH的理论范围为 ;酸化的目的是 ;Fe元素在
(填操作单元的名称)过程中除去。
(3)蒸发结晶时,过度蒸发将导致 ;冷却结晶所得母液中,除NaCr O 外,
2 2 7
可在上述流程中循环利用的物质还有 。(4)利用膜电解技术(装置如图所示),以NaCrO 为主要原料制备NaCr O 的总反
2 4 2 2 7
应方程式为:
4NaCrO+4HO=====2NaCr O+4NaOH+2H↑+O↑
2 4 2 2 2 7 2 2
则NaCr O 在__________(填“阴”或“阳”)极室制得,电解时通过膜的离子主要
2 2 7
为__________。