文档内容
专练 39 弱电解质的电离平衡
一、单项选择题
1.[2022·广东深圳模拟]下列说法正确的是( )
A.醋酸溶液的浓度增大,醋酸的电离程度随之增大
B.0.1 mol·L-1的CHCOOH溶液,升高温度,CHCOOH的电离程度增大
3 3
C.常温下,在0.1 mol·L-1的醋酸溶液中,水电离出的H+浓度为10-13 mol·L-1
D.盐酸中的c(H+)比醋酸溶液中的c(H+)大
2.[2022·浙江十校联盟月考]下列说法正确的是( )
A.为确定某酸HA是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则HA是弱
2 2
酸;若pH<7,则HA是强酸
2
B.常温下,pH=3的醋酸溶液中加入少量醋酸钠固体,溶液pH增大,醋酸的电离程
度增大
C.25 ℃时,将0.1 mol·L-1的HA溶液加水稀释至pH=3.0,所得溶液中的c(OH-)=
1×10-11 mol·L-1
D.用同浓度的NaOH溶液分别与等体积等pH的盐酸和醋酸溶液恰好完全反应,盐酸
消耗的NaOH溶液体积多
3.[2022·哈尔滨师大青冈实验中学月考]下列无法证明某酸HA是弱酸的实验方案是(
)
A.室温下,测得0.1 mol·L-1HA溶液的pH>1,证明HA是弱酸
B.碳酸钠溶液中滴入0.1 mol·L-1的HA溶液,产生大量无色气体
C.室温下测得某HA溶液的pH=a,用蒸馏水稀释100倍测得溶液pH=b,且b-a<
2
D.室温下,用pH试纸测得0.1 mol·L-1 NaA溶液的pH>7
4.[2021·浙江1月]25 ℃时,下列说法正确的是 ( )
A.NaHA溶液呈酸性,可以推测HA为强酸
2
B.可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C.0.010 mol·L-1、0.10 mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D.100 mL pH= 10.00的NaCO 溶液中水电离出的H+的物质的量为1.0×10-5 mol
2 3
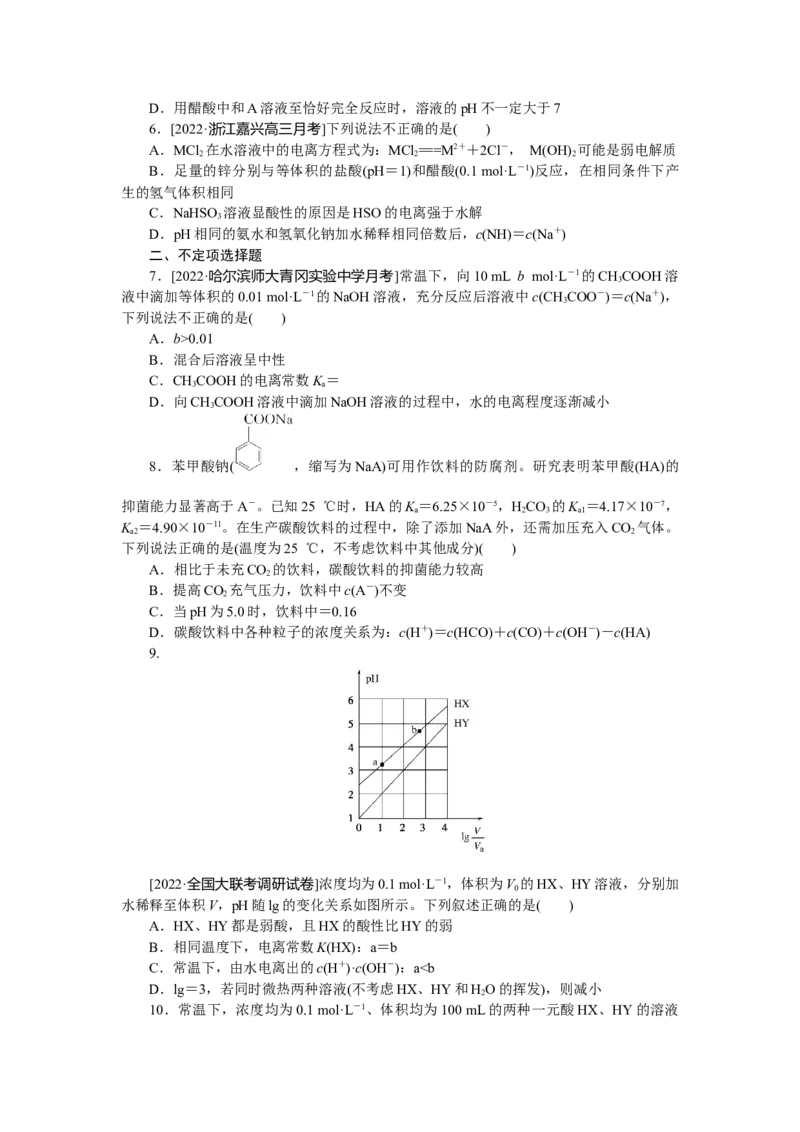
5.室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如
图所示。下列说法正确的是( )
A.稀释前两溶液中H+浓度的大小关系:A=10B
B.稀释前,A溶液中由水电离出的OH-的浓度大于10-7 mol·L-1
C.取等体积M点的A、B两种碱液,加入同浓度的硫酸溶液至恰好完全反应时,所
消耗硫酸溶液的体积相同D.用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7
6.[2022·浙江嘉兴高三月考]下列说法不正确的是( )
A.MCl 在水溶液中的电离方程式为:MCl ===M2++2Cl-, M(OH) 可能是弱电解质
2 2 2
B.足量的锌分别与等体积的盐酸(pH=1)和醋酸(0.1 mol·L-1)反应,在相同条件下产
生的氢气体积相同
C.NaHSO 溶液显酸性的原因是HSO的电离强于水解
3
D.pH相同的氨水和氢氧化钠加水稀释相同倍数后,c(NH)=c(Na+)
二、不定项选择题
7.[2022·哈尔滨师大青冈实验中学月考]常温下,向10 mL b mol·L-1的CHCOOH溶
3
液中滴加等体积的0.01 mol·L-1的NaOH溶液,充分反应后溶液中c(CHCOO-)=c(Na+),
3
下列说法不正确的是( )
A.b>0.01
B.混合后溶液呈中性
C.CHCOOH的电离常数K=
3 a
D.向CHCOOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
3
8.苯甲酸钠( ,缩写为NaA)可用作饮料的防腐剂。研究表明苯甲酸(HA)的
抑菌能力显著高于A-。已知25 ℃时,HA的K=6.25×10-5,HCO 的K =4.17×10-7,
a 2 3 a1
K =4.90×10-11。在生产碳酸饮料的过程中,除了添加NaA外,还需加压充入CO 气体。
a2 2
下列说法正确的是(温度为25 ℃,不考虑饮料中其他成分)( )
A.相比于未充CO 的饮料,碳酸饮料的抑菌能力较高
2
B.提高CO 充气压力,饮料中c(A-)不变
2
C.当pH为5.0时,饮料中=0.16
D.碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO)+c(CO)+c(OH-)-c(HA)
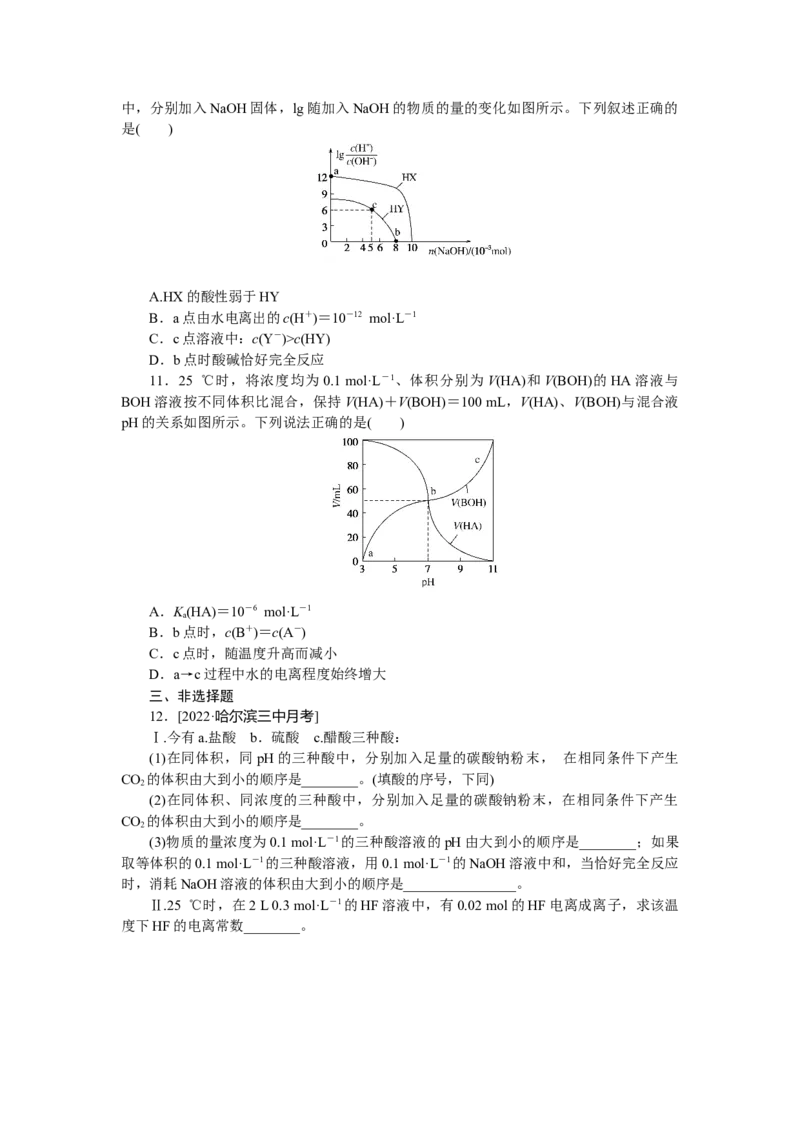
9.
[2022·全国大联考调研试卷]浓度均为0.1 mol·L-1,体积为V 的HX、HY溶液,分别加
0
水稀释至体积V,pH随lg的变化关系如图所示。下列叙述正确的是( )
A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.相同温度下,电离常数K(HX):a=b
C.常温下,由水电离出的c(H+)·c(OH-):ac(HY)
D.b点时酸碱恰好完全反应
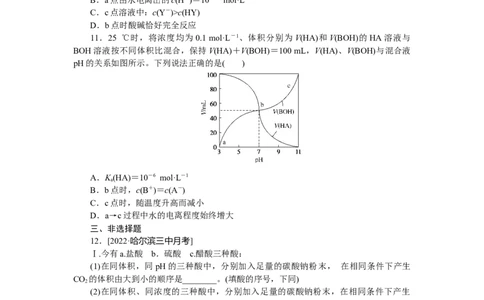
11.25 ℃时,将浓度均为0.1 mol·L-1、体积分别为V(HA)和V(BOH)的HA溶液与
BOH溶液按不同体积比混合,保持V(HA)+V(BOH)=100 mL,V(HA)、V(BOH)与混合液
pH的关系如图所示。下列说法正确的是( )
A.K(HA)=10-6 mol·L-1
a
B.b点时,c(B+)=c(A-)
C.c点时,随温度升高而减小
D.a→c过程中水的电离程度始终增大
三、非选择题
12.[2022·哈尔滨三中月考]
Ⅰ.今有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)在同体积,同pH的三种酸中,分别加入足量的碳酸钠粉末, 在相同条件下产生
CO 的体积由大到小的顺序是________。(填酸的序号,下同)
2
(2)在同体积、同浓度的三种酸中,分别加入足量的碳酸钠粉末,在相同条件下产生
CO 的体积由大到小的顺序是________。
2
(3)物质的量浓度为0.1 mol·L-1的三种酸溶液的pH由大到小的顺序是________;如果
取等体积的0.1 mol·L-1的三种酸溶液,用0.1 mol·L-1的NaOH溶液中和,当恰好完全反应
时,消耗NaOH溶液的体积由大到小的顺序是________________。
Ⅱ.25 ℃时,在2 L 0.3 mol·L-1的HF溶液中,有0.02 mol的HF电离成离子,求该温
度下HF的电离常数________。