文档内容
第八篇 化学实验
专项 52 微型工艺流程的分析
化学工艺流程题是近几年高考的热点,将化工生产过程中的主要生产阶段即生产流程用框图的形式表
示出来,并根据生产流程中有关的化学知识步步设问,形成与化工生产紧密联系的化工工艺试题,是无机
框图题的创新;它以现代工业生产为基础,与化工生产成本、产品提纯、环境保护等相融合,主要涉及物
质的性质、分离提纯、反应原理、实验操作、产率计算等基本实验原理在化工生产中的实际应用,是高考
化学命题的常考题型。由于此类试题陌生度高,对学生的能力要求也大,加上有的试题文字信息量大,所
以这类题的得分不是很理想。
1.(2022•河北省选择性考试) 溶液可作为替代氟利昂的绿色制冷剂。合成 工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为LiCO+2HBr=CO ↑ +2LiBr +H O
2 3 2 2
D.参与反应的n(Br):n(BaS):n(H SO )为1:1:1
2 2 4
【答案】A
【解析】由流程可知,氢溴酸中含有少量的溴,加入硫化钡将溴还原生成溴化钡和硫,再加入硫酸除
杂,得到的滤渣为硫酸钡和硫;加入碳酸锂进行中和,得到的溴化锂溶液经浓缩等操作后得到产品溴化锂。
A项,还原工序逸出的Br 用NaOH溶液吸收,吸收液中含有溴化钠和次溴酸钠等物质,若直接返回还原
2
工序,则产品中会有一定量的溴化钠,导致产品的纯度降低,A错误;B项,除杂工序中产生的滤渣为硫
酸钡和硫,硫属于非极性分子形成的分子晶体,而硫酸钡属于离子晶体,根据相似相溶原理可知,硫可溶
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司于煤油,而硫酸钡不溶于煤油,因此可用煤油进行组分分离,B正确;C项,中和工序中,碳酸锂和氢溴
酸发生反应生成溴化锂、二氧化碳和水,该反应的化学方程式为 LiCO+2HBr=CO ↑ +2LiBr +H O,C正
2 3 2 2
确;D项,根据电子转化守恒可知,溴和硫化钡反应时物质的量之比为1:1;根据硫酸钡的化学组成及钡
元素守恒可知,n(BaS):n(H SO )为1:1,因此,参与反应的n(Br):n(BaS):n(H SO )为1:1:1,D正
2 4 2 2 4
确;故选A。
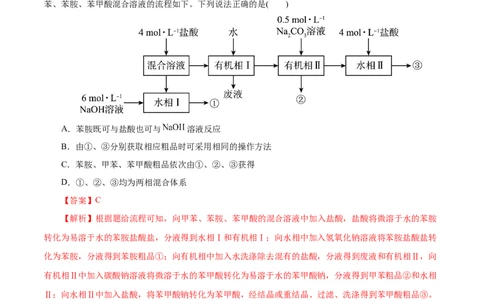
2.(2022•山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲
苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
【答案】C
【解析】根据题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺
转化为易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转
化为苯胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向
有机相Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相
Ⅱ;向水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲酸粗品③。
A项,苯胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,A错误;B项,得到苯胺粗品
①的分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过滤、洗涤,获取两者的操作方法
不同,B错误;C项,苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,C正确;D项,①、②
为液相,③为固相,都不是两相混合体系,D错误;故选C。
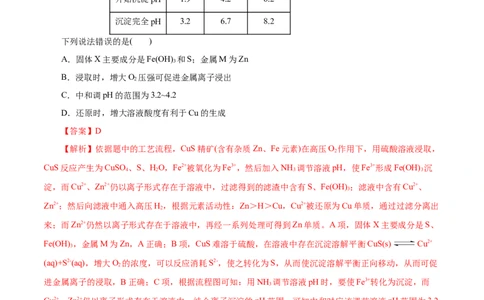
3.(2022•山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为
主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是( )
A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
【答案】D
【解析】依据题中的工艺流程,CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,
2
CuS反应产生为CuSO 、S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH) 沉
4 2 3 3
淀,而Cu2+、Zn2+仍以离子形式存在于溶液中,过滤得到的滤渣中含有S、Fe(OH) ;滤液中含有Cu2+、
3
Zn2+;然后向滤液中通入高压H,根据元素活动性:Zn>H>Cu,Cu2+被还原为Cu单质,通过过滤分离出
2
来;而Zn2+仍然以离子形式存在于溶液中,再经一系列处理可得到Zn单质。A项,固体X主要成分是S、
Fe(OH) ,金属M为Zn,A正确;B项,CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s) Cu2+
3
(aq)+S2-(aq),增大O 的浓度,可以反应消耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促
2
进金属离子的浸取,B正确;C项,根据流程图可知:用NH 调节溶液pH时,要使Fe3+转化为沉淀,而
3
Cu2+、Zn2+仍以离子形式存在于溶液中,结合离子沉淀的pH范围,可知中和时应该调节溶液pH范围为3.2
~4.2,C正确;D项,在用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H+,与溶液中OH-结合形成
2 2
HO,若还原时增大溶液的酸度,c(H+)增大,不利于H 失去电子还原Cu单质,因此不利于Cu的生成,D
2 2
错误;故选D。
4.(2021•湖南选择性考试)一种工业制备无水氯化镁的工艺流程如图:
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
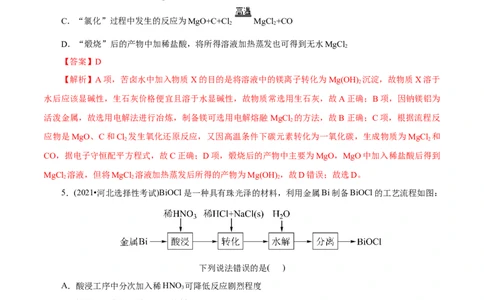
C.“氯化”过程中发生的反应为MgO+C+Cl MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
【答案】D
【解析】A项,苦卤水中加入物质X的目的是将溶液中的镁离子转化为Mg(OH) 沉淀,故物质X溶于
2
水后应该显碱性,生石灰价格便宜且溶于水显碱性,故物质常选用生石灰,故A正确;B项,因钠镁铝为
活泼金属,故选用电解法进行冶炼,制备镁可选用电解熔融 MgCl 的方法,故B正确;C项,根据流程反
2
应物是MgO、C和Cl 发生氧化还原反应,又因高温条件下碳元素转化为一氧化碳,生成物质为MgCl 和
2 2
CO,据电子守恒配平方程式,故C正确;D项,煅烧后的产物中主要为MgO,MgO中加入稀盐酸后得到
MgCl 溶液,但将MgCl 溶液加热蒸发后所得的产物为Mg(OH) ,故D错误;故选D。
2 2 2
5.(2021•河北选择性考试)BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
下列说法错误的是( )
A.酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CHCOONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
【答案】D
【解析】A项,硝酸为强氧化剂,可与金属铋反应,酸浸工序中分次加入稀HNO,反应物硝酸的用
3
量减少,可降低反应剧烈程度,A正确;B项,金属铋与硝酸反应生成的硝酸铋会发生水解反应生成
BiONO ,水解的离子方程式为Bi3++NO-+H O BiONO +2H+,转化工序中加入稀HCl,使氢离子浓度
3 3 2 3
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司增大,根据勒夏特列原理分析,硝酸铋水解平衡左移,可抑制生成BiONO ,B正确;C项,氯化铋水解生
3
成BiOCl的离子方程式为Bi3++Cl-+ H O BiOCl+2H+,水解工序中加入少量CHCOONa(s),醋酸根会
2 3
结合氢离子生成弱电解质醋酸,使氢离子浓度减小,根据勒夏特列原理分析,氯化铋水解平衡右移,促进
Bi3+水解,C正确;D项,氯化铋水解生成BiOCl的离子方程式为Bi3++Cl-+ H O BiOCl+2H+,水解工
2
序中加入少量NH NO (s),铵根离子水解生成氢离子,使氢离子浓度增大,根据勒夏特列原理分析,氯化
4 3
铋水解平衡左移,不利于生成BiOCl,且部分铋离子与硝酸根、水也会发生反应Bi3++NO-+H O
3 2
BiONO +2H+,也不利于生成BiOCl,综上所述,D错误;故选D。
3
6.(2020•山东卷)实验室分离Fe3+和Al3+的流程如下:
知Fe3+在浓盐酸中生成黄色配离子(FeCl ),该配离子在乙醚(Et O,沸点34.6℃)中生成缔合物
4 2
。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
【答案】A
【解析】A项,萃取振荡时,分液漏斗下口应倾斜向上,A错误;B项,分液时,密度大的液体在下层,
密度小的液体在上层,下层液体由分液漏斗下口放出,下层液体放完后,密度小的上层液体从分液漏斗上
口倒出,B正确;C项,Fe3+在浓盐酸中生成黄色配离子,该离子在乙醚中生成缔合物,乙醚与水不互溶,
故分液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目的,C正确;D项,蒸馏时选用直形
冷凝管,能使馏分全部转移到锥形瓶中,而不会残留在冷凝管中,D正确;故选A。
7.(2020•山东卷)以菱镁矿(主要成分为MgCO ,含少量SiO,Fe O 和A1 O)为原料制备高纯镁砂的工
3 2 2 3 2 3
艺流程如下:
5
原创精品资源学科网独家享有版权,侵权必究!
5
学科网(北京)股份有限公司已知浸出时产生的废渣中有SO ,Fe(OH) 和Al(OH) 。下列说法错误的是( )
2 3 3
A.浸出镁的反应为MgO+2NH Cl=MgCl +2NH↑+H O
4 2 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.流程中可循环使用的物质有NH 、NH Cl
3 4
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物K 的不同
sp
【答案】B
【解析】菱镁矿煅烧后得到轻烧粉,MgCO 转化为MgO,加入氯化铵溶液浸取,浸出的废渣有SiO、
3 2
Fe(OH) 、Al(OH) ,同时产生氨气,则此时浸出液中主要含有Mg2+,加入氨水得到Mg(OH) 沉淀,煅烧得
3 3 2
到高纯镁砂。A项,高温煅烧后Mg元素主要以MgO的形式存在,MgO可以与铵根水解产生的氢离子反
应,促进铵根的水解,所以得到氯化镁、氨气和水,化学方程式为MgO+2NH Cl=MgCl +2NH↑+H O,故
4 2 3 2
A正确;B项,一水合氨受热易分解,沉镁时在较高温度下进行会造成一水合氨大量分解,挥发出氨气,
降低利用率,故B错误;C项,浸出过程产生的氨气可以回收制备氨水,沉镁时氯化镁与氨水反应生成的
氯化铵又可以利用到浸出过程中,故C正确;D项,Fe(OH) 、Al(OH) 的K 远小于Mg(OH) 的K ,所以
3 3 sp 2 sp
当pH达到一定值时Fe3+、Al3+产生沉淀,而Mg2+不沉淀,从而将其分离,故D正确;故选B。
1.工艺流程题过程解读
(1)读流程图
6
原创精品资源学科网独家享有版权,侵权必究!
6
学科网(北京)股份有限公司①箭头:箭头进入的是投料(反应物)、出去的是主产物或副产物(生成物)。
②三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
(2)解题要点
①审题要点:a.了解生产目的、原料及产品;b.了解题目提供的信息;c.分析各步的反应条件、原
理及物质成分;d.理解物质分离、提纯、条件控制等操作的目的及要点。
②答题切入点:a.原料及产品的分离提纯,b.生产目的及反应原理;c.生产要求及反应条件;d.
有关产率、产量及组成的计算;e.绿色化学。
2.读流程寻破题关键
(1)看原料:明确化工生产或化学实验所需的材料。
(2)看目的:把握题干中的“制备”或“提纯”等关键词,确定化工生产或化学实验的目的。
(3)看箭头:进入的是投料(反应物);出去的是生成物(包括主产物和副产物)。
(4)看三线:主线为主产品,分支为副产品,回头为循环物。
(5)找信息:明确反应条件的控制和分离提纯方法。(6)关注所加物质的可能作用:参与反应、提供反应
氛围、满足定量要求。
3.明方法科学破题
(1)首尾分析法:对一些线型流程工艺(从原料到产品为一条龙的生产工序)试题,首先对比分析流程图
中第一种物质(原材料)与最后一种物质(产品),从对比分析中找出原料与产品之间的关系,弄清生产过程中
原料转化为产品的基本原理和除杂、分离、提纯产品的化工工艺,然后结合题设的问题,逐一推敲解答。
(2)截段分析法:对于用同样的原材料生产两种或多种产品(包括副产品)的工艺流程题,用截段分析法
更容易找到解题的切入点。关键在于看清主、副产品是如何分开的,以此确定截几段更合适,一般截段以
产品为准点。
(3)交叉分析法:有些化工生产选用多组原材料,先合成一种或几种中间产品,再用这一中间产品与部
分其他原材料生产所需的主流产品,这种题适合用交叉分析法。就是将提供的工业流程示意图结合常见化
合物的制取原理划分成几条生产流水线,然后上下交叉分析。
7
原创精品资源学科网独家享有版权,侵权必究!
7
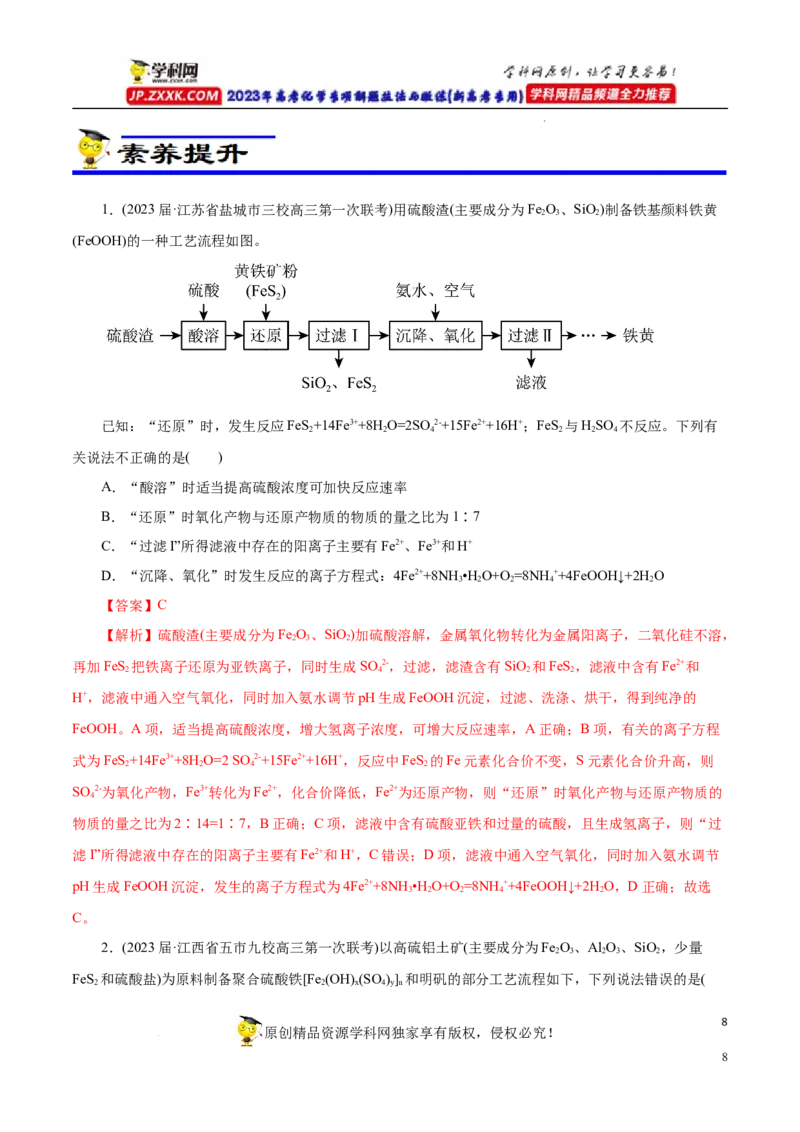
学科网(北京)股份有限公司1.(2023届·江苏省盐城市三校高三第一次联考)用硫酸渣(主要成分为Fe O、SiO)制备铁基颜料铁黄
2 3 2
(FeOOH)的一种工艺流程如图。
已知:“还原”时,发生反应FeS+14Fe3++8H O=2SO 2-+15Fe2++16H+;FeS 与HSO 不反应。下列有
2 2 4 2 2 4
关说法不正确的是( )
A.“酸溶”时适当提高硫酸浓度可加快反应速率
B.“还原”时氧化产物与还原产物质的物质的量之比为1∶7
C.“过滤I”所得滤液中存在的阳离子主要有Fe2+、Fe3+和H+
D.“沉降、氧化”时发生反应的离子方程式:4Fe2++8NH•H O+O=8NH++4FeOOH↓+2H O
3 2 2 4 2
【答案】C
【解析】硫酸渣(主要成分为Fe O、SiO)加硫酸溶解,金属氧化物转化为金属阳离子,二氧化硅不溶,
2 3 2
再加FeS 把铁离子还原为亚铁离子,同时生成SO 2-,过滤,滤渣含有SiO 和FeS,滤液中含有Fe2+和
2 4 2 2
H+,滤液中通入空气氧化,同时加入氨水调节pH生成FeOOH沉淀,过滤、洗涤、烘干,得到纯净的
FeOOH。A项,适当提高硫酸浓度,增大氢离子浓度,可增大反应速率,A正确;B项,有关的离子方程
式为FeS+14Fe3++8H O=2 SO 2-+15Fe2++16H+,反应中FeS 的Fe元素化合价不变,S元素化合价升高,则
2 2 4 2
SO 2-为氧化产物,Fe3+转化为Fe2+,化合价降低,Fe2+为还原产物,则“还原”时氧化产物与还原产物质的
4
物质的量之比为2∶14=1∶7,B正确;C项,滤液中含有硫酸亚铁和过量的硫酸,且生成氢离子,则“过
滤I”所得滤液中存在的阳离子主要有Fe2+和H+,C错误;D项,滤液中通入空气氧化,同时加入氨水调节
pH生成FeOOH沉淀,发生的离子方程式为4Fe2++8NH•H O+O=8NH++4FeOOH↓+2H O,D正确;故选
3 2 2 4 2
C。
2.(2023届·江西省五市九校高三第一次联考)以高硫铝土矿(主要成分为Fe O、Al O、SiO,少量
2 3 2 3 2
FeS 和硫酸盐)为原料制备聚合硫酸铁[Fe (OH) (SO )] 和明矾的部分工艺流程如下,下列说法错误的是(
2 2 x 4 y n
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司)
已知:赤泥液的主要成分为NaCO。
2 3
A.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关
B.赤泥液的作用是吸收“焙烧”阶段中产生的SO
2
C.在“聚合”阶段,若增加Fe O 用量,会使[Fe (OH) (SO )] 中x变大
2 3 2 x 4 y n
D.从“滤液”到“明矾”的过程中还应有“除硅”步骤
【答案】A
【解析】高硫铝土矿经焙烧后,FeS 中的S元素转化为SO 被除去,生成的SO 用赤泥液吸收,防止
2 2 2
其污染环境。高硫铝土矿经碱浸后,Al O 转化为AlO- ,SiO 转化为SiO2-。过滤后将滤渣经酸浸氧化后,
2 3 2 2 3
Fe2+全部被转化为Fe3+,用于制备聚合硫酸铁。AlO-进入滤液中,可用于制备明矾。A项,聚合硫酸铁可
2
用于净水,原理是聚合硫酸铁中的Fe3+水解生成的Fe(OH) 胶体可吸附水中的悬浮物和杂质,与Fe3+的氧化
3
性无关,故A项错误;B项,赤泥液主要成分是NaCO,可吸收焙烧产生的SO ,故B项正确;C项,聚
2 3 2
合硫酸铁中的OH-来源于Fe O,因此增加Fe O 用量会使[Fe (OH) (SO )] 中x变大,故C项正确;D项,
2 3 2 3 2 x 4 y n
制备明矾的滤液中含有SiO2-,应预先除去,故D项正确。故选A。
3
3.(2023届·河南省重点高中高三联考)已知苯甲酸乙酯的沸点为212.6℃、乙醚-环己烷-水共沸物的沸
点为62.1℃。实验室利用苯甲酸、乙醇、环己烷和浓硫酸混合加热制备苯甲酸乙酯,现从反应混合物中分
离苯甲酸乙酯、苯甲酸和环己烷的流程如图。下列说法错误的是( )
A.操作a所使用的主要玻璃仪器为分液漏斗和烧杯
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司B.操作b和操作c均为重结晶
C.无水 的作用为干燥有机相Ⅱ
D.该流程中苯甲酸先转化为苯甲酸钠,再转化为苯甲酸
【答案】B
【解析】由题给流程可知,向混合物中加入饱和碳酸钠溶液洗涤,将苯甲酸转化为苯甲酸钠,分液得
到含有苯甲酸乙酯和环己烷的有机相和水相;向水相中加入乙醚萃取水相中的苯甲酸乙酯和环己烷,分液
得到有机相和萃取液;有机相混合得到有机相Ⅰ,有机相经蒸馏得到共沸物和有机相Ⅱ;向有机相中加入
无水硫酸镁除去水分,干燥有机相Ⅱ,过滤、蒸馏得到苯甲酸乙酯;向萃取液中加入稀硫酸,将苯甲酸钠
转化为苯甲酸,过滤得到苯甲酸粗品,经重结晶得到苯甲酸。A项,操作a为分液,分液所使用的主要玻
璃仪器为分液漏斗和烧杯,故A正确;B项,操作b为蒸馏,操作c均为重结晶,故B错误;C项,加入
无水硫酸钠镁的作用是除去水分,干燥有机相Ⅱ,故C正确;D项,该流程中苯甲酸先与饱和碳酸钠溶液
反应转化为苯甲酸钠,苯甲酸钠再与稀硫酸反应转化为苯甲酸,故D正确;故选B。
4.(2023届·甘肃省白银市高三开学考试)一种从钛白酸性废水(主要含 ,还含微量 )中富
集钪并制备氧化钪(Sc O)的工艺流程如图。
2 3
已知:“有机相”中主要含有Ti4+、Fe2+、Sc3+
下列说法错误的是( )
A.“萃取分液”需要用到的玻璃仪器有分液漏斗和烧杯
B.加入HO 的目的是将Fe2+氧化为Fe3+
2 2
C.“滤渣1”的主要成分是Ti(OH) 、Fe(OH) 、Sc(OH)
4 3 3
D.1mol草酸钪完全焙烧分解时,转移电子的物质的量为12mol
【答案】D
【解析】从钛白酸性废水(主要含Ti4+、Fe2+、微量Sc3+)中富集钪,酸洗时加入HO 的目的是将Fe2+氧
2 2
化为Fe3+,加入氢氧化钠溶液进行反萃取,过滤得到“滤渣1”的主要成分是Ti(OH) 、Fe(OH) 、Sc(OH) ,
4 3 3
然后加入10%盐酸调pH溶解Sc(OH) 转化为含Sc3+的溶液,再加入草酸溶液得到草酸钪,草酸钪与氧气焙
3
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司烧时反应生成Sc O 和CO。A项,“萃取分液”需要用到的玻璃仪器主要有分液漏斗和烧杯,故A正确;
2 3 2
B项,可知,“有机相”中主要含有Ti4+、Fe2+、Sc3+,酸洗时加入HO 的目的是将Fe2+氧化为Fe3+,有利
2 2
于后面沉淀除去,故B正确;C项,“滤渣1”的主要成分是Ti(OH) 、Fe(OH) 、Sc(OH) ,故C正确;D项,
4 3 3
草酸钪与氧气焙烧时反应生成Sc O 和CO,化学方程式为:2Sc (C O)+3O 2Sc O+12CO ,1mol草酸
2 3 2 2 2 4 3 2 2 3 2
钪完全焙烧分解时,转移电子的物质的量为6mol,D错误;故选D。
5.(2023届·河北省邢台市名校联盟高三开学考试)某工厂采用辉铋矿(主要成分为BiS,含有FeS、
2 3 2
SiO 杂质)与软锰矿(主要成分为MnO )联合焙烧法制备BiOCl,工艺流程如图所示。焙烧时过量的MnO 分
2 2 2
解为MnO,下列说法错误的是( )
2 3
A.BiS 和FeS 联合焙烧转化为BiO、Fe O
2 3 2 2 3 2 3
B.水浸所得滤液的主要成分是MnSO
4
C.酸浸所得滤渣的主要成分是SiO,气体X为Cl
2 2
D.向酸浸滤液中加入金属Bi的目的是消耗H+,促进 水解
【答案】D
【解析】联合焙烧:发生转化为:BiS→BiO+SO、FeS→Fe O+SO、MnO →MnO+MnSO ,故联
2 3 2 3 2 2 2 3 2 2 2 3 4
合焙烧后得到BiO、Fe O、MnO、MnSO 和SiO;水浸:MnSO 进入滤液,滤渣为BiO、Fe O、
2 3 2 3 2 3 4 2 4 2 3 2 3
MnO 和SiO;酸浸:加入过量浓盐酸后,BiO 和Fe O 发生转化:BiO→Bi3+、Fe O→Fe3+,因MnO
2 3 2 2 3 2 3 2 3 2 3 2 3
有氧化性,会与浓盐酸发生氧化还原反应:MnO+6H++2Cl-=2Mn2++Cl↑+3H O,气体X为Cl,滤渣主要
2 3 2 2 2
为不溶于浓盐酸的SiO,滤液中金属离子为Bi3+、Fe3+、Mn2+;转化:加入Bi将Fe3+转化为Fe2+,调节pH
2
得到BiOCl。A项,BiS 和FeS 联合焙烧转化为BiO、Fe O,故A正确;B项,水浸所得滤液的主要成
2 3 2 2 3 2 3
分是MnSO ,故B正确;C项,酸浸所得滤渣的主要成分是SiO,气体X为Cl,故C正确;D项,向酸
4 2 2
浸滤液中加入金属Bi的目的是将Fe3+转化为Fe2+,调节pH得到BiOCl,故D错误;故选D。
6.(2023届·浙江省七彩阳光新高考研究联盟高三返校联考)黑钨矿的主要成分为FeWO、MnWO (含
4 4
SiO 杂质)。已知:4FeWO+O +4Na CO 2Fe O+4Na WO+4CO
2 4 2 2 3 2 3 2 4 2
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司2MnWO +O +2Na CO 2MnO +2Na WO+2CO
4 2 2 3 2 2 4 2
工业上以黑钨矿为原料利用纯碱烧结水浸法冶炼金属钨的流程如图。下列说法不正确的是( )
A.为加快水浸的溶解速率,应将烧结物粉碎
B.滤渣1经铝热反应可制得金属铁和锰,滤渣2为硅酸
C.同浓度的钨酸根离子结合质子的能力比硅酸根离子更强
D.“除杂”步骤中加入的盐酸应适量,溶液的pH须控制在特定范围内
【答案】C
【解析】黑钨矿的主要成分为FeWO、MnWO (含SiO 杂质),烧结物的主要成分为 Fe O、
4 4 2 2 3
MnO 、NaSiO、NaWO,加水过滤,滤渣 1 是难溶于水的 Fe O、MnO ;滤液中含有 NaSiO、
2 2 3 2 4 2 3 2 2 3
NaWO,加入盐酸调节 pH,生成硅酸沉淀,除去 NaSiO,再加盐酸生成钨酸沉淀,钨酸加热分解为
2 4 2 3
WO,还原得到W单质。A项,将烧结物粉碎可以增大反应物的接触面积,加快水浸的溶解速率,故A正
3
确;B项,由分析可知,滤渣 1 是难溶于水的 Fe O、MnO ,经铝热反应可制得金属铁和锰,滤渣2为
2 3 2
硅酸,故B正确;C项,流程中硅酸根离子先于钨酸根离子沉淀,说明同浓度的钨酸根离子结合质子的能
力比硅酸根离子更弱,故C错误;D项,“除杂”步骤中加入的盐酸应适量,溶液的pH须控制在特定范
围内,若加入盐酸过多,可能会提前生成钨酸沉淀,故D正确;故选C。
7.(2022·辽宁省葫芦岛市二模)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成
氨以及氨催化制硝酸的流程示意图。下列说法不正确的是 ( )
A.可以利用NH 易液化的性质分离出NH
3 3
B.合成氨以及氨催化制硝酸的流程中氮元素均被氧化
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司C.可以用NH 进行氨氧化物的尾气处理
3
D.吸收塔中通入A是为了提高原料的利用率
【答案】B
【解析】A项,利用NH 易液化的性质分离出NH ,促进平衡正向移动,A项正确;B项,合成氨中
3 3
氮气中氮元素化合价降低做氧化剂,被还原发生还原反应,氨催化制硝酸的流程中氮元素化合价由-3价升
高到+2价,被氧化,B项错误;C项,氨气具有还原性,氮氧化物具有氧化性,二者反应生成无毒气体氮
气,可以用NH 进行氮氧化物的尾气处理,C项正确;D项,一氧化氮与氧气反应生成二氧化氮,二氧化
3
氮、氧气和水反应生成硝酸, A 为O,吸收塔中通入A是为了提高原料的利用率,D项正确;故选B。
2
8.(2022·山东省临沂市三模)以天然气为原料合成氨是新的生产氮肥的方法,其工艺流程如下。下列
说法正确的是( )
A.反应①使用催化剂可提高反应速率和甲烷的平衡转化率
B.反应②的原子利用率为100%
C.生成1.0 mol NH NO 至少需要0.75 mol CH
4 3 4
D.反应③理论上当n( NH):n(O )= 4:3时,恰好完全反应
3 2
【答案】C
【解析】A项,反应①使用催化剂可以提高反应速率,但不能提高甲烷的平衡转化率,A错误;B项,
反应②的化学方程式为CO+2NH CO(NH)+H O,则该反应的原子利用率小于100%,B错误;C
2 3 2 2 2
项,由天然气经过各步转化,最终生成NH NO 涉及的化学反应有:CH+2H O CO+4H ,N+3H
4 3 4 2 2 2 2 2
2NH ,2NH +2O =NHNO +H O,则有NH NO ~2NH~3H ~ CH,故生成1.0mol NH NO 至
3 3 2 4 3 2 4 3 3 2 4 4 3
少需要0.75mol CH ,C正确;D项,反应③中,NH 和O 反应生成NH NO ,该反应的化学方程式为
4 3 2 4 3
2NH +2O =NHNO +H O,则理论上当n(NH ):n(O )=1:1时,恰好完全反应,D错误;故选C。
3 2 4 3 2 3 2
13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司9.(2022·北京市人大附中三模)用如下方法回收废旧CPU中的单质Au(金)、Ag和Cu
已知:浓硝酸不能单独将Au溶解,通常采用王水[V(浓硝酸):V(浓盐酸)=1∶3]溶解Au。
下列说法不正确的是( )
A.浓、稀HNO 均可作酸溶试剂,溶解等量的Cu,选择稀硝酸可节约原料
3
B.HNO- NaCl与王水溶金原理相同,反应原理可以表示为:
3
Au+4NaCl+5HNO =HAuCl+NO↑+4NaNO +2H O
3 4 3 2
C.用王水溶金时,利用了HNO 的氧化性,浓盐酸的主要作用是增强溶液的酸性
3
D.用适当浓度的盐酸、氯化钠溶液、氨水和铁粉可从酸溶后的溶液中回收Cu和Ag,试剂1应选择
NaCl溶液
【答案】C
【解析】A项,Cu与稀HNO 反应的方程式为3Cu+8HNO =3Cu(NO )+2NO↑+4H O,溶解1molCu需
3 3 3 2 2
要硝酸为 ,Cu与浓HNO 反应的方程式为Cu+4HNO =Cu(NO )+2NO↑+2H O,溶解1molCu需要硝酸
3 3 3 2 2 2
为4mol,故溶解等量的Cu,选择稀硝酸可节约原料,故A正确;B项,根据化合价的变化规律可知,金
元素的化合价从0价升高为+3价,是还原剂,硝酸是氧化剂,氮元素的化合价从+5价降低为+2价,产物
是NO,根据得失电子守恒、元素守恒配平方程式为Au+4NaCl+5HNO =HAuCl+NO↑+4NaNO +2H O,故B
3 4 3 2
正确;C项,用王水溶金时,硝酸中N的化合价降低,做氧化剂,利用了HNO 的氧化性,浓盐酸提供了
3
氯离子,利于生成四氯合金离子,其主要作用是减小金离子的电势,增强金的还原性,故C错误;D项,
根据图中信息可知,含有铜离子和银离子的溶液加入试剂1后得到的是物质1和物质3,物质3加入试剂3
后得到的是二氨合银离子,试剂3是氨水,物质3是氯化银,试剂1是NaC1溶液,物质1是氯化铜,氯化
铜加入过量铁粉得到物质2是铜和铁单质,经过试剂2,过滤后得到铜单质,试剂2是盐酸,除去过量的
铁粉,二氨合银离子经过还原可以得到银单质,实现了铜和银的分离,故D正确;故选C。
10.(2022·湖南省高三模拟)铵明矾[NH Al(SO )·12H O]是分析化学中常用的基准试剂,其制备过程如
4 4 2 2
图:
14
原创精品资源学科网独家享有版权,侵权必究!
14
学科网(北京)股份有限公司下列说法不正确的是( )
A.过程Ⅰ过滤可得到NaHCO 晶体
3
B.过程Ⅱ加入稀硫酸的目的是为了除去滤液A中混有的NaHCO 杂质
3
C.向铵明矾溶液中加入足量 溶液,反应的离子方程式为NH ++Al3++5OH-= NH ·H O+ AlO-
4 3 2 2
+2H O
2
D.铵明矾能析出是因为其溶解度比(NH )SO 、Al (SO ) 的大
4 2 4 2 4 3
【答案】D
【解析】NaHCO 的溶解度较小,所以在饱和碳酸氢铵溶液中加入过量的硫酸钠溶液会产生NaHCO
3 3
沉淀,过滤后得滤液中有(NH )SO 和少量的NaHCO ,将(NH )SO 溶液用稀硫酸调节pH值为2,使
4 2 4 3 4 2 4
NaHCO 生成硫酸钠,得溶液B为(NH )SO 溶液和少量的硫酸钠溶液,在B溶液中加入硫酸铝可得铵明矾。
3 4 2 4
A项,结合流程分析可知,过程Ⅰ过滤可得到NaHCO 晶体,故A正确;B项,结合流程分析可知,将
3
(NH )SO 溶液用稀硫酸调节pH值为2,使NaHCO 生成硫酸钠,即过程Ⅱ加入稀硫酸的目的是为了除去
4 2 4 3
滤液A中混有的NaHCO 杂质,故B正确;C项,向铵明矾溶液中逐滴加入过量的NaOH溶液,生成偏铝
3
酸钠、一水合氨、硫酸钠和水,离子方程式为NH ++Al3++5OH-= NH ·H O+ AlO-+2H O,故C正确;D项,
4 3 2 2 2
在B溶液中加入硫酸铝可得铵明矾,说明铵明矾能析出是因为其溶解度比(NH )SO 、Al (SO ) 的均小,故
4 2 4 2 4 3
D错误;故选D。
11.(2022·江苏省淮安市高三考前模拟)以含钴废渣(主要成分为CoO和Co O,含少量Al O 和ZnO)为
2 3 2 3
原料制备CoCO 的工艺流程如图:
3
下列说法正确的是( )
A.酸浸时可采用高温提高酸浸速率
B.除铝时加入NaCO 溶液过滤后所得滤渣是Al (CO)
2 3 2 3 3
15
原创精品资源学科网独家享有版权,侵权必究!
15
学科网(北京)股份有限公司C.萃取时萃取剂总量一定,分多次加入萃取比一次加入萃取效果更好
D.沉钴时将含Co2+的溶液缓慢滴加到NaCO 溶液中,可提高CoCO 的产率
2 3 3
【答案】C
【解析】钴废渣主要 成分为CoO、Co O,还含有Al O、ZnO等杂质,加入硫酸酸浸并通入二氧化
2 3 2 3
硫,纵观整个流程知最后得到CoCO,说明该过程中二氧化硫起还原作用,硫酸与氧化铝、氧化锌反应,
3
所得溶液中含有硫酸铝、硫酸锌等,加入碳酸钠溶液调节溶液的pH,使铝离子转化为氢氧化铝沉淀并过滤
除去;加入萃取剂,萃取锌离子,在有机层中加入稀硫酸,可得到硫酸锌,在水相中加入碳酸钠溶液生成
CoCO 固体。A项,因为温度过高,可能会使用溶液起化学反应,从而无法达到溶浸的目的,酸浸时适当
3
升高温度可提高酸浸速率,A项错误;B项,除铝时加入NaCO 溶液,发生的反应为:2Al3++3CO 2-
2 3 3
+3H O=2Al(OH) ↓+3CO ↑,过滤后所得滤渣是Al(OH) ,B项错误;C项,萃取过程中,多次萃取能使萃取
2 3 2 3
效率提高,C项正确;D项,将含Co2+的溶液缓慢滴加到NaCO 溶液中,碳酸钠过量,液碱性过强,会生
2 3
成Co(OH) 沉淀,降低CoCO 的产率,D项错误;故选C。
2 3
12.(2022·北京市中关村中学三模)1941年,我国科学家侯德榜结合地域条件改进索尔维制碱法,提出
纯碱与铵肥(NH Cl)的联合生产工艺,后被命名为“侯氏制碱法”。主要工艺流程如下图。下列说法正确的
4
是
已知:侯氏制碱法总反应:2NaCl+H O+2NH +CO =Na CO+2NHCl
2 3 2 2 3 4
索尔维制碱法总反应:2NaCl+CaCO =Na CO+CaCl (CaCl 作为废液排放)
3 2 3 2 2
A.气体1、气体2均为CO
2
B.溶液2中,含碳微粒主要是
C.侯氏制碱法和索尔维制碱法中原料NaCl的原子利用率相同
D.盐析池中加入NaCl,c(Cl-)增大,NH Cl(s) NH +(aq)+Cl-(aq)的平衡逆向移动,NH Cl析出
4 4 4
16
原创精品资源学科网独家享有版权,侵权必究!
16
学科网(北京)股份有限公司【答案】D
【解析】在饱和NaCl溶液中先通入NH ,然后通入CO 气体,发生反应:
3 2
NaCl+H O+NH +CO =NaHCO↓+NHCl,过滤分离得到的固体1是NaHCO ,将固体1在煅烧炉中加热,发
2 3 2 3 4 3
生分解反应:2NaHCO NaCO+CO ↑+H O,得到纯碱和气体1是CO 气体;溶液1中含有NaCl、
3 2 3 2 2 2
NaHCO 、NH Cl;在冷却池中通入NH ,使溶液显碱性,同时增大了溶液中c(NH +),NH Cl(s) NH +
3 4 3 4 4 4
(aq)+Cl-(aq)逆向移动;析出NH Cl固体可作氮肥;溶液2含有NaCl、NaCO、(NH )CO、NH Cl。在盐
4 2 3 4 2 3 4
析池中加入NaCl,c(Cl-)增大,NH Cl(s) NH +(aq)+Cl-(aq)的平衡逆向移动,NH Cl析出,析出盐后
4 4 4
的溶液3循环回转到沉淀池中,再用于制取纯碱。A项,气体1为CO,气体2为NH ,A错误;B项,向
2 3
冷析池中通入NH ,增大溶液中c(NH +),便于析出盐NH Cl,此时溶液显碱性,因此溶液2中,含碳微粒
3 4 4
主要是CO2-,B错误;C项,侯氏制碱法中Na+用于制取纯碱NaCO,Cl-用于制取NH Cl,NH Cl可作氮
3 2 3 4 4
肥,也可用于金属加工除锈等,原子利用率较高;而索尔维法制取纯碱时,反应产生的CaCl 作为废液排
2
出,原子利用率大大降低,故侯氏制碱法中原料NaCl的原子利用率比索尔维制碱法中原料NaCl的原子利
用率高,C错误;D项,盐析池中加入NaCl固体,增大了溶液中c(Cl-)增大,使盐NH Cl的溶解结晶平衡
4
NH Cl(s) NH +(aq)+Cl-(aq)逆向移动,从而使NH Cl结晶析出,D正确;故选D。
4 4 4
13.(2022·江苏省南京、镇江市部分名校学情调研考试)由绿矾(FeSO ·7H O)制备三草酸合铁酸钾晶体
4 2
{ K[Fe(C O) ]·3H O}的流程如图
3 2 4 3 2
下列说法正确的是( )
A.“溶解”时加硫酸的目的是抑制 水解
B.将“沉淀”所得的FeC O 加入酸性高锰酸钾溶液,观察到溶液褪色,说明产物中含C O2-
2 4 2 4
C.“氧化”过程中HO 被还原为O
2 2 2
D.隔绝空气加热K[Fe(C O) ]·3H O,分解产物为KCO、Fe O、CO、HO
3 2 4 3 2 2 3 2 3 2 2
【答案】A
【解析】由题给流程可知,绿矾溶于稀硫酸得到酸性硫酸亚铁溶液,向溶液中加入草酸溶液得到草酸
亚铁沉淀,向沉淀中加入草酸钾、草酸和过氧化氢混合溶液将草酸亚铁氧化得到三草酸合铁酸钾晶体。A
17
原创精品资源学科网独家享有版权,侵权必究!
17
学科网(北京)股份有限公司项,亚铁离子在溶液中易发生水解,溶解时加入稀硫酸的目的是抑制亚铁离子的水解,故A正确;B项,
向草酸亚铁沉淀中加入酸性高锰酸钾溶液时,亚铁离子和草酸根离子都能与酸性高锰酸钾溶液反应,使溶
液褪色,则观察到溶液褪色不能说明产物中含草酸根离子,故B错误;C项,氧化过程中过氧化氢为反应
的氧化剂,被草酸亚铁还原为水,故C错误;D项,由氧化还原反应规律可知,隔绝空气加热三草酸合铁
酸钾晶体时,三草酸合铁酸钾晶体受热分解生成碳酸钾、氧化铁、一氧化碳和水,故D错误;故选A。
14.(2022·广东省广州市广大附中、广外、铁一中学高三三模联考)《开宝本草》记载“取钢煅作叶如
笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣”。铁华粉[主要
成分为(CHCOO) Fe ·H O ]可用如下方法检测。下列相关说法不正确的是( )
3 2 2
A.在铁华粉中加入稀硝酸,再滴加KSCN溶液,一定会变红
B.制备铁华粉的主要反应为Fe+2CH COOH=(CH COO) Fe+H ↑
3 3 2 2
C.气体X的产生是因为发生了复分解反应
D.由上述实验可知,OH-结合Fe3+的能力大于CN-
【答案】A
【解析】铁华粉中加入稀硫酸并加热,产生的刺激性气味的气体X为醋酸蒸气;铁华粉中加入稀盐酸
生成氢气和滤液有氢气生成说明铁华粉中含有铁单质,滤液中加入铁氰化钾溶液生成蓝色沉淀,说明有滤
液中有亚铁离子,该沉淀不溶于稀盐酸,但与NaOH可反应生成棕色沉淀。A项,根据分析可知铁华粉中
含有铁单质,硝酸的量比较少时,生成的Fe3+能与Fe反应生成Fe2+,当溶液中不存在Fe3+时,滴入KSCN
溶液不会变红,A错误;B项,根据题干中信息可知,制备铁华粉的主要反应为
Fe+2CH COOH=(CH COO) Fe+H ↑,B正确;C项,气体X为醋酸蒸气,反应为:
3 3 2 2
(CHCOO) Fe+H SO =2CH COOH+FeSO ,属于复分解反应,C正确;D项,由上述实验可知,氢氧根离子
3 2 2 4 3 4
能与蓝色沉淀反应,生成棕色沉淀,说明有氢氧化铁沉淀生成,说明氢氧根离子结合铁离子的能力强于
CN-,D正确;故选A。
15.(2022·山东省济宁市三模)以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是(
18
原创精品资源学科网独家享有版权,侵权必究!
18
学科网(北京)股份有限公司)
A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B.人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C.过滤步骤说明硫酸亚铁晶体难溶于水
D.实验过程不直接蒸发结晶的原因是防止FeSO 水解生成Fe(OH)
4 2
【答案】B
【解析】废铁屑用稀硫酸酸浸后得到FeSO 溶液,FeSO 溶液经结晶、过滤得到硫酸亚铁晶体。A项,
4 4
取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明酸浸后的溶液中不存在Fe3+,但不能说明废铁
屑中不含+3价铁元素,因为废铁屑中若含+3价铁元素,在酸浸时会被Fe还原成Fe2+,A项错误;B项,
人体血红素是亚铁离子配合物,硫酸亚铁可提供亚铁离子,从而可用于治疗缺铁性贫血,B项正确;C项,
硫酸亚铁晶体溶于水,题给实验过程中是经结晶析出晶体后过滤的,C项错误;D项,实验过程不直接蒸
发结晶的原因是:防止硫酸亚铁被氧化、防止硫酸亚铁晶体失去结晶水,D项错误;故选B。
16.(2022·湖南省永州市第一中学二模)MnCO 可用作脱硫的催化剂以及生产金属锰的原料,由含
3
Mn2+的废液(有少量的Fe2+、Fe3+)制备MnCO 的一种工艺流程如下:
3
下列说法错误的是( )
A.“沉锰”时加过量NH HCO 发生反应的离子方程式为Mn2++ HCO -=MnCO↓+H+
4 3 3 3
B.“氧化”时加入酸化的HO 的目的是将Fe2+氧化为Fe3+
2 2
C.“纯化”过程中发生了水解反应,生成Fe(OH) 沉淀
3
D.工艺流程中“一系列操作”为过滤、洗涤、干燥
【答案】A
【解析】废液中含有少量的Fe2+、Fe3+,应除去,先加酸化的双氧水把亚铁离子氧化为三价铁离子2
Fe2++2H++H O=2H O+2 Fe3+,再调节溶液的酸碱性使铁离子水解为沉淀而除去三价铁离子,再加入过量的
2 2 2
19
原创精品资源学科网独家享有版权,侵权必究!
19
学科网(北京)股份有限公司NH HCO 发生反应的离子方程式为Mn2++2HCO-=MnCO↓+H O+CO↑,再经过过滤、洗涤、干燥等一系列
4 3 3 3 2 2
操作得到固体MnCO 。A项, “沉锰”时加过量NH HCO 发生反应的离子方程式为Mn2++2 HCO -
3 4 3 3
=MnCO↓+H O+CO↑,故A错误;B项, “氧化”时加入酸化的HO 的目的是将Fe2+氧化为Fe3+,故B
3 2 2 2 2
正确;C项,Fe3+在酸性条件下会发生水解反应,生成Fe(OH) 沉淀,故C正确;D项,“沉锰”时得到的
3
沉淀经过滤、洗涤、干燥等一系列操作得到固体MnCO ,故D正确;故选A。
3
17.(2022·江苏省连云港市高三高考考前模拟考试)某新型纳米材料氧缺位铁酸盐ZnFe O(3