文档内容
专题 05 元素及其化合物
1.(2022·浙江卷)下列消毒剂的有效成分属于盐的是
A.高锰酸钾溶液 B.过氧乙酸溶液 C.双氧水 D.医用酒精
【答案】A
【解析】A.高锰酸钾溶液的有效成分为KMnO ,其在水溶液中电离出K+和 ,故KMnO 属于盐,A
4 4
符合题意;
B.过氧乙酸溶液的有效成分是CHCOOOH,在水溶液中电离出CHCOOO-和H+,即水溶液中的阳离子全
3 3
部为H+,故其属于酸,不合题意;
C.双氧水是由H和O组成的化合物,故其属于氧化物,C不合题意;
D.医用酒精的有效成分为CHCHOH,其属于有机物,不属于盐,D不合题意;
3 2
故答案为:A。
2.(2022·浙江卷)下列说法不正确的是
A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C.氧化铝熔点高,常用于制造耐高温材料
D.用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
【答案】A
【解析】A.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,可用于制造晶体管、集成电
路等,而二氧化硅常用于制造光导纤维,A错误;
B.钠的焰色反应为黄色,可用作透雾能力强的高压钠灯,B正确;
C.耐高温材料应具有高熔点的性质,氧化铝熔点高,可用作耐高温材料,C正确;
D.石灰石的主要成分为碳酸钙,石灰石-石膏法脱硫过程中发生反应:CaCO CaO+CO ↑,
3 2
SO +CaCO =CaSO +CO ,2CaSO+O =2CaSO ,得到了石膏,D正确;
2 3 3 2 3 2 4
答案选A。
3.(2022·浙江卷)下列说法正确的是
A.工业上通过电解六水合氯化镁制取金属镁
B.接触法制硫酸时,煅烧黄铁矿以得到三氧化硫C.浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
【答案】D
【解析】A.六水合氯化镁没有自由移动的离子,不能导电,工业上通过电解熔融的无水氯化镁制取金属
镁,A不正确;
B.接触法制硫酸时,煅烧黄铁矿只能得到二氧化硫,二氧化硫在接触室经催化氧化才能转化为三氧化硫,
B不正确;
C.在常温下铁与浓硝酸发生钝化反应,在铁表面生成一层致密的氧化物薄膜并阻止反应继续发生,所以
可用铁质容器贮运浓硝酸,C不正确;
D.“洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用,若两者混用会发生归中
反应生成氯气,不仅达不到各自预期的作用效果,还会污染环境,D正确;
综上所述,本题选D。
4.(2022·浙江卷)关于化合物 的性质,下列推测不合理的是
A.与稀盐酸反应生成 、 、
B.隔绝空气加热分解生成FeO、 、
C.溶于氢碘酸(HI),再加 萃取,有机层呈紫红色
D.在空气中,与 高温反应能生成
【答案】B
【解析】已知化合物 中Fe的化合价为+3价,CHO-带一个单位负电荷,据此分析解题。
3
A.由分析可知,化合物 中Fe的化合价为+3价,故其与稀盐酸反应生成 、 、
,反应原理为:FeO(OCH)+3HCl=FeCl +H O+CHOH,A不合题意;
3 3 2 3
B.由分析可知,化合物 中Fe的化合价为+3价,C为-1,若隔绝空气加热分解生成FeO、
、 则得失电子总数不相等,不符合氧化还原反应规律,即不可能生成FeO、 、 ,B符合题意;C.由分析可知,化合物 中Fe的化合价为+3价,故其溶于氢碘酸(HI)生成的Fe3+能将I-氧化为
I,反应原理为:2FeO(OCH)+6HI=2FeI +I +2H O+2CHOH,再加 萃取,有机层呈紫红色,C不合题
2 3 2 2 2 3
意;
D.化合物 在空气中高温将生成Fe O、CO 和HO,然后Fe O 为碱性氧化物,SiO 为酸性氧
2 3 2 2 2 3 2
化物,故化合物 与 高温反应能生成 ,D不合题意;
故答案为:B。
5.(2022·广东卷)劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项 劳动项目 化学知识
A 面包师用小苏打作发泡剂烘焙面包 Na 2 CO 3可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
C 工人将模具干燥后再注入熔融钢水 铁与 H 2 O 高温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
【答案】A
【解析】A.小苏打是碳酸氢钠,不是碳酸钠,主要用来做膨松剂,故A符合题意;
B.熟石灰是氢氧化钙,具有碱性,可以用于处理酸性废水,故B不符合题意;
C.熔融的铁与水蒸气在高温下反应会生成四氧化三铁和氢气,因此必须将模具干燥,故C不符合题意;
D.钢板上镀铝,保护钢板,金属铝表面形成致密氧化膜而保护金属铝不被腐蚀,,故D不符合题意。
综上所述,答案为A。
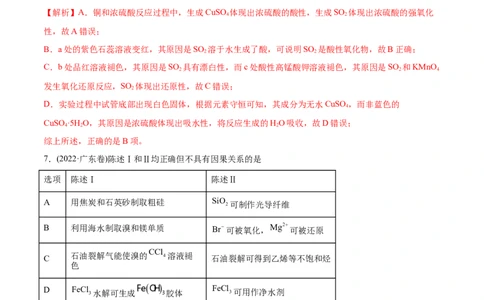
6.(2022·广东卷)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列
分析正确的是A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
【答案】B
【解析】A.铜和浓硫酸反应过程中,生成CuSO 体现出浓硫酸的酸性,生成SO 体现出浓硫酸的强氧化
4 2
性,故A错误;
B.a处的紫色石蕊溶液变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧化物,故B正确;
2 2
C.b处品红溶液褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾溶液褪色,其原因是SO 和KMnO
2 2 4
发生氧化还原反应,SO 体现出还原性,故C错误;
2
D.实验过程中试管底部出现白色固体,根据元素守恒可知,其成分为无水CuSO ,而非蓝色的
4
CuSO ·5H O,其原因是浓硫酸体现出吸水性,将反应生成的HO吸收,故D错误;
4 2 2
综上所述,正确的是B项。
7.(2022·广东卷)陈述Ⅰ和Ⅱ均正确但不具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用焦炭和石英砂制取粗硅 SiO 2可制作光导纤维
B 利用海水制取溴和镁单质 Br可被氧化, Mg2 可被还原
CCl
C
石油裂解气能使溴的 4溶液褪
石油裂解可得到乙烯等不饱和烃
色
D FeCl 3水解可生成 FeOH 3胶体 FeCl 3可用作净水剂
【答案】A
【解析】A.焦炭具有还原性,工业上常利用焦炭与石英砂(SiO)在高温条件下制备粗硅,这与SiO 是否做
2 2
光导纤维无因果关系,故A符合题意;
B.海水中存在溴离子,可向其中通入氯气等氧化剂将其氧化为溴单质,再经过萃取蒸馏物理操作分离提
纯溴单质,另外,通过富集海水中的镁离子,经过沉淀、溶解等操作得到无水氯化镁,随后电解熔融氯化
镁可制备得到镁单质,陈述I和陈述II均正确,且具有因果关系,B不符合题意;
C.石油在催化剂加热条件下进行裂解可得到乙烯等不饱和烃,从而使溴的CCl 溶液褪色,陈述I和陈述
4II均正确,且具有因果关系,C不符合题意;
D.FeCl 溶液中铁离子可发生水解,生成具有吸附性的氢氧化铁胶体,从而可用作净水机,陈述I和陈述
3
II均正确,且具有因果关系,D不符合题意;
综上所述,答案为A。
1.(2022·四川·泸县五中三模)化学与生活密切相关。下列叙述错误的是
A.不锈钢是一种主要含Fe、Cr、Ni且不易生锈的合金钢
B.陶瓷属于无机非金属材料,陶瓷中不含金属元素
C.煤层气中含有甲烷,可用作清洁燃料和化工原料
D.适量SO 可用于对食物杀菌防腐、抗氧化
2
【答案】B
【解析】A.不锈钢属于合金钢,是一种Fe、Cr、Ni形成的铁合金,故A正确;
B.陶瓷属于无机非金属材料,其主要成分为硅酸盐,一般含有金属元素,故B错误;
C.煤层气中含有甲烷,甲烷是一种清洁燃料,也是一种重要的化工原料,故C正确;
D.SO 具有漂白性、还原性,在红酒中加少量二氧化硫可用于防腐、保鲜,抗氧化,故D正确;
2
故选B。
2.(2022·宁夏·固原一中一模)下列说法正确的是
A.镀锌铁破损后,铁易被腐蚀
B.红酒中添加适量SO 可以起到杀菌和抗氧化的作用
2
C.牙膏中添加氟化物可用于预防龋齿,原因是氟化物具有氧化性
D.自来水厂常用明矾、O、ClO 等作水处理剂,其作用都是杀菌消毒
3 2
【答案】B
【解析】A.锌比铁活泼,破损后形成原电池,锌会作为负极保护铁,A错误;
B.SO 具有抑制某些细菌生长的能力,还有较强的还原性,适量的SO 可以起到杀菌和抗氧化的作用,B
2 2
正确;
C.牙齿表面含有Ca
5
(PO
4
)
3
OH,牙膏中添加氟化物时发生的反应为Ca
5
(PO
4
)
3
OH(s)+F-(aq)⇌Ca
5
(PO
4
)
3
F+OH-
(aq),最终在牙齿表面形成难溶性的Ca (PO )F,达到防止龋齿的目的,过程中没有发生氧化还原反应,与
5 4 3
氟化物具有氧化性无关,C错误;
D.明矾水解产生氢氧化铝胶体,可以净水,但没有杀菌消毒作用,D错误;
综上所述答案为B。3.(2022·安徽·淮北市教育科学研究所一模)下列物质的性质与应用有对应关系的是
A.氨气沸点低,工业上常用液氨作制冷剂
B.HNO 有强氧化性,可用于溶解银
3
C.NaHCO 溶液显碱性,常作烘焙糕点的膨松剂
3
D.ClO 具有还原性,可用于自来水的杀菌消毒
2
【答案】B
【解析】A.氨气易液化,液氨汽化会吸收大量的热,导致周围环境的温度降低,所以氨气可用作制冷剂,
与氨气的沸点低无关,故A不符合题意;
B.HNO 具有强氧化性,可与Pt、Au除外的大多数金属发生氧化还原反应,可溶解银、铜等不活泼金属,
3
故B符合题意;
C.NaHCO 用作糕点的膨松剂,是利用碳酸氢钠不稳定,受热分解生成大量的二氧化碳,故C不符合题意;
3
D.ClO 具有强氧化性,能使蛋白质变性而失去生理活性,可用于自来水的杀菌消毒,故D不符合题意;
2
故选:B。
4.(2022·浙江·三模)下列说法不正确的是
A.工业盐酸和硝酸均呈黄色的原因相同
B.CHCH=CH+Cl→CHClCH=CH +HCl,该反应为取代反应
3 2 2 2 2
C.古法可用CaSO、FeSO 、CuSO 的加热分解制硫酸
4 4 4
D.NH 与O 的混合气体经过灼热的催化剂层后的物质中含有NO
3 2 2
【答案】A
【解析】A.工业盐酸显黄色是因为制取盐酸要用到氯气,而氯气在通过铁的管道时,会把铁氧化,从而
使制得的盐酸里面混有三价铁,而显黄色;浓硝酸显黄色,是因为硝酸见光分解生成NO ,NO 溶于浓硝
2 2
酸中显黄色,A不正确;
B.CHCH=CH+Cl→CHClCH=CH +HCl,该反应Cl原子取代丙烯中甲基上的氢原子,同时生成HCl,为
3 2 2 2 2
取代反应,B正确;
C.CaSO、FeSO 、CuSO 等硫酸盐受热分解产生硫氧化物,古法可用该方法制硫酸,C正确;
4 4 4
D.NH 与O 的混合气体经过灼热的催化剂层后生成NO,NO遇O 生成NO ,D正确;
3 2 2 2
故选A。
5.(2022·湖北·应城市第一高级中学模拟预测)我国古代劳动人民用“失蜡法”铸造青铜器:用蜂蜡作成铸
件模型,再用黏土敷成外范,烧成陶模,烧制过程蜡模全部融化流失,使整个铸件模型变成空壳,再往内
浇灌青铜熔液,便铸成器物。下列说法不正确的是
A.青铜是我国最早使用的合金材料,主要成分为铜和锡B.蜂蜡的主要成分为有机物,其中的酯类物质难溶于水
C.黏土(AlO·2SiO·2H O)是由氧化物构成的混合物
2 3 2 2
D.陶制器皿属于传统硅酸盐材料,耐高温、耐腐蚀
【答案】C
【解析】A.青铜是我国最早使用的合金材料,是铜、锡的合金,故A正确;
B.蜂蜡的主要成分为酯类有机物,酯类物质难溶于水,故B正确;
C.黏土主要是由硅酸盐构成的混合物,故C错误;
D.陶制器皿属于传统硅酸盐材料,耐高温、耐腐蚀,故D正确;
选C。
6.(2022·安徽·模拟预测)制备下列气体所需的反应物和发生装置均可行的是
选项 A B C D
气体 一氧化氮 氯气 硫化氢 氨气
浓盐酸、高锰酸钾溶
反应物 铜丝、稀硝酸 硫化钠固体、浓硫酸 铵盐、熟石灰
液
发生装
置
【答案】A
【解析】A.Cu与稀硝酸反应生成NO,抽动铜丝可使反应停止,图中装置可制备NO,A正确;
B.高锰酸钾溶液与浓盐酸直接反应制备氯气,不需要加热,所以不需要酒精灯,B错误;
C.硫化钠固体与浓硫酸发生氧化还原反应不生成硫化氢,应选稀硫酸,C错误;
D.铵盐固体、熟石灰为固固加热制备氨气,不能用固液反应产生气体的装置,D错误;
故选A。
7.(2022·湖北·襄阳四中模拟预测)下列有关Fe、Co、Ni及其化合物的说法错误的是
A.Fe、 Co、Ni 均位于第四周期第VIII族
B.Fe、 Co、Ni 基态原子未成对电子数分别为4、3、2
C.Fe、 Co、Ni以及它们的合金为黑色金属材料
D.FeO 在空气中受热会迅速变为Fe O
3 4
【答案】C
【解析】A.Fe、Co、Ni位于元素周期表中第四周期第VIII族,A选项正确;B.Fe是26号元素,基态铁原子的价电子排布式为3d64s2。Co、Ni的基态原子的价电子排布式分别为
3d74s2、3d84s2,三种元素原子的核外未成对电子数分别为4、3、2,B选项正确;
C.黑色金属材料通常是指铁和以铁为基础元素的合金,C选项错误;
D.Fe2+具有较强还原性,在空气中加热易被部分氧化为+3价生成稳定的Fe O,D选项正确;
3 4
答案选C。
8.(2022·内蒙古包头·二模)在含有大量漂粉精的溶液中,下列有关叙述正确的是
A.加入K+、 、 、I-等离子,可以大量共存。
B.可用pH试纸测定该溶液的pH
C.向该溶液中滴加少量 溶液,反应的离子方程式为:
D.该溶液中滴入一定量的浓盐酸,每产生 ,转移电子数约为 个
【答案】D
【解析】A.漂粉精又名高效漂白粉,主要成分是Ca(ClO) ,ClO-与I-发生氧化还原反应,不能共存,故A
2
错误;
B. Ca(ClO) 溶液具有漂白性,能将pH试纸漂白,不能用pH试纸测定该溶液的pH,故B错误;
2
C.滴入少量FeSO 溶液,溶液仍显碱性,次氯酸根能够氧化亚铁离子,反应生成氢氧化铁沉淀,正确的
4
离子方程式为:2Fe2++5ClO-+5H O=Cl-+2Fe(OH) ↓+4HClO,故C错误;
2 3
D.ClO-与Cl-发生反应的离子方程式为:ClO-+Cl-+2H+=Cl+H O,反应中产生1mol Cl 转移电子1mol,即
2 2 2
转移电子数约为6.02×1023个,故D正确;
故选:D。
9.(2022·新疆喀什·一模)物质的化学性质在日常生活和生产中有着广泛的运用。下列有关说法正确的是
A.O 是一种氧化性极强的气体,可用作餐具的消毒剂
3
B.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸
C.SiO 用于制作光导纤维是因为它能导电
2
D.FeCl 可以作止血剂是因为Fe3+具有强氧化性
3
【答案】A
【解析】A.O 在常温下,是一种有特殊臭味的淡蓝色气体,具有极强氧化性,可用作自来水的消毒剂,
3
故A正确;
B.铝与浓硝酸常温下发生钝化,在表面形成一层致密的氧化物保护膜,阻止反应继续进行,可用铝制容
器存放浓硝酸,故B错误;C.SiO 具有能够使光线进行全反射的性质,因此可用于制作光导纤维,故C错误;
2
D.血液属于胶体,加入电解质溶液(FeCl 溶液)可以使胶体聚沉,血液凝聚达到止血效果,故D错误;
3
答案选A。
10.(2022·陕西·西安中学模拟预测)如图a、b、c表示相应仪器中加入加入试剂,可用图中装置制取、净化、
收集气体的是
编号 气体 a b c
A NH 浓氨水 固体氢氧化钠 浓硫酸
3
B CO 盐酸 碳酸钙 饱和NaHCO 溶液
2 3
C Cl 浓盐酸 二氧化锰 饱和NaCl溶液
2
D NO 浓硝酸 铜屑 NaOH溶液
2
【答案】B
【解析】A.浓氨水受热易分解,NaOH固体与溶于浓氨水促进氨水的分解产生氨气,氨气为碱性气体不
能用酸性干燥剂,A项错误;
B.碳酸钙和稀盐酸反应为实验室制备二氧化碳气体,由于盐酸具有挥发性,制备出来的气体中混有少量
的氯化氢气体,可用饱和NaHCO 溶液除去,B项正确;
3
C.浓盐酸和二氧化锰在加热条件下为实验室制备Cl,常温下浓盐酸与二氧化锰不反应,C项错误;
2
D.浓硝酸和铜可产生NO 气体,随着反应进行浓硝酸逐渐变成稀硝酸,则生成的气体为NO,且NaOH溶
2
液可与NO 发生化学反应,D项错误;
2
答案选B。
11.(2022·重庆市育才中学模拟预测)下列实验现象描述正确的是
CaCl CO
A.向 2溶液中通入 2,生成白色沉淀
FeSO NaOH
B.向 4溶液中滴加 溶液,立即产生红褐色沉淀
H SO
2 3
C.向 溶液中加入少量品红溶液,振荡后溶液变为红色KMnO H O
D.向酸性 4溶液中加入过量 2 2溶液,溶液紫红色褪去
【答案】D
CaCl CO
【解析】A.向 2溶液中通入 2,不会发生反应,无明显现象,A错误;
FeSO NaOH
B.向 4溶液中滴加 溶液,先生成白色沉淀,后沉淀迅速变成灰绿色,最终变成红褐色,B错
误;
H SO
2 3
C.向 溶液中加入少量品红溶液,二氧化硫和水生成亚硫酸的反应为可逆反应,振荡后二氧化硫与品
红溶液反应使溶液变为无色,C错误;
KMnO H O
D.向酸性 4溶液中加入过量 2 2溶液,过氧化氢作为还原剂,高锰酸钾被还原成锰离子,溶液紫
红色褪去,D正确;
故选D。
12.(2022·山东淄博·三模)在“价一类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关
系。图中的字母分别代表硫及其常见化合物,相关推断不合理的是
A.b、d、f既具有氧化性又具有还原性
B.硫酸型酸雨的形成过程涉及b到c的转化
C.d与c在一定条件下反应可生成b或a
D.d在加热条件下与强碱溶液反应生成e和f,且
【答案】C
【解析】A.根据图中信息,b为 ,d为S,f为亚硫酸盐,其中S元素价态都处于中间价态,既有氧
化性,又有还原性,A正确;
B.酸雨形成涉及到 被氧气氧化转化为 ,B正确;C.d为S,c为 ,硫与浓硫酸加热反应,根据价态变化规律,只能生成b ,不能生成氢硫酸,
C错误;
D.d在加热条件下与强碱溶液反应生成氢硫酸盐和亚硫酸盐,两者之比2∶1,D正确;
故选:C。
13.(2022·上海市南洋模范中学模拟预测)如图:某同学用高锰酸钾和浓盐酸制备氯气,验证氯气性质实验
装置。相关说法错误的是
A.脱脂棉中的无水氯化钙可以用碱石灰代替
B.该实验装置可证明干燥的氯气没有漂白作用
C.湿润石蕊试纸先变红,但也不能说明生成了酸性物质
D.淀粉碘化钾试纸先变蓝后褪色,说明氯气将I 氧化
2
【答案】A
【解析】A.无水氯化钙主要是干燥氯气,碱石灰会与氯气反应,因此脱脂棉中的无水氯化钙不能用碱石
灰代替,故A错误;
B.从左边出来的干燥氯气,先与干燥品红接触,品红不褪色,说明干燥的氯气没有漂白作用,故B正确;
C.由于HCl易挥发,因此挥发的HC l使湿润石蕊试纸先变红,因此不能说明生成了酸性物质,故C正确;
D.淀粉碘化钾试纸先变蓝后褪色,先变蓝,是碘离子被氯气氧化为单质碘,单质碘遇淀粉变蓝,后褪色,
说明氯气将I 氧化,故D正确。
2
综上所述,答案为A。
14.(2022·河南开封·三模)物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其
部分化合物的价态-类别图。下列说法正确的是A.常温下,a和f的浓溶液反应可生成b和c
B.附着有b的试管,常用酒精清洗
C.分别往d、e的溶液中滴加少量氯化钡溶液,均可产生白色沉淀
D.常温下等物质的量浓度的g、h两种钠盐溶液的pH:g<h
【答案】A
【解析】a为HS、b为S、c为SO 、d为SO 、e为亚硫酸、f为硫酸、g为亚硫酸盐、h为硫酸盐,据此分
2 2 3
析解题。
A.硫化氢和浓硫酸能发生氧化还原反应,方程式为 HS+HSO (浓)=S↓+SO ↑+2H O,A正确;
2 2 4 2 2
B.硫微溶于酒精,易溶于二硫化碳,故附着有b的试管,常用二硫化碳洗涤,B错误;
C.亚硫酸的酸性弱于盐酸,故亚硫酸与氯化钡不反应,C错误;
D.硫酸钠为强酸强碱盐,溶液呈中性,亚硫酸钠为强碱弱酸盐,亚硫酸根离子水解使溶液呈碱性,故等
浓度时的亚硫酸钠溶液的pH大于硫酸钠溶液的pH,D错误;
答案选A。
15.(2022·河南河南·三模)下列实验的现象与结论均正确的是
选项 操作 现象 结论
将铜片加入盛有稀硝酸的试 试管口有红棕 Cu把稀HNO 中氮元素还
A 3
管中 色气体产生 原为了NO
2
B 灼热的铁丝插入氯气瓶中 铁丝剧烈燃烧 Fe与Cl 反应生成FeCl
2 3
C 将洁净铁丝放入浓硫酸中 无明显现象 没有发生化学反应
用HCl气体做喷泉实验 可以形成喷泉
只有极易溶于水的气体才
D
能用来做喷泉实验
【答案】B
【解析】A.将铜片加入盛有稀硝酸的试管中,Cu把稀HNO 中氮元素还原为了NO,NO在瓶口与O 反
3 2
应生成红棕色的气体NO ,A不合题意;
2点燃
B.灼热的铁丝插入氯气瓶中,铁丝能剧烈燃烧,Fe与Cl 反应生成FeCl ,方程式为:2Fe+3Cl
2 3 2
2FeCl ,B符合题意;
3
C.将洁净铁丝放入浓硫酸中,无明显现象是由于常温下铁遇到浓硫酸发生钝化,钝化属于化学变化,C
不合题意;
D.HCl极易溶于水,用HCl气体做喷泉实验,可以形成喷泉,但并不是只有极易溶于水的气体才能用来
做喷泉实验,如NaOH和CO、NO 和HO由于反应使得气体的压强快速下降也能形成喷泉,D不合题意;
2 2 2
故答案为:B。
16.(2022·河南郑州·一模)部分含铁物质的分类与相应化合价关系如图所示。下列推断错误的是
A.可以通过化合反应制备b
B.将NaOH溶液缓慢滴入e溶液中可制得d的胶体
C.可实现a→b→c→d→e→b→a的循环转化
D.实验室检验Fe3+,可以用NaOH溶液,也可以用KSCN溶液
【答案】B
【解析】根据图示,a是Fe、b可能是FeCl 、c是Fe(OH) 、d是Fe(OH) 、e可能是FeCl 。
2 2 3 3
A.FeCl 和Fe发生化合反应生成FeCl ,故A正确;
3 2
B.将NaOH溶液缓慢滴入FeCl 溶液中生成红褐色Fe(OH) 沉淀,故B错误;
3 3
C.Fe和盐酸反应生成FeCl ,FeCl 和NaOH溶液反应生成Fe(OH) ,Fe(OH) 和氧气反应生成Fe(OH) ,
2 2 2 2 3
Fe(OH) 和盐酸反应生成FeCl ,FeCl 和铁反应生成FeCl ,FeCl 和锌反应生成铁,故C正确;
3 3 3 2 2
D.Fe3+和NaOH溶液反应生成红褐色Fe(OH) 沉淀,Fe3+和KSCN反应溶液变为血红色,故D正确;
3
选B。
17.(2022·江西上饶·模拟预测)H S、SO 、SO 、HSO 、NaSO 、NaHSO、NaHSO 等是硫元素重要的化
2 2 3 2 4 2 3 3 4
合物,下列有关说法正确的是
A.标准状况下,1molH S、1molSO 、1molSO 所占体积都约为22.4L
2 2 3
B.硫在氧气中燃烧时,氧气少量时生成SO ,氧气过量时生成SO
2 3
C.SO 是一种无色有刺激性气味有毒的气体,故不可用作葡萄酒的食品添加剂
2D.向NaHSO 溶液中分别滴加稀HSO 和NaHSO 溶液,发生的离子反应方程式相同
3 2 4 4
【答案】D
【解析】A.标准状况下SO 是固体,1molSO 所占体积不是22.4L,故A错误;
3 3
B.硫在氧气中燃烧时,无论氧气是否过量,产物只有SO ,故B错误;
2
C.二氧化硫具有还原性,SO 可用作葡萄酒的食品添加剂,故C错误;
2
D.向NaHSO 溶液中分别滴加稀HSO 和NaHSO 溶液,发生的离子反应方程式都是
3 2 4 4
,故D正确;
选D。
18.(2022·山西临汾·三模)下列生产活动与相应化学原理不相符的是
选项 生产活动 化学原理
A 过氧化钠用于呼吸面具的制造 过氧化钠与人呼出的HO、CO 都能发生反应生成O
2 2 2
B 葡萄酒生产时用SO 做食品添加剂 二氧化硫具有还原性,且有防腐作用
2
C
用氧化铁和铝粉组成的混合物焊接 氧化铁和铝粉剧烈反应放出大量的热,使产物单质铁呈熔融
钢轨 状态
D 用乙二醇合成涤纶 乙二醇与水分子间可形成氢键,可互溶
【答案】D
【解析】A.NaO 与人呼出的HO、CO 都能反应生成O,O 又可以供给人呼吸,A运用了相应化学原理,
2 2 2 2 2 2
A不合题意;
B.SO 具有还原性可做抗氧化剂,防止葡萄酒中还原性物质被氧化,且能杀灭生产过程中产生的杂菌,做
2
防腐剂,B运用了相应化学原理,B不合题意;
C.氧化铁和铝粉发生铝热反应生成单质铁,反应放出大量热使产物单质铁呈熔融状态,铁水流到钢轨槽
中将两段钢轨焊接在一起,C运用了相应化学原理,C不合题意;
D.乙二醇合成涤纶是利用乙二醇中两个羟基,可发生缩聚反应得到高分子化合物,与乙二醇和水分子间
存在氢键可互溶无关,D没有运用相应化学原理,D符合题意;
故选D。
19.(2022·陕西·西安工业大学附中模拟预测)如图是铜及部分含铜粒子的价荷图。下列推断合理的是A.Cu变成a可以加入稀盐酸
B. 转化成Cu(OH) 需要加碱
2
C.在酸性环境中,Cu O可以反应生成a和CuO
2
D.如果将高铜酸根离子( )填入坐标,应该填在b的位置
【答案】D
【解析】A.a中Cu元素为+2价,在酸性条件下,Cu变为a需要失去电子,发生氧化反应,故需要加入强
氧化剂,盐酸不能与铜反应,选项A错误;
B.由图可知, Cu(OH) 转化为 需要碱性条件,而 转化成Cu(OH) 需要酸性条件,选
2 2
项B错误;
C.Cu O中Cu元素为+1价,在酸性条件下可以发生歧化反应生成+ 2价铜和单质铜,选项C错误;
2
D.( )中铜元素为+3价,离子带1个单位负电荷,故填入坐标,应该填在b的位置,选项D正确;
答案选D。