文档内容
专题 14 元素及其化合物知识的综合应用
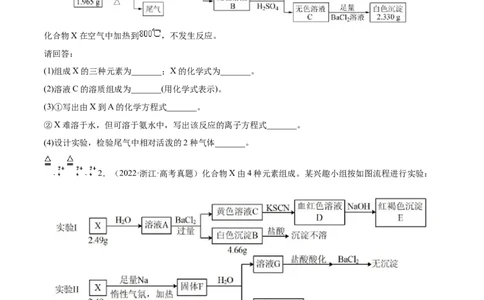
1.(2022·浙江·高考真题)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
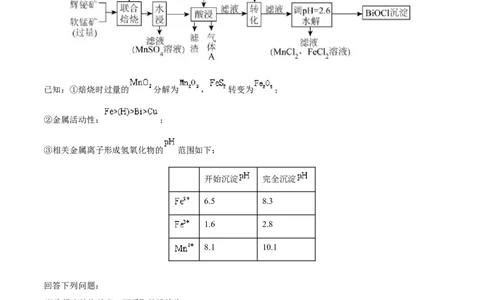
2.(2022·浙江·高考真题)化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
(1)组成X的元素有______,X的化学式为______。
(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合由弱
到强的排序______。(3)X与足量Na反应生成固体F的化学方程式是______。
(4)设计实验确定溶液G中阴离子______。
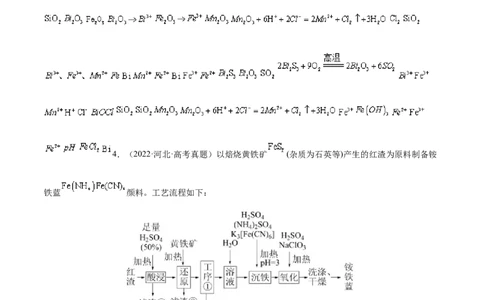
3.(2022·辽宁·高考真题)某工厂采用辉铋矿(主要成分为 ,含有 、 杂
质)与软锰矿(主要成分为 )联合焙烧法制备 和 ,工艺流程如下:
已知:①焙烧时过量的 分解为 , 转变为 ;
②金属活动性: ;
③相关金属离子形成氢氧化物的 范围如下:
开始沉淀 完全沉淀
6.5 8.3
1.6 2.8
8.1 10.1
回答下列问题:
(1)为提高焙烧效率,可采取的措施为___________。
a.进一步粉碎矿石
b.鼓入适当过量的空气
c.降低焙烧温度
(2) 在空气中单独焙烧生成 ,反应的化学方程式为___________。
(3)“酸浸”中过量浓盐酸的作用为:①充分浸出 和 ;②___________。(4)滤渣的主要成分为___________(填化学式)。
(5)生成气体A的离子方程式为___________。
(6)加入金属 的目的是___________。
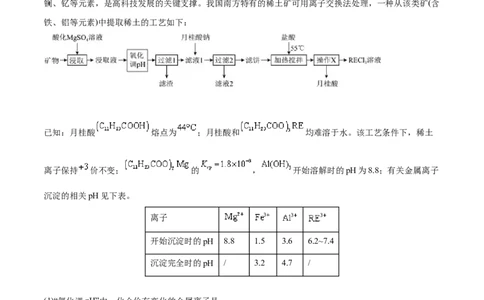
4.(2022·河北·高考真题)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵
铁蓝 颜料。工艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
(4)工序①的名称为_______,所得母液循环使用。(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不
引入杂质)。
5.(2022·广东·高考真题)稀土( )包括
镧、钇等元素,是高科技发展的关键支撑。我国南方特有的稀土矿可用离子交换法处理,一种从该类矿(含
铁、铝等元素)中提取稀土的工艺如下:
已知:月桂酸 熔点为 ;月桂酸和 均难溶于水。该工艺条件下,稀土
离子保持 价不变; 的 , 开始溶解时的pH为8.8;有关金属离子
沉淀的相关pH见下表。
离子
开始沉淀时的pH 8.8 1.5 3.6 6.2~7.4
沉淀完全时的pH / 3.2 4.7 /
(1)“氧化调pH”中,化合价有变化的金属离子是_______。
(2)“过滤1”前,用 溶液调pH至_______的范围内,该过程中 发生反应的离子方程式为_______。
(3)“过滤2”后,滤饼中检测不到 元素,滤液2中 浓度为 。为尽可能多地提取 ,可提
高月桂酸钠的加入量,但应确保“过滤2”前的溶液中 低于_______ (保留两位有效数
字)。(4)①“加热搅拌”有利于加快 溶出、提高产率,其原因是_______。
②“操作X”的过程为:先_______,再固液分离。
(5)该工艺中,可再生循环利用的物质有_______(写化学式)。
(6)稀土元素钇(Y)可用于制备高活性的合金类催化剂 。
①还原 和 熔融盐制备 时,生成1mol 转移_______ 电子。
② 用作氢氧燃料电池电极材料时,能在碱性溶液中高效催化 的还原,发生的电极反应为_______。
1.(2021·浙江)固体化合物X由3种元素组成,某学习小组开展如下探究实验。
其中,白色沉淀B能溶于NaOH溶液。请回答:
(1)白色固体C的化学式是_______,蓝色溶液D中含有的溶质是_______(用化学式表示)。
(2)化合物X的化学式是_______;化合物X的一价阴离子与CH 具有相同的空间结构,写出该阴离子的
4
电子式_______。
(3)蓝色溶液A与 作用,生成一种气体,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀。①写出该反应的离子方程式_______。
②设计实验验证该白色沉淀的组成元素_______。
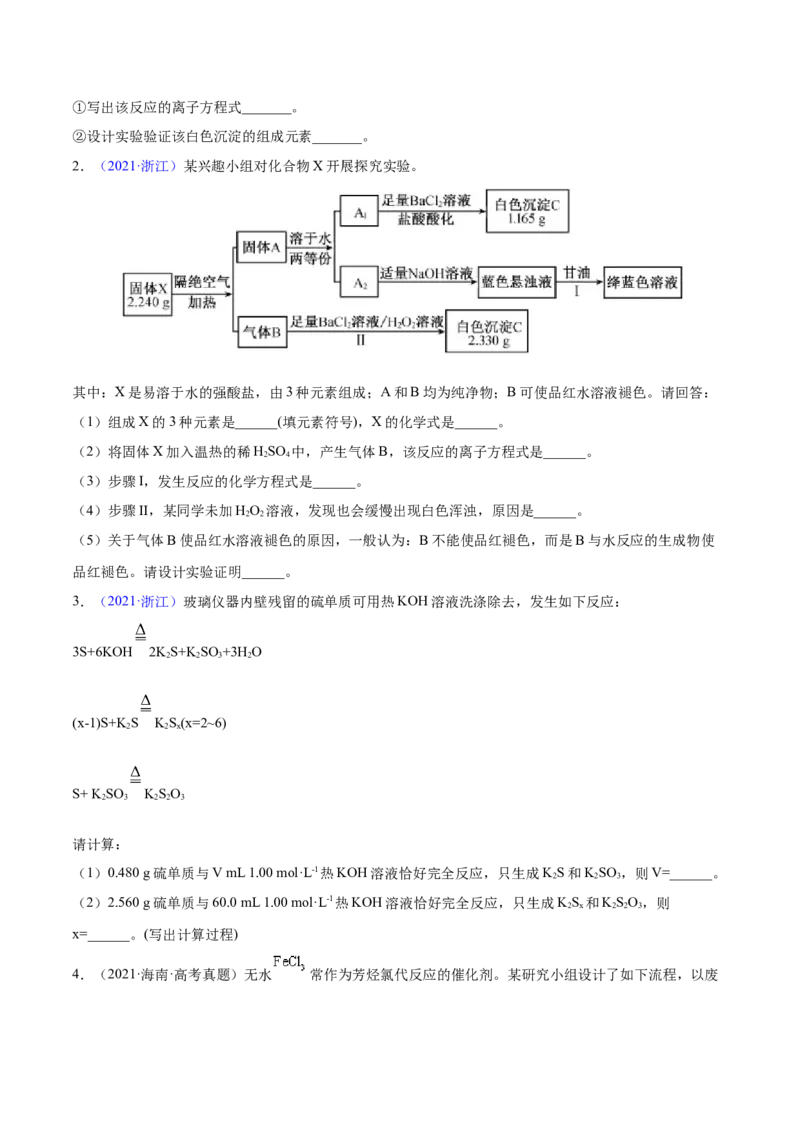
2.(2021·浙江)某兴趣小组对化合物X开展探究实验。
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:
(1)组成X的3种元素是______(填元素符号),X的化学式是______。
(2)将固体X加入温热的稀HSO 中,产生气体B,该反应的离子方程式是______。
2 4
(3)步骤I,发生反应的化学方程式是______。
(4)步骤II,某同学未加HO 溶液,发现也会缓慢出现白色浑浊,原因是______。
2 2
(5)关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使
品红褪色。请设计实验证明______。
3.(2021·浙江)玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S+6KOH 2KS+KSO +3H O
2 2 3 2
(x-1)S+KS KS(x=2~6)
2 2 x
S+ K SO KSO
2 3 2 2 3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS和KSO ,则V=______。
2 2 3
(2)2.560 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成KS 和KSO,则
2 x 2 2 3
x=______。(写出计算过程)
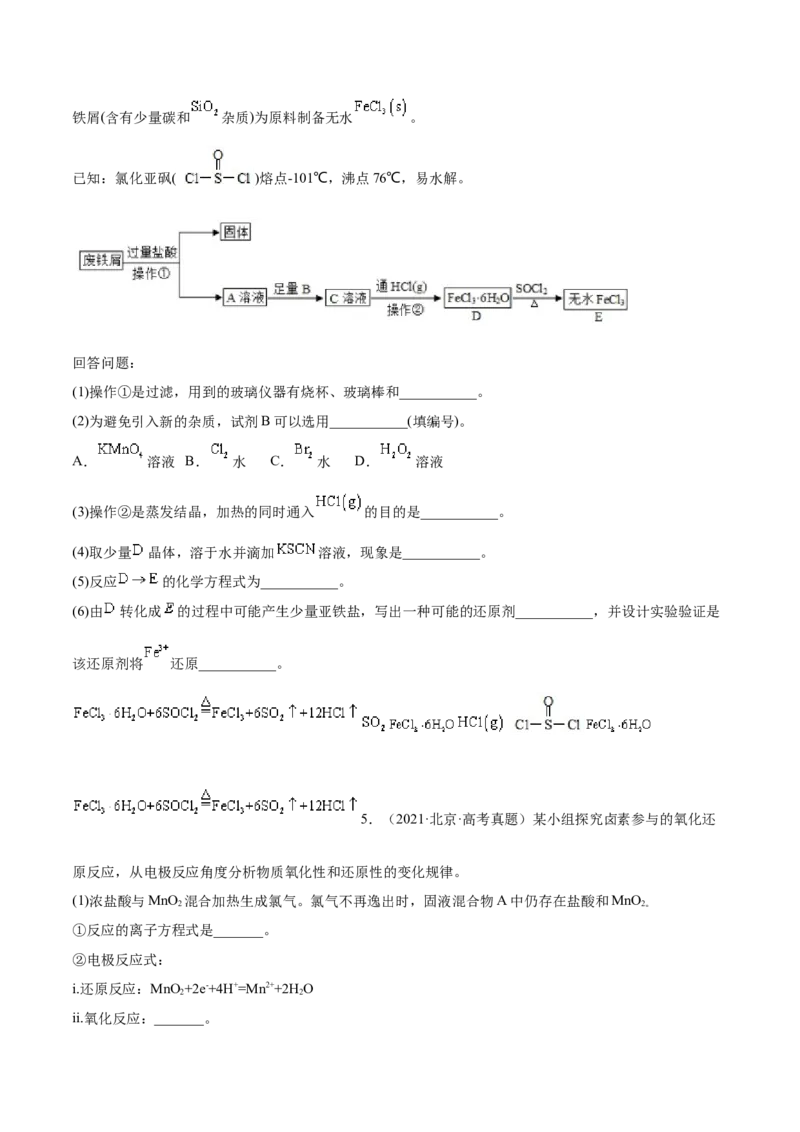
4.(2021·海南·高考真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 B. 水 C. 水 D. 溶液
(3)操作②是蒸发结晶,加热的同时通入 的目的是___________。
(4)取少量 晶体,溶于水并滴加 溶液,现象是___________。
(5)反应 的化学方程式为___________。
(6)由 转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________,并设计实验验证是
该还原剂将 还原___________。
5.(2021·北京·高考真题)某小组探究卤素参与的氧化还
原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO
2 2。
①反应的离子方程式是_______。
②电极反应式:
i.还原反应:MnO +2e-+4H+=Mn2++2H O
2 2
ii.氧化反应:_______。③根据电极反应式,分析A中仍存在盐酸和MnO 的原因。
2
i.随c(H+)降低或c(Mn2+)浓度升高,MnO 氧化性减弱。
2
ii.随c(Cl-)降低,_______。
④补充实验证实了③中的分析。
实验操作 试剂 产物
I 较浓HSO 有氯气
2 4
II a 有氯气
III a+b 无氯气
a是_______,b是_______。
(2)利用c(H+)浓度对MnO 氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能
2
与MnO 反应所需的最低c(H+)由大到小的顺序是_______,从原子结构角度说明理由______________。
2
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO 。经实验
2
证实了推测,该化合物是_______。
(4)Ag分别与1mol·L1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:_______。
(5)总结:物质氧化性和还原性变化的一般规律是_______。
6.(2021·北京·高考真题)铁黄是一种重要的化工产品。由生产钛白粉废渣制备铁黄的过程如下。
资料:
i.钛白粉废渣成分:主要为FeSO ·H O,含少量TiOSO 和不溶物
4 2 4
ii.TiOSO +(x+1)H O TiO·xH O↓+HSO
4 2 2 2 2 4
iii.0.1 mol/L Fe2+生成⇌Fe(OH)
2
,开始沉淀时pH=6.3,完全沉淀时pH=8.3;
0.1 mol/L Fe3+生成FeOOH,开始沉淀时pH=1.5,完全沉淀时pH=2.8
(1)纯化
①加入过量铁粉的目的是_______。
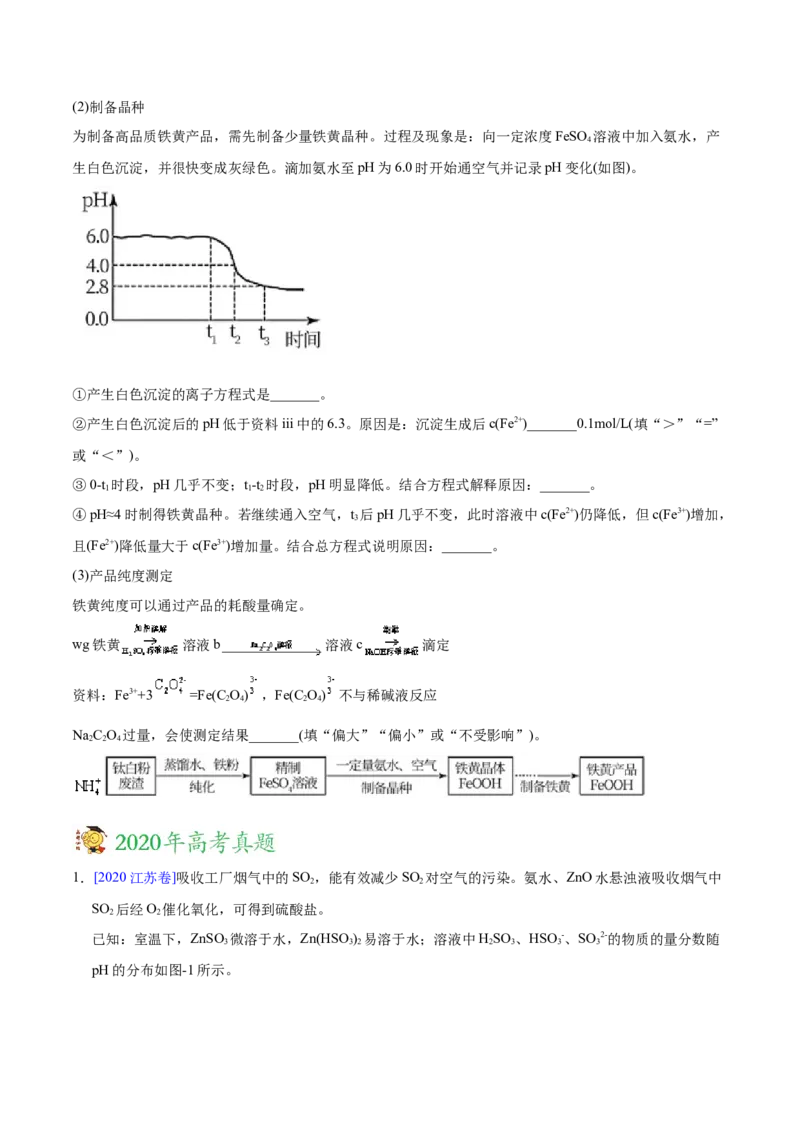
②充分反应后,分离混合物的方法是_______。(2)制备晶种
为制备高品质铁黄产品,需先制备少量铁黄晶种。过程及现象是:向一定浓度FeSO 溶液中加入氨水,产
4
生白色沉淀,并很快变成灰绿色。滴加氨水至pH为6.0时开始通空气并记录pH变化(如图)。
①产生白色沉淀的离子方程式是_______。
②产生白色沉淀后的pH低于资料iii中的6.3。原因是:沉淀生成后c(Fe2+)_______0.1mol/L(填“>”“=”
或“<”)。
③0-t 时段,pH几乎不变;t-t 时段,pH明显降低。结合方程式解释原因:_______。
1 1 2
④pH≈4时制得铁黄晶种。若继续通入空气,t 后pH几乎不变,此时溶液中c(Fe2+)仍降低,但c(Fe3+)增加,
3
且(Fe2+)降低量大于c(Fe3+)增加量。结合总方程式说明原因:_______。
(3)产品纯度测定
铁黄纯度可以通过产品的耗酸量确定。
wg铁黄 溶液b 溶液c 滴定
资料:Fe3++3 =Fe(C O) ,Fe(C O) 不与稀碱液反应
2 4 2 4
NaC O 过量,会使测定结果_______(填“偏大”“偏小”或“不受影响”)。
2 2 4
1.[2020江苏卷]吸收工厂烟气中的SO ,能有效减少SO 对空气的污染。氨水、ZnO水悬浊液吸收烟气中
2 2
SO 后经O 催化氧化,可得到硫酸盐。
2 2
已知:室温下,ZnSO 微溶于水,Zn(HSO ) 易溶于水;溶液中HSO 、HSO -、SO 2-的物质的量分数随
3 3 2 2 3 3 3
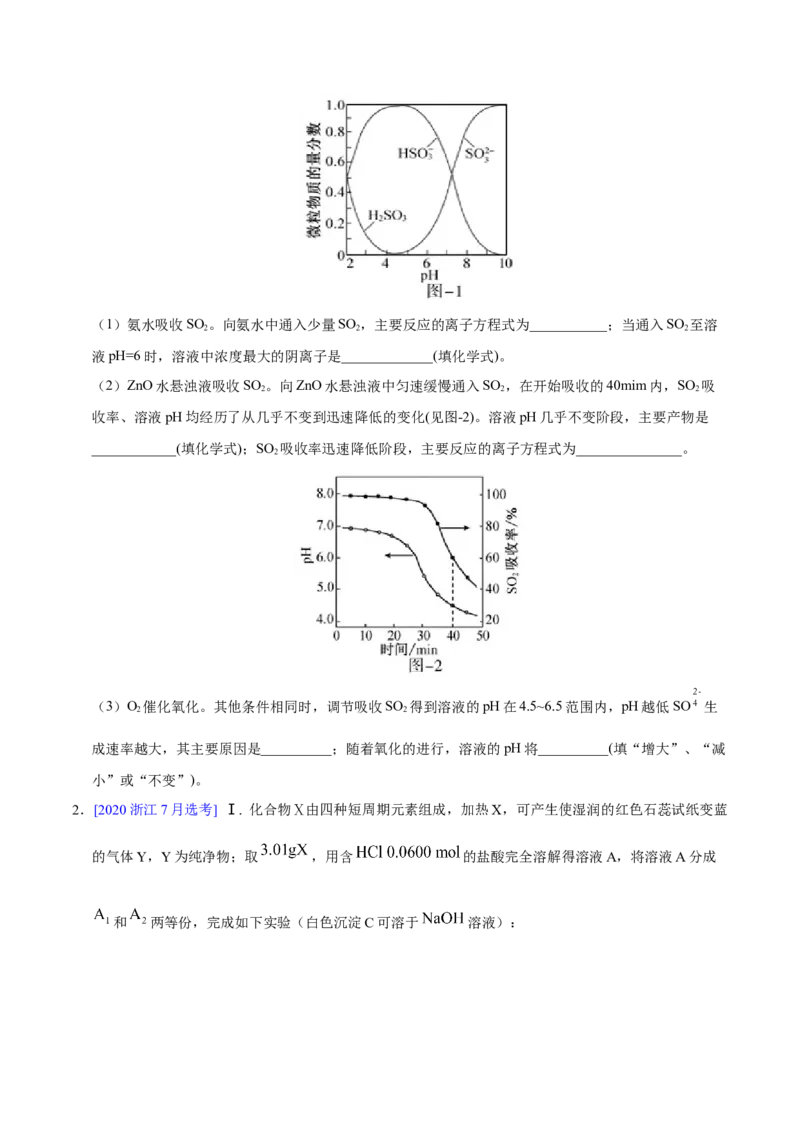
pH的分布如图-1所示。(1)氨水吸收SO 。向氨水中通入少量SO ,主要反应的离子方程式为___________;当通入SO 至溶
2 2 2
液pH=6时,溶液中浓度最大的阴离子是_____________(填化学式)。
(2)ZnO水悬浊液吸收SO 。向ZnO水悬浊液中匀速缓慢通入SO ,在开始吸收的40mim内,SO 吸
2 2 2
收率、溶液pH均经历了从几乎不变到迅速降低的变化(见图-2)。溶液pH几乎不变阶段,主要产物是
____________(填化学式);SO 吸收率迅速降低阶段,主要反应的离子方程式为_______________。
2
(3)O 催化氧化。其他条件相同时,调节吸收SO 得到溶液的pH在4.5~6.5范围内,pH越低SO 生
2 2
成速率越大,其主要原因是__________;随着氧化的进行,溶液的pH将__________(填“增大”、“减
小”或“不变”)。
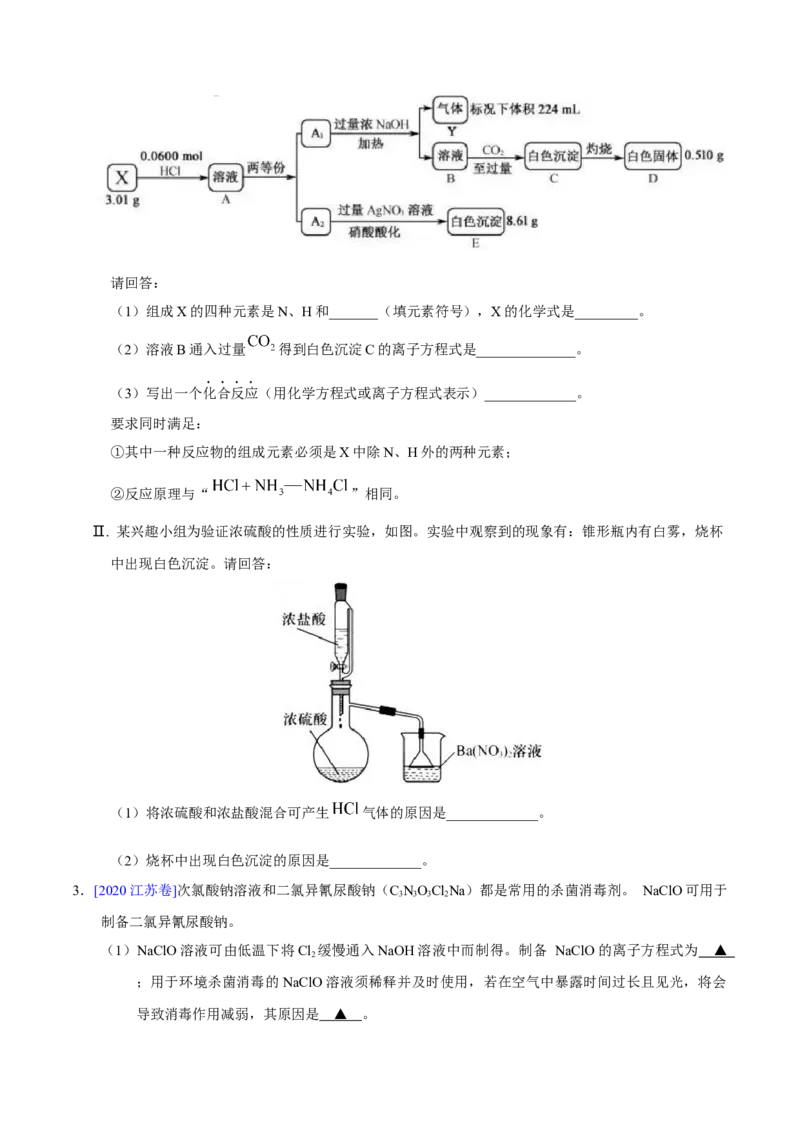
2.[2020浙江7月选考] Ⅰ. 化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝
的气体Y,Y为纯净物;取 ,用含 的盐酸完全溶解得溶液A,将溶液A分成
和 两等份,完成如下实验(白色沉淀C可溶于 溶液):请回答:
(1)组成X的四种元素是N、H和_______(填元素符号),X的化学式是_________。
(2)溶液B通入过量 得到白色沉淀C的离子方程式是______________。
(3)写出一个化合反应(用化学方程式或离子方程式表示)_____________。
要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“ ”相同。
Ⅱ. 某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯
中出现白色沉淀。请回答:
(1)将浓硫酸和浓盐酸混合可产生 气体的原因是_____________。
(2)烧杯中出现白色沉淀的原因是_____________。
3.[2020江苏卷]次氯酸钠溶液和二氯异氰尿酸钠(C NOClNa)都是常用的杀菌消毒剂。 NaClO可用于
3 3 3 2
制备二氯异氰尿酸钠。
(1)NaClO溶液可由低温下将Cl 缓慢通入NaOH溶液中而制得。制备 NaClO的离子方程式为 ▲
2
;用于环境杀菌消毒的NaClO溶液须稀释并及时使用,若在空气中暴露时间过长且见光,将会
导致消毒作用减弱,其原因是 ▲ 。(2)二氯异氰尿酸钠优质品要求有效氯大于60%。通过下列实验检测二氯异氰尿酸钠样品是否达到
优质品标准。实验检测原理为
准确称取1.1200 g样品,用容量瓶配成250.0 mL溶液;取25.00 mL上述溶液于碘量瓶中,加入
适量稀硫酸和过量KI溶液,密封在暗处静置5 min;用 NaSO 标准溶液滴定至
2 2 3
溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗NaSO 溶液20.00 mL。
2 2 3
①通过计算判断该样品是否为优质品。
(写出计算过程, )
②若在检测中加入稀硫酸的量过少,将导致样品的有效氯测定值 ▲ (填“偏高”或“偏
低”)