文档内容
专题突破(九) 有关电解质溶液的四大常数及应用
电解质溶液中的四大常数包括水的离子积常数(K )、电离平衡常数(K 或K )、盐类水解
w a b
平衡常数(K )和溶度积常数(K ),有关四大常数的计算及应用是高考测试的重点和热点,此
h sp
类题体现《中国高考评价体系》对以解决实际问题为核心的实践操作能力群的要求,要求考
生科学收集、处理并解释实验数据,能够对问题解决方案的合理性、可行性进行基于事实和
逻辑的论证。
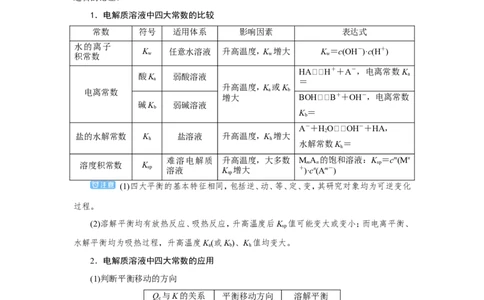
1.电解质溶液中四大常数的比较
常数 符号 适用体系 影响因素 表达式
水的离子
K 任意水溶液 升高温度,K 增大 K =c(OH-)·c(H+)
积常数 w w w
HAH++A-,电离常数K
酸K 弱酸溶液 a
a =
升高温度,K 或K
电离常数 a b
增大 BOHB++OH-,电离常数
碱K 弱碱溶液
b
K =
b
A-+HOOH-+HA,
2
盐的水解常数 K 盐溶液 升高温度,K 增大
h h
水解常数K =
h
难溶电解质 升高温度,大多数 M A 的饱和溶液:K =cm(Mn
溶度积常数 K m n sp
sp 溶液 K 增大 +)·cn(Am-)
sp
(1)四大平衡的基本特征相同,包括逆、动、等、定、变,其研究对象均为可逆变化
过程。
(2)溶解平衡均有放热反应、吸热反应,升高温度后K 值可能变大或变小;而电离平衡、
sp
水解平衡均为吸热过程,升高温度K(或K )、K 值均变大。
a b h
2.电解质溶液中四大常数的应用
(1)判断平衡移动的方向
Q 与K的关系 平衡移动方向 溶解平衡
c
Q>K 逆向 沉淀生成
c
Q=K 不移动 饱和溶液
c
Q<K 正向 不饱和溶液
c
(2)四大常数之间的定量关系
①K = ②K =
h h
(3)判断离子浓度比值的大小变化。例如,将NH ·H O溶液加水稀释,c(OH-)减小,由于
3 2
电离平衡常数为,此值不变,故的值增大。(4)利用四大平衡常数进行有关计算。
(2020·全国卷Ⅲ,27题节选)某油脂厂废弃的油脂加氢镍催化剂主要含金属 Ni、
Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍
晶体(NiSO ·7H O):
4 2
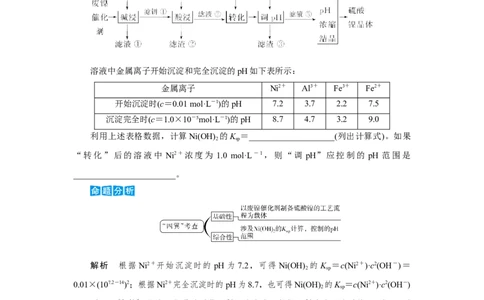
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5mol·L-1)的pH 8.7 4.7 3.2 9.0
利用上述表格数据,计算Ni(OH) 的K =____________________(列出计算式)。如果
2 sp
“转化”后的溶液中 Ni2+浓度为 1.0 mol·L-1,则“调 pH”应控制的 pH 范围是
________________________。
解析 根据 Ni2+开始沉淀时的 pH 为 7.2,可得 Ni(OH) 的 K =c(Ni2+)·c2(OH-)=
2 sp
0.01×(107.2-14)2;根据Ni2+完全沉淀时的pH为8.7,也可得Ni(OH) 的K =c(Ni2+)·c2(OH-)
2 sp
=10-5×(108.7-14)2。“调pH”是为了使Fe3+沉淀完全,根据Fe3+完全沉淀时的pH为3.2可
知,pH≥3.2;同时不能使 Ni2+沉淀,则 Q[Ni(OH) ]≤K [Ni(OH) ],则 c(Ni2+)·c2(OH
c 2 sp 2
-)≤0.01×(107.2-14)2,根据c(Ni2+)=1.0mol·L-1,可求得c(OH-)≤10-7.8mol·L-1,对应c(H
+)≥10-6.2mol·L-1,则pH≤6.2,则“调pH”控制的pH范围是3.2~6.2。
答案 0.01×(107.2—14)2[或10-5×(108.7—14)2] 3.2~6.2
(2021·河北承德一中检测)常温下,向1 L 0.1 mol·L-1 一元酸HR溶液中逐渐通入
氨气[已知常温下,K (NH ·H O)=1.76×10-5],使溶液的温度和体积保持不变,混合溶液的
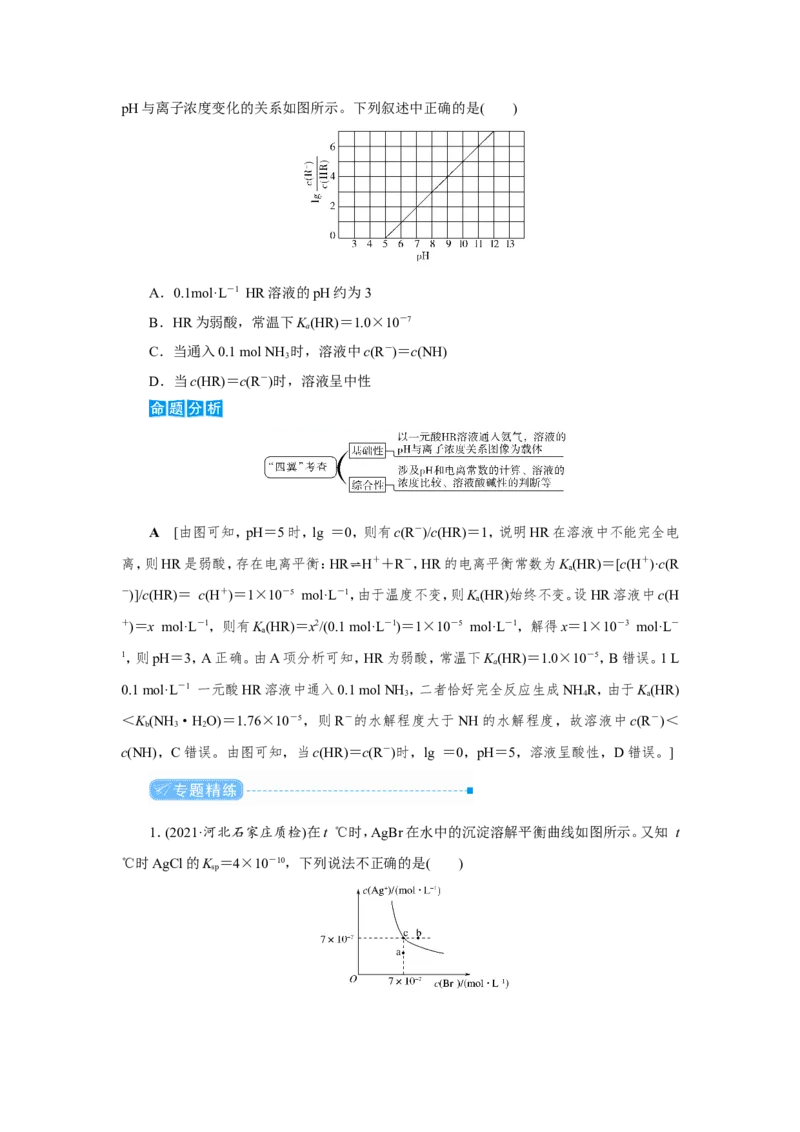
b 3 2pH与离子浓度变化的关系如图所示。下列叙述中正确的是( )
A.0.1mol·L-1 HR溶液的pH约为3
B.HR为弱酸,常温下K (HR)=1.0×10-7
a
C.当通入0.1 mol NH 时,溶液中c(R-)=c(NH)
3
D.当c(HR)=c(R-)时,溶液呈中性
A [由图可知,pH=5时,lg =0,则有c(R-)/c(HR)=1,说明HR在溶液中不能完全电
离,则HR是弱酸,存在电离平衡:HR⇌H++R-,HR的电离平衡常数为K
a
(HR)=[c(H+)·c(R
-)]/c(HR)= c(H+)=1×10-5 mol·L-1,由于温度不变,则K(HR)始终不变。设HR溶液中c(H
a
+)=x mol·L-1,则有K(HR)=x2/(0.1 mol·L-1)=1×10-5 mol·L-1,解得x=1×10-3 mol·L-
a
1,则pH=3,A正确。由A项分析可知,HR为弱酸,常温下K (HR)=1.0×10-5,B错误。1 L
a
0.1 mol·L-1 一元酸HR溶液中通入0.1 mol NH ,二者恰好完全反应生成NH R,由于K(HR)
3 4 a
<K (NH ·HO)=1.76×10-5,则R-的水解程度大于NH的水解程度,故溶液中c(R-)<
b 3 2
c(NH),C错误。由图可知,当c(HR)=c(R-)时,lg =0,pH=5,溶液呈酸性,D错误。]
1.(2021·河北石家庄质检)在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知 t
℃时AgCl的K =4×10-10,下列说法不正确的是( )
spA.在t ℃ 时,AgBr的K 为4.9×10-13
sp
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点变到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t ℃时,AgCl(s)+Br-(aq)⇌AgBr(s)+Cl-(aq)的平衡常数K≈816
B [根据图中c点的c(Ag+)和c(Br-)可得,该温度下AgBr的K 为4.9×10-13,A正确;
sp
在AgBr饱和溶液中加入NaBr固体后,c(Br-)增大,溶解平衡逆向移动,c(Ag+)减小,B错误;
在a点时Q<K ,故为AgBr的不饱和溶液,C正确;在t ℃时,平衡常数K==,代入数据得
c sp
K≈816,D正确。]
2.(2021·天津部分区联考)一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00 mL,再加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol·L-1 AgNO 溶液(过量),充分摇匀。
1 1 3
③用c mol·L-1 KSCN标准溶液进行滴定,至终点时消耗标准溶液V mL。
2 2
[已知:K (AgBr)=7.7×10-13,Ag++SCN-===AgSCN(白色)↓,K (AgSCN)=1×10-12]
sp sp
下列说法不正确的是( )
A.滴定终点时,溶液变为红色
B.该滴定法需在碱性条件下进行
C.AgBr(s)+SCN-(aq)⇌AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该水样中c(Br-)= mol·L-1
B [在碱性条件下,Fe3+生成氢氧化铁沉淀,B项错误;K====0.77,C项正确;达到
滴定终点时,n(SCN-)+n(Br-)=n(Ag+),n(Br-)=cV×10-3-cV×10-3,c(Br-)= mol·L
1 1 2 2
-1= mol·L-1,D项正确。]
3.(2021·辽宁辽阳质检)磷的含氧酸有磷酸(H PO )、亚磷酸(H PO )、次磷酸(H PO )等多
3 4 3 3 3 2
种,它们在工业上都是重要的化工原料。
(1)亚磷酸(H PO )是一种二元弱酸,写出HPO 与过量NaOH溶液反应的化学方程式:
3 3 3 3
________________________________________________________。某温度下,0.01 mol·L-1
HPO 溶液的pH为2.7,该温度下,HPO 的一级电离常数K =________(已知:lg 2=0.3 ,lg
3 3 3 3 a1
3=0.5,lg 5=0.7,HPO 的第二步电离忽略不计)。
3 3
(2)某实验小组用NaOH溶液处理含HPO 废水,当溶液中c(Na+)=c(H PO)+2c(HPO)
3 3 2
时,溶液呈____________________________________________________________性(填
“酸”“碱”或“中”)。
(3)已知:常温下,磷酸(H PO )的K =7.11×10-3,K =6.23×10-8、K =4.5×10-13,则
3 4 a1 a2 a3常 温 下 , NaHPO 溶 液 中 HPO 、 HPO 和 PO 的 浓 度 由 大 到 小 的 顺 序 为
2 4 2
______________________________________。
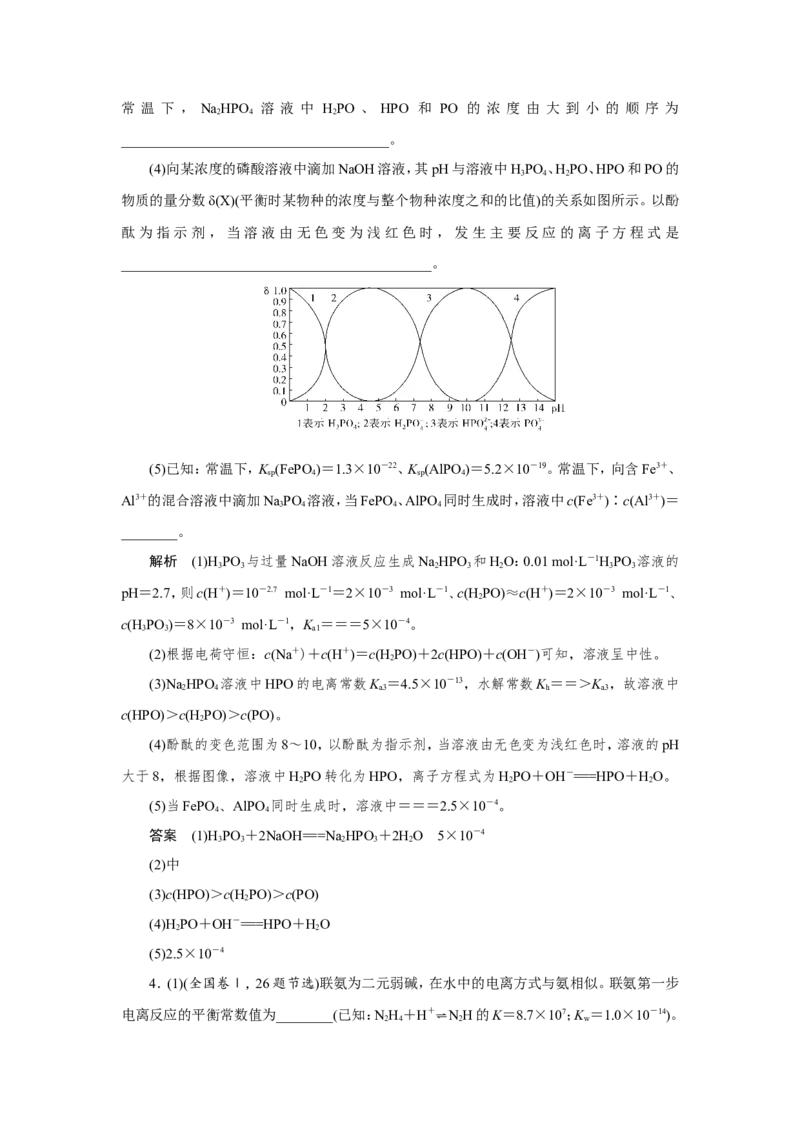
(4)向某浓度的磷酸溶液中滴加NaOH溶液,其pH与溶液中HPO 、HPO、HPO和PO的
3 4 2
物质的量分数δ(X)(平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。以酚
酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是
____________________________________________。
(5)已知:常温下,K (FePO )=1.3×10-22、K (AlPO )=5.2×10-19。常温下,向含Fe3+、
sp 4 sp 4
Al3+的混合溶液中滴加NaPO 溶液,当FePO 、AlPO 同时生成时,溶液中c(Fe3+)∶c(Al3+)=
3 4 4 4
________。
解析 (1)H PO 与过量NaOH溶液反应生成NaHPO 和HO:0.01 mol·L-1HPO 溶液的
3 3 2 3 2 3 3
pH=2.7,则c(H+)=10-2.7 mol·L-1=2×10-3 mol·L-1、c(H PO)≈c(H+)=2×10-3 mol·L-1、
2
c(H PO )=8×10-3 mol·L-1,K ===5×10-4。
3 3 a1
(2)根据电荷守恒:c(Na+)+c(H+)=c(H PO)+2c(HPO)+c(OH-)可知,溶液呈中性。
2
(3)Na HPO 溶液中HPO的电离常数K =4.5×10-13,水解常数K ==>K ,故溶液中
2 4 a3 h a3
c(HPO)>c(H PO)>c(PO)。
2
(4)酚酞的变色范围为8~10,以酚酞为指示剂,当溶液由无色变为浅红色时,溶液的pH
大于8,根据图像,溶液中HPO转化为HPO,离子方程式为HPO+OH-===HPO+HO。
2 2 2
(5)当FePO 、AlPO 同时生成时,溶液中===2.5×10-4。
4 4
答案 (1)H PO +2NaOH===Na HPO +2HO 5×10-4
3 3 2 3 2
(2)中
(3)c(HPO)>c(H PO)>c(PO)
2
(4)H PO+OH-===HPO+HO
2 2
(5)2.5×10-4
4.(1)(全国卷Ⅰ,26题节选)联氨为二元弱碱,在水中的电离方式与氨相似。联氨第一步
电离反应的平衡常数值为________(已知:N
2
H
4
+H+ ⇌N
2
H的K=8.7×107;K
w
=1.0×10-14)。联氨与硫酸形成的酸式盐的化学式为________。
(2)(全国卷Ⅱ,27题节选)在化学分析中采用KCrO 为指示剂,以AgNO 标准溶液滴定
2 4 3
溶液中Cl-,利用Ag+与CrO生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完
全(浓度等于10×10-5 mol·L-1)时,溶液中c(Ag+)为________ mol·L-1,此时溶液中c(CrO)等
于________ mol·L-1。(已知:Ag CrO、AgCl的K 分别为2.0×10-12和2.0×10-10)。
2 4 sp
(3)(海南卷,14题节选)已知:K
w
=1.0×10-14,Al(OH) 3⇌AlO+H++H
2
O K
a
=2.0×10-
13。Al(OH) 溶于NaOH溶液反应的平衡常数等于________。
3
解析 (1)NH
3
在水中的电离方式为NH
3
+H
2
O⇌NH+OH-,联氨在水中的电离方式
与氨相似,据此推知联氨第一步电离方程式为N
2
H
4
+H
2
O⇌N
2
H+OH-,K
b1
=。又知N
2
H
4
+H
+ ⇌N
2
H的K=8.7×107,H
2
O⇌H++OH-的K
w
=1.0×10-14,综合上述两式可得,K
b1
==
K·K =(8.7×107)×(1.0×10-14)=8.7×10-7。因为联氨为二元弱碱,第二步电离方程式为NH
w 2
+H
2
O⇌N
2
H+OH-,故与硫酸形成的酸式盐为N
2
H
6
(HSO
4
)
2
。
(2)AgCl在水中存在溶解平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),则有K
sp
(AgCl)=c(Ag+)·c(Cl
-),当溶液中Cl-恰好沉淀完全时 c(Cl-)=1.0×10-5 mol·L-1,则溶液中c(Ag+)===
2.0×10-5mol·L-1。Ag CrO 的 K (Ag CrO)=c2(Ag+)·c(CrO),则溶液中 c(CrO)=
2 4 sp 2 4
K (Ag CrO)/ c2(Ag+)=[(2.0×10-12)/(2.0×10-5)2 ]mol·L-1=5.0×10-3 mol·L-1。
sp 2 4
(3)Al(OH) 溶于NaOH溶液的反应为Al(OH) +OH-===AlO+2HO,该反应的平衡常数
3 3 2
为K=c(AlO/c(OH-)。又知Al(OH) 3⇌AlO+H++H
2
O的K
a
=2.0×10-13 ,H
2
O⇌H++OH-的
K =1.0×10-14,综合上述两式可得,K====20。
w
答案 (1)8.7×10-7 NH(HSO ) (2)2.0×10-5 5.0×10-3 (3)20
2 6 4 2