文档内容
成一中 2022-2023 学年第一学期高三开学检测
化学试卷
一、单选题(本大题共20小题,共60分)
1. 热还原法治炼金属的反应一定是( )
.
A 氧化还原反应 B. 置换反应 C. 复分解反应 D. 分解反应
2. 唐代中药学著作《新修本草》中,有关于“青矾”的记录为“本来绿色,新出窟未见风者,正如琉璃,
……,烧之赤色”。据此推测,“青矾”的主要成分为
A. CuSO ·5H O B. FeSO ·7H O C. KAl(SO )·12H O D. ZnSO·7H O
4 2 4 2 4 2 2 4 2
3. 下列叙述中正确个数的是
①标准状况下,6.02×1023个分子所占体积约是22.4L;
②1molH O中含有2mol氢和2mol氧;
2
③0.012kg12C中含有约6.02×1023个碳原子;
的
④两种物质 物质的量相同,则它们在标准状况下的体积相同;
的
⑤同温同体积时,气体物质 物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比
⑦2mol水的摩尔质量是1mol水的摩尔质量的2倍。
A. 2个 B. 3个 C. 4个 D. 5个
4. 设N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 标准状况下,2.24L四氯化碳中含有共价键总数为0.4N
A
B. 46g NO 和NO 的混合气体中,含有的氮原子数为1N
2 2 4 A
C. 1L1.0mol/L的盐酸中含有HCl分子数为N
A
D. 一定条件下,将2molSO 与1molO 充分反应,得到SO 的分子数为2N
2 2 3 A
5. 下列实验现象描述正确的是
选项 实验 现象
向饱和NaCO 溶液中通入足量的CO 气
A 2 3 2 无明显现象
体
铝箔熔化,失去光泽,熔化的铝
B 在酒精灯上加热铝箔
滴落下来
C 向久置于空气中的FeSO 溶液中滴加 立刻产生大量白色沉淀
4
下载最新免费模拟卷,到公众号:一枚试卷君NaOH溶液
钠先熔化成光亮的小球,燃烧时
D 加热放在坩埚中的小块钠 火焰为黄色,燃烧后生成淡黄色
固体
A. A B. B C. C D. D
6. 常温下,铝土矿 含有 、FeO、 、 等物质 用硫酸浸。下列说法中错误的是
A. 向浸出后的溶液加入过量NaOH溶液后存在: 、 、 、
B. 向浸出后的溶液加入过量氨水后存在: 、 、 、
C. 向浸出后的溶液通入过量HI后存在: 、 、 、 、
D. 若铝土矿改用NaOH溶液浸,浸出后的溶液中存在: 、 、 、
7. 在下列关于钠及其化合物的性质说法错误的是
A. 为鉴别KCO 和NaHCO 两种白色固体,可分别配成溶液,做焰色反应实验,观察火焰的颜色
2 3 3
B. 热稳定性、水中的溶解性以及与酸反应的速度都是:NaCO>NaHCO
2 3 3
C. 钠不可以从硫酸铜溶液中置换出铜
D. NaO与NaO 的阴、阳离子个数比相同
2 2 2
8. 氢化钙可以作为生氢剂(其中CaH 中氢元素为-1价),反应方程式如下:
2
,其中水的作用是
A. 既不是氧化剂也不是还原剂 B. 是氧化剂
C. 是还原剂 D. 既是氧化剂又是还原剂
9. 下列有关物质分类或归类正确的一组是
①液氯、干冰、磁性氧化铁均为化合物 ②氢氟酸、盐酸、水玻璃均为混合物 ③明矾、小苏打、烧碱
均为电解质 ④牛奶、豆浆、漂粉精均为胶体 ⑤NaO、NaCO、NaSiO 均为钠盐
2 2 2 3 2 3
A. ②③ B. ①② C. ③④ D. ②③⑤
10. 用铝箔包裹 金属钠,用针扎若干个小孔,放入水中,完全反应后,放出的气体体积(标准状况)
为
A. 无法确定 B. C. 大于 D. 小于11. 下列说法正确的是
A. Fe在稀硝酸中发生钝化
B. 向FeCl 溶液中滴加NH SCN溶液,溶液显红色
2 4
C. Cu与FeCl 溶液反应可生成CuCl
3 2
D. 铝的金属活泼性强,可用于制作铝金属制品
12. 向FeCl 、CuCl 混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是
3 2
.
A 溶液中一定含有Fe2+ B. 溶液中一定含有Cu2+
C. 剩余固体中一定含有Cu D. 加入KSCN溶液一定不变红
13. 高一学生小强的化学笔记中有如下内容:
①物质按照组成可以分为单质和化合物;
②单质又可分为金属和非金属;
③化合物主要包括:酸、碱、盐和氧化物;
④按照分散剂粒子直径大小可将分散系分为溶液、浊液和胶体;
⑤只要在水溶液中能导电的化合物就是电解质;
⑥按照树状分类法可将化学反应分为:氧化还原反应和离子反应;
⑦氧化还原反应的本质是化合价升降。
你认为他的笔记中有几处错误
A. 三处 B. 四处 C. 五处 D. 六处
14. 下列关于铝热反应2Al+Fe O Al O+2Fe的说法不正确的是( )
2 3 2 3
A. 该反应中Al作还原剂
B. 该反应中氧化产物与还原产物的物质的量比为1∶2
C. 该反应中冶炼1 mol Fe转移2 mol电子
D. 该反应可用于焊接钢轨
15. 设 代表阿伏加德罗常数的值,下列有关说法正确的是
A. 冰醋酸晶体中,含阴离子数目为
B. 标准状况下, 中含有分子的数目为
C. 常温下, 与 混合气体中含分子数为
D. 投入 的浓硝酸中,充分反应后转移电子数为16. 设 代表阿伏加德罗常数的值,下列有关说法正确的是
A. 冰醋酸晶体中,含阴离子数目为
B. 标准状况下, 中含有分子的数目为
C. 常温下, 与 混合气体中含分子数为
D. 投入 的浓硝酸中,充分反应后转移电子数为
17. 下列铁的化合物通过化合反应、置换反应、复分解反应均能得到的是
A. FeCl B. Fe (SO ) C. Fe O D. Fe(OH)
2 2 4 3 3 4 3
18. 向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下
列结论错误的是
A. 该溶液中一定含有SCN- B. 氧化性:Fe3+>Cl
2
C. Fe2+与SCN-不能形成红色物质 D. Fe2+被氧化为Fe3+
19. 假定把 的相对原子质量改为 ,那么下列叙述错误的是
A. 此时 的相对原子质量为 B. 个 与 个 的质量比为
C. 的摩尔质量为 D. 标准状况下, 的体积约为11.2L
20. 已知酸性 ,下列有关叙述中正确的是
①向 溶液中通入少量二氧化碳的离子反应方程式为
②向 和 混合溶液中加入足量 溶液,用 萃取后,取上层中的液体少许并加入 溶
液,有淡黄色沉淀生成
③向 溶液中滴加少量氯水,反应的离子方程式为
④“84”消毒液(有效成分 )和“洁厕灵”(主要成分盐酸)混合使用时放出氯气,其离子方程式为
⑤在海带灰的浸出液(含有 )中滴加 得到 ,其离子方程式为A. ②④ B. ①③⑤ C. ②③ D. ①④⑤
二、简答题(本大题共3小题,共30分)
21. “化学——我们的生活,我们的未来”,学习化学应该明白“从生活中来,到生活中去”的道理。请填空:
(1)我们学习过很多颜色的化学物质,写出下列物质的颜色:
过氧化钠固体___________,氢氧化铁胶体___________。
(2)写出下列物质的电离方程式:
Al (SO )___________,Ba(OH) ___________。
2 4 3 2
的
(3)通过学习,我们掌握了胶体 知识,请完成下列问题:
鉴别胶体和溶液的方法(只需写出方法名称,不用展开写)___________,胶体和溶液的本质区别是
___________。
(4)某同学写出以下三个化学方程式(未配平)
①NO+HNO―→NO+H O
3 2 3 2
②NH +NO―→HNO+H O
3 2 2
③NO+H O―→HNO +HNO
2 4 2 3 2
其中你认为一定不可能实现的是___________。
(5)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO (浓) CO↑+4NO↑+2H O,该反应中氧化剂和
3 2 2 2
还原剂的物质的量之比为___________;如果产生标准状况下22.4LCO ,则转移的电子的物质的量为
2
___________mol。
(6)有下列6种物质:NaSO 、NaSO 、KSO 、I、HSO 、KIO 组成一个氧化还原反应,请回答下列问
2 4 2 3 2 4 2 2 4 3
题:
i.将除NaSO 的5种物质分别填入下面对应的横线上,组成化学方程式并配平:_____+Na SO +_____—
2 3 2 3
_____+_____+_____+HO,___________。
2
ii.反应物中发生氧化反应的物质是___________(填化学式),被还原的元素是___________;
iii.反应中1mol氧化剂___________(填“得到”或“失去”)___________mol电子。
22. 回答下列问题
(1)铝是地壳中含量最多的金属元素,画出铝原子结构示意图_______。在酒精灯的火焰上灼烧铝片,可
观察到铝熔化但不滴落,说明铝的熔点比较_______(高、低),外层氧化铝薄膜是_______(疏松、致密)的。
(2)根据反应 ,回答下列问题:①画双线桥,请标出变价元素化合价、电子得失及转移数目_______。
②还原剂是_______,被_______(氧化、还原)。
③当有 反应时,转移_______ 电子,生成 _______L(标准状态下)。
23. 现有下列几种物质:蔗糖、氯化钡固体、干冰、硫酸钡、纯碱、铁、盐酸、硝酸银溶液,按要求回答
问题:
(1)难溶于水的电解质的是_______。
(2)写出纯碱在水中的电离方程式________________________。
(3)将足量的干冰升华后所得的气体通入烧碱溶液中,发生反应的离子方程式为____________。
(4)a、b、c、d是NaCO、BaCl、盐酸、AgNO 四种溶液中的一种,现将它们两两混合,现象如下表所示:
2 3 2 3
反应物 a+b c+d a+d a+c b+d
现象 白色沉淀 白色沉淀 白色沉淀 白色沉淀 无色气体
①b是________(用化学式填写),
②写出 a+c 反应的离子方程式________________________。
三、推断题(本大题共1小题,共10分)
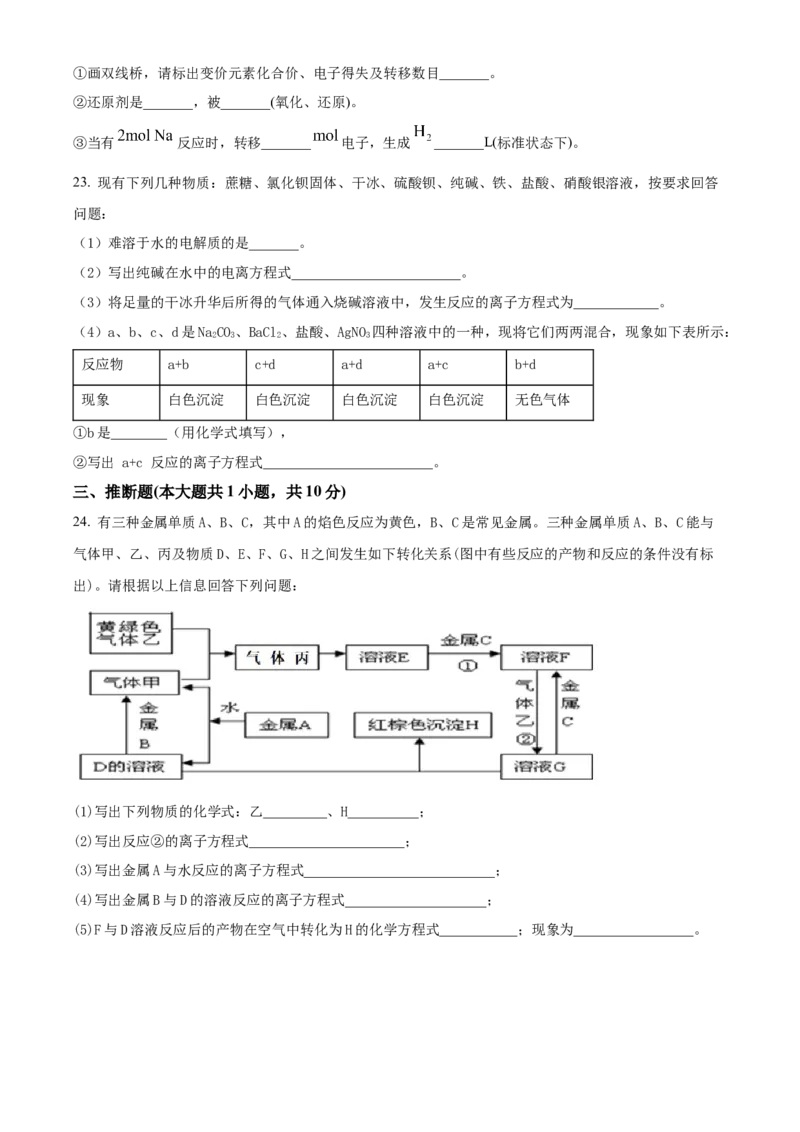
24. 有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与
气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标
出)。请根据以上信息回答下列问题:
(1)写出下列物质的化学式:乙_________、H__________;
(2)写出反应②的离子方程式______________________;
(3)写出金属A与水反应的离子方程式___________________________;
(4)写出金属B与D的溶液反应的离子方程式____________________;
(5)F与D溶液反应后的产物在空气中转化为H的化学方程式___________;现象为_________________。下载最新免费模拟卷,到公众号:一枚试卷君