文档内容
微专题突破3 新情景下方程式的书写
业精于勤,荒于嬉;行成于思,毁于随。——韩愈
目标定位
1.能根据题中提供的信息结合已有知识,正确书写信息方程式。
2.能从四个方面——配平、反应条件、符号使用及产物在所给环境中能否存在等,判断所写方程式的正误。
教学重点难点
非氧化还原反应及氧化还原方程式书写。
教学方法
应用有关思维方法解决问题
教学过程
【规律点和易错点】
孙猴子七十二般变化,都逃不出你的手心
书写方程式的程序
一看反应物系统—→二审给定条件—→三定反应程度—→四析生成物—→五辨生成物特征—→六配平
①
—→七检查
细致审查给定条件——物料状态·溶液浓度·加热程度·压强·催化剂·光·电·点燃·加入方式、顺序·物质的
②
量之比·少量、适量、足量
化学方程式思维方向立体化——对该反应实质的探究——为什么能发生?在何条件下发生?该反应的
③
意义和价值——概念的建立和深化、理论的证明或发展、自然现象的解释与认识、生产生活中的应用。
陌生氧化还原反应方程式的书写步骤
① 结合物质的类别、化合价情况确认反应发生的本质
② 确定最关键的反应物和生成物
③ 由电子守恒配平关键反应物和生成物
④ 再根据守恒配平或补充其他辅助反应物和产物
⑤ 依据题目信息写好反应条件
⑥ 结合反应条件和反应体系所处的环境对各物质的存在形式、状态进行修正
考考
1.(2024·江苏卷)回收磁性合金钕铁硼(Nd Fe B)可制备半导体材料铁酸铋和光学材料氧化钕。
2 14
的
向 NdCl 溶液中加入(NH )CO 溶液,Nd3+可转化为 Nd(OH)CO 沉淀。该反应 离子方程式为
3 4 2 3 3
_______________________________________________________。
【答案】2Nd3++3CO2-+HO=2Nd(OH)CO↓+CO↑
3 2 3 2
【解析】向NdCl 溶液中加入(NH )CO 溶液,Nd3+和CO2-相互促进对方水解生成Nd(OH)CO 沉淀和
3 4 2 3 3 3
CO,该反应的离子方程式为2Nd3++3CO2-+HO=2Nd(OH)CO↓+CO↑。
2 3 2 3 2
2.(2024·江苏卷)贵金属银应用广泛。Ag与稀HNO 制得AgNO,常用于循环处理高氯废水。
3 3
还原AgCl。在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol·L-1盐酸后静置,充分反应得到Ag。
①铁将AgCl转化为单质Ag的化学方程式为___________________________________________。
②不与铁圈直接接触的AgCl也能转化为Ag的原因是__________________________________________
___________________________________________________________。
【答案】①Fe+2AgCl=FeCl +2Ag ②形成了以Fe、Ag为负极,AgCl为正极,盐酸为电解质溶液的原
2
电池,正极AgCl得到电子,电极反应式为AgCl+e—=Ag+Cl-,生成Ag微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
【解析】①在足量0.5 mol·L-1盐酸中静置,铁将AgCl转化为单质Ag,反应的化学方程式为:Fe+2AgCl
=FeCl +2Ag;②不与铁圈直接接触的AgCl也能转化为Ag,是因为形成了以Fe、Ag为负极,AgCl为正极,
2
盐酸为电解质溶液的原电池,正极AgCl得到电子,电极反应式为AgCl+e—=Ag+Cl-,生成Ag。
3.(2024·江苏卷)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
一定条件下,将氮气和氢气按n(N)∶n(H)=1∶3混合匀速通入合成塔,发生反应N+3H α-F
2 2 2 2 e/A
高温、2NH 。海绵状的α-Fe作催化剂,多孔Al O 作为α-Fe的“骨架”和气体吸附剂。
高压 3 2 3
H 中含有CO会使催化剂中毒。CHCOO[Cu(NH )]和氨水的混合溶液能吸收CO生成
2 3 3 2
CHCOO[Cu(NH )CO]溶液,该反应的化学方程式为________________________________________________。
3 3 3
【答案】CHCOO[Cu(NH )]+NH ·HO+CO=CHCOO[Cu(NH )CO]+HO
3 3 2 3 2 3 3 3 2
【解析】根据题给反应物及生成物书写即可。
【问题解决1】
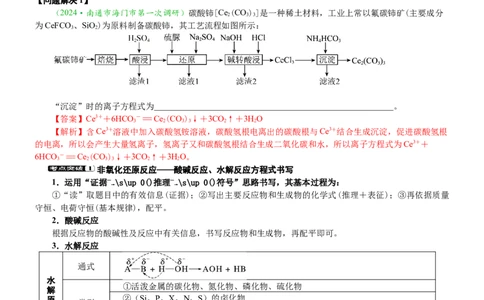
(2024·南通市海门市第一次调研)碳酸铈[Ce (CO)]是一种稀土材料,工业上常以氟碳铈矿(主要成分
2 3 3
为CeFCO、SiO)为原料制备碳酸铈,其工艺流程如图所示:
3 2
“沉淀”时的离子方程式为________________________________________________________。
【答案】Ce3++6HCO -=Ce (CO)↓+3CO↑+3HO
3 2 3 3 2 2
【解析】含Ce3+溶液中加入碳酸氢铵溶液,碳酸氢根电离出的碳酸根与Ce3+结合生成沉淀,促进碳酸氢根
的电离,所以会产生大量氢离子,氢离子又和碳酸氢根结合生成二氧化碳和水,所以离子方程式为Ce3++
6HCO -=Ce (CO)↓+3CO↑+3HO。
3 2 3 3 2 2
非氧化还原反应——酸碱反应、水解反应方程式书写
1.运用“证据— \s\up 0()推理— \s\up 0()符号”思路书写,其基本过程为:
→ →
①“读”取题目中的有效信息(证据);②写出主要反应物和生成物的化学式(推理+表征);③再依据质量
守恒、电荷守恒(基本规律),配平。
2.酸碱反应
根据反应物的酸碱性及反应中有关信息,书写反应物和生成物,再配平即可。
3.水解反应
通式
水
①活泼金属的碳化物、氮化物、磷化物、硫化物
解
原 ②(Si、P、X、N、S)的卤化物
类型
理 ③有机化合物的活泼金属有机化合物:C HONa、RCOONa、RCOR、RCOX、
2 5
RCONH
2
说明 根据水:①均裂HO=—H+—OH、②异裂HO=H++OH-来考虑
2 2
运用类比的方法,可以确定相同反应原理的产物。如CaC 与HO反应的原理为水解反应,水电离成H+和
2 2
OH-,然后分别与Ca2+和C 2-结合,生成Ca(OH) 和C H ,可以推知像CaC 这样金属与非金属结合成的离子
2 2 2 2 2
型化合物AlC 、MgC 、LiC 、MgN、NaO 等与水反应均类似,故可以顺利判断出生成物。
4 3 2 3 2 2 3 2 2 2
4.用HCO -沉淀金属阳离子离子方程式的书写
3
HCO -在水溶液中既存在电离平衡(HCO - H++CO2-)又存在水解平衡(HCO -+HO HCO+OH
3 3 3 3 2 2 3
-)
2
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找(1)若金属阳离子(以Ca2+为例)的K (CaCO )<K [Ca(OH)],则溶液中的金属阳离子(Ca2+)主要结合
sp 3 sp 2
HCO -电离产生的CO2-生成碳酸盐沉淀(CaCO ),反应的离子方程式为Ca2++2HCO -=CaCO ↓+HO+
3 3 3 3 3 2
CO↑。
2
(2)若金属阳离子(以Mg2+为例)的K (MgCO )>K [Mg(OH)],则溶液中的金属阳离子(Mg2+)主要结
sp 3 sp 2
合HCO -水解产生的OH-生成氢氧化物沉淀[Mg(OH)],反应的离子方程式为Mg2++2HCO -=Mg(OH)↓
3 2 3 2
+2CO↑。
2
(3)示例
沉铈过程中,生成Ce (CO)·nHO的离子方程式为2Ce3++6HCO -+(n-3)HO=Ce (CO)·nHO+
2 3 3 2 3 2 2 3 3 2
3CO↑。
2
考点精练
1.(2023·苏州上学期期末)异丙醇铝Al[OCH(CH)] 加入到75℃中,充分搅拌可生成Al(OH) 胶体。
3 2 3 3
生成Al(OH) 胶体的化学方程式为___________________________________________________________________。
3
【答案】Al[OCH(CH)]+3HO======Al(OH)(胶体)+3HOCH(CH)
3 2 3 2 3 3 2
【解析】Al[OCH(CH)] 在75℃水中,充分搅拌可生成Al(OH) 胶体,方程式为Al[OCH(CH)]+
3 2 3 3 3 2 3
3HO======Al(OH)(胶体)+3HOCH(CH),故答案为Al[OCH(CH)]+3HO======Al(OH)(胶体)+
2 3 3 2 3 2 3 2 3
3HOCH(CH)
3 2
2.(2023·盐城五校)偏铝酸钙可由水硬铝石[AlO(OH)]与石灰石在高温下煅烧得到。写出该反应的化学
方程式:________________________________________________________。
【答案】2AlO(OH)+CaCO ====Ca(AlO)+CO↑+HO
3 2 2 2 2
【解析】由题意有:CaCO +AlO(OH)— \s\up 0()Ca(AlO) ,推测生成物还有 CO 和 HO,配平得
3 → 2 2 2 2
2AlO(OH)+CaCO ====Ca(AlO)+CO↑+HO。
3 2 2 2 2
3.(2024·无锡上学期期中)Cr(VI)在水溶液中有HCrO、HCrO -、CrO2-和Cr O2-四种存在形式
2 4 4 4 2 7
(HCrO 是二元弱酸),HCrO -部分转化为Cr O2-的离子方程式为________________________________。
2 4 4 2 7
【答案】2HCrO - Cr O2-+HO
4 2 7 2
【解析】Cr(VI)在水溶液中有HCrO、HCrO -、CrO2-和Cr O2-四种存在形式(HCrO 是二元弱酸),
2 4 4 4 2 7 2 4
HCrO -部分转化为Cr O2-的离子方程式为HCrO - Cr O2-,根据电荷守恒有2HCrO - Cr O2-,再由
4 2 7 4 2 7 4 2 7
质量守恒得2HCrO - Cr O2-+HO。
4 2 7 2
【问题解决2】
(2023·如皋期末)将Fe O 与蔗糖(C H O )一起焙烧,可生成FeO与CO 。写出焙烧时所发生反应的化
2 3 12 22 11 2
学方程式:____________________________________________________________。
【答案】24Fe O+C H O =====48FeO+12CO↑+11HO
2 3 12 22 11 2 2
【解析】由题意Fe O+C H O — \s\up 0()FeO+CO↑,C H O 中碳的价态为0价,铁元素降低1价,
2 3 12 22 11 → 2 12 22 11
碳元素升高24价,据电子守恒有24Fe O+1C H O — \s\up 0()24FeO+12CO↑,再据质量守恒得24Fe O+
2 3 12 22 11 → 2 2 3
C H O =====48FeO+12CO↑+11HO。
12 22 11 2 2
氧化还原反应信息方程式书写
①找出氧化剂和还原剂;②从反应现象、物质性质、价态变化、得失电子等角度推断氧化(还
第一步
原)产物;③利用电子守恒配平。
根据电荷守恒,根据溶液的酸碱性,通过在反应方程式的两端添加H+或OH-使方程式两端的
第二步
电荷守恒。
第三步 根据原子守恒,通过在反应方程式两端添加HO(或其他小分子)使方程式两端的原子守恒。
2
解题关键:根据题目信息,依据反应环境正确判断反应物和生成物,借助于电子守恒、电荷守恒、原子守
恒进行配平和验证。
考点精练微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
1.(2023·苏州期末)325 ℃时,水在Mn粉表面产生的H 可将CO 转化成甲酸,同时生成MnO。由
2 2
HO、Mn、CO 制备甲酸的化学方程式为____________________________________________________________。
2 2
【答案】Mn+CO+HO=====MnO+HCOOH
2 2
【解析】HCOOH中C元素的价态为+2。由题意可知Mn+HO+CO— \s\up 0()MnO+HCOOH,Mn元素
2 2 →
升高2价,C元素总+4降+2,降低2价,故反应式为Mn+CO+HO=====MnO+HCOOH。
2 2
2.(2023·苏州上学期期末)NH COONH 具有强还原性,生产尿素过程中,常通入适量氧气防止镍制容
2 4
器表面的金属钝化膜(NiO)被破坏。
①NH COONH 与 NiO 反 应 产 生 N 的 化 学 方 程 式 为
2 4 2
_________________________________________________。
②生产时通入的CO 气体中常混有少量HS。有氧气存在的条件下,HS腐蚀反应容器的速率会更快,其原
2 2 2
因是_________________________________________________________________________________________。
【答案】①NH COONH +3NiO=N +3Ni+3HO+CO ②HS与O 反应生成SO ,SO 、O 、HO反应
2 4 2 2 2 2 2 2 2 2 2
生成硫酸,酸性增强,腐蚀能力增强
【解析】①NH COONH 与NiO反应产生N,由氧化还原分析,NiO生成Ni,故化学方程式为
2 4 2
NH COONH+3NiO=N+3Ni+3HO+CO;②生产时通入的CO 气体中常混有少量HS。有氧气存在的条件
2 4 2 2 2 2 2
下,发生反应2HS+3O=2SO +2HO,2HO+O+2SO =2HSO ,硫酸腐蚀性更强。
2 2 2 2 2 2 2 2 4
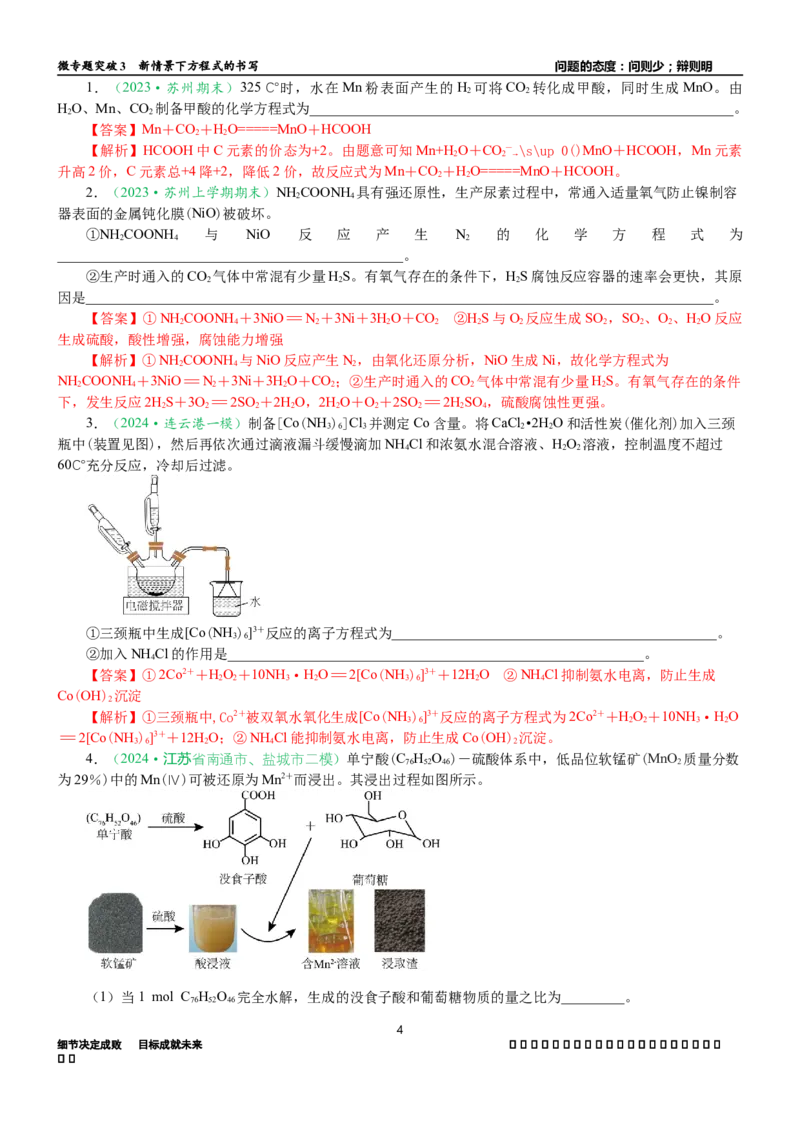
3.(2024·连云港一模)制备[Co(NH )]Cl 并测定Co含量。将CaCl •2HO和活性炭(催化剂)加入三颈
3 6 3 2 2
瓶中(装置见图),然后再依次通过滴液漏斗缓慢滴加NH Cl和浓氨水混合溶液、HO 溶液,控制温度不超过
4 2 2
60℃充分反应,冷却后过滤。
①三颈瓶中生成[Co(NH )]3+反应的离子方程式为______________________________________________。
3 6
②加入NH Cl的作用是___________________________________________________________。
4
【答案】①2Co2++HO+10NH ·HO=2[Co(NH )]3++12HO ②NH Cl抑制氨水电离,防止生成
2 2 3 2 3 6 2 4
Co(OH) 沉淀
2
【解析】①三颈瓶中,Co2+被双氧水氧化生成[Co(NH )]3+反应的离子方程式为2Co2++HO+10NH ·HO
3 6 2 2 3 2
=2[Co(NH )]3++12HO;②NH Cl能抑制氨水电离,防止生成Co(OH) 沉淀。
3 6 2 4 2
4.(2024·江苏省南通市、盐城市二模)单宁酸(C H O )-硫酸体系中,低品位软锰矿(MnO 质量分数
76 52 46 2
为29%)中的Mn(Ⅳ)可被还原为Mn2+而浸出。其浸出过程如图所示。
(1)当1 mol C H O 完全水解,生成的没食子酸和葡萄糖物质的量之比为_________。
76 52 46
4
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找(2)写出葡萄糖还原MnO 生成CO 的离子反应方程式:
2 2
____________________________________________________________________。
【答案】(1)10∶1 (2)C H O+12MnO +24H+=12Mn2++6CO↑+18HO
6 12 6 2 2 2
【解析】(1)设1 mol C H O 完全水解,生成的没食子酸x mol、葡萄糖y mol,根据C守恒:7x+6y
76 52 46
=76……①,没食子酸、葡萄糖比单宁酸分子中多的氧、氢原子都由水提供,则=……②,解得x=10,带入
①得y=1,生成的没食子酸和葡萄糖物质的量之比为10∶1;(2)葡萄糖还原MnO 生成CO ,根据得失电子
2 2
守恒,离子反应方程式为C H O+12MnO +24H+=12Mn2++6CO↑+18HO。
6 12 6 2 2 2
【问题解决3】
(2024·南通市海安市)工业上可由菱锌矿(主要成分为ZnCO,还含有Ni、Cd、Fe、Mn等元素)制备
3
ZnO。工艺如图所示:
已知:①“酸浸”后的溶液pH=1,所含金属离子主要有Zn2+、Fe3+、Cd2+、Mn2+、Ni2+。
②弱酸性溶液中KMnO 氧化Mn2+时,产物中含Mn元素物质只有MnO 。
4 2
(1)“氧化除杂”时,KMnO 与Mn2+的离子方程式为
4
_________________________________________________________。
(2)“沉锌”生成碱式碳酸锌[ZnCO•2Zn(OH)•2HO]沉淀,写出生成该沉淀的化学方程式:
3 2 2
_______________________________________________________________________。
【答案】(1)2MnO -+3Mn2++2HO=5MnO ↓+4H+ (2)3ZnSO +3NaCO +4HO=
4 2 2 4 2 3 2
ZnCO•2Zn(OH)•2HO+2CO↑+3NaSO
3 2 2 2 2 4
【解析】菱锌矿(主要成分为ZnCO,还含有Ni、Cd、Fe、Mn等元素)制备ZnO,加入稀硫酸“酸浸”后
3
得到含Zn2+、Fe3+、Cd2+、Mn2+、Ni2+的滤液,滤渣为不溶于酸的杂质,滤液调节pH后Fe3+使转化为
Fe(OH),加入KMnO “氧化除杂”使Mn2+转化为MnO ,除去Fe3+、Mn2+;接着“还原除杂”除去、Ni2+
3 4 2
Cd2+;最后向含ZnSO 的溶液中加入NaCO 溶液生成碱式碳酸锌[ZnCO•2Zn(OH)•2HO]沉淀,碱式碳酸锌经
4 2 3 3 2 2
“高温灼烧”得到ZnO。
(1)在“氧化除杂”时,KMnO 与Mn2+发生氧化还原反应产生MnO ,根据得失电子守恒、电荷守恒及
4 2
原子守恒,可得反应的离子方程式为2MnO -+3Mn2++2HO=5MnO ↓+4H+;(2)根据分析,向含ZnSO
4 2 2 4
的溶液中加入NaCO 溶液生成碱式碳酸锌[ZnCO•2Zn(OH)•2HO]沉淀,反应的化学的方程式为3ZnSO+
2 3 3 2 2 4
3NaCO+4HO=ZnCO•2Zn(OH)•2HO+2CO↑+3NaSO 。
2 3 2 3 2 2 2 2 4
化工流程方程式书写
1.细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的去除情况。
2.确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
先从流程图中找出反应物和生成物,其次依据有关反应原理确定所缺少的生成物,之后配平,第三根据电
荷守恒确定可能是什么离子参加反应或生成何种离子,最后根据质量守恒确定其他所缺少的物质(一般是水)。
考点精练
1.(2023·南通一调)从废脱硝催化剂(主要成分为TiO 、VO)中回收TiO 和VO 具有重要意义。碱溶
2 2 5 2 2 5
法回收TiO 和VO。部分工艺流程如下:
2 2 5
“酸洗”时NaTi O 转化为TiOCl 或TiOSO ;“水解”后得到HTiO。写出“热碱浸取”时TiO 发生反
2 3 7 2 4 2 3 2微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
应的离子方程式:_______________________________________________________。
【答案】3TiO+2Na++2OH-====NaTi O+HO
2 2 3 7 2
【解析】由流程图可知“热碱浸取”时TiO 发生的反应为:TiO+Na++OH-— \s\up 0()NaTi O,由钠
2 2 → 2 3 7
守恒TiO+2Na++OH-— \s\up 0()NaTi O,再由电荷守恒TiO+2Na++2OH-— \s\up 0()NaTi O,最后由
2 → 2 3 7 2 → 2 3 7
质量守恒3TiO+2Na++2OH-====NaTi O+HO。
2 2 3 7 2
2.(2023·苏州上学期期末)工业上利用高钛炉渣(主要成分为TiO 、CaTiO 及SiO 、Fe O 等)制备
2 3 2 2 3
TiO。
2
已知:①TiO 、FeO 在高温下与NaOH反应生成NaTiO 、NaFeO ,弱碱性条件下NaTiO 、NaFeO 水解
2 3 2 3 2 2 3 2
会生成TiO(OH) 、Fe(OH) 沉淀;②TiO(OH) 难溶于稀酸或稀碱,可以溶解在浓酸或浓碱中;③Fe3+水解能
2 3 2
力显著强于Fe2+,Fe(OH) 容易吸附沉淀。
3
Ⅰ.硫酸法制备TiO
2
(1)焙烧、浸取
①“焙烧”时可将CaTiO 转化为TiOSO ,该反应的化学方程式为___________________________________。
3 4
②酸浸渣的主要成分为___________。
【答案】①CaTiO +2HSO ====CaSO+TiOSO +2HO ②CaSO、SiO
3 2 4 4 4 2 4 2
【解析】高钛炉渣(主要成分为TiO、CaTiO 及SiO、Fe O 等)中加入浓硫酸焙烧,CaTiO 转化为
2 3 2 2 3 3
TiOSO 、CaSO,然后加入稀硫酸“浸取”,经过滤得到的酸浸渣为CaSO、SiO,滤液中含有TiOSO 、
4 4 4 2 4
Fe (SO ),滤液经沸腾水解,过滤得到TiO(OH),TiO(OH) 经系列处理得到TiO。
2 4 3 2 2 2
①“焙烧”时可将CaTiO 转化为TiOSO ,根据原子守恒,反应的化学方程式为
3 4
CaTiO +2H SO ====CaSO+TiOSO+2HO;②根据分析,酸浸渣的主要成分为CaSO、SiO。
3 2 4 4 4 2 4 2
3.(2024·泰州市下学期一模)VO 广泛用于冶金、化工行业,可制取多种含钒化合物。
2 5
(1)实验室制备氧钒(Ⅳ)碱式碳酸铵晶体,过程如下:
“还原”步骤中生成N ,反应的化学方程式为__________________________________________________;
2
若不加NH,HCl也能还原VO 生成VO2+和Cl,分析反应中不生成Cl 的原因________________________。
2 4 2 5 2 2
【答案】①2VO+NH+8HCl=4VOCl +N↑+6HO ②NH 的还原性强于HCl
2 5 2 4 2 2 2 2 4
【解析】由题给流程可知,五氧化二钒与肼、HCl反应生成VOCl 、氮气和水,VOCl 与碳酸氢铵溶液反应
2 2
制得氧钒(Ⅳ)碱式碳酸铵晶体。
由分析可知,还原步骤发生的反应为五氧化二钒与肼、HCl反应生成VOCl 、氮气和水,反应的化学方程
2
式为2VO +NH +8HCl=4VOCl +N↑+6HO;由题给信息可知,五氧化二钒也能与氯化氢反应生成
2 5 2 4 2 2 2
VOCl 和氯气,反应中不生成氯气说明肼的还原性强于氯化氢,会优先与五氧化二钒反应,故答案为:2VO +
2 2 5
NH+8HCl=4VOCl +N↑+6HO;NH 的还原性强于HCl。
2 4 2 2 2 2 4
【问题解决4】
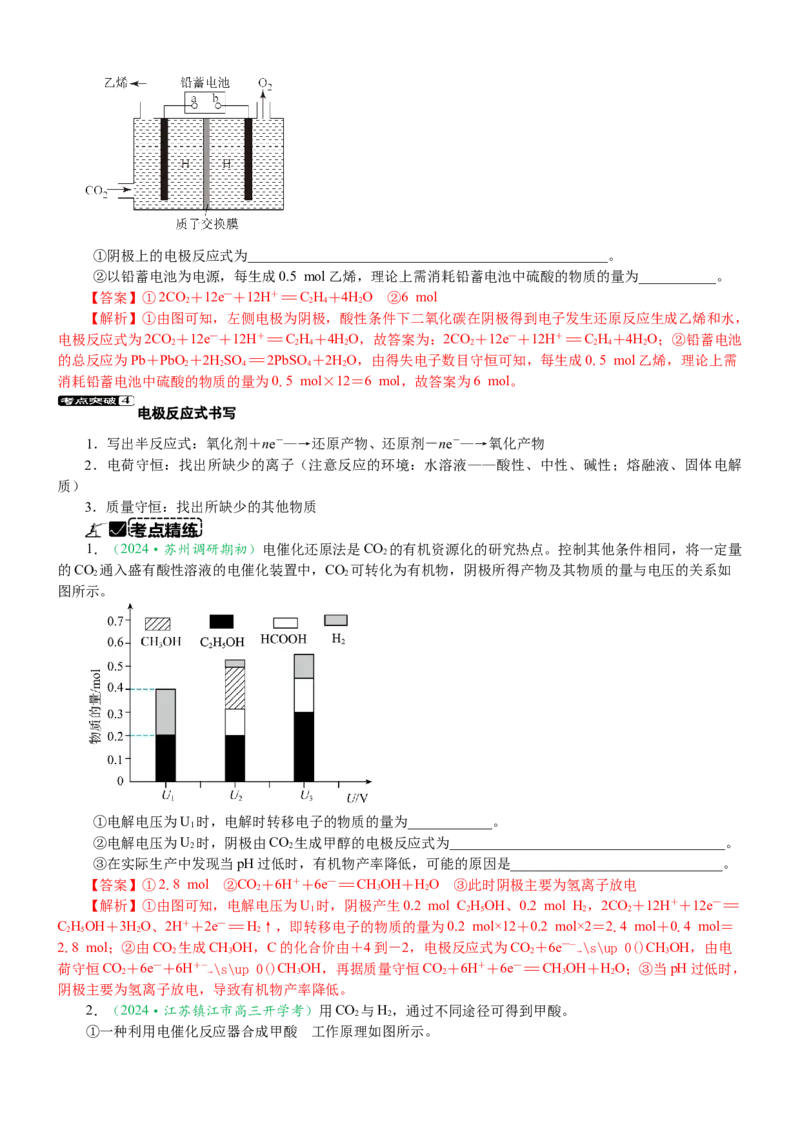
(2024·连云港上学期调研一)一种电化学法将CO 转化为乙烯的原理如图所示:
2
6
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找①阴极上的电极反应式为___________________________________________________。
②以铅蓄电池为电源,每生成0.5 mol乙烯,理论上需消耗铅蓄电池中硫酸的物质的量为___________。
【答案】①2CO+12e—+12H+=C H+4HO ②6 mol
2 2 4 2
【解析】①由图可知,左侧电极为阴极,酸性条件下二氧化碳在阴极得到电子发生还原反应生成乙烯和水,
电极反应式为2CO+12e—+12H+=C H+4HO,故答案为:2CO+12e—+12H+=C H+4HO;②铅蓄电池
2 2 4 2 2 2 4 2
的总反应为Pb+PbO +2HSO =2PbSO +2HO,由得失电子数目守恒可知,每生成0.5 mol乙烯,理论上需
2 2 4 4 2
消耗铅蓄电池中硫酸的物质的量为0.5 mol×12=6 mol,故答案为6 mol。
电极反应式书写
1.写出半反应式:氧化剂+ne-—→还原产物、还原剂-ne-—→氧化产物
2.电荷守恒:找出所缺少的离子(注意反应的环境:水溶液——酸性、中性、碱性;熔融液、固体电解
质)
3.质量守恒:找出所缺少的其他物质
考点精练
1.(2024·苏州调研期初)电催化还原法是CO 的有机资源化的研究热点。控制其他条件相同,将一定量
2
的CO 通入盛有酸性溶液的电催化装置中,CO 可转化为有机物,阴极所得产物及其物质的量与电压的关系如
2 2
图所示。
①电解电压为U 时,电解时转移电子的物质的量为____________。
1
②电解电压为U 时,阴极由CO 生成甲醇的电极反应式为_______________________________________。
2 2
③在实际生产中发现当pH过低时,有机物产率降低,可能的原因是______________________________。
【答案】①2.8 mol ②CO+6H++6e—=CHOH+HO ③此时阴极主要为氢离子放电
2 3 2
【解析】①由图可知,电解电压为U 时,阴极产生0.2 mol C HOH、0.2 mol H,2CO+12H++12e—=
1 2 5 2 2
C HOH+3HO、2H++2e—=H↑,即转移电子的物质的量为0.2 mol×12+0.2 mol×2=2.4 mol+0.4 mol=
2 5 2 2
2.8 mol;②由CO 生成CHOH,C的化合价由+4到-2,电极反应式为CO+6e—— \s\up 0()CHOH,由电
2 3 2 → 3
荷守恒CO+6e—+6H+— \s\up 0()CHOH,再据质量守恒CO+6H++6e—=CHOH+HO;③当pH过低时,
2 → 3 2 3 2
阴极主要为氢离子放电,导致有机物产率降低。
2.(2024·江苏镇江市高三开学考)用CO 与H,通过不同途径可得到甲酸。
2 2
①一种利用电催化反应器合成甲酸 的工作原理如图所示。微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
①生成HCOOH的电极反应方程式为_______________________________。
②325℃时,水在Mn粉表面产生的H 与CO 反应生成甲酸和MnO。直接加热CO 与H 难以生成甲酸,该
2 2 2 2
条件下能较快生成甲酸的原因是_____________________________________________________________。
【答案】①CO+2e—+2H+=HCOOH ②反应生成的MnO是氢气与二氧化碳反应生成甲酸的催化剂,
2
降低反应所需活化能
【解析】①根据图中信息阳极是氢离子失去电子变为氢离子,阴极是二氧化碳得到电子和氢离子结合生成
HCOOH,因此生成HCOOH的电极反应方程式为CO+2e—+2H+=HCOOH;故答案为:CO+2e—+2H+=
2 2
HCOOH;②325℃时,水在Mn粉表面产生的H 与CO 反应生成甲酸和MnO。直接加热CO 与H 难以生成甲
2 2 2 2
酸,该条件下能较快生成甲酸的原因是反应生成的MnO是氢气与二氧化碳反应生成甲酸的催化剂,降低反应所
需活化能;故答案为:反应生成的MnO是氢气与二氧化碳反应生成甲酸的催化剂,降低反应所需活化能。
【问题解决5】
(2024·连云港上学期调研一)水体中的Cr O2-、HCrO -、SO 2-是高毒性的重金属离子,可用Cr(Ⅵ)表
2 7 4 4
示。处理含Cr(Ⅵ)废水的方法有沉淀法、还原法等。
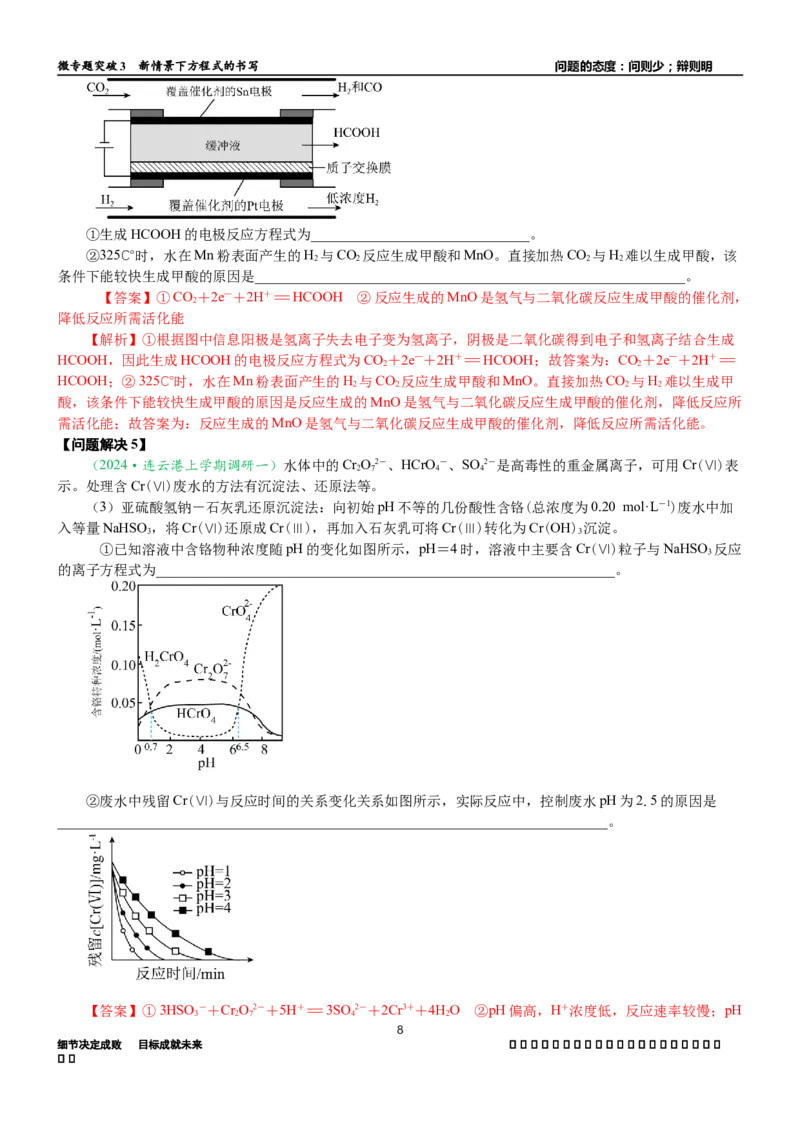
(3)亚硫酸氢钠-石灰乳还原沉淀法:向初始pH不等的几份酸性含铬(总浓度为0.20 mol·L-1)废水中加
入等量NaHSO,将Cr(Ⅵ)还原成Cr(Ⅲ),再加入石灰乳可将Cr(Ⅲ)转化为Cr(OH) 沉淀。
3 3
①已知溶液中含铬物种浓度随pH的变化如图所示,pH=4时,溶液中主要含Cr(Ⅵ)粒子与NaHSO 反应
3
的离子方程式为_________________________________________________________________。
②废水中残留Cr(Ⅵ)与反应时间的关系变化关系如图所示,实际反应中,控制废水pH为2.5的原因是
______________________________________________________________________________。
【答案】①3HSO -+Cr O2-+5H+=3SO 2-+2Cr3++4HO ②pH偏高,H+浓度低,反应速率较慢;pH
3 2 7 4 2
8
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找偏低,H+浓度大,HSO -易转化为SO 气体逸出
3 2
【解析】①由图可知,溶液pH为4时,溶液中Cr(Ⅵ)粒子为重铬酸根离子,溶液中发生的反应为酸性条
件下溶液中重铬酸根离子与亚硫酸氢根离子反应生成硫酸根离子、铬离子和水,反应的离子方程式为3HSO -+
3
Cr O2-+5H+=3SO 2-+2Cr3++4HO,故答案为:3HSO -+Cr O2-+5H+=3SO 2-+2Cr3++4HO;②由图
2 7 4 2 3 2 7 4 2
可知,溶液pH越大,反应速率越慢,实际生产中,溶液pH偏高,溶液中氢离子浓度低,反应速率较慢,不利
于工业生产;溶液pH偏低,氢离子浓度大,易与亚硫酸氢根离子反应生成二氧化硫气体逸出,导致Cr(Ⅵ)去
除率降低,故答案为:pH偏高,H+浓度低,反应速率较慢;pH偏低,H+浓度大,HSO -易转化为SO 气体逸
3 2
出。
图象方程式
根据图象中的有关物质的量是增大还是减小或转化关系,确定反应物还是生成物,再根据有关原理配平。
考点精练
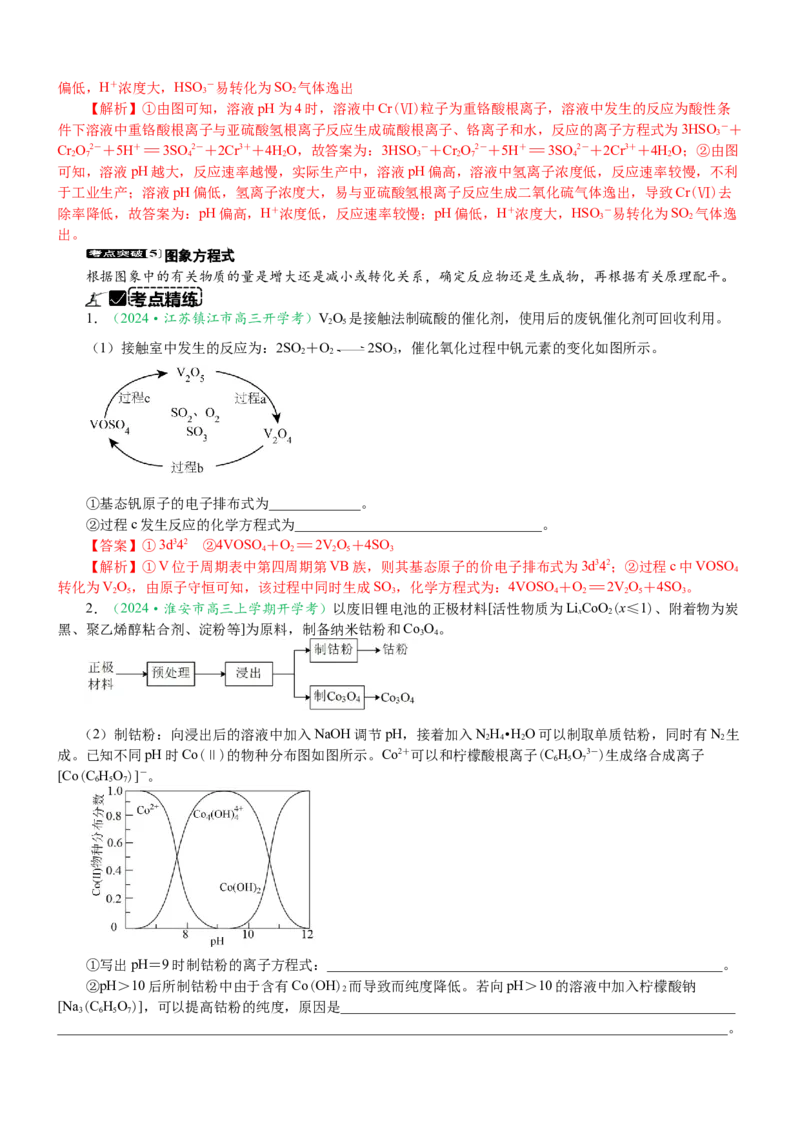
1.(2024·江苏镇江市高三开学考)VO 是接触法制硫酸的催化剂,使用后的废钒催化剂可回收利用。
2 5
(1)接触室中发生的反应为:2SO +O 2SO ,催化氧化过程中钒元素的变化如图所示。
2 2 3
①基态钒原子的电子排布式为_____________。
②过程c发生反应的化学方程式为___________________________________。
【答案】①3d342 ②4VOSO+O=2VO+4SO
4 2 2 5 3
【解析】①V位于周期表中第四周期第VB族,则其基态原子的价电子排布式为3d342;②过程c中VOSO
4
转化为VO,由原子守恒可知,该过程中同时生成SO ,化学方程式为:4VOSO+O=2VO+4SO 。
2 5 3 4 2 2 5 3
2.(2024·淮安市高三上学期开学考)以废旧锂电池的正极材料[活性物质为LiCoO(x≤1)、附着物为炭
x 2
黑、聚乙烯醇粘合剂、淀粉等]为原料,制备纳米钴粉和Co O。
3 4
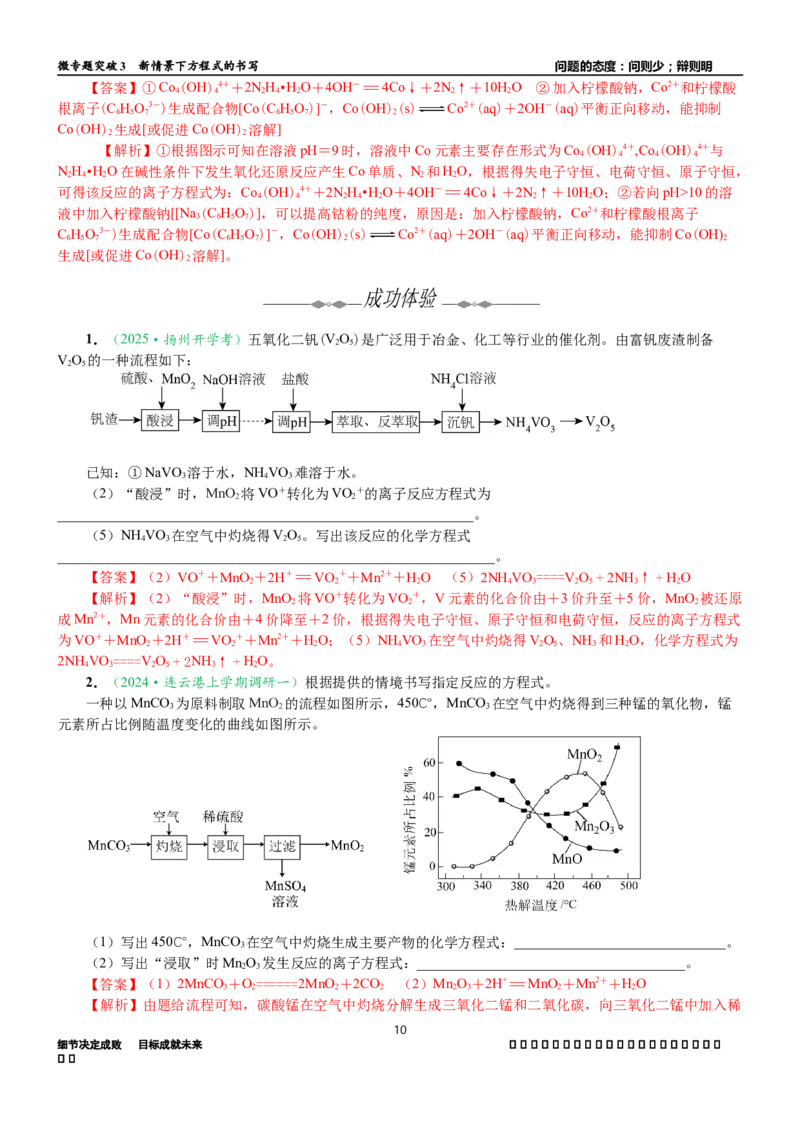
(2)制钴粉:向浸出后的溶液中加入NaOH调节pH,接着加入NH•HO可以制取单质钴粉,同时有N 生
2 4 2 2
成。已知不同pH时Co(Ⅱ)的物种分布图如图所示。Co2+可以和柠檬酸根离子(C HO3-)生成络合成离子
6 5 7
[Co(C HO)]-。
6 5 7
①写出pH=9时制钴粉的离子方程式:________________________________________________________。
②pH>10后所制钴粉中由于含有Co(OH) 而导致而纯度降低。若向pH>10的溶液中加入柠檬酸钠
2
[Na (C HO)],可以提高钴粉的纯度,原因是________________________________________________________
3 6 5 7
_______________________________________________________________________________________________。微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
【答案】①Co(OH)4++2NH•HO+4OH-=4Co↓+2N↑+10HO ②加入柠檬酸钠,Co2+和柠檬酸
4 4 2 4 2 2 2
根离子(C HO3-)生成配合物[Co(C HO)]-,Co(OH)(s) Co2+(aq)+2OH-(aq)平衡正向移动,能抑制
6 5 7 6 5 7 2
Co(OH) 生成[或促进Co(OH) 溶解]
2 2
【解析】①根据图示可知在溶液pH=9时,溶液中Co元素主要存在形式为Co(OH)4+,Co(OH)4+与
4 4 4 4
NH•HO在碱性条件下发生氧化还原反应产生Co单质、N 和HO,根据得失电子守恒、电荷守恒、原子守恒,
2 4 2 2 2
可得该反应的离子方程式为:Co(OH)4++2NH•HO+4OH-=4Co↓+2N↑+10HO;②若向pH>10的溶
4 4 2 4 2 2 2
液中加入柠檬酸钠[[Na (C HO)],可以提高钴粉的纯度,原因是:加入柠檬酸钠,Co2+和柠檬酸根离子
3 6 5 7
C HO3-)生成配合物[Co(C HO)]-,Co(OH)(s) Co2+(aq)+2OH-(aq)平衡正向移动,能抑制Co(OH)
6 5 7 6 5 7 2 2
生成[或促进Co(OH) 溶解]。
2
成功体验
1.(2025·扬州开学考)五氧化二钒(VO)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备
2 5
VO 的一种流程如下:
2 5
已知:①NaVO 溶于水,NH VO 难溶于水。
3 4 3
(2)“酸浸”时,MnO 将VO+转化为VO+的离子反应方程式为
2 2
___________________________________________________________。
(5)NH VO 在空气中灼烧得VO。写出该反应的化学方程式
4 3 2 5
______________________________________________________________。
【答案】(2)VO++MnO +2H+=VO++Mn2++HO (5)2NH VO ====VO+2NH ↑+HO
2 2 2 4 3 2 5 3 2
【解析】(2)“酸浸”时,MnO 将VO+转化为VO+,V元素的化合价由+3价升至+5价,MnO 被还原
2 2 2
成Mn2+,Mn元素的化合价由+4价降至+2价,根据得失电子守恒、原子守恒和电荷守恒,反应的离子方程式
为VO++MnO +2H+=VO++Mn2++HO;(5)NH VO 在空气中灼烧得VO、NH 和HO,化学方程式为
2 2 2 4 3 2 5 3 2
2NH VO ====VO+2NH ↑+HO。
4 3 2 5 3 2
2.(2024·连云港上学期调研一)根据提供的情境书写指定反应的方程式。
一种以MnCO 为原料制取MnO 的流程如图所示,450℃,MnCO 在空气中灼烧得到三种锰的氧化物,锰
3 2 3
元素所占比例随温度变化的曲线如图所示。
(1)写出450℃,MnCO 在空气中灼烧生成主要产物的化学方程式:______________________________。
3
(2)写出“浸取”时MnO 发生反应的离子方程式:______________________________________。
2 3
【答案】(1)2MnCO +O======2MnO +2CO (2)MnO+2H+=MnO +Mn2++HO
3 2 2 2 2 3 2 2
【解析】由题给流程可知,碳酸锰在空气中灼烧分解生成三氧化二锰和二氧化碳,向三氧化二锰中加入稀
10
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找硫酸浸取,三氧化二锰转化为二氧化锰和硫酸锰,过滤得到硫酸锰溶液和二氧化锰。
(1)由图可知,450℃时,二氧化锰的锰元素所占比例最大,说明碳酸锰在空气中灼烧分解生成二氧化锰
和二氧化碳,反应的化学方程式为2MnCO +O======2MnO +2CO,故答案为:2MnCO +O======2MnO +
3 2 2 2 3 2 2
2CO;(2)由分析可知,浸取时发生的反应为三氧化二锰与稀硫酸反应生成二氧化锰和硫酸锰,反应的离子
2
方程式为MnO+2H+=MnO +Mn2++HO,故答案为:MnO+2H+=MnO +Mn2++HO。
2 3 2 2 2 3 2 2
3.(2024·江苏南京市、盐城市一模)“碳中和”目标如期实现的关键技术之一是CO 的再资源化利用。
2
(2)XO基掺杂NaCO 形成XO-NaCO(X=Mg、Ca、Cd等),能用于捕获CO,原理如下图所示。已
2 3 2 3 2
知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
①X=Ca时,再生的化学方程式为__________________________________________。
②X=Mg相比X=Ca,其优点有______________________________________________________________。
【答案】①NaCa(CO)====CaO+NaCO+CO↑ ②等质量的MgO和CaO相比,MgO吸收的CO 的量
2 3 2 2 3 2 2
多;Ca2+和Mg2+电荷数相等、Mg2+半径小,再生时MgCO 分解温度低,更节能
3
【解析】(2)① X=Ca 时,NaCa(CO) 加热生成 CaO-NaCO 和 CO ,再生的化学方程式为
2 3 2 2 3 2
NaCa(CO)====CaO-NaCO +CO↑,故答案为NaCa(CO)====CaO-NaCO +CO↑;②已知阳离子电荷
2 3 2 2 3 2 2 3 2 2 3 2
数越高、半径越小,阴离子越易受其影响而分解,所以X=Mg相比X=Ca,其优点有等质量的MgO和CaO相
比,MgO吸收的CO 的量多;Ca2+和Mg2+电荷数相等、Mg2+半径小,再生时MgCO 分解温度低,更节能,故
2 3
答案为等质量的MgO和CaO相比,MgO吸收的CO 的量多;Ca2+和Mg2+电荷数相等、Mg2+半径小,再生时
2
MgCO 分解温度低,更节能。
3
4.(2024·无锡上学期期中)工业上可电解MnSO 溶液制备电池用高纯MnO 。
4 2
(1)MnSO 溶液的制备
4
利用菱锰矿粉(主要成分为MnCO,还含有少量FeCO、Al O、CoO、SiO 等杂质)制备MnSO 溶液的流程
3 3 2 3 2 4
如下:
已知:25℃时,K [(Mn(OH))]=2.0×10-13,K (CoS)=4.0×10-21,K (MnS)=2.5×10-13。在本实验条件下
sp 2 sp sp
Co2+不能被MnO 氧化。
2
①“酸浸”过程中加入过量硫酸的目的是_______________________________________________________。
②“氧化”过程中发生反应的离子方程式为_______________________________________________。
③“除钴”过程中加入过量的难溶电解质MnS,所得悬浊液中=___________。
【答案】①使碳酸锰完全溶解,防止Mn2+水解 ②MnO +2Fe2++4H+=2Fe3++Mn2++2HO
2 2
③1.6×10-8
【解析】制备硫酸锰的流程中,第一步酸浸过程中二氧化硅不溶于硫酸,滤液中含Mn2+、Fe2+、Co2+、
Al3+,二氧化锰固体将Fe2+氧化为Fe3+,石灰乳是Fe3+、Al3+沉淀为氢氧化铁和氢氧化铝,硫化锰固体将Co2+
沉淀为CoS。
①过量硫酸的目的是使碳酸锰完全溶解,防止Mn2+水解;②二氧化锰可以将Fe2+氧化为Fe3+,离子方程式
为MnO +2Fe2++4H+=2Fe3++Mn2++2HO;③===1.6×10-8。
2 2
5.(2023·江苏南京市高三学期调研)MnSO 可用于制备多种物质。
4
由MnSO 制备CuMnO 催化剂。
4 x
①基态Mn2+的价电子排布式为___________;SO 2-的空间结构为__________________。
4
②将一定量KMnO 和MnSO 固体投入超纯水中混合搅拌,在120℃下反应10小时,得到黑色固体MnO ,
4 4 2微专题突破3 新情景下方程式的书写 问题的态度:问则少;辩则明
反应的离子方程式为___________________________________________________;再加入CuSO 和NaCO 溶液,
4 2 3
经过搅拌、陈化、造粒、干燥、煅烧等工序得到比表面积较高的催化剂。其中一种成分的晶胞结构如图所示,
每个O2-周围紧邻的Cu2+的个数为___________。
【答案】①3d5 ②正四面体形 ③3Mn2++2MnO -+2HO=====5MnO ↓+4H+ ④4
4 2 2
【解析】①锰为25号元素,失去2个电子形成基态Mn2+,基态Mn2+价电子排布式为3d5;SO 2-中心S原
4
子价层电子对数=4+=4,则中心S原子为sp3杂化,其空间结构为正四面体形;②KMnO 和MnSO 加入超纯
4 4
水中得到黑色固体MnO ,反应的离子方程式为3Mn2++2MnO -+2HO=====5MnO ↓+4H+;Cu2+离子数目=
2 4 2 2
1+8×=3,O2-离子数目=8×+4×=3,每个Cu2+周围紧邻的的O2-个数为4,则每个O2-周围紧邻的Cu2+的
个数也为4。或如图 黑球表示O2-紧邻的Cu2+,晶胞中每个O2-周围紧邻的Cu2+的个数为
4。
12
细节决定成败 目标成就未来 找找找找找找找找找找找找找找找找找找找找
找找