文档内容
押新高考卷第 11-12 题
微型实验、微型工艺流程、晶胞分析与计算
核心考点 考情统计 考向预测
2023·福建卷,7 结合文字叙述或实验装置,考查物质的检验、物质的制备、
2023·湖北卷,8 性质的验证、化学性质递变规律与化学反应规律的研究、化
微型实验
2023·湖北卷, 学常见仪器的使用、物质的分离除杂提纯过程中的方法、试
13 剂的选择与操作、实验方案的设计与评价等
2023·福建卷,6
2023·辽宁卷, 选择题中的微型工艺流程题常以工艺流程图为载体,考查元
10 素化合物、化学实验、氧化还原反应等知识点,常涉及滤
微型工艺流
2023·山东卷, 渣、滤液的成分判断、pH的调节范围、可循环利用的物
程
13 质、物质的分离和提纯操作方法、反应条件的选取、氧化还
2023·河北卷, 原反应的计算等
10
2023·重庆卷,9
2023·河北卷,11
根据所给晶胞结构进行分析、推断和计算,常涉及晶体类型
2023·辽宁卷,
晶胞分析与 判断、均摊法求晶体的化学式;配位数;晶体熔沸点比较及
14
计算 原因解释;晶体密度、晶胞粒子间距、微粒半径、晶胞粒子
2023·湖北卷,
分数坐标、空间利用率等的计算
15
2023·湖南卷,11
考点一 微型实验
1.(2023·福建卷)从苯甲醛和 溶液反应后的混合液中分离出苯甲醇和苯甲酸的过程如下:已知甲基叔丁基醚的密度为 。下列说法错误的是
A.“萃取”过程需振荡、放气、静置分层
B.“有机层”从分液漏斗上口倒出
C.“操作X”为蒸馏,“试剂Y”可选用盐酸
D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
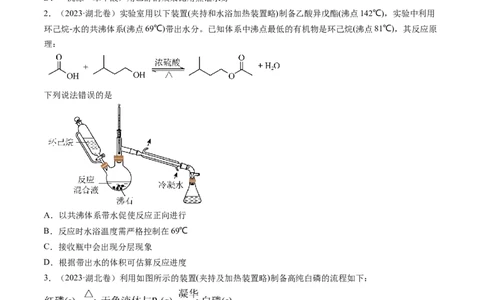
2.(2023·湖北卷)实验室用以下装置(夹持和水浴加热装置略)制备乙酸异戊酯(沸点142℃),实验中利用
环己烷-水的共沸体系(沸点69℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点81℃),其反应原
理:
下列说法错误的是
A.以共沸体系带水促使反应正向进行
B.反应时水浴温度需严格控制在69℃
C.接收瓶中会出现分层现象
D.根据带出水的体积可估算反应进度
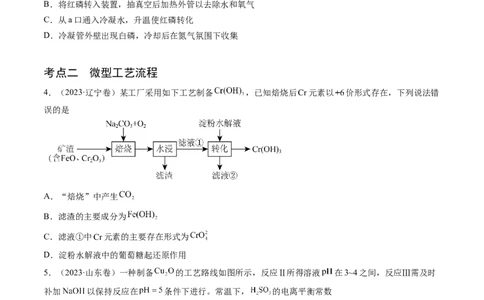
3.(2023·湖北卷)利用如图所示的装置(夹持及加热装置略)制备高纯白磷的流程如下:
下列操作错误的是A.红磷使用前洗涤以除去表面杂质
B.将红磷转入装置,抽真空后加热外管以去除水和氧气
C.从a口通入冷凝水,升温使红磷转化
D.冷凝管外壁出现白磷,冷却后在氮气氛围下收集
考点二 微型工艺流程
4.(2023·辽宁卷)某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下列说法错
误的是
A.“焙烧”中产生
B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为
D.淀粉水解液中的葡萄糖起还原作用
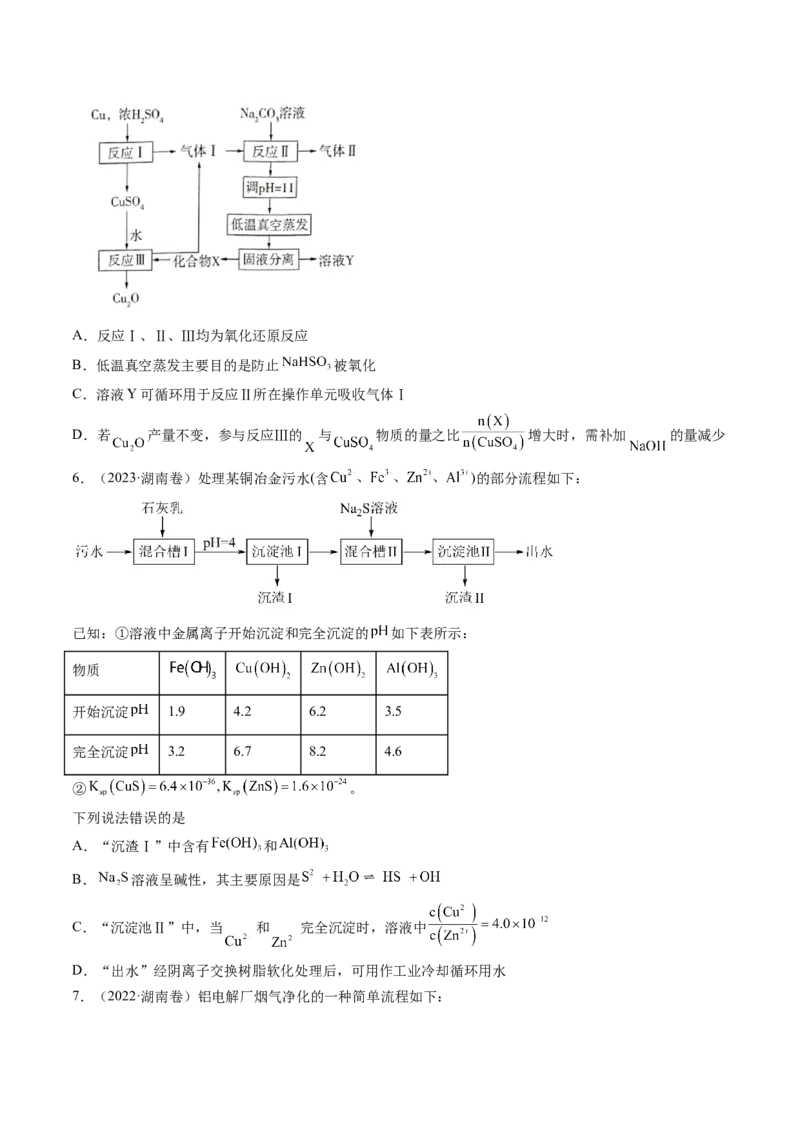
5.(2023·山东卷)一种制备 的工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及时
补加 以保持反应在 条件下进行。常温下, 的电离平衡常数
。下列说法正确的是A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.低温真空蒸发主要目的是防止 被氧化
C.溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
D.若 产量不变,参与反应Ⅲ的 与 物质的量之比 增大时,需补加 的量减少
6.(2023·湖南卷)处理某铜冶金污水(含 )的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
物质
开始沉淀 1.9 4.2 6.2 3.5
完全沉淀 3.2 6.7 8.2 4.6
② 。
下列说法错误的是
A.“沉渣Ⅰ”中含有 和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当 和 完全沉淀时,溶液中
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
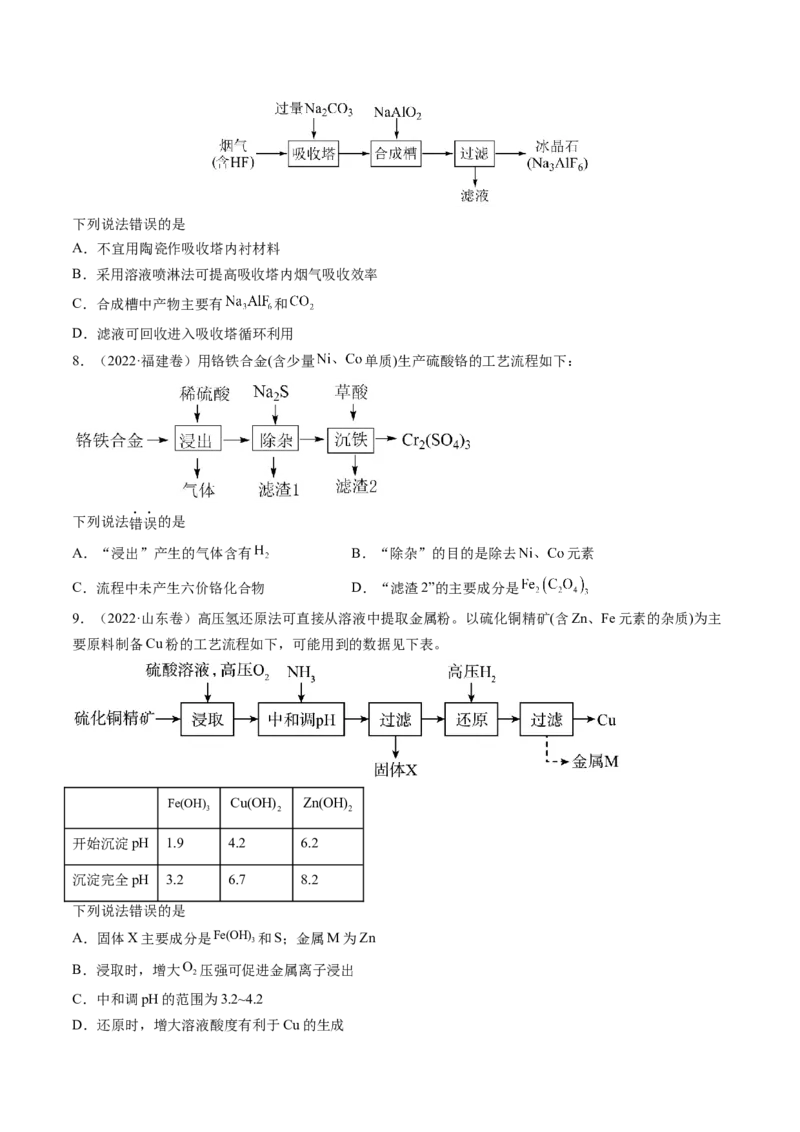
7.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:下列说法错误的是
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
8.(2022·福建卷)用铬铁合金(含少量 单质)生产硫酸铬的工艺流程如下:
下列说法错误的是
A.“浸出”产生的气体含有 B.“除杂”的目的是除去 元素
C.流程中未产生六价铬化合物 D.“滤渣2”的主要成分是
9.(2022·山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主
要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是
A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成考点三 晶胞分析与计算
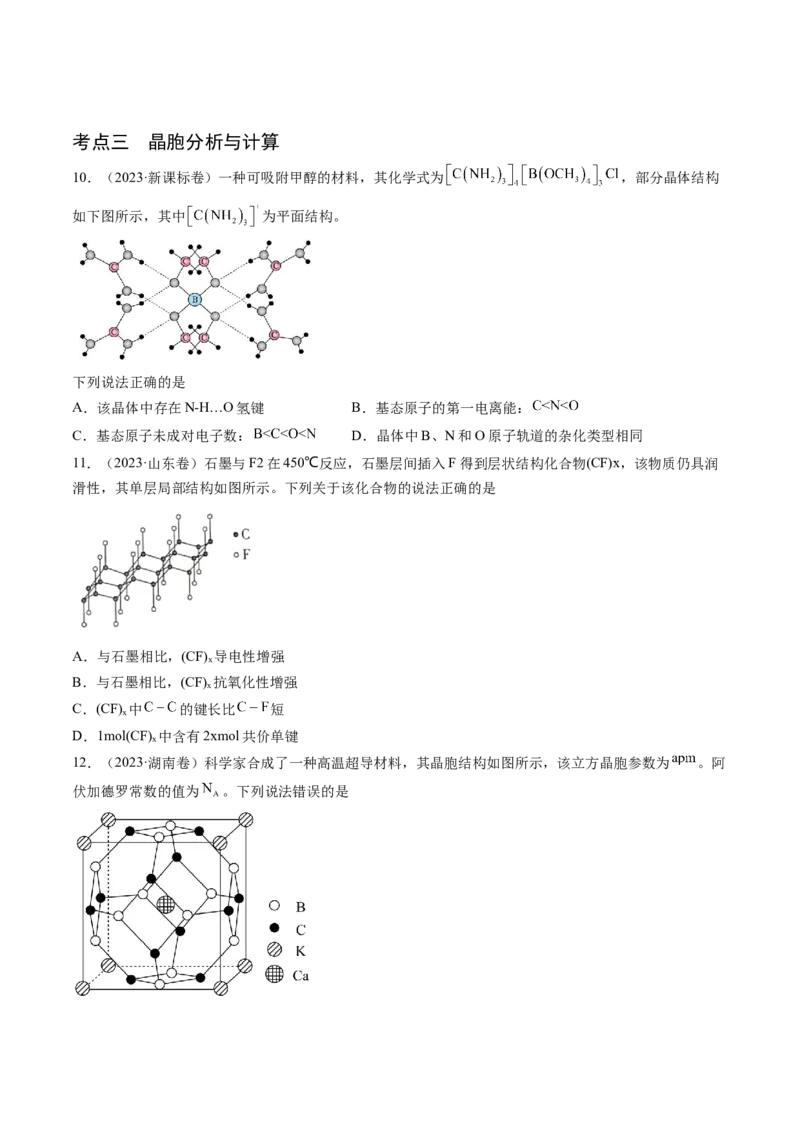
10.(2023·新课标卷)一种可吸附甲醇的材料,其化学式为 ,部分晶体结构
如下图所示,其中 为平面结构。
下列说法正确的是
A.该晶体中存在N-H…O氢键 B.基态原子的第一电离能:
C.基态原子未成对电子数: D.晶体中B、N和O原子轨道的杂化类型相同
11.(2023·山东卷)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具润
滑性,其单层局部结构如图所示。下列关于该化合物的说法正确的是
A.与石墨相比,(CF) 导电性增强
x
B.与石墨相比,(CF) 抗氧化性增强
x
C.(CF) 中 的键长比 短
x
D.1mol(CF) 中含有2xmol共价单键
x
12.(2023·湖南卷)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。阿
伏加德罗常数的值为 。下列说法错误的是A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
13.(2023·湖北卷)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重要应用。
,属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似 的
结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
14.(2023·辽宁卷)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),
进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
一、微型实验设计中易出现的7大误区
(1)进行某些易燃易爆实验时要防爆炸(如H 还原CuO时应先通H ,再加热。可燃性气体点燃前先验纯
2 2等)。
(2)防氧化(如H 还原CuO后要“先灭灯再停氢”,切割白磷宜在水中进行等)。
2
(3)防吸水(实验取用和制取易吸水、潮解、水解的物质时宜采取必要措施防止吸水,以保证达到实验目
的)。
(4)冷凝回流:有些反应中,为减少易挥发液体反应物的损耗和充分利用原料,需在反应装置上加装冷凝回
流装置(如长玻璃管、冷凝管等)。
(5)易挥发液体产物(导出时为蒸气)的及时冷却。
(6)仪器拆卸的科学性与安全性(可从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑)。
(7)其他,如实验操作顺序,试剂加入顺序等。
二、常见易错的实验操作
实验操作及现象 结论 判断 解释
结论混淆了范围:NaOH焰色反应火
一定是钠盐,该
用铂丝蘸取某溶液进行焰色 焰也是黄色,检验钾要透过蓝色钴玻
(1) 溶液中一定不含 错
反应,火焰呈黄色 璃,透过蓝色钴玻璃呈现紫色说明含
有K+
有钾元素,否则不含有
向乙醇中加入浓硫酸,加
热,溶液变黑,将产生的气 挥发的乙醇、乙烯、副反应生成的
(2) [来 该气体是乙烯 错
源:学#科#网] 体通入酸性KMnO 4 溶液,溶 SO 2 都能使酸性 KMnO 4 溶液褪色
液褪色
向溶液 X中滴加NaOH稀溶 NH 极易溶于水,在溶液中加入稀
3
(3) 液,将湿润的红色石蕊试纸 溶液X中无N 错 NaOH溶液,生成的氨水浓度小,不
置于试管口,试纸不变蓝 加热NH 不会挥发出来
3
淀粉−碘化钾试纸检验的是具有强氧
用湿润的淀粉−碘化钾试纸检
(4) 该气体是Cl 错 化性的气体,Y可能是Cl,也可能是
2 2
验气体Y,试纸变蓝
O、NO 等气体
3 2
将某气体通入品红溶液中, 该 气 体 一 定 是
(5) 错 O、Cl 也能使品红褪色
3 2
品红褪色 SO
2
溶液Y中可能含有Ag+;②若溶液Y
向溶液Y中滴加硝酸,再滴
Y 中 一 定 含 有
中含有SO2,滴加硝酸时能被氧化成
3
(6) 加BaCl 溶液,有白色沉淀生 错
成
2 SO2
4
[来源:Z*xx*k.Com] SO2 4 ,加入BaCl 2 也会有白色沉淀产
生
碳碳双键和醛基都能使酸性高锰酸钾
向 CH CHCHO 中 滴 入 该有机物中含有
2
(7) 错 褪色,故用KMnO 溶液无法证明分
4
KMnO 酸性溶液,溶液褪色 碳碳双键
4
子中含有碳碳双键
蘸有浓氨水的玻璃棒靠近溶
只要是挥发性的浓酸遇蘸有浓氨水的
(8) X一定是浓盐酸 错
液X,有白烟产生
玻璃棒都能产生白烟,浓盐酸、浓硝酸都符合
稀硫酸在淀粉水解中作催化剂,在未
在淀粉溶液中加入适量稀硫
中和硫酸的情况下加入的新制
酸微热,向水解后的溶液中
(9) 说明淀粉未水解 错 Cu(OH) 会与硫酸反应生成CuSO ,
2 4
加入新制 Cu(OH) 并加热,
2
在加热时得不到沉淀,应该先加氢氧
无砖红色沉淀
化钠中和硫酸后再加新制Cu(OH)
2
向某溶液中滴加 KSCN 溶
( 10 该溶液中一定含
液,溶液不变色,滴加氯水 正确 Fe2+的检验方法正确
) Fe2+
后溶液显红色
溴乙烷与 NaOH 溶液共热 NaOH 与 AgNO 溶液反应生成的
3
( 11 溴乙烷未发生水
后,滴加AgNO 溶液,未出 错 AgOH极不稳定,分解生成黄褐色的
3
) 解
现淡黄色沉淀 氧化银,干扰溴离子的检验
在硫酸钡沉淀中加入浓碳酸 溶解度大的容易向溶解度小的物质转
( 12 说明K (BaCO)<
sp 3
钠溶液充分搅拌后,取沉淀 错 化;但K 相近时,溶解度小的也能
sp
) K (BaSO)
sp 4
(洗净)放入盐酸中有气泡产生 向溶解度大的物质转化
三、晶体的化学式、晶体中原子的配位数、晶体类型
1.晶胞结构的分析
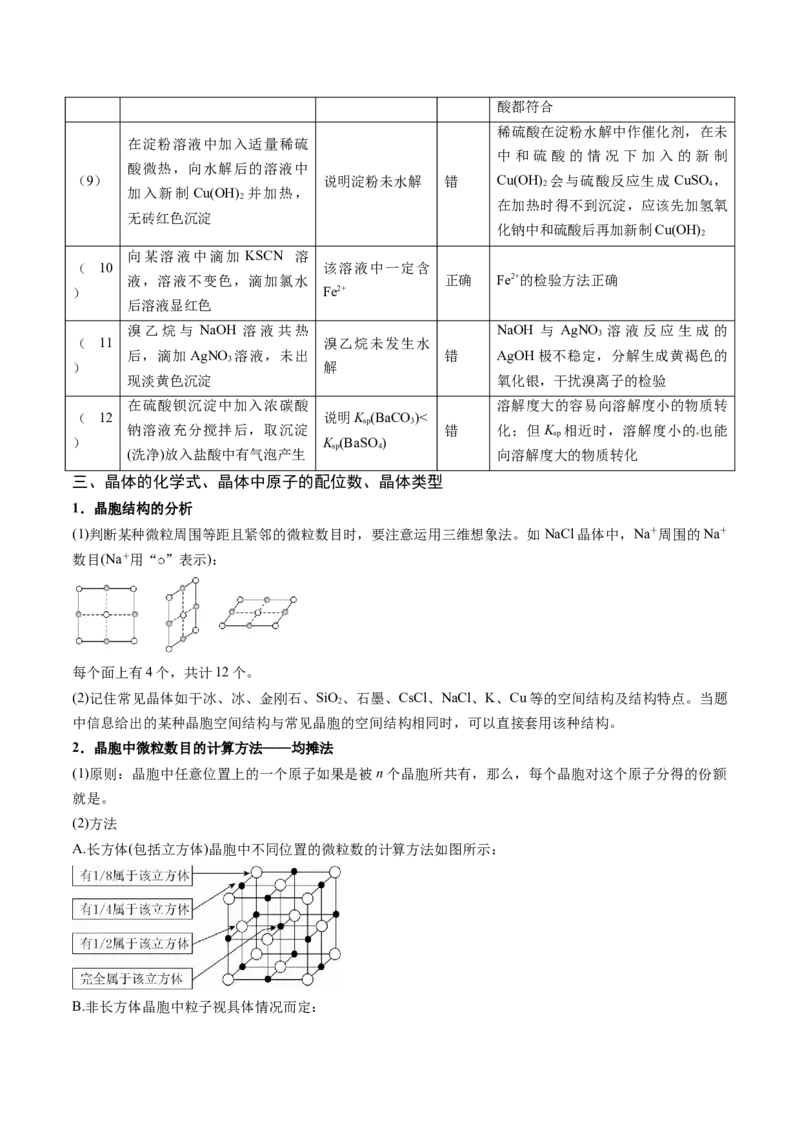
(1)判断某种微粒周围等距且紧邻的微粒数目时,要注意运用三维想象法。如NaCl晶体中,Na+周围的Na+
数目(Na+用“ ”表示):
每个面上有4个,共计12个。
(2)记住常见晶体如干冰、冰、金刚石、SiO 、石墨、CsCl、NaCl、K、Cu等的空间结构及结构特点。当题
2
中信息给出的某种晶胞空间结构与常见晶胞的空间结构相同时,可以直接套用该种结构。
2.晶胞中微粒数目的计算方法——均摊法
(1)原则:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额
就是。
(2)方法
A.长方体(包括立方体)晶胞中不同位置的微粒数的计算方法如图所示:
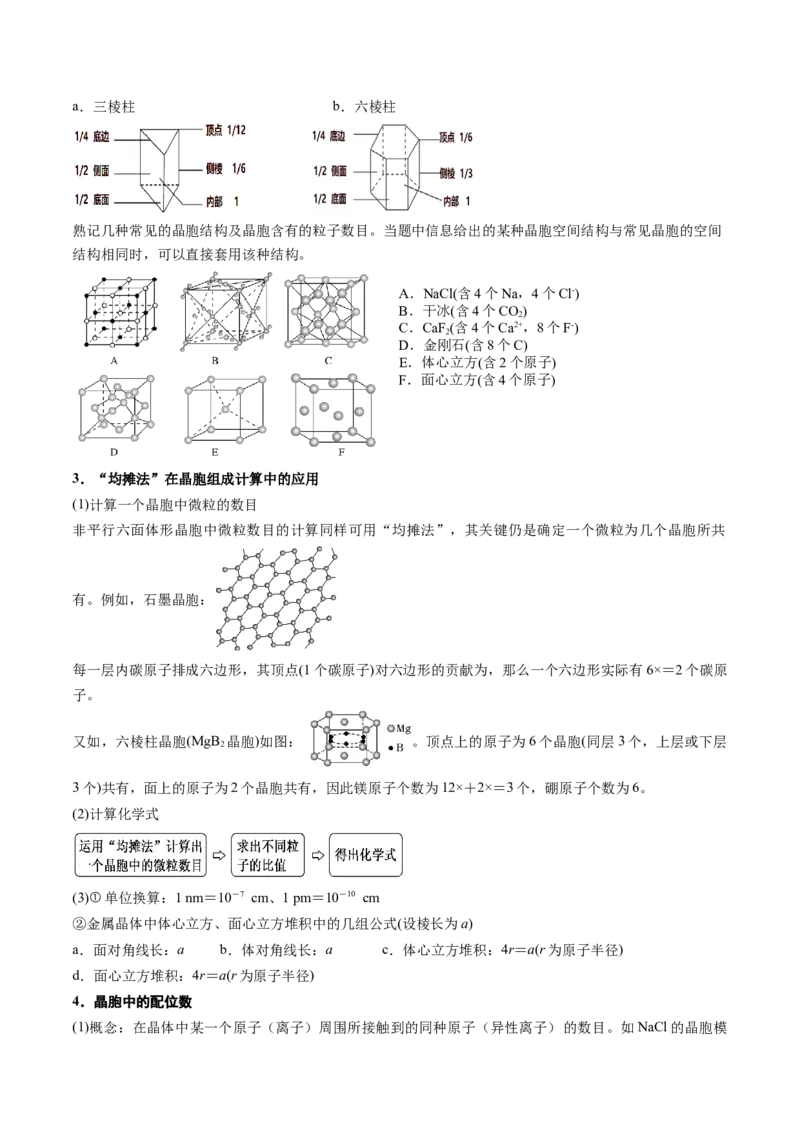
B.非长方体晶胞中粒子视具体情况而定:a.三棱柱 b.六棱柱
熟记几种常见的晶胞结构及晶胞含有的粒子数目。当题中信息给出的某种晶胞空间结构与常见晶胞的空间
结构相同时,可以直接套用该种结构。
A.NaCl(含4个Na,4个Cl-)
B.干冰(含4个CO)
2
C.CaF (含4个Ca2+,8个F-)
2
D.金刚石(含8个C)
E.体心立方(含2个原子)
F.面心立方(含4个原子)
3.“均摊法”在晶胞组成计算中的应用
(1)计算一个晶胞中微粒的数目
非平行六面体形晶胞中微粒数目的计算同样可用“均摊法”,其关键仍是确定一个微粒为几个晶胞所共
有。例如,石墨晶胞:
每一层内碳原子排成六边形,其顶点(1个碳原子)对六边形的贡献为,那么一个六边形实际有6×=2个碳原
子。
又如,六棱柱晶胞(MgB 晶胞)如图: 。顶点上的原子为6个晶胞(同层3个,上层或下层
2
3个)共有,面上的原子为2个晶胞共有,因此镁原子个数为12×+2×=3个,硼原子个数为6。
(2)计算化学式
(3)①单位换算:1 nm=10-7 cm、1 pm=10-10 cm
②金属晶体中体心立方、面心立方堆积中的几组公式(设棱长为a)
a.面对角线长:a b.体对角线长:a c.体心立方堆积:4r=a(r为原子半径)
d.面心立方堆积:4r=a(r为原子半径)
4.晶胞中的配位数
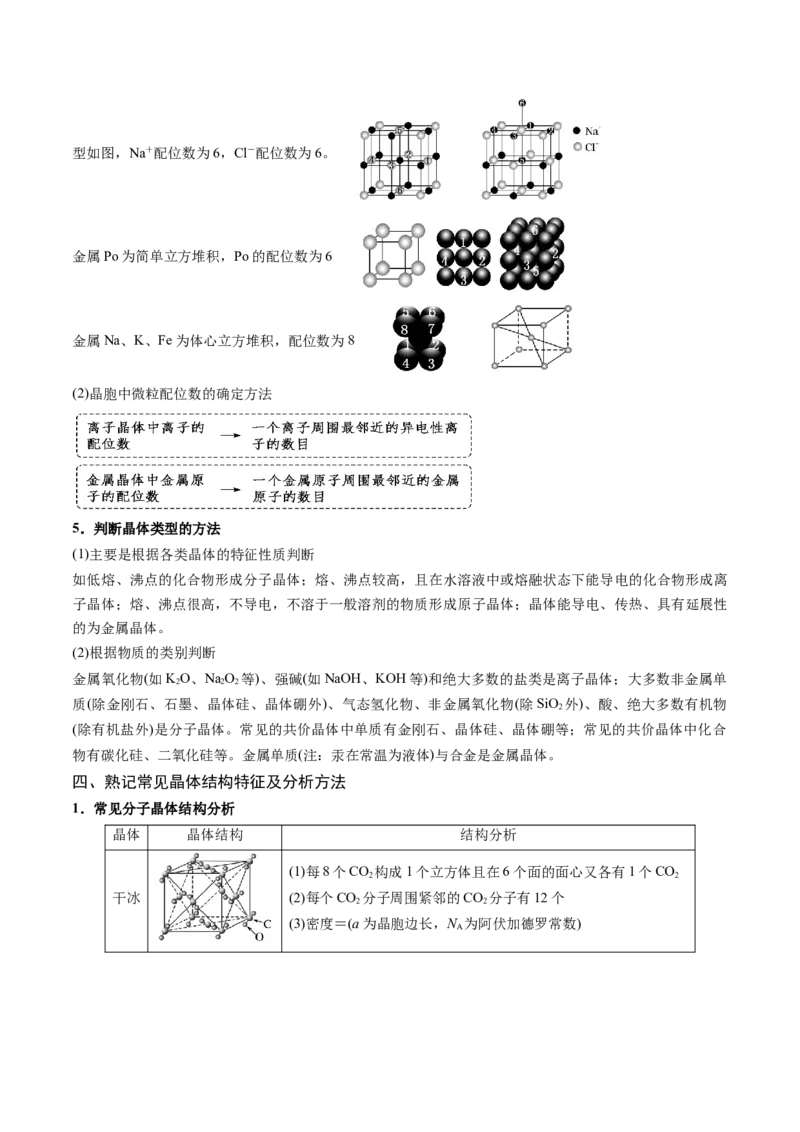
(1)概念:在晶体中某一个原子(离子)周围所接触到的同种原子(异性离子)的数目。如NaCl的晶胞模型如图,Na+配位数为6,Cl-配位数为6。
金属Po为简单立方堆积,Po的配位数为6
金属Na、K、Fe为体心立方堆积,配位数为8
(2)晶胞中微粒配位数的确定方法
5.判断晶体类型的方法
(1)主要是根据各类晶体的特征性质判断
如低熔、沸点的化合物形成分子晶体;熔、沸点较高,且在水溶液中或熔融状态下能导电的化合物形成离
子晶体;熔、沸点很高,不导电,不溶于一般溶剂的物质形成原子晶体;晶体能导电、传热、具有延展性
的为金属晶体。
(2)根据物质的类别判断
金属氧化物(如KO、NaO 等)、强碱(如NaOH、KOH等)和绝大多数的盐类是离子晶体;大多数非金属单
2 2 2
质(除金刚石、石墨、晶体硅、晶体硼外)、气态氢化物、非金属氧化物(除SiO 外)、酸、绝大多数有机物
2
(除有机盐外)是分子晶体。常见的共价晶体中单质有金刚石、晶体硅、晶体硼等;常见的共价晶体中化合
物有碳化硅、二氧化硅等。金属单质(注:汞在常温为液体)与合金是金属晶体。
四、熟记常见晶体结构特征及分析方法
1.常见分子晶体结构分析
晶体 晶体结构 结构分析
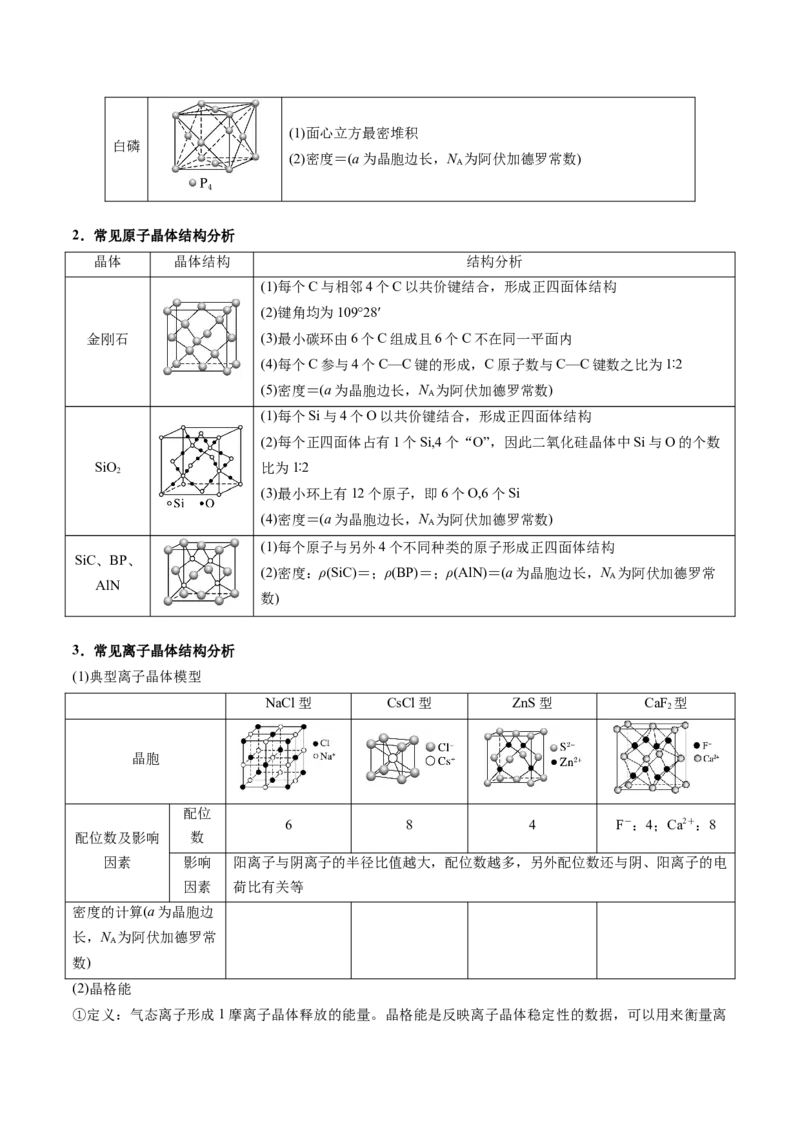
(1)每8个CO 构成1个立方体且在6个面的面心又各有1个CO
2 2
干冰 (2)每个CO 分子周围紧邻的CO 分子有12个
2 2
(3)密度=(a为晶胞边长,N 为阿伏加德罗常数)
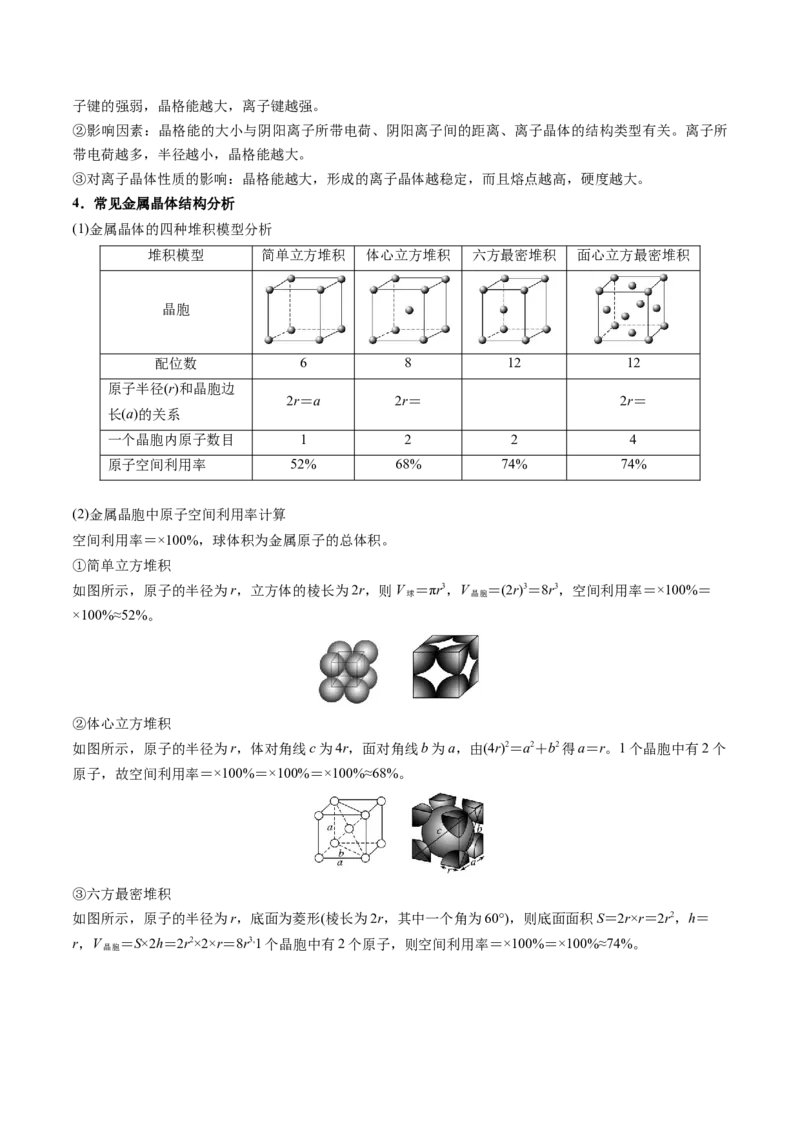
A(1)面心立方最密堆积
白磷
(2)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
2.常见原子晶体结构分析
晶体 晶体结构 结构分析
(1)每个C与相邻4个C以共价键结合,形成正四面体结构
(2)键角均为109°28′
金刚石 (3)最小碳环由6个C组成且6个C不在同一平面内
(4)每个C参与4个C—C键的形成,C原子数与C—C键数之比为1∶2
(5)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个Si与4个O以共价键结合,形成正四面体结构
(2)每个正四面体占有1个Si,4个“O”,因此二氧化硅晶体中Si与O的个数
SiO 比为1∶2
2
(3)最小环上有12个原子,即6个O,6个Si
(4)密度=(a为晶胞边长,N 为阿伏加德罗常数)
A
(1)每个原子与另外4个不同种类的原子形成正四面体结构
SiC、BP、
(2)密度:ρ(SiC)=;ρ(BP)=;ρ(AlN)=(a为晶胞边长,N 为阿伏加德罗常
A
AlN
数)
3.常见离子晶体结构分析
(1)典型离子晶体模型
NaCl型 CsCl型 ZnS型 CaF 型
2
晶胞
配位
6 8 4 F-:4;Ca2+:8
配位数及影响 数
因素 影响 阳离子与阴离子的半径比值越大,配位数越多,另外配位数还与阴、阳离子的电
因素 荷比有关等
密度的计算(a为晶胞边
长,N 为阿伏加德罗常
A
数)
(2)晶格能
①定义:气态离子形成1摩离子晶体释放的能量。晶格能是反映离子晶体稳定性的数据,可以用来衡量离子键的强弱,晶格能越大,离子键越强。
②影响因素:晶格能的大小与阴阳离子所带电荷、阴阳离子间的距离、离子晶体的结构类型有关。离子所
带电荷越多,半径越小,晶格能越大。
③对离子晶体性质的影响:晶格能越大,形成的离子晶体越稳定,而且熔点越高,硬度越大。
4.常见金属晶体结构分析
(1)金属晶体的四种堆积模型分析
堆积模型 简单立方堆积 体心立方堆积 六方最密堆积 面心立方最密堆积
晶胞
配位数 6 8 12 12
原子半径(r)和晶胞边
2r=a 2r= 2r=
长(a)的关系
一个晶胞内原子数目 1 2 2 4
原子空间利用率 52% 68% 74% 74%
(2)金属晶胞中原子空间利用率计算
空间利用率=×100%,球体积为金属原子的总体积。
①简单立方堆积
如图所示,原子的半径为r,立方体的棱长为2r,则V =πr3,V =(2r)3=8r3,空间利用率=×100%=
球 晶胞
×100%≈52%。
②体心立方堆积
如图所示,原子的半径为r,体对角线c为4r,面对角线b为a,由(4r)2=a2+b2得a=r。1个晶胞中有2个
原子,故空间利用率=×100%=×100%=×100%≈68%。
③六方最密堆积
如图所示,原子的半径为r,底面为菱形(棱长为2r,其中一个角为60°),则底面面积S=2r×r=2r2,h=
r,V =S×2h=2r2×2×r=8r3,1个晶胞中有2个原子,则空间利用率=×100%=×100%≈74%。
晶胞④面心立方最密堆积
如图所示,原子的半径为r,面对角线为4r,a=2r,V =a3=(2r)3=16r3,1个晶胞中有4个原子,则空间
晶胞
利用率=×100%=×100%≈74%。
(3)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol该晶胞中含有x mol 微粒,其质量为xM g(M为微粒的相对分子质
量);若该晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3N g,因此有xM=ρa3N 。
A A
考点一 微型实验
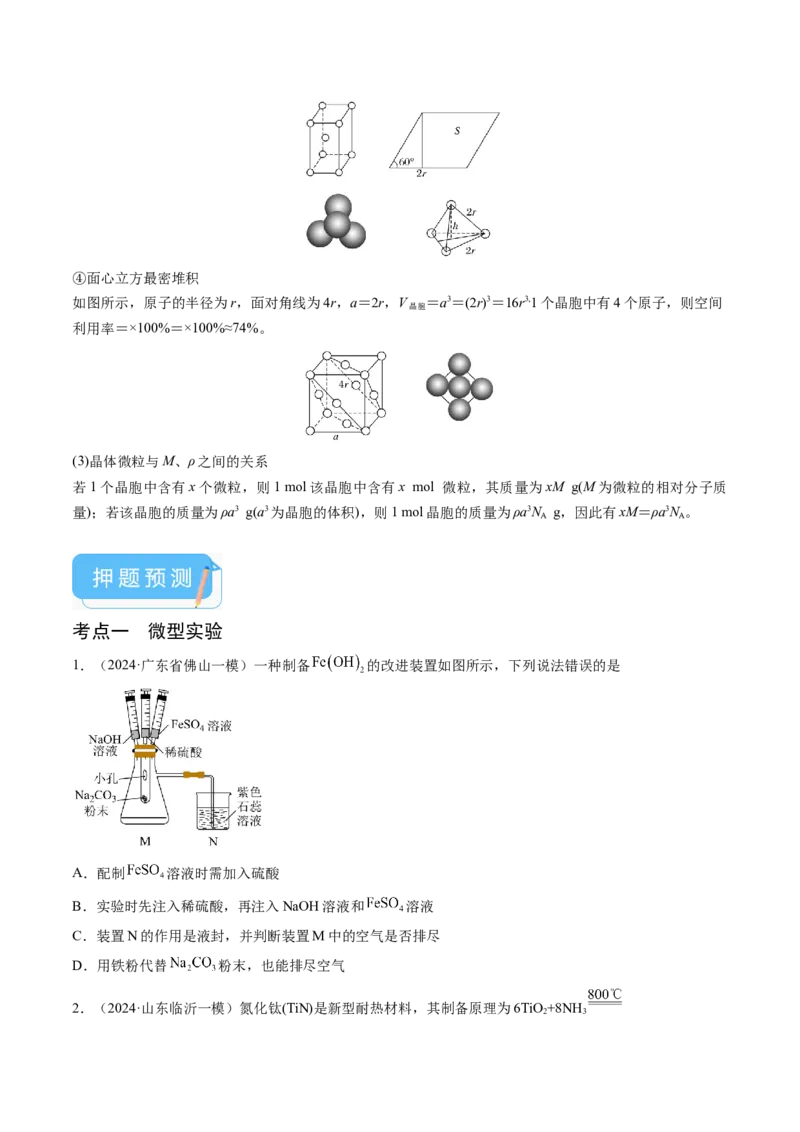
1.(2024·广东省佛山一模)一种制备 的改进装置如图所示,下列说法错误的是
A.配制 溶液时需加入硫酸
B.实验时先注入稀硫酸,再注入NaOH溶液和 溶液
C.装置N的作用是液封,并判断装置M中的空气是否排尽
D.用铁粉代替 粉末,也能排尽空气
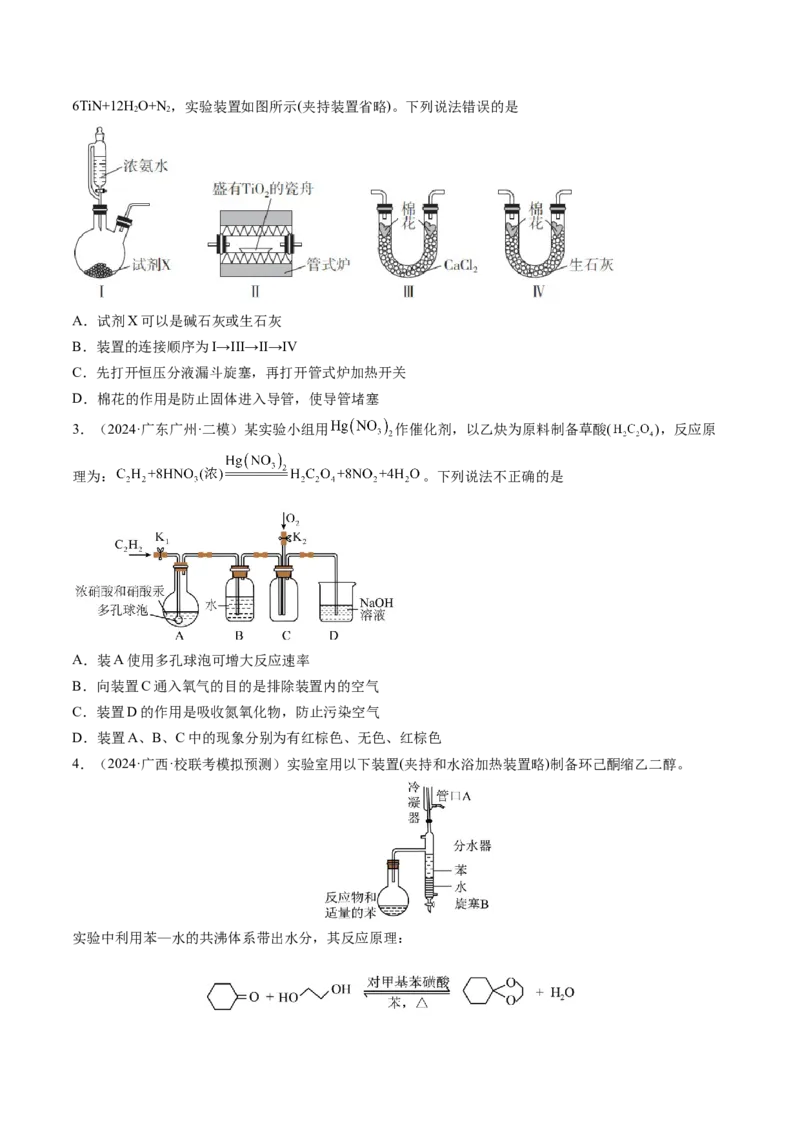
2.(2024·山东临沂一模)氮化钛(TiN)是新型耐热材料,其制备原理为6TiO+8NH
2 36TiN+12HO+N,实验装置如图所示(夹持装置省略)。下列说法错误的是
2 2
A.试剂X可以是碱石灰或生石灰
B.装置的连接顺序为I→III→II→IV
C.先打开恒压分液漏斗旋塞,再打开管式炉加热开关
D.棉花的作用是防止固体进入导管,使导管堵塞
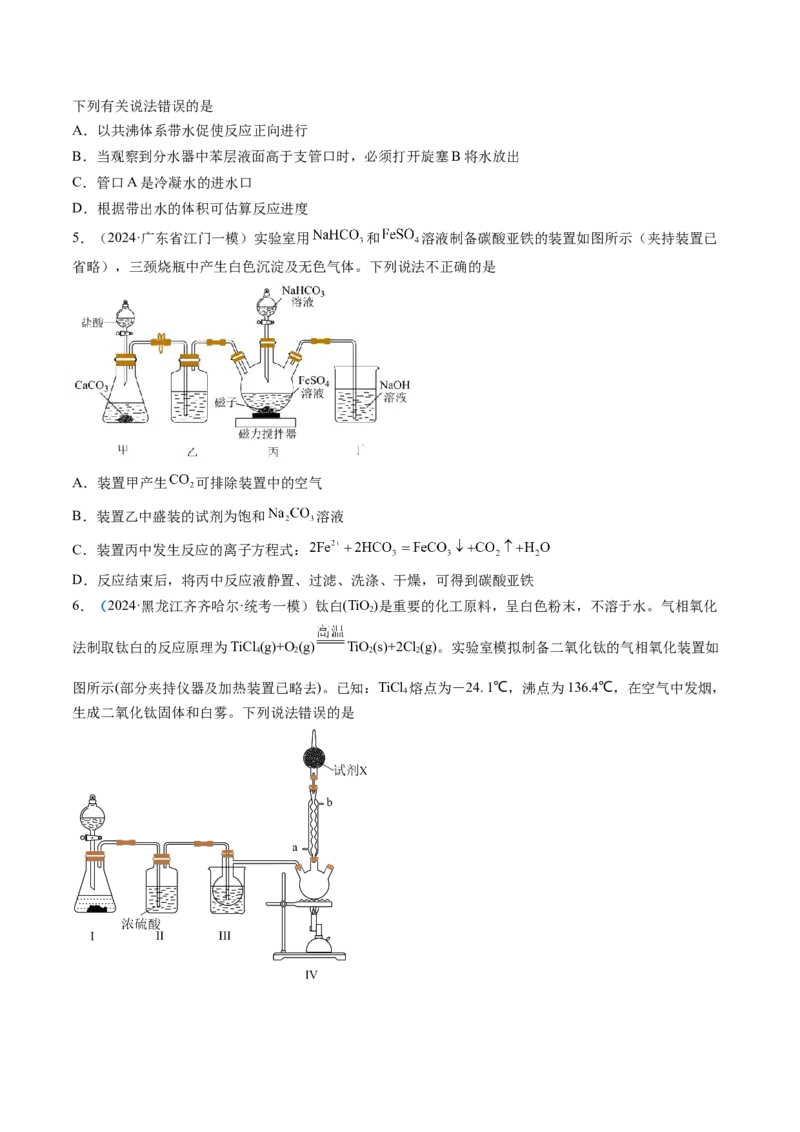
3.(2024·广东广州·二模)某实验小组用 作催化剂,以乙炔为原料制备草酸( ),反应原
理为: 。下列说法不正确的是
A.装A使用多孔球泡可增大反应速率
B.向装置C通入氧气的目的是排除装置内的空气
C.装置D的作用是吸收氮氧化物,防止污染空气
D.装置A、B、C中的现象分别为有红棕色、无色、红棕色
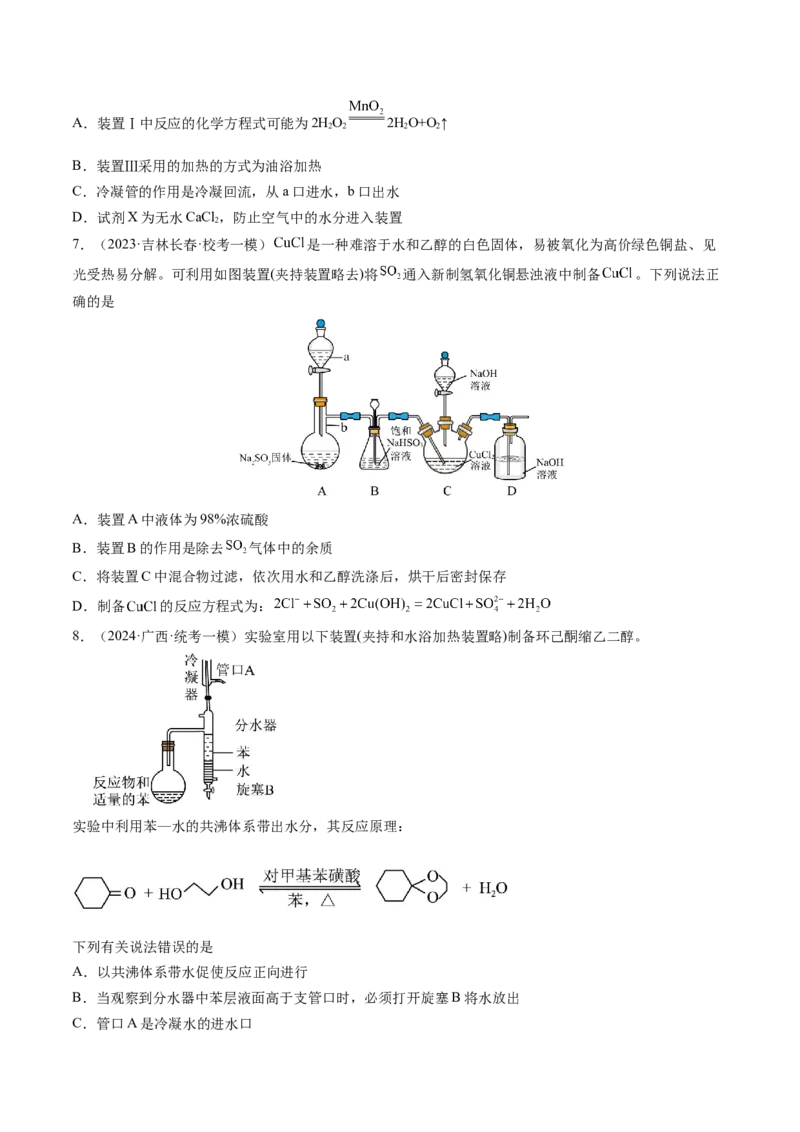
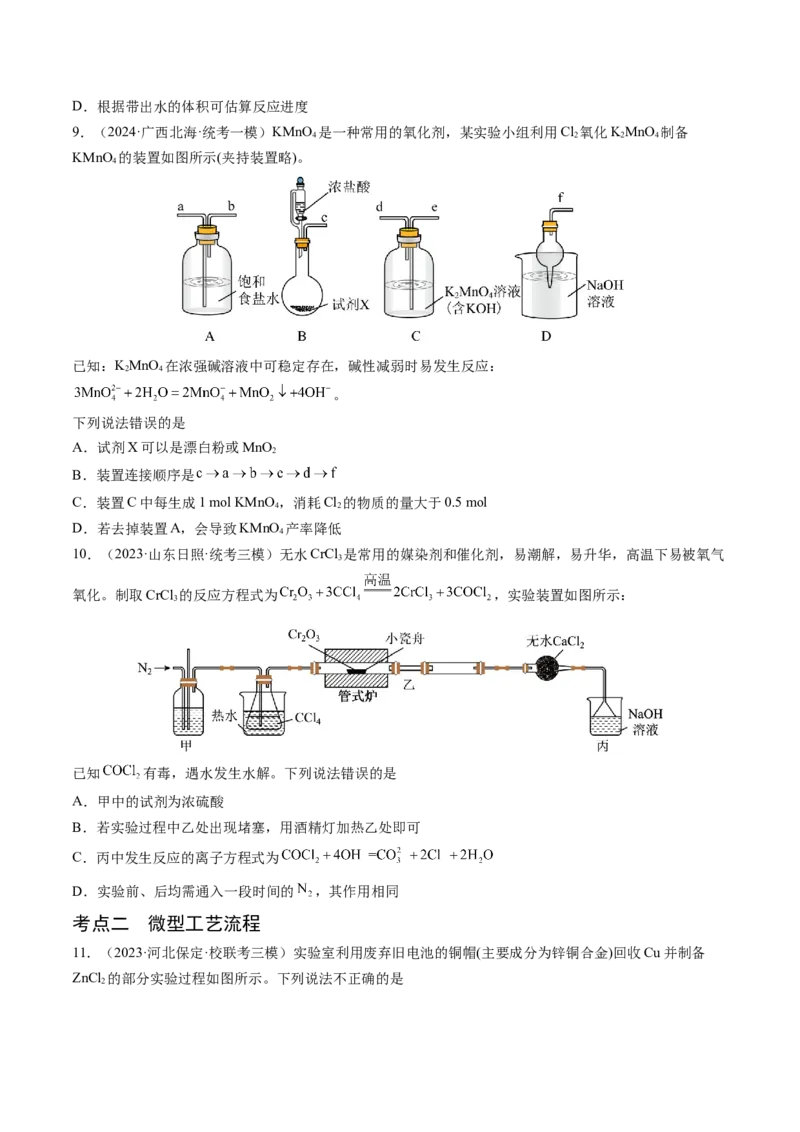
4.(2024·广西·校联考模拟预测)实验室用以下装置(夹持和水浴加热装置略)制备环己酮缩乙二醇。
实验中利用苯—水的共沸体系带出水分,其反应原理:下列有关说法错误的是
A.以共沸体系带水促使反应正向进行
B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出
C.管口A是冷凝水的进水口
D.根据带出水的体积可估算反应进度
5.(2024·广东省江门一模)实验室用 和 溶液制备碳酸亚铁的装置如图所示(夹持装置已
省略),三颈烧瓶中产生白色沉淀及无色气体。下列说法不正确的是
A.装置甲产生 可排除装置中的空气
B.装置乙中盛装的试剂为饱和 溶液
C.装置丙中发生反应的离子方程式:
D.反应结束后,将丙中反应液静置、过滤、洗涤、干燥,可得到碳酸亚铁
6.(2024·黑龙江齐齐哈尔·统考一模)钛白(TiO)是重要的化工原料,呈白色粉末,不溶于水。气相氧化
2
法制取钛白的反应原理为TiCl (g)+O(g) TiO(s)+2Cl (g)。实验室模拟制备二氧化钛的气相氧化装置如
4 2 2 2
图所示(部分夹持仪器及加热装置已略去)。已知:TiCl 熔点为-24. 1℃,沸点为136.4℃,在空气中发烟,
4
生成二氧化钛固体和白雾。下列说法错误的是A.装置Ⅰ中反应的化学方程式可能为2HO 2HO+O↑
2 2 2 2
B.装置Ⅲ采用的加热的方式为油浴加热
C.冷凝管的作用是冷凝回流,从a口进水,b口出水
D.试剂X为无水CaCl ,防止空气中的水分进入装置
2
7.(2023·吉林长春·校考一模) 是一种难溶于水和乙醇的白色固体,易被氧化为高价绿色铜盐、见
光受热易分解。可利用如图装置(夹持装置略去)将 通入新制氢氧化铜悬浊液中制备 。下列说法正
确的是
A.装置A中液体为98%浓硫酸
B.装置B的作用是除去 气体中的余质
C.将装置C中混合物过滤,依次用水和乙醇洗涤后,烘干后密封保存
D.制备 的反应方程式为:
8.(2024·广西·统考一模)实验室用以下装置(夹持和水浴加热装置略)制备环己酮缩乙二醇。
实验中利用苯—水的共沸体系带出水分,其反应原理:
下列有关说法错误的是
A.以共沸体系带水促使反应正向进行
B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出
C.管口A是冷凝水的进水口D.根据带出水的体积可估算反应进度
9.(2024·广西北海·统考一模)KMnO 是一种常用的氧化剂,某实验小组利用Cl 氧化KMnO 制备
4 2 2 4
KMnO 的装置如图所示(夹持装置略)。
4
已知:KMnO 在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
。
下列说法错误的是
A.试剂X可以是漂白粉或MnO
2
B.装置连接顺序是
C.装置C中每生成1 mol KMnO,消耗Cl 的物质的量大于0.5 mol
4 2
D.若去掉装置A,会导致KMnO 产率降低
4
10.(2023·山东日照·统考三模)无水CrCl 是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气
3
氧化。制取CrCl 的反应方程式为 ,实验装置如图所示:
3
已知 有毒,遇水发生水解。下列说法错误的是
A.甲中的试剂为浓硫酸
B.若实验过程中乙处出现堵塞,用酒精灯加热乙处即可
C.丙中发生反应的离子方程式为
D.实验前、后均需通入一段时间的 ,其作用相同
考点二 微型工艺流程
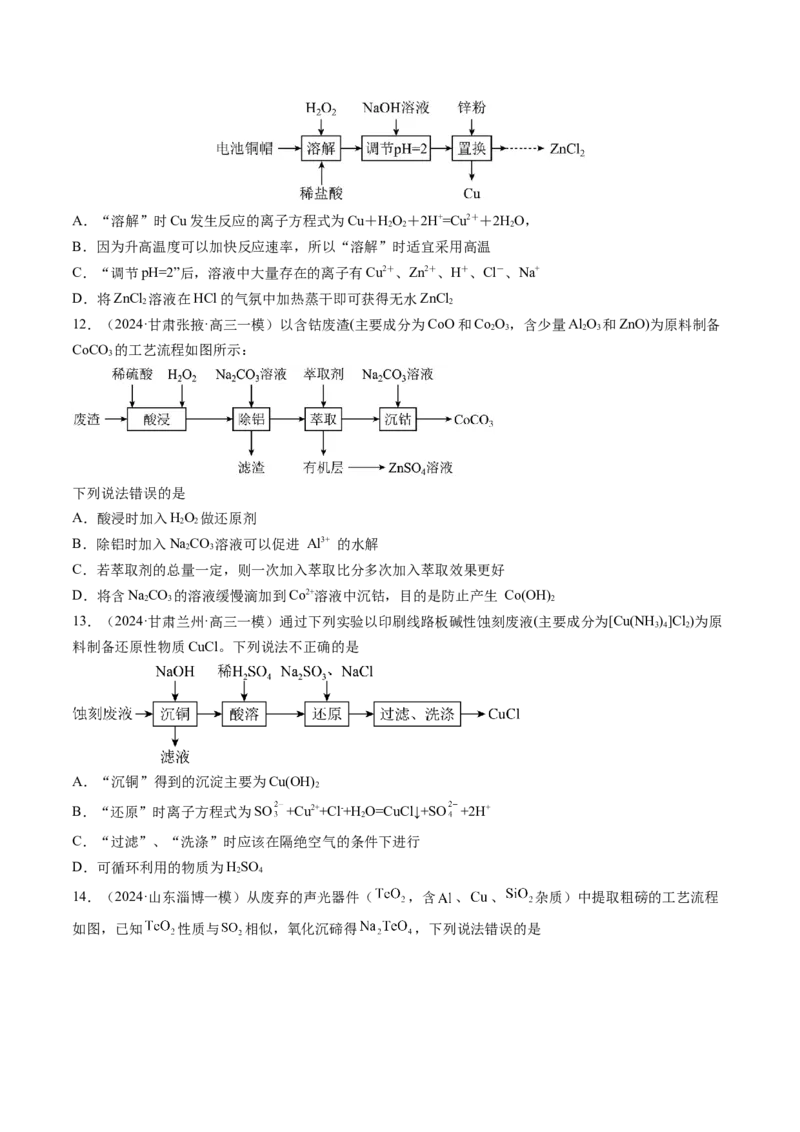
11.(2023·河北保定·校联考三模)实验室利用废弃旧电池的铜帽(主要成分为锌铜合金)回收Cu并制备
ZnCl 的部分实验过程如图所示。下列说法不正确的是
2A.“溶解”时Cu发生反应的离子方程式为Cu+HO+2H+=Cu2++2HO,
2 2 2
B.因为升高温度可以加快反应速率,所以“溶解”时适宜采用高温
C.“调节pH=2”后,溶液中大量存在的离子有Cu2+、Zn2+、H+、Cl-、Na+
D.将ZnCl 溶液在HCl的气氛中加热蒸干即可获得无水ZnCl
2 2
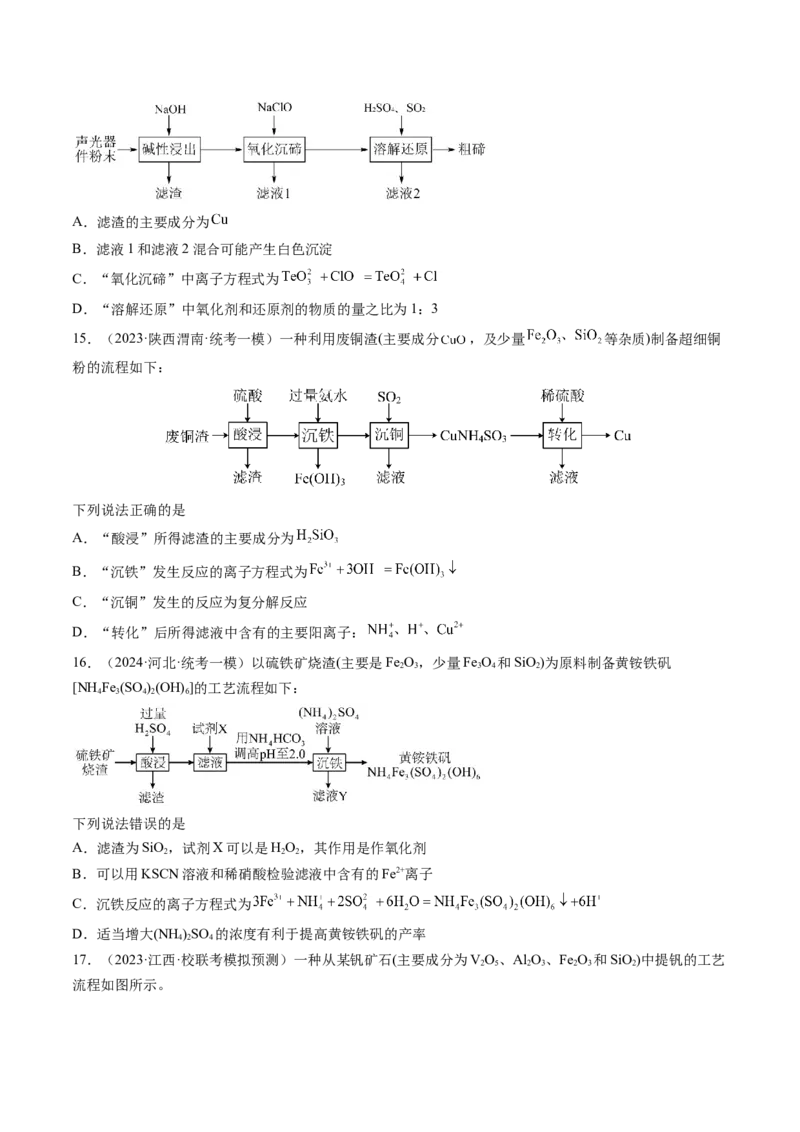
12.(2024·甘肃张掖·高三一模)以含钴废渣(主要成分为CoO和Co O,含少量Al O 和ZnO)为原料制备
2 3 2 3
CoCO 的工艺流程如图所示:
3
下列说法错误的是
A.酸浸时加入HO 做还原剂
2 2
B.除铝时加入NaCO 溶液可以促进 Al3+ 的水解
2 3
C.若萃取剂的总量一定,则一次加入萃取比分多次加入萃取效果更好
D.将含NaCO 的溶液缓慢滴加到Co2+溶液中沉钴,目的是防止产生 Co(OH)
2 3 2
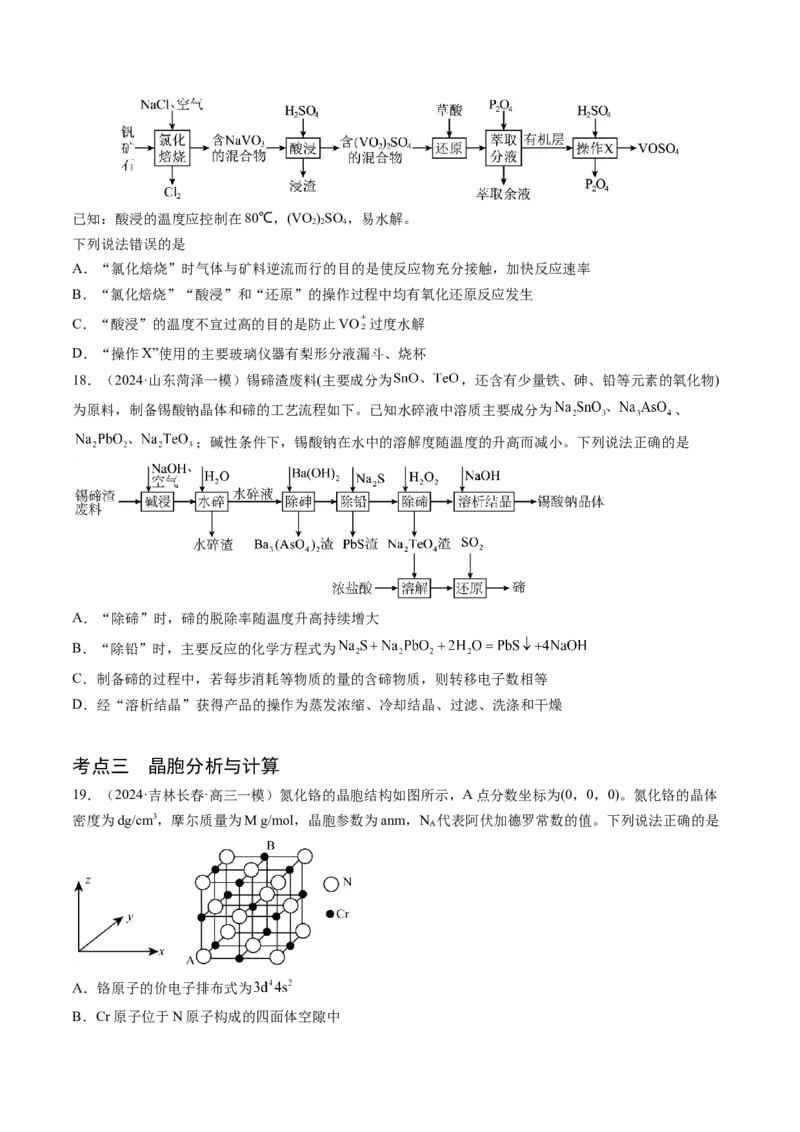
13.(2024·甘肃兰州·高三一模)通过下列实验以印刷线路板碱性蚀刻废液(主要成分为[Cu(NH )]Cl )为原
3 4 2
料制备还原性物质CuCl。下列说法不正确的是
A.“沉铜”得到的沉淀主要为Cu(OH)
2
B.“还原”时离子方程式为SO +Cu2++Cl-+H O=CuCl↓+SO +2H+
2
C.“过滤”、“洗涤”时应该在隔绝空气的条件下进行
D.可循环利用的物质为HSO
2 4
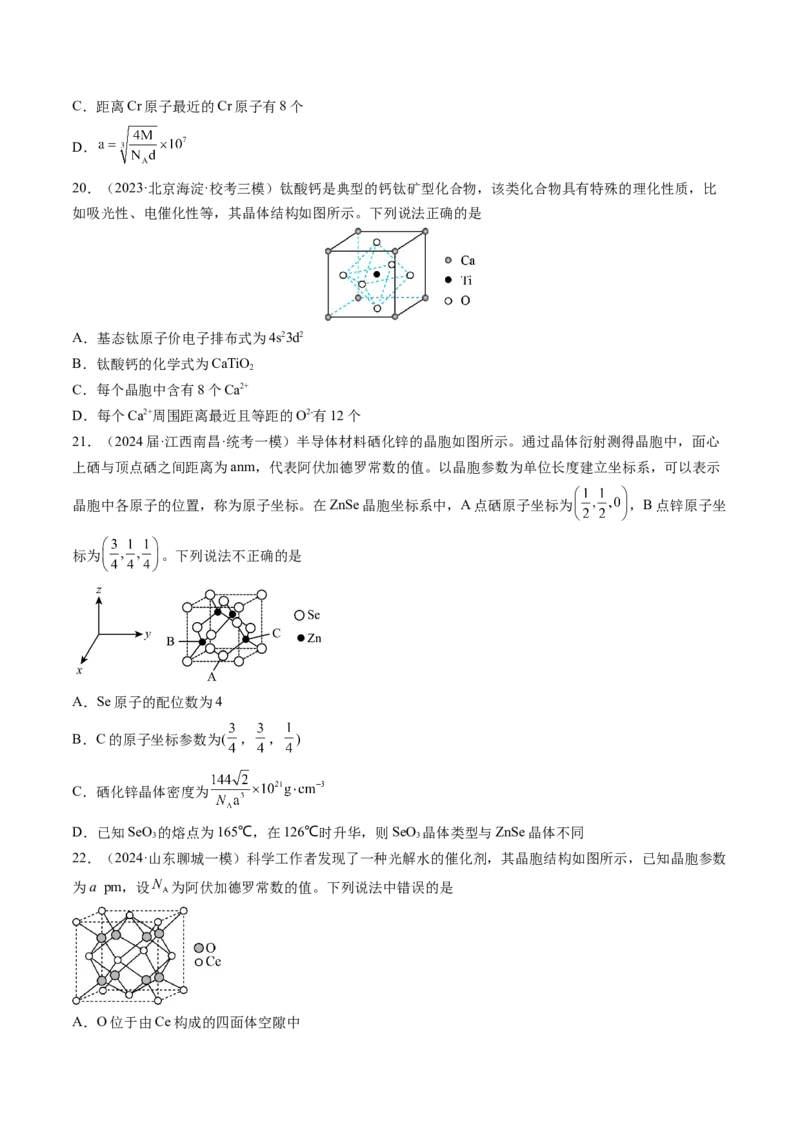
14.(2024·山东淄博一模)从废弃的声光器件( ,含 、 、 杂质)中提取粗磅的工艺流程
如图,已知 性质与 相似,氧化沉碲得 ,下列说法错误的是A.滤渣的主要成分为
B.滤液1和滤液2混合可能产生白色沉淀
C.“氧化沉碲”中离子方程式为
D.“溶解还原”中氧化剂和还原剂的物质的量之比为1:3
15.(2023·陕西渭南·统考一模)一种利用废铜渣(主要成分 ,及少量 等杂质)制备超细铜
粉的流程如下:
下列说法正确的是
A.“酸浸”所得滤渣的主要成分为
B.“沉铁”发生反应的离子方程式为
C.“沉铜”发生的反应为复分解反应
D.“转化”后所得滤液中含有的主要阳离子:
16.(2024·河北·统考一模)以硫铁矿烧渣(主要是Fe O,少量Fe O 和SiO)为原料制备黄铵铁矾
2 3 3 4 2
[NH Fe (SO )(OH) ]的工艺流程如下:
4 3 4 2 6
下列说法错误的是
A.滤渣为SiO,试剂X可以是HO,其作用是作氧化剂
2 2 2
B.可以用KSCN溶液和稀硝酸检验滤液中含有的Fe2+离子
C.沉铁反应的离子方程式为
D.适当增大(NH )SO 的浓度有利于提高黄铵铁矾的产率
4 2 4
17.(2023·江西·校联考模拟预测)一种从某钒矿石(主要成分为VO、Al O、Fe O 和SiO)中提钒的工艺
2 5 2 3 2 3 2
流程如图所示。已知:酸浸的温度应控制在80℃,(VO )SO ,易水解。
2 2 4
下列说法错误的是
A.“氯化焙烧”时气体与矿料逆流而行的目的是使反应物充分接触,加快反应速率
B.“氯化焙烧”“酸浸”和“还原”的操作过程中均有氧化还原反应发生
C.“酸浸”的温度不宜过高的目的是防止VO 过度水解
D.“操作X”使用的主要玻璃仪器有梨形分液漏斗、烧杯
18.(2024·山东菏泽一模)锡碲渣废料(主要成分为 ,还含有少量铁、砷、铅等元素的氧化物)
为原料,制备锡酸钠晶体和碲的工艺流程如下。已知水碎液中溶质主要成分为 、
;碱性条件下,锡酸钠在水中的溶解度随温度的升高而减小。下列说法正确的是
A.“除碲”时,碲的脱除率随温度升高持续增大
B.“除铅”时,主要反应的化学方程式为
C.制备碲的过程中,若每步消耗等物质的量的含碲物质,则转移电子数相等
D.经“溶析结晶”获得产品的操作为蒸发浓缩、冷却结晶、过滤、洗涤和干燥
考点三 晶胞分析与计算
19.(2024·吉林长春·高三一模)氮化铬的晶胞结构如图所示,A点分数坐标为(0,0,0)。氮化铬的晶体
密度为dg/cm3,摩尔质量为M g/mol,晶胞参数为anm,N 代表阿伏加德罗常数的值。下列说法正确的是
A
A.铬原子的价电子排布式为
B.Cr原子位于N原子构成的四面体空隙中C.距离Cr原子最近的Cr原子有8个
D.
20.(2023·北京海淀·校考三模)钛酸钙是典型的钙钛矿型化合物,该类化合物具有特殊的理化性质,比
如吸光性、电催化性等,其晶体结构如图所示。下列说法正确的是
A.基态钛原子价电子排布式为4s23d2
B.钛酸钙的化学式为CaTiO
2
C.每个晶胞中含有8个Ca2+
D.每个Ca2+周围距离最近且等距的O2-有12个
21.(2024届·江西南昌·统考一模)半导体材料硒化锌的晶胞如图所示。通过晶体衍射测得晶胞中,面心
上硒与顶点硒之间距离为anm,代表阿伏加德罗常数的值。以晶胞参数为单位长度建立坐标系,可以表示
晶胞中各原子的位置,称为原子坐标。在ZnSe晶胞坐标系中,A点硒原子坐标为 ,B点锌原子坐
标为 。下列说法不正确的是
A.Se原子的配位数为4
B.C的原子坐标参数为( , , )
C.硒化锌晶体密度为
D.已知SeO 的熔点为165℃,在126℃时升华,则SeO 晶体类型与ZnSe晶体不同
3 3
22.(2024·山东聊城一模)科学工作者发现了一种光解水的催化剂,其晶胞结构如图所示,已知晶胞参数
为a pm,设 为阿伏加德罗常数的值。下列说法中错误的是
A.O位于由Ce构成的四面体空隙中B.Ce在晶胞中的配位数为8
C.Ce与Ce最近的距离为
D.该晶体的摩尔体积
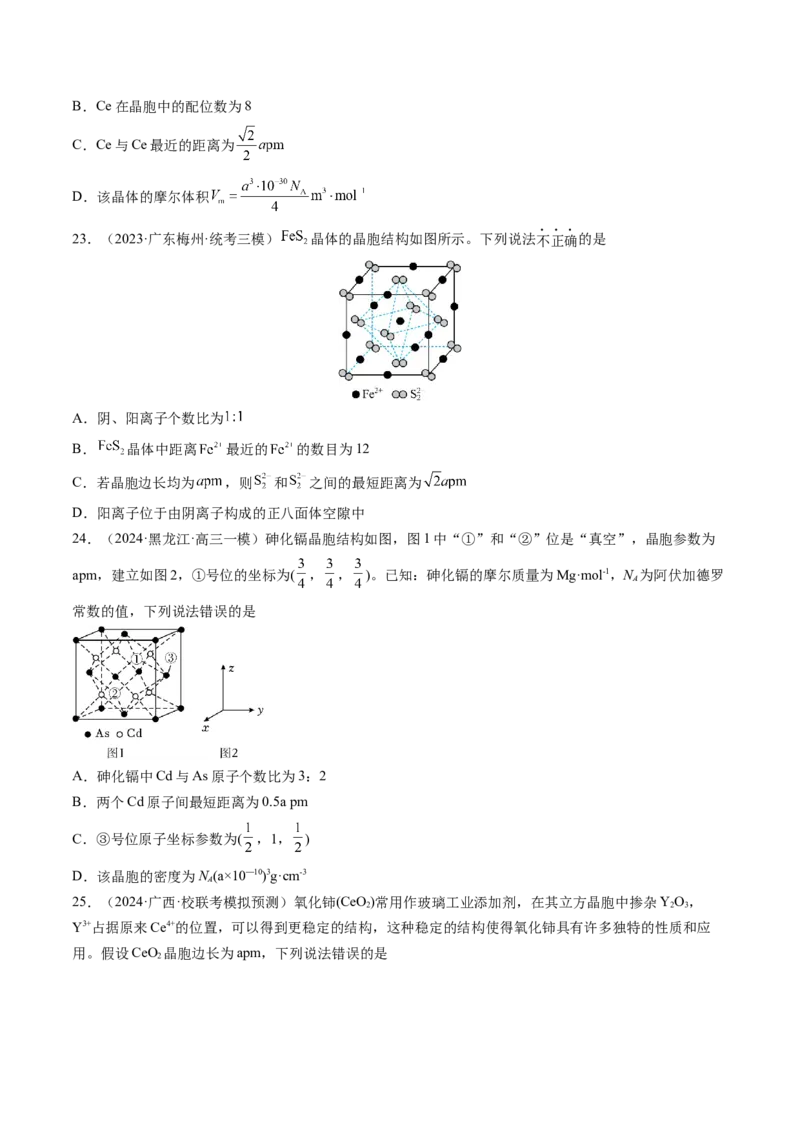
23.(2023·广东梅州·统考三模) 晶体的晶胞结构如图所示。下列说法不正确的是
A.阴、阳离子个数比为
B. 晶体中距离 最近的 的数目为12
C.若晶胞边长均为 ,则 和 之间的最短距离为
D.阳离子位于由阴离子构成的正八面体空隙中
24.(2024·黑龙江·高三一模)砷化镉晶胞结构如图,图1中“①”和“②”位是“真空”,晶胞参数为
apm,建立如图2,①号位的坐标为( , , )。已知:砷化镉的摩尔质量为Mg·mol-1,N 为阿伏加德罗
A
常数的值,下列说法错误的是
A.砷化镉中Cd与As原子个数比为3:2
B.两个Cd原子间最短距离为0.5a pm
C.③号位原子坐标参数为( ,1, )
D.该晶胞的密度为N (a×10—10)3g·cm-3
A
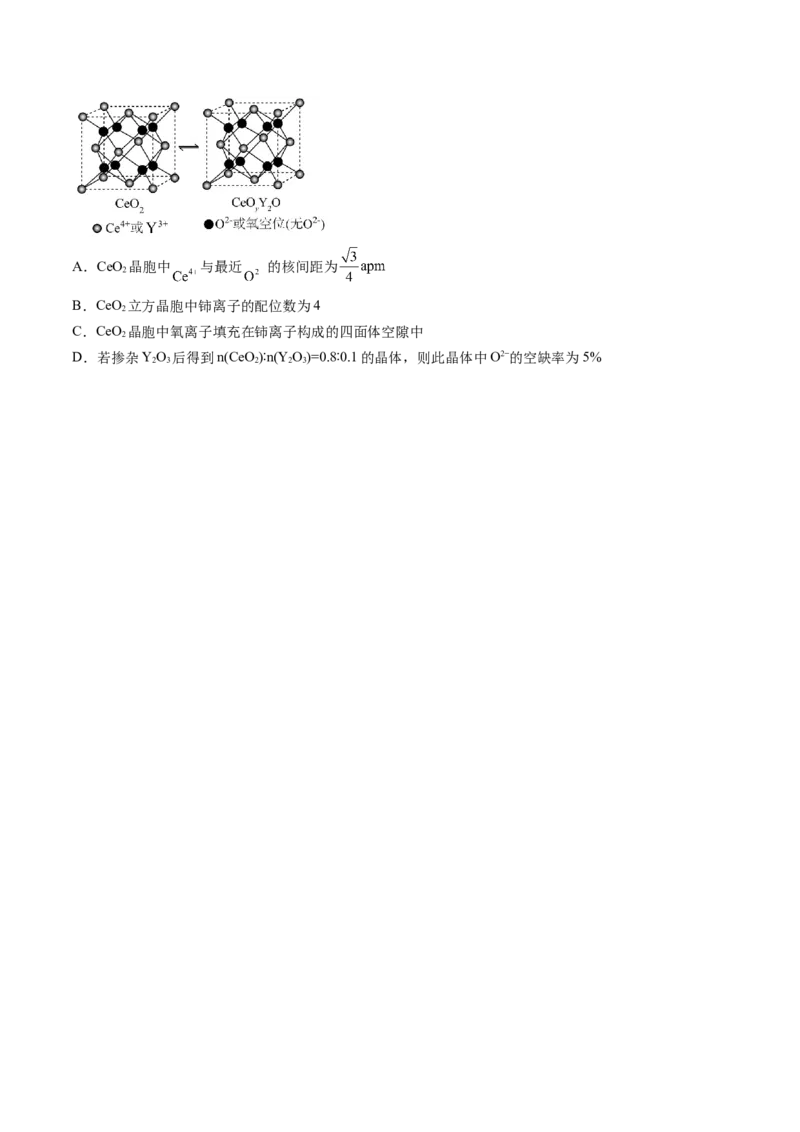
25.(2024·广西·校联考模拟预测)氧化铈(CeO)常用作玻璃工业添加剂,在其立方晶胞中掺杂YO,
2 2 3
Y3+占据原来Ce4+的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应
用。假设CeO 晶胞边长为apm,下列说法错误的是
2A.CeO 晶胞中 与最近 的核间距为
2
B.CeO 立方晶胞中铈离子的配位数为4
2
C.CeO 晶胞中氧离子填充在铈离子构成的四面体空隙中
2
D.若掺杂YO 后得到n(CeO)∶n(Y O)=0.8∶0.1的晶体,则此晶体中O2−的空缺率为5%
2 3 2 2 3