文档内容
第 10 讲 氯及其化合物
1.向新制氯水中加入少量下列物质,能增强溶液漂白能力的是( )
A.碳酸钙粉末 B.稀硫酸
C.氯化钙溶液 D.二氧化硫水溶液
2.下列关于新制氯水及久置氯水的说法,不正确的是( )
A.新制的氯水呈浅黄绿色,而久置的氯水无色
B.新制的氯水漂白作用强,而久置的氯水漂白作用很弱
C.新制的氯水所含成分多,而久置的氯水所含成分少
D.新制的氯水中无氯离子,而久置的氯水中则含氯离子
3.氯胺(NH Cl)是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的 4~5倍。
2
下列有关氯胺的说法一定不正确的是( )
A.氯胺的水解产物为NH OH(羟氨)和HCl
2
C.氯胺中氯元素的化合价为+1价
D.氯胺的消毒原理与漂白粉相似
4.下列制取Cl、探究其漂白性,收集并进行尾气处理的原理和装置合理的是( )
2
5.Cl 是一种重要的工业原料,液氯储存区贴有的说明卡如下:
2
包装 钢瓶
储运要求 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪
泄漏处理 NaOH、NaHSO 溶液吸收
3
下列解释事实的方程式不正确的是( )
A.电解饱和食盐水制取Cl:2Cl-+2HO=====2OH-+H↑+Cl↑
2 2 2 2B.氯气用于自来水消毒:Cl+HO2H++Cl-+ClO-
2 2
C.浓氨水检验泄漏的氯气,产生白烟:8NH +3Cl === 6NH Cl+N
3 2 4 2
D.氯气“泄漏处理”中NaHSO 溶液的作用:HSO+Cl+HO === SO+3H++2Cl-
3 2 2
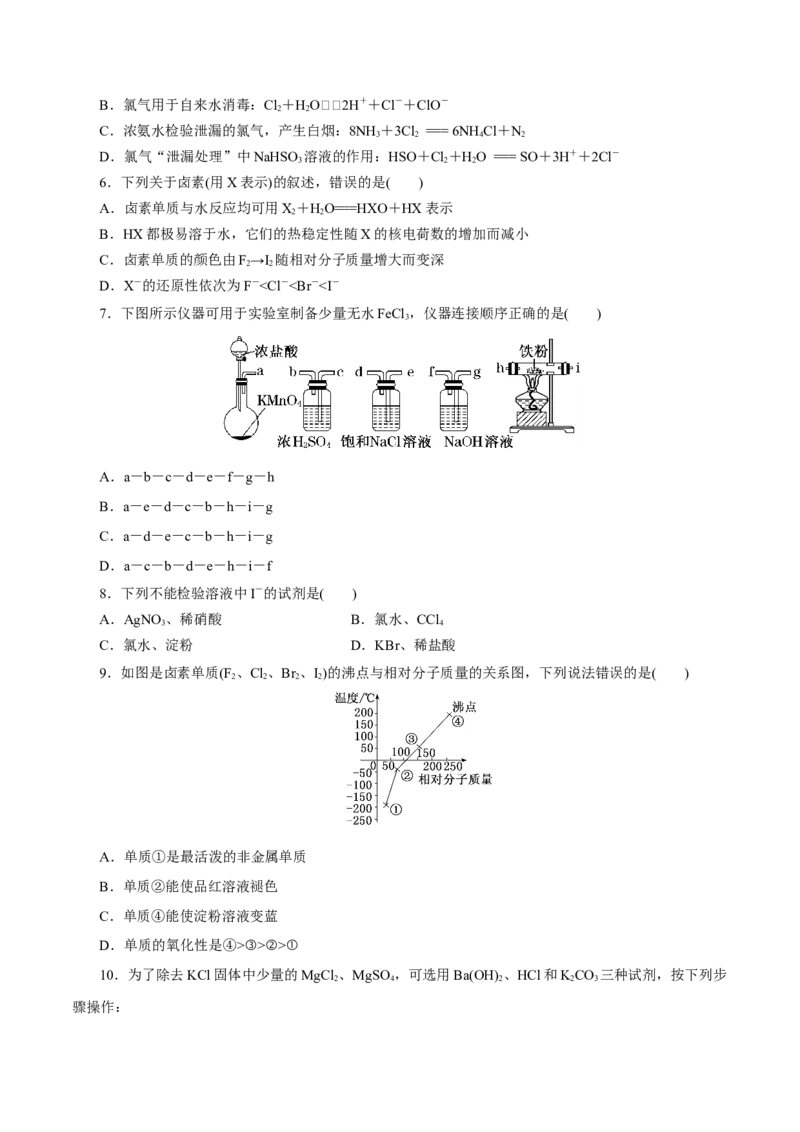
6.下列关于卤素(用X表示)的叙述,错误的是( )
A.卤素单质与水反应均可用X+HO===HXO+HX表示
2 2
B.HX都极易溶于水,它们的热稳定性随X的核电荷数的增加而减小
C.卤素单质的颜色由F→I 随相对分子质量增大而变深
2 2
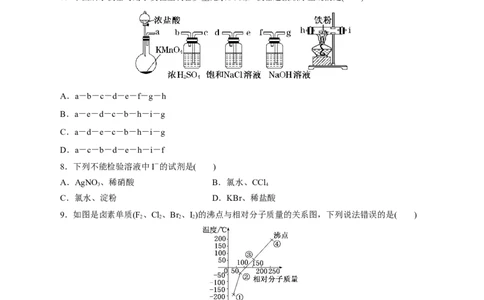
D.X-的还原性依次为F-③>②>①
10.为了除去KCl固体中少量的MgCl 、MgSO ,可选用Ba(OH) 、HCl和KCO 三种试剂,按下列步
2 4 2 2 3
骤操作:――→―――→――→――→――→――→
(1)写出三种试剂的化学式:A__________,B__________,C__________。
(2)根据题意,回答下列问题:
①加入过量A的目的是__________________________________________________;
②加入过量B的目的是_____________________________________________;
③加热煮沸的目的是___________________________________________。
(3)操作Ⅰ是__________,操作Ⅱ是__________。
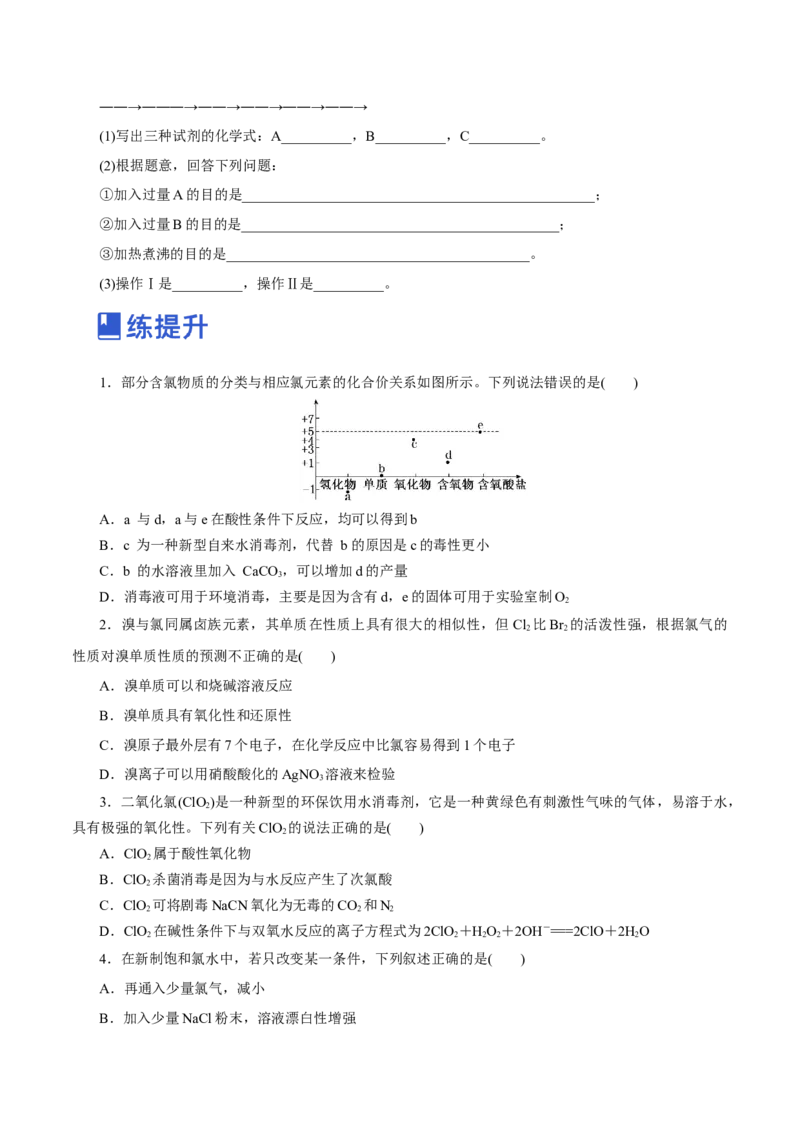
1.部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法错误的是( )
A.a 与d,a与e在酸性条件下反应,均可以得到b
B.c 为一种新型自来水消毒剂,代替 b的原因是c的毒性更小
C.b 的水溶液里加入 CaCO ,可以增加d的产量
3
D.消毒液可用于环境消毒,主要是因为含有d,e的固体可用于实验室制O
2
2.溴与氯同属卤族元素,其单质在性质上具有很大的相似性,但Cl 比Br 的活泼性强,根据氯气的
2 2
性质对溴单质性质的预测不正确的是( )
A.溴单质可以和烧碱溶液反应
B.溴单质具有氧化性和还原性
C.溴原子最外层有7个电子,在化学反应中比氯容易得到1个电子
D.溴离子可以用硝酸酸化的AgNO 溶液来检验
3
3.二氧化氯(ClO )是一种新型的环保饮用水消毒剂,它是一种黄绿色有刺激性气味的气体,易溶于水,
2
具有极强的氧化性。下列有关ClO 的说法正确的是( )
2
A.ClO 属于酸性氧化物
2
B.ClO 杀菌消毒是因为与水反应产生了次氯酸
2
C.ClO 可将剧毒NaCN氧化为无毒的CO 和N
2 2 2
D.ClO 在碱性条件下与双氧水反应的离子方程式为2ClO +HO+2OH-===2ClO+2HO
2 2 2 2 2
4.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,减小
B.加入少量NaCl粉末,溶液漂白性增强C.加入少量的碳酸钠粉末,pH增大,溶液漂白性增强
D.光照过程中,有气泡冒出,溶液的导电性减弱
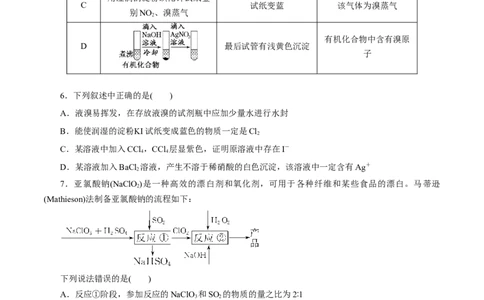
5.下列实验操作、现象和结论均正确的是( )
选项 实验操作 现象 结论
A 用双氧水滴定淀粉KI溶液 溶液变蓝 达到滴定终点
向食用加碘盐中加入食醋和
该食用加碘盐中含有
B KI溶液,再加入CCl 振荡, 下层呈紫红色
4
KIO
3
静置
用湿润的淀粉碘化钾试纸鉴
C 试纸变蓝 该气体为溴蒸气
别NO 、溴蒸气
2
有机化合物中含有溴原
D 最后试管有浅黄色沉淀
子
6.下列叙述中正确的是( )
A.液溴易挥发,在存放液溴的试剂瓶中应加少量水进行水封
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl
2
C.某溶液中加入CCl ,CCl 层显紫色,证明原溶液中存在I-
4 4
D.某溶液加入BaCl 溶液,产生不溶于稀硝酸的白色沉淀,该溶液中一定含有Ag+
2
7.亚氯酸钠(NaClO)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊
2
(Mathieson)法制备亚氯酸钠的流程如下:
下列说法错误的是( )
A.反应①阶段,参加反应的NaClO 和SO 的物质的量之比为2∶1
3 2
B.若反应①通过原电池来实现,则ClO 是正极产物
2
C.反应②中的HO 可用NaClO 代替
2 2 4
D.反应②条件下,ClO 的氧化性大于HO
2 2 2
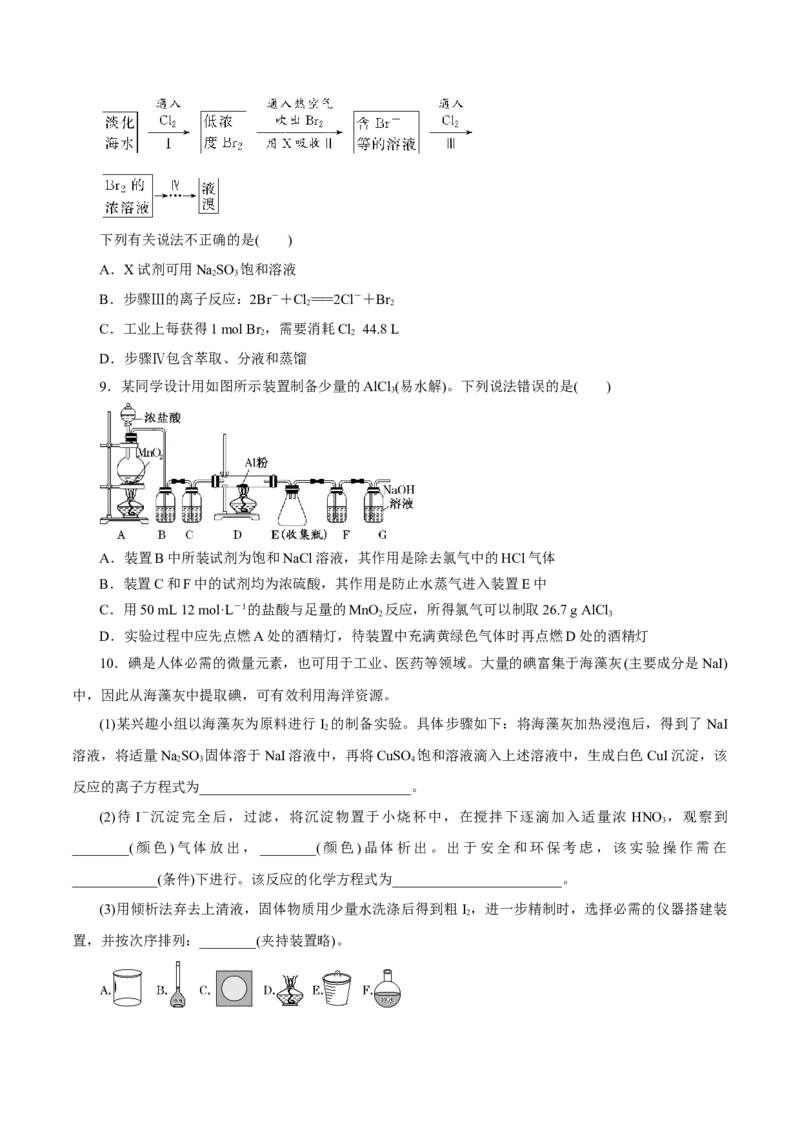
8.从淡化海水中提取溴的流程如下:下列有关说法不正确的是( )
A.X试剂可用NaSO 饱和溶液
2 3
B.步骤Ⅲ的离子反应:2Br-+Cl===2Cl-+Br
2 2
C.工业上每获得1 mol Br ,需要消耗Cl 44.8 L
2 2
D.步骤Ⅳ包含萃取、分液和蒸馏
9.某同学设计用如图所示装置制备少量的AlCl (易水解)。下列说法错误的是( )
3
A.装置B中所装试剂为饱和NaCl溶液,其作用是除去氯气中的HCl气体
B.装置C和F中的试剂均为浓硫酸,其作用是防止水蒸气进入装置E中
C.用50 mL 12 mol·L-1的盐酸与足量的MnO 反应,所得氯气可以制取26.7 g AlCl
2 3
D.实验过程中应先点燃A处的酒精灯,待装置中充满黄绿色气体时再点燃D处的酒精灯
10.碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰(主要成分是NaI)
中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行I 的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了 NaI
2
溶液,将适量NaSO 固体溶于NaI溶液中,再将CuSO 饱和溶液滴入上述溶液中,生成白色CuI沉淀,该
2 3 4
反应的离子方程式为______________________________。
(2)待 I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓 HNO ,观察到
3
________(颜色)气体放出,________(颜色)晶体析出。出于安全和环保考虑,该实验操作需在
____________(条件)下进行。该反应的化学方程式为________________________。
(3)用倾析法弃去上清液,固体物质用少量水洗涤后得到粗 I ,进一步精制时,选择必需的仪器搭建装
2
置,并按次序排列:________(夹持装置略)。1.(2020·浙江7月选考)黄色固体X,可能含有漂白粉、FeSO、Fe(SO)、CuCl、KI之中的几种或全部。将
4 2 4 3 2
X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )
A.X中含KI,可能含有CuCl
2
B.X中含有漂白粉和FeSO
4
C.X中含有CuCl,Y中含有Fe(OH)
2 3
D.用HSO 酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl
2 4 2
2.(2020·天津卷)在全国人民众志成城抗击新冠病毒期间,使用的“84消毒液”的主要有效成分是( )
A.NaOH B.NaCl
C.NaClO D.NaCO
2 3