文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷05
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.神舟十六号载人飞船顺利发射,我国航天航空事业再次迎来飞速发展。下列有关说法错误的是
A.飞船采用的太阳能刚性电池阵:将太阳能转化为电能
B.航天员的航天服使用的多种合成纤维:有机高分子材料
C.飞船返回舱使用的高温结构陶瓷:新型无机非金属材料
D.火箭燃料偏二甲肼(CH)N-NH :属于烃类
3 2 2
2.用化学用语表示 中的相关微粒,其中正确的是
A. 的电子式: B.中子数为20的 原子:
C. 的结构式: D. 分子中 原子杂化方式为 杂化
3.N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.30gSiO 中含有硅氧键个数为N
2 A
B.将1molNH Cl与少量的稀氨水混合后,溶液呈中性,则溶液中NH 数目为N
4 A
C.标准状况下,44.8LNO和22.4LO 反应后的分子数是2N
2 A
D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
4.下列指定反应的离子方程式正确的是
A.碘化亚铁溶液通入少量的氯气:2Fe2++2I-+2Cl=2Fe3++I +4Cl-
2 2
B.用HO 从酸化的海带灰浸出液中制取碘:2I-+H O+2H+=I +2H O
2 2 2 2 2 2
C.Fe(OH) 胶体的制备:Fe3++3NH•H O=Fe(OH) (胶体)+3NH
3 3 2 3
D.等物质的量的NaHCO 溶液与Ca(OH) 溶液混合:2HCO +Ca2++2OH-=CaCO ↓+CO
3 2 3
5.下列实验装置或操作能达到预期目的的是
A.用图甲分离乙醇和乙酸B.用图乙测量H 体积
2
C.用图丙除去乙烯中混有的SO
2
D.用图丁操作排出盛有KMnO 溶液滴定管尖嘴内的气泡
4
6.下列方案设计、现象和结论正确的是
选
实验目的 实验方案 现象或结论
项
判断KCl的化学键 将KCl固体溶于水,进行导电
A 溶液可导电,说明KCl中含有离子键
类型 性实验
向鸡蛋清溶液中滴加饱和 溶液变浑浊,再加水浑浊消失说明鸡蛋清
B 检验蛋白质性质
(NH )SO 溶液 溶液发生了盐析
4 2 4
检验溶液中是否含 取少量该溶液于试管中,滴加 有白色沉淀生成,说明该溶液中一定含有
C
有SO BaCl 溶液 SO
2
探究不同价态硫元 向NaS与NaSO 的混合溶液中 溶液变浑浊,说明NaS与NaSO 之间发生
2 2 3 2 2 3
D
素的转化 加入硝酸 了氧化还原反应
7.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物(Z W RX)。
x 2-x 4
已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧
化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料,基态Z原子核外s,p能级上电子
总数相等。下列叙述正确的是
A.原子半径:Z>R>Y>X
B.X的第一电离能比同周期相邻元素小
C.X的简单氢化物的热稳定性强于Y的简单氢化物
D.熔点:ZY>RX
2 2
8.CaC 晶体的晶胞结构与 NaCl 晶体的晶胞结构相似(如图所示),但CaC 晶体中含有哑铃形的 ,使晶
2 2
胞沿一个方向拉长,下列关于CaC 晶体的说法正确的是
2
A.每个 Ca2+ 周围距离最近且相等的 的数目为 6
B.CaC 晶体,每个晶胞中含有 4 个 Ca2+ 和 4 个
2
C.6.4 gCaC 晶体中含有 0.2 mol 阴离子
2
D.每个 Ca2+周围距离最近且相等的 Ca2+有 12 个
9.利用付一克烷基化反应,由K、L制取M的反应过程如下:下列说法错误的是
A.K的化学名称为3-甲基苯酚
B.M中所有碳原子共平面
C.L、M中均含有手性碳原子
D.K、M均能与溴水、酸性高锰酸钾溶液反应
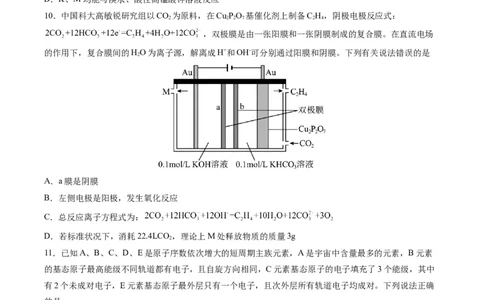
10.中国科大高敏锐研究组以CO 为原料,在Cu PO 基催化剂上制备C H,阴极电极反应式:
2 2 2 7 2 4
,双极膜是由一张阳膜和一张阴膜制成的复合膜。在直流电场
的作用下,复合膜间的HO为离子源,解离成H+和OH-可分别通过阳膜和阴膜。下列有关说法错误的是
2
A.a膜是阴膜
B.左侧电极是阳极,发生氧化反应
C.总反应离子方程式为:
D.若标准状况下,消耗22.4LCO ,理论上M处释放物质的质量3g
2
11.已知A、B、C、D、E是原子序数依次增大的短周期主族元素,A是宇宙中含量最多的元素,B元素
的基态原子最高能级不同轨道都有电子,且自旋方向相同,C元素基态原子的电子填充了3个能级,其中
有2个未成对电子,E元素基态原子最外层只有一个电子,且次外层所有轨道电子均成对。下列说法正确
的是
A.BD 是非极性分子 B.最低价氢化物的沸点:B>C
3
C.A与E通过离子键形成化合物 D.B、C、E组成的化合物水溶液一定呈碱性
12.氢溴酸在医药和石化工业上有广泛用途,模拟工业制备氢溴酸的流程如图所示。下列说法不正确的是A.混合①使用冰水的目的是防止Br 和HBr挥发
2
B.为充分除去粗品中的Br ,需加入过量的NaSO
2 2 3
C.蒸馏时,加完“滤液”后,先通冷凝水,再点燃酒精灯加热
D.工业氢溴酸常带有淡淡的黄色,可能是因为含有Br
2
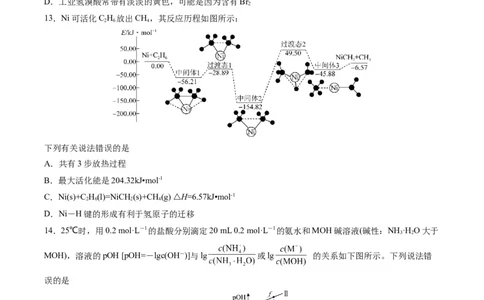
13.Ni可活化C H 放出CH,其反应历程如图所示:
2 6 4
下列有关说法错误的是
A.共有3步放热过程
B.最大活化能是204.32kJ•mol-1
C.Ni(s)+C H(l)=NiCH (s)+CH(g) △H=6.57kJ•mol-1
2 6 2 4
D.Ni-H键的形成有利于氢原子的迁移
14.25℃时,用0.2 mol·L-1的盐酸分别滴定20 mL 0.2 mol·L-1的氨水和MOH碱溶液(碱性:NH ·H O大于
3 2
MOH),溶液的pOH [pOH=-lgc(OH-)]与lg 或lg 的关系如下图所示。下列说法错
误的是
A.曲线I对应的是滴定NH ·H O的曲线
3 2
B.b、e点溶液中加入盐酸的体积均为10 mLC.a点对应的溶液pH=11
D.f点溶液满足:c(M+) = c(Cl-)
第Ⅱ卷
二、非选择题:共4题,共58分。
15.(14分)三水合硝酸铜[ , ]是一种重要的无机试剂,常用作搪瓷着
色剂,也用于镀铜、制氧化铜及农药等。回答下列问题:
I.三水合硝酸铜 的制备。
实验室常用废铜屑与稀硝酸反应制备硝酸铜溶液,过滤出剩余铜屑,再经蒸发浓缩、冷却结晶、过滤、乙
醇洗涤后得到三水合硝酸铜晶体。
(1)制备硝酸铜时发生反应的离子方程式为 。
(2)若废铜屑中含有杂质铁,则检验所得硝酸铜溶液中含有铁元素的方法为 。
II. 溶液的配制。
(3)实验室里需要 溶液。用三水合硝酸铜 配制该溶液时,
下列仪器不需要的是 (填仪器名称)。
(4)所需三水合硝酸铜固体的质量为 g。
(5)配制过程中,下列操作将导致溶液浓度偏小的是___________(填序号)。
A.加水定容时俯视刻度线
B.容量瓶未干燥处理
C.定容加水时超过刻度线后,立即吸出多余的水
D.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
III.三水合硝酸铜 热分解实验。
(6)将 样品置于瓷坩埚中缓慢加热,其热重曲线(样品质量随温度变化的曲线)如图
所示。在 过程中有红棕色气体产生,反应的化学方程式为 。继续升温至 时生成
的固体产物为 (填化学式)。16.(14分) 作为一种新型锂电池正极材料受到广泛关注。由菱锰矿( ,含有少量 、
、 、 等元素)制备 的流程如下:
已知: , , 。
回答下列问题:
(1)硫酸溶矿主要反应的化学方程式为 。为提高溶矿速率,可采取的措施 (举1
例)。
(2)加入少量 的作用是 。
(3)溶矿反应完成后,反应器中溶液 ,此时 ;用石灰乳调节至
,除去的金属离子是 。
(4)加入少量 溶液除去 ,生成的沉淀有 。
(5)在电解槽中,发生电解反应的离子方程式为 。
(6)煅烧窑中,生成 反应的化学方程式是 。
17.(15分)我国力争于2030年前做到碳达峰、2060年前实现碳中和,体现了中国对解决气候问题的担
当。CO 是目前大气中含量最高的一种温室气体。因此,控制和治理CO 是解决温室效应的有效途径、
2 2
CO、捕获与CO 重整是CO 利用的研究热点,
2 2
(1)在催化剂作用下,可用CO 与H 反应制取甲酸。已知:
2 2
共价键 C=O C-O H-H H-O C-H
键能/(kJ·mol⁻¹) 799 343 436 463 413
则 △H= kJ∙mol−1。
(2)在刚性密闭容器中,HCOOH平衡时的体积分数随投料比[
]的变化如图所示:①图中T、T 表示不同的反应温度。判断T T(填“>”“<”或“=”),依据为 ;
1 2 1 2
②图中a= ;
③A、B、C三点CO(g)的平衡转化率α 、α 、α ,由大到小的顺序为 。
2 A B C
(3)CO 可以被NaOH溶液捕获,若所得溶液pH=13,CO 主要转化为 (写离子符号);若所得
2 2
溶液
溶液pH= (室温下,
的
;
)。
(4)CaO可在较高温度下捕集CO,在更高温度下将捕集的CO 释放利用。与CaCO、热分解制备的CaO
2 2
相比,CaC O·H O热分解制备的CaO具有更好的CO 捕集性能。其原囚是 。
2 4 2 2
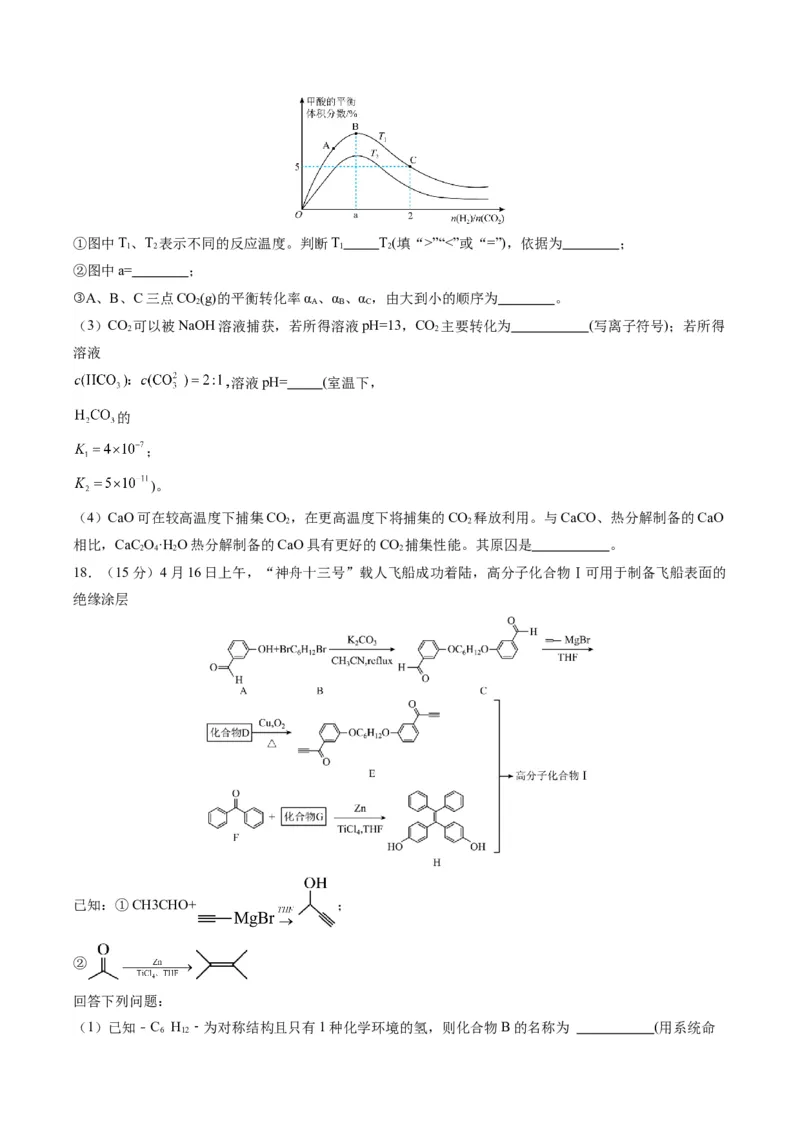
18.(15分)4月16日上午,“神舟十三号”载人飞船成功着陆,高分子化合物Ⅰ可用于制备飞船表面的
绝缘涂层
已知:①CH3CHO+ ;
②
回答下列问题:
(1)已知﹣C H ﹣为对称结构且只有1种化学环境的氢,则化合物B的名称为 (用系统命
6 12名法命名)。
(2)化合物D中含氧官能团的名称为 。
(3)由D生成E的反应类型为 。
(4)F+G→H+ZnO的化学方程式为 。
(5)化合物A有多种同分异构体,其中满足下列条件的同分异构体有 种(不包含A及立体异
构);其中不能发生显色反应的结构简式为 。
a.含有苯环
b.能发生银镜反应
(6)以 、 为原料,设计四步反应合成 的路线: (其他试剂任
选)。