文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷05
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1. 捕集利用与封存技术成为 减排的重要手段。下列关于 综合利用与处理方法错误的是
A.碱液吸收法 B.环加成制高聚物
C.电化学氧化法 D.加氢制碳氢化合物
【答案】A
【解析】CO 属于酸性氧化物,可以用碱液吸收CO,A项正确;CO 的结构式为O=C=O,CO 中含有π
2 2 2 2
键,CO 能通过环加成制聚碳酸酯高聚物,B项正确;CO 中碳元素的化合价为+4价,为碳元素的最高价,
2 2
CO 具有氧化性,CO 可通过电化学还原法处理,C项错误;CO 与H 在一定条件下可以反应生成CH 等
2 2 2 2 4
碳氢化合物,如CO+4H CH+2H O,D项正确。
2 2 4 2
2.下列有关化学用语的表述正确的是
A.NH Br的电子式: B.O 分子的球棍模型:
4 3
C.NaBH 中H元素的化合价为+1 D.CuSO •5H O中含离子键、共价键、配位键、氢键
4 4 2
【答案】D
【解析】NH Br的电子式: ,A项错误;O 分子中心O原子为sp2杂化,有一个孤电
4 3
子对,因此O 分子为V形结构,球棍模型为: ,B项错误;NaBH 中Na为+1价,B为+3
3 4
价 , 即 H 元 素 的 化 合 价 为 -1 , C 项 错 误 ; CuSO •5H O 的 结 构 示 意 图 为 :
4 2,由图可知,CuSO •5H O中含离子键、共价键、配位键、氢键,D
4 2
项正确。
3. 以菱镁矿(主要成分是 ,含少量 )为原料制取高纯氧化镁需要经历酸浸、调pH、过滤、灼
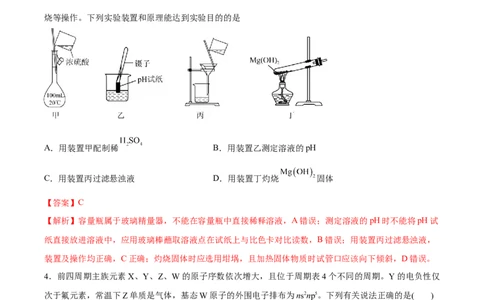
烧等操作。下列实验装置和原理能达到实验目的的是
A.用装置甲配制稀 B.用装置乙测定溶液的pH
C.用装置丙过滤悬浊液 D.用装置丁灼烧 固体
【答案】C
【解析】容量瓶属于玻璃精量器,不能在容量瓶中直接稀释溶液,A错误;测定溶液的pH时不能将pH试
纸直接放进溶液中,应用玻璃棒蘸取溶液点在试纸上与比色卡对比读数,B错误;用装置丙过滤悬浊液,
装置及操作均正确,C正确;灼烧固体时应选用坩埚,且加热固体物质时试管口应该向下倾斜,D错误。
4.前四周期主族元素X、Y、Z、W的原子序数依次增大,且位于周期表4个不同的周期。Y的电负性仅
次于氟元素,常温下Z单质是气体,基态W原子的外围电子排布为ns2np5。下列有关说法正确的是( )
A. W位于元素周期表中第四周期ⅤA族 B. Z的最高价氧化物的水化物为弱酸
C. X与Y组成的化合物分子间可形成氢键 D. Z和W形成的化合物中W显负价
【答案】C
【解析】四种元素位于4个不同周期,则X为H元素,Y的电负性仅次于氟元素,则Y为O元素,W位于
第四周期,且最外层为7个e-的主族元素,则W为Br,Z位于第三周期,且为气体,则Z为Cl。A项,A
项,Br位于第四周期VIIA族,错误;B项,HClO 为强酸,错误;C项,HO或HO 分子间均可以形成
4 2 2 2
氢键,正确;D项,BrCl中,Cl的非金属性强于Br,Cl的电负性强于Br,所以Cl显负价,Br显正价,错
误。阅读下列材料,回答5~7题:
ⅤA族氮、磷、砷(As)、锑(Sb)元素及其化合物应用广泛。氨是重要的化工原料,广泛用于生产铵盐、硝
酸、纯碱、医药等;肼( )的燃烧热为 ,是常用的火箭燃料。白磷( )晶胞如图所示,P元
素可形成多种含氧酸,其中次磷酸( )为一元弱酸, 为三元中强酸。锑是带有银色光泽的灰色
金属,铅锑合金一般用作铅蓄电池的负极材料。
5.下列说法正确的是
A. 是由极性键形成的非极性分子 B. 易液化是由于 与 分子间形成氢键
C.ⅤA族元素单质的晶体类型相同 D.白磷晶体中1个 分子周围有12个紧邻的 分子
【答案】D
【解析】 中含共价键P-Cl键,属于极性键,中心原子P价层电子对数: ,含1对
孤电子对,为三角锥形,属于极性分子,A错误; 易液化是由于 分子间形成氢键,B错误;VA
族氮、磷、砷(As)、锑(Sb)元素由非金属元素向金属过渡,氮、磷、砷形成的单质是分子晶体,锑(Sb)单质
晶体类型是金属晶体,C错误;由白磷晶胞结构图可知,与晶胞顶点距离最近且相等的白磷分子有3个,
分别位于3个面心,为2个晶胞所共用;而晶胞顶点上的白磷分子为8个晶胞所共用,则晶体中与1个
分子紧邻的 分子有: ,D正确。
6.下列化学反应表示正确的是
A.肼燃烧的热化学方程式: ;B. 与水反应:
C.次磷酸与足量NaOH溶液反应:
D.铅蓄电池放电时的负极反应:
【答案】B
【解析】肼( )的燃烧热为 ,即1mol 燃烧生成氮气和液态水时放出624kJ热量,热化
学方程式: ; ,A错误;NO 与水反应生成硝酸和
2
一氧化氮气体,反应的离子方程式为: ,B正确;次磷酸( )为一元
弱酸,1mol次磷酸只能消耗1molNaOH,反应方程式为: ,C错误;铅
蓄电池放电时的负极反应是铅失电子生成硫酸铅沉淀,电极反应为:Pb+ -2e-=PbSO,D错误。
4
7.下列物质的性质与用途具有对应关系的是
A. 易分解,可用作氮肥
B. 极易溶于水,可用于工业制硝酸
C. 具有脱水性,可用于实验室乙醇制取乙烯
D.铅锑合金导热性好,可用作铅蓄电池的电极材料
【答案】C
【解析】 可用作氮肥是因为它含有氮元素(植物生长的营养元素之一),而不是因为它受热易分
解,A错误; 催化氧化生成一氧化氮,一氧化氮与氧气反应生成二氧化氮,二氧化氮与水反应生成硝
酸,可以用于工业制硝酸,与 极易溶于水无关,B错误; 具有脱水性,与浓硫酸类似,可以作催
化剂使乙醇发生消去反应生成乙烯,C正确;铅锑合金一般用作铅蓄电池的负极材料,是因为铅锑合金能导电,和导热性无关,D错误。
8.元素及其化合物的转化在工业生产中具有极其重要的用途。下列物质间转化能实现的是
A.工业制取漂白粉:饱和食盐水 漂白粉
B.工业制取镁: 溶液 无水 Mg
C.工业制取硫酸:
D.工业制取纯碱:饱和食盐水 固体 固体
【答案】D
【解析】工业制取漂白粉是将Cl 通入石灰乳中制得,A项错误;由于MgCl 水解生成Mg(OH) 和HCl,
2 2 2
HCl易挥发,故直接蒸干MgCl 溶液得不到无水MgCl ,B项错误;硫与过量的O 燃烧只能生成SO ,SO
2 2 2 2 2
经催化氧化才能制得SO ,C项错误;向饱和食盐水中先通入NH ,后通入CO,可以制得NaHCO 固体,
3 3 2 3
然后NaHCO 受热分解得到纯碱,D项正确。
3
9.化合物Z是制备药物洛索洛芬钠的关键中间体,可由下列反应制得。
下列说法正确的是
A.X分子中含有1个手性碳原子 B.Y能发生消去反应
C.Z中的含氧官能团为羰基和醚键 D. 最多能与 反应
【答案】A
【解析】根据手性碳原子的定义可知,甲基的对位基团与苯环直接相连的C原子为手性碳原子,X分子中
只有这1个手性碳原子,A正确;与溴原子相连的β-C上无氢原子,不能发生消去反应,B错误;Z中的含
氧官能团为酯基和醚键,C错误;溴原子与酯基可以和氢氧化钠发生反应,1molZ最多能与2molNaOH反
应,D错误。
10.750℃时,NH 和O 发生以下两个反应:
3 2
①4NH (g)+5O(g) 4NO(g)+6H O(g) △H
3 2 2 1
②4NH (g)+3O(g) 2N(g)+6HO(g) △H
3 2 2 2 2
下列说法正确的是A.反应①的平衡常数可表示为K=
1
B.反应②的△S<0
C.反应①中每生成2molNO,转移电子数约为6.02×1024
D.反应②的△H=2E(N≡N)+12E(H-O)-12E(N-H)-3E(O=O)
2
【答案】C
【解析】反应①的平衡常数可表示为K= ,A项错误;反应②的气体的计量数减少,即△S
1
大于0,B项错误;由方程式可知生成1molNO时电子转移5mol,所以反应①中每生成2molNO,转移
10mol电子,约为6.02×1024,C项正确;反应②的△H=-2E(N≡N) ,D
2
项错误。
11.室温下,下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
用pH计测量浓度均为0.1 mol·L-1的NaCN溶液和
A 酸性:CHCOOH>HCN
CHCOONa溶液的pH,比较溶液pH大小 3
3
向CO还原Fe O 所得到的产物中加入稀盐酸,滴加
B 2 3 Fe O 全部被还原
KSCN溶液,观察颜色变化 2 3
C 将SO 通入滴有酚酞的NaOH溶液,观察溶液颜色变化 SO 具有漂白性
2 2
向KCl和KI的混合溶液中滴加AgNO 溶液,观察沉淀
D 3 溶解度:AgI