文档内容
铁及其化合物
【学习目标与素养】
1.宏观辨识与微观探析:结合真实情景中的应用和通过实验探究,了解铁及其氧化物、
氢氧化物的主要性质。结合真实情景中的应用和通过实验探究,了解铁盐、亚铁盐的主要性
质。
2.科学探究与创新意识:能依据教材给出的问题,设计简单的实验方案制备 Fe(OH)
。
2
3.变化观念:掌握Fe2+、Fe3+的检验方法及相互转化。
4.科学态度与社会责任:了解铁、铁的氧化物、氢氧化物在生产、生活中的应用。了解
铁盐、亚铁盐在生产、生活中的应用。
【学习重难点】
学习并掌握铁的单质、氧化物、氢氧化物、亚铁盐的性质。
熟练掌握铁三角的关系。
【学习过程】
【第一课时】
(一)基础知识填充
一、铁的单质
1.铁元素的存在
铁元素在地壳中的含量仅次于氧、硅和铝,居第四位,主要以 + 2 价和 + 3 价化合物的形
态存在。
2.物理性质
铁有延展性和导热性,铁能导电,但导电性不如铜和铝。铁能被磁体吸引。
3.铁的化学性质
铁元素性质活泼,有较强的还原性,主要化合价为+2价和+3价。
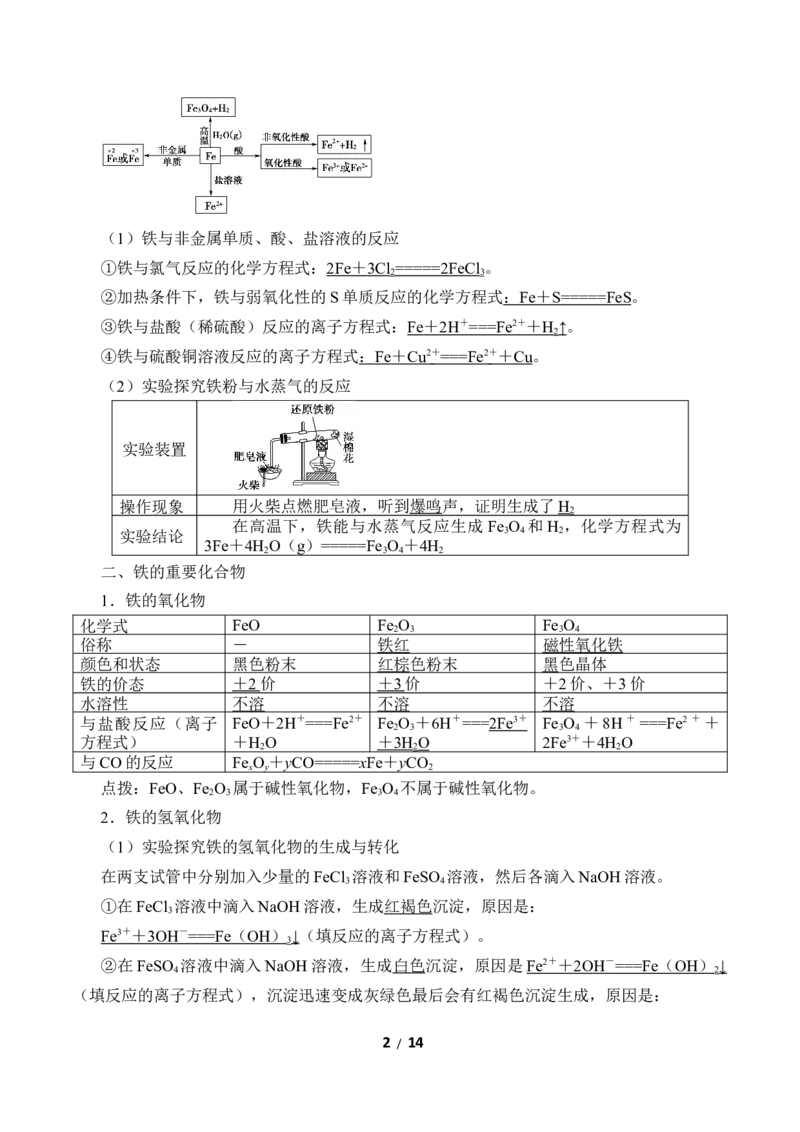
1 / 14(1)铁与非金属单质、酸、盐溶液的反应
①铁与氯气反应的化学方程式: 2Fe + 3Cl ===== 2FeCl 。
2 3
②加热条件下,铁与弱氧化性的S单质反应的化学方程式 : F e + S ===== FeS 。
③铁与盐酸(稀硫酸)反应的离子方程式: Fe + 2H + ===Fe 2 + + H ↑。
2
④铁与硫酸铜溶液反应的离子方程式 : F e + C u 2 + ===F e 2 + + C u。
(2)实验探究铁粉与水蒸气的反应
实验装置
操作现象 用火柴点燃肥皂液,听到爆鸣声,证明生成了H
2
在高温下,铁能与水蒸气反应生成 Fe O 和H ,化学方程式为
实验结论 3 4 2
3Fe+4H O(g)=====Fe O +4H
2 3 4 2
二、铁的重要化合物
1.铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗称 - 铁红 磁性氧化铁
颜色和状态 黑色粉末 红棕色粉末 黑色晶体
铁的价态 + 2 价 + 3 价 +2价、+3价
水溶性 不溶 不溶 不溶
与盐酸反应(离子 FeO+2H+===Fe2+ Fe O +6H+=== 2Fe 3 + Fe O +8H+===Fe2++
2 3 3 4
方程式) +H O + 3H O 2Fe3++4H O
2 2 2
与CO的反应 Fe O +yCO=====xFe+yCO
x y 2
点拨:FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物。
2 3 3 4
2.铁的氢氧化物
(1)实验探究铁的氢氧化物的生成与转化
在两支试管中分别加入少量的FeCl 溶液和FeSO 溶液,然后各滴入NaOH溶液。
3 4
①在FeCl 溶液中滴入NaOH溶液,生成红褐色沉淀,原因是:
3
Fe 3 + + 3OH - ===Fe ( OH ) ↓(填反应的离子方程式)。
3
②在FeSO 溶液中滴入NaOH溶液,生成白色沉淀,原因是 Fe 2 + + 2OH - ===Fe ( OH ) ↓
4 2
(填反应的离子方程式),沉淀迅速变成灰绿色最后会有红褐色沉淀生成,原因是:
2 / 144Fe ( OH ) + O + 2H O===4Fe ( OH ) (填反应的化学方程式)。
2 2 2 3
思考:利用教科书中的方法制备 Fe(OH) 时,为得到较为纯净的 Fe(OH) ,可采取
2 2
哪些措施?
提示:①Fe2+溶液必须是新制的并放入铁粉,防止Fe2+被氧化成Fe3+;②除去溶液中溶
解的O ,方法是加热煮沸NaOH溶液;③滴管末端插入试管内的液面以下;④必要时可在液
2
面上加植物油或苯进行液封。
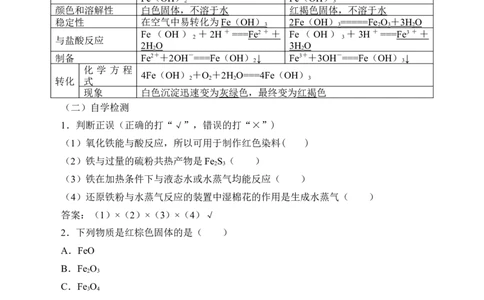
(2)Fe(OH) 、Fe(OH) 的比较
2 3
Fe(OH) Fe(OH)
2 3
颜色和溶解性 白色固体,不溶于水 红褐色固体,不溶于水
稳定性 在空气中易转化为 Fe ( OH ) 2Fe ( OH ) ===== Fe O + 3H O
3 3 2 3 2
Fe(OH) +2H+=== Fe 2 + + Fe(OH) +3H+=== Fe 3 + +
与盐酸反应 2 3
2H O 3H O
2 2
制备 Fe2++2OH-===Fe(OH) ↓ Fe3++3OH-===Fe(OH) ↓
2 3
化 学 方 程
4Fe(OH) +O +2H O===4Fe(OH)
转化 式 2 2 2 3
现象 白色沉淀迅速变为灰绿色,最终变为红褐色
(二)自学检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)氧化铁能与酸反应,所以可用于制作红色染料( )
(2)铁与过量的硫粉共热产物是Fe S ( )
2 3
(3)铁在加热条件下与液态水或水蒸气均能反应( )
(4)还原铁粉与水蒸气反应的装置中湿棉花的作用是生成水蒸气( )
答案:(1)×(2)×(3)×(4)√
2.下列物质是红棕色固体的是( )
A.FeO
B.Fe O
2 3
C.Fe O
3 4
D.Fe(OH)
2
答案:B
3.在FeSO 溶液中滴入NaOH溶液,生成白色沉淀,沉淀迅速变成灰绿色最后会有红褐
4
色沉淀生成,原因是4Fe(OH) +O +2H O===4Fe(OH) ,该反应中氧化剂是________,
2 2 2 3
还原剂是________。
答案:O ;Fe(OH)
2 2
(三)重难点突破
3 / 14实验室制备Fe(OH) 装置的改进
2
1.制备关键:防止Fe(OH) 与空气中的氧气接触。
2
2.防止Fe(OH) 氧化的方法
2
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入试管的亚铁盐溶液底部,并慢慢挤出 NaOH
溶液。
(3)在亚铁盐溶液上面充入保护气,如H 、N 、稀有气体等。
2 2
(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
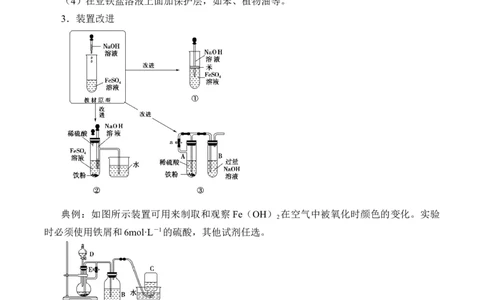
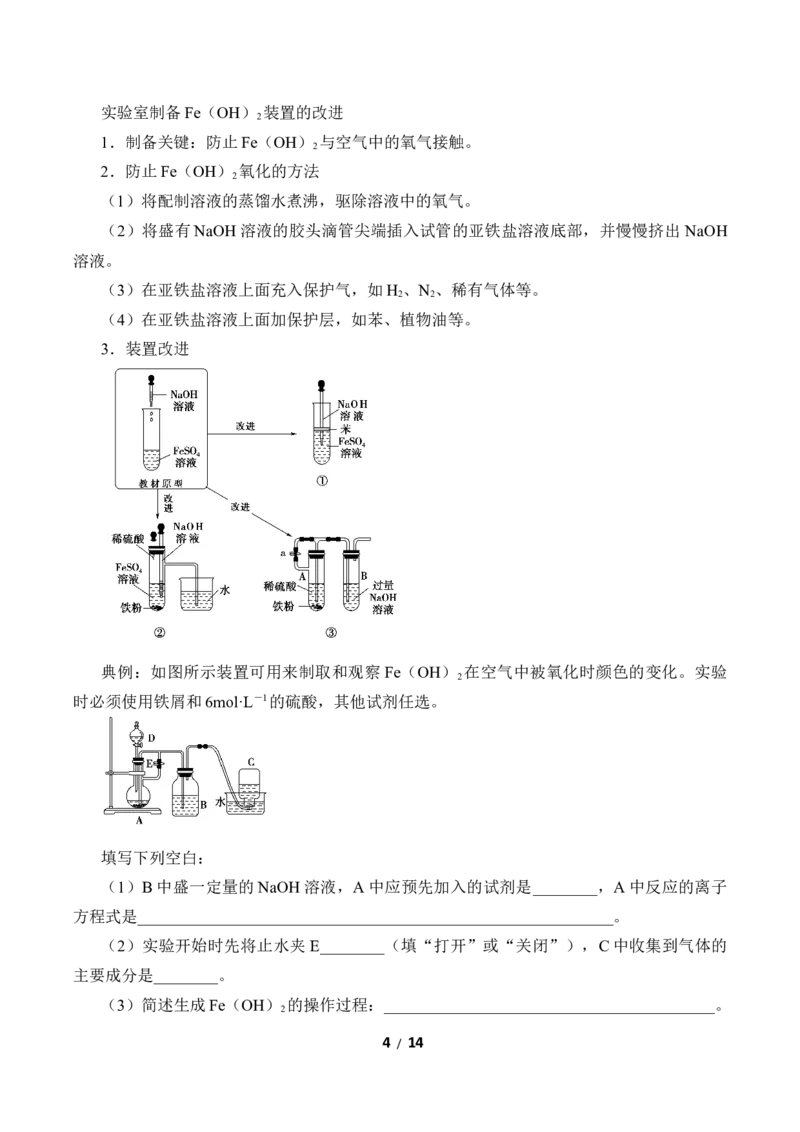
3.装置改进
典例:如图所示装置可用来制取和观察Fe(OH) 在空气中被氧化时颜色的变化。实验
2
时必须使用铁屑和6mol·L-1的硫酸,其他试剂任选。
填写下列空白:
(1)B中盛一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的离子
方程式是___________________________________________________________。
(2)实验开始时先将止水夹 E________(填“打开”或“关闭”),C中收集到气体的
主要成分是________。
(3)简述生成Fe(OH) 的操作过程:_________________________________________。
2
4 / 14(4)拔去装置 B 中的橡皮塞,使空气进入,写出有关反应的化学方程式:
___________________________________________________。
解析:实验开始时先打开止水夹 E,让生成的 H 把 A、B 装置中的空气排出,让 Fe
2
(OH) 在H 气氛中生成,以便较长时间观察 Fe(OH) 的颜色。H 充满B后关闭止水夹
2 2 2 2
E,A中的FeSO 溶液沿竖直长导管进入B瓶,与NaOH反应。
4
答案:(1)铁屑;Fe+2H+===Fe2++H ↑
2
(2)打开;H
2
(3)关闭止水夹E,A中压强增大,把FeSO 溶液压入B瓶中进行反应
4
(4)4Fe(OH) +O +2H O===4Fe(OH)
2 2 2 3
【第二课时】
(一)基础知识填充
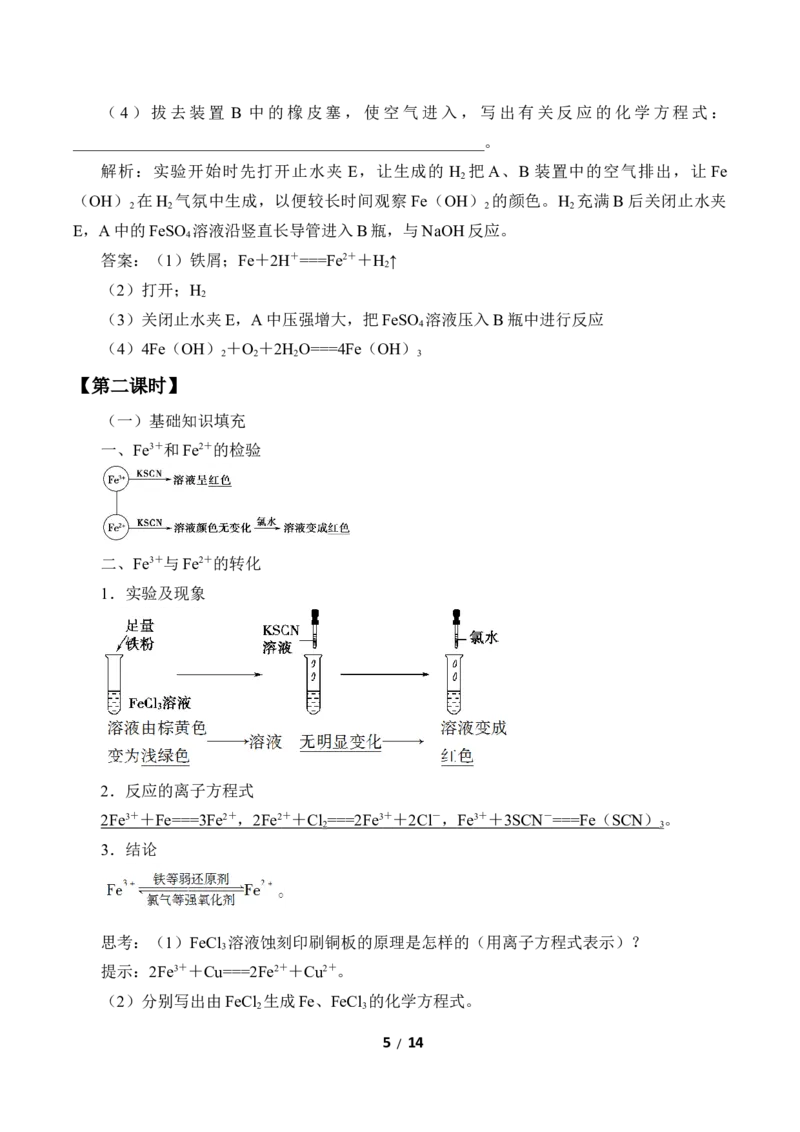
一、Fe3+和Fe2+的检验
二、Fe3+与Fe2+的转化
1.实验及现象
2.反应的离子方程式
2Fe 3 + + Fe===3Fe 2 + , 2Fe 2 + + Cl ===2Fe 3 + + 2Cl - , Fe 3 + + 3SCN - ===Fe ( SCN ) 。
2 3
3.结论
思考:(1)FeCl 溶液蚀刻印刷铜板的原理是怎样的(用离子方程式表示)?
3
提示:2Fe3++Cu===2Fe2++Cu2+。
(2)分别写出由FeCl 生成Fe、FeCl 的化学方程式。
2 3
5 / 14提示:FeCl +Zn===ZnCl +Fe,2FeCl +Cl ===2FeCl 。
2 2 2 2 3
(二)自学检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)用酸性KMnO 溶液检验FeCl 溶液中是否含有FeCl ( )
4 3 2
(2)检验绿矾晶体(FeSO ·7H O)是否已氧化变质,可将绿矾晶体溶于稀硫酸后滴加
4 2
KSCN溶液,再观察溶液是否变红( )
(3)向FeCl 溶液中滴加适量的KSCN溶液,会产生红色的沉淀( )
3
(4)Fe2+可以被Cl 氧化为Fe3+,说明Fe2+具有氧化性( )
2
答案:(1)×(2)√(3)×(4)×
2.随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,
防止食品氧化变质,在包装袋中可以放入的化学物质是( )
A.无水硫酸铜
B.硫酸亚铁
C.食
D.生石灰
答案:B
解析:无水硫酸铜能吸收水分,不能防止食物被氧化,硫酸亚铁具有还原性,可以作为
防止富脂食品氧化变质的物质,食盐不能吸收水分,生石灰能防止食品受潮,但不能防止食
品被氧化。
3.A、B、C、D四种物质(或离子)均含有同一种元素,其中 A是常见单质,它们之间
存在如图所示的转化关系:
若B、C均属于盐类,B溶液呈黄色,遇氨水能形成红褐色沉淀;D是一种不溶性碱;
B、C中的阴离子均是Cl-,则A只有与________(填分子式)反应才能得到B;实验室制备
的 D 物 质 不 稳 定 , 相 应 反 应 的 化 学 方 程 式 为
_____________________________________________。
解析:由B的性质知其是FeCl ,故A是铁,C是FeCl ,D是Fe(OH) ,铁只有与氯气
3 2 2
反应才能得到FeCl ;Fe(OH) 在空气中易变质生成Fe(OH) 。
3 2 3
答案:Cl ;4Fe(OH) +2H O+O ===4Fe(OH)
2 2 2 2 3
(三)重难点突破
重难点1:Fe2+、Fe3+、Fe的相互转变——“铁三角”
6 / 141.Fe只具有还原性,可以被氧化剂氧化为Fe2+、Fe3+
如 : Fe + S=====FeS , Fe + 2Fe3 + ===3Fe2 + , Fe + Cu2 + ===Cu + Fe2 + ; 2Fe +
3Cl =====2FeCl 3Fe+4H O(g)=====Fe O +4H 。
2 3, 2 3 4 2
2.Fe2+既具有氧化性又具有还原性
如:2Fe2++Cl ===2Fe3++2Cl-,Zn+Fe2+===Zn2++Fe FeO+CO=====Fe+CO 。
2 2
3.Fe3+具有较强氧化性,可被还原为Fe2+或Fe
如:2Fe3++Cu===2Fe2++Cu2+,
Fe O +3CO=====2Fe+3CO ,
2 3 2
Fe O +2Al=====2Fe+Al O 。
2 3 2 3
典例训练:
1.硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列
物质中的( )
A.锌粉
B.镁粉
C.铁粉
7 / 14D.铝粉
答案:C
解析:铁粉可将硫酸铁转化为硫酸亚铁,将硫酸铜转化为硫酸亚铁和单质铜,然后过滤
即可提纯硫酸亚铁,锌、镁、铝都有可能将亚铁离子置换成铁,并且会引入新的杂质锌离子、
镁离子或铝离子等。
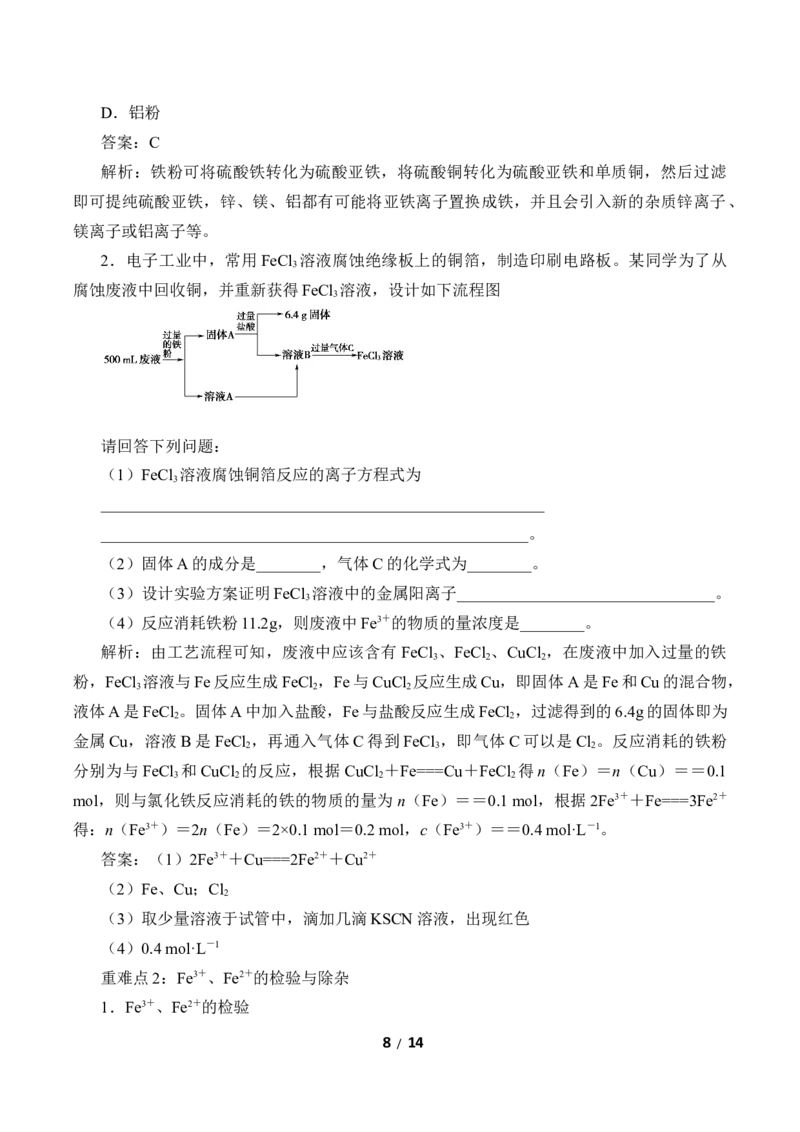
2.电子工业中,常用FeCl 溶液腐蚀绝缘板上的铜箔,制造印刷电路板。某同学为了从
3
腐蚀废液中回收铜,并重新获得FeCl 溶液,设计如下流程图
3
请回答下列问题:
(1)FeCl 溶液腐蚀铜箔反应的离子方程式为
3
_______________________________________________________
_____________________________________________________。
(2)固体A的成分是________,气体C的化学式为________。
(3)设计实验方案证明FeCl 溶液中的金属阳离子________________________________。
3
(4)反应消耗铁粉11.2g,则废液中Fe3+的物质的量浓度是________。
解析:由工艺流程可知,废液中应该含有 FeCl 、FeCl 、CuCl ,在废液中加入过量的铁
3 2 2
粉,FeCl 溶液与Fe反应生成FeCl ,Fe与CuCl 反应生成Cu,即固体A是Fe和Cu的混合物,
3 2 2
液体A是FeCl 。固体A中加入盐酸,Fe与盐酸反应生成FeCl ,过滤得到的6.4g的固体即为
2 2
金属Cu,溶液B是FeCl ,再通入气体C得到FeCl ,即气体C可以是Cl 。反应消耗的铁粉
2 3 2
分别为与FeCl 和CuCl 的反应,根据CuCl +Fe===Cu+FeCl 得n(Fe)=n(Cu)==0.1
3 2 2 2
mol,则与氯化铁反应消耗的铁的物质的量为 n(Fe)==0.1 mol,根据2Fe3++Fe===3Fe2+
得:n(Fe3+)=2n(Fe)=2×0.1 mol=0.2 mol,c(Fe3+)==0.4 mol·L-1。
答案:(1)2Fe3++Cu===2Fe2++Cu2+
(2)Fe、Cu;Cl
2
(3)取少量溶液于试管中,滴加几滴KSCN溶液,出现红色
(4)0.4 mol·L-1
重难点2:Fe3+、Fe2+的检验与除杂
1.Fe3+、Fe2+的检验
8 / 14Fe2+ Fe3+
(1)观察法 浅绿色 棕黄色
① 现 象 : 白 色 沉 淀 ――→ 灰 绿
色――→红褐色沉淀
①现象:红褐色沉淀
(2)加碱法 ②反应:Fe2++2OH-===Fe(OH)
②反应:Fe3++3OH-===Fe(OH)
(NaOH) ↓(白色);
2 ↓(红褐色)
4Fe ( OH ) + O + 2H O===4Fe 3
2 2 2
(OH) (红褐色)
3
①现象:加入 KSCN 溶液无明显现
象,再滴入氯水变成红色溶液 ①现象:加入 KSCN 溶液,溶液变
(3)加盐法 ②反应:2Fe2++Cl ===2Fe3++2Cl 为红色
2
(SCN-) -; ② 反 应 : Fe3 + + 3SCN - ===Fe
Fe3++3SCN-===Fe(SCN) (红 (SCN) (红色)
3 3
色)
2.检验Fe2+的注意事项
(1)只含Fe2+的溶液:检验Fe2+加入试剂的顺序
待测液――――――→不变色――――――→红色(含Fe2+、不含Fe3+)。
①加KSCN溶液前,防止加氧化性物质,使Fe2+被氧化。如H O 、NO(H+)等。
2 2
②氧化剂不能选用酸性 KMnO 溶液,原因:酸性 KMnO 溶液本身显紫红色,对 Fe
4 4
(SCN) 红色有干扰;酸性 KMnO 溶液能氧化KSCN,溶液不变红色,不能证明不含 Fe2
3 4
+。
(2)同时含有Fe2+和Fe3+的溶液
Fe2+对检验Fe3+无干扰,可以滴加 KSCN溶液检验Fe3+;Fe3+对检验Fe2+有干扰,不能
采用加KSCN溶液检验Fe2+,通常向溶液中滴加适量酸性KMnO 溶液,溶液紫红色褪色说明
4
含有Fe2+。
(3)检验铁的氧化物中是否有+2价铁时,正确的思路为
少量固体―――――→溶液―――――――――→紫色褪去。
①步骤a中不能选用盐酸,原因是酸性KMnO 溶液可以氧化盐酸。
4
②步骤a中,不能选用稀硝酸,原因是稀硝酸可以将Fe2+氧化为Fe3+。
3.含Fe2+、Fe3+的除杂问题
主要成分 杂质 除杂方法
FeCl (aq) FeCl (aq) 加入氯水或H O
3 2 2 2
FeCl (aq) FeCl (aq) 加过量铁粉后过滤
2 3
FeCl (aq) CuCl (aq) 加过量铁粉后过滤
2 2
典例训练:
3.选择合适试剂完成甲、乙两组实验。
甲组:检验含Fe3+的溶液中是否含有Fe2+;
9 / 14乙组:检验含Fe2+的溶液中是否含有Fe3+。
下列试剂及加入试剂顺序能达到实验目的的是( )
试剂
甲组 乙组
选项
A 新制氯水、KSCN溶液 NaOH溶液
B 酸性KMnO 溶液 KSCN溶液
4
C KOH溶液 溴水
D 溴水 酸性KMnO 溶液
4
答案:B
解析:甲组,在Fe3+存在的条件下检验Fe2+,要排除Fe3+的干扰。所选试剂具备下列条
件:一是能与Fe2+发生有明显现象的反应;二是与 Fe3+不反应。溴水符合条件,实验现象是
溴水颜色变浅,酸性KMnO 溶液也符合条件:5Fe2++MnO+8H+===5Fe3++Mn2++4H O,
4 2
实验现象是溶液紫色变浅。乙组,在Fe2+存在的条件下检验Fe3+,用KSCN溶液检验Fe3+即
可,Fe2+不会造成干扰。
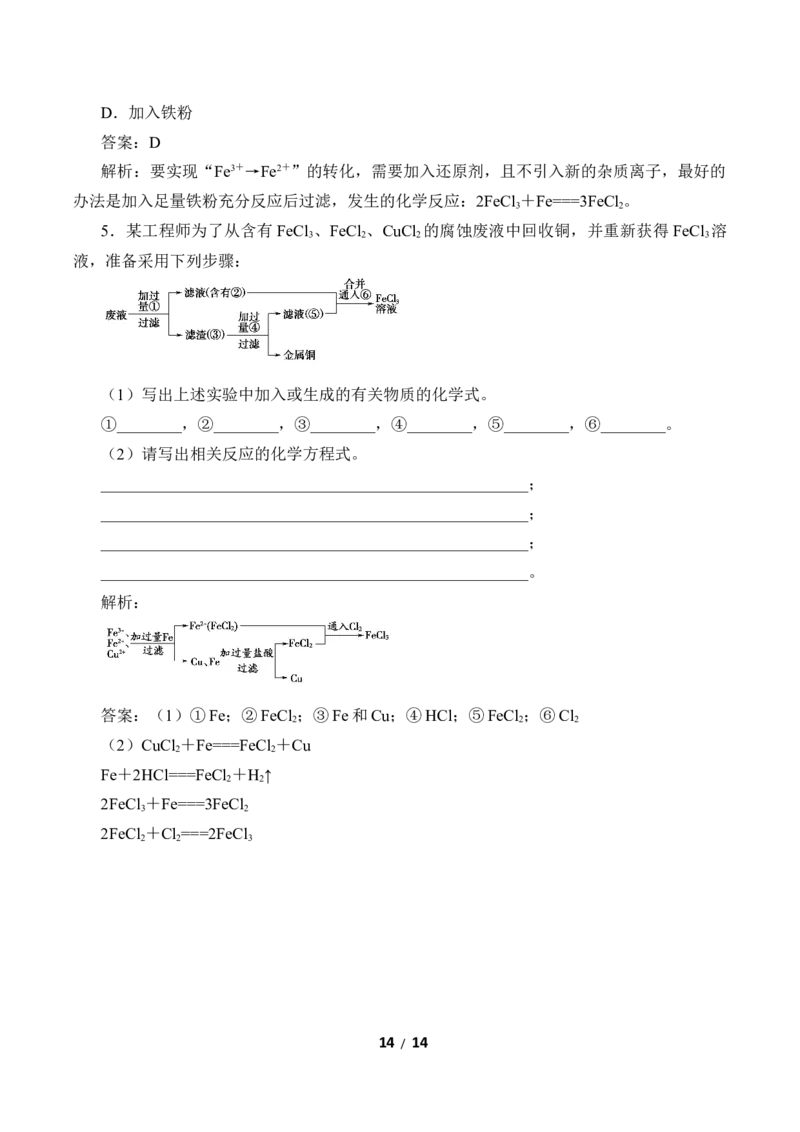
4.硫酸亚铁缓释片可以补铁、防治贫血,但存放不当很容易变质,药片中的 Fe2+被氧化
生成 Fe3+。若将药片配成溶液,需使用刚刚煮沸过又冷却的蒸馏水,原因是
___________________________。实验室检验Fe3+,除了可以用碱外,常用的试剂是(填化学
式)________,若________________,则证明有Fe3+。
解析:硫酸亚铁缓释片溶于水时,药片中的 Fe2+易被水中溶解的O 氧化为Fe3+,因此将
2
药片配成溶液时,应预先将蒸馏水煮沸,以除去水中溶解的O ;检验Fe3+,还可以用KSCN
2
溶液,Fe3+与SCN-发生反应使溶液变红色。
答案:防止水中溶解的氧气氧化Fe2+;KSCN;溶液变成红色
【反馈检测】
第一课时
1.常温下,将铁片放入下列溶液中,不发生反应的是( )
A.稀硫酸
B.氯水
C.氢氧化钠溶液
D.硫酸铜溶液
答案:C
解析:铁与稀硫酸反应:Fe+H SO ===FeSO +H ↑;氯水呈酸性、强氧化性可以和铁反
2 4 4 2
应; 铁与硫酸铜发生置换反应:Fe+CuSO ===FeSO +Cu;铁与氢氧化钠溶液不发生反应,
4 4
C项符合题意。
10 / 142.下列关于铁与水蒸气反应的说法中不正确的是( )
A.反应中有氢气产生
B.此反应需在加热条件下才能发生
C.生成的铁的化合物中铁全部呈+3价
D.该反应中水作氧化剂
答案:C
解析:Fe与H O(g)反应生成Fe O ,Fe的化合价为+2、+3。
2 3 4
3.有关铁的氧化物的说法中,不正确的是( )
A.赤铁矿主要成分是Fe O ,Fe O 是红棕色的,常用作红色油漆和涂料
2 3 2 3
B.Fe O 是黑色晶体,其中的铁显+2价,的铁显+3价
3 4
C.FeO、Fe O 、Fe O 都不溶于水,但都能和盐酸反应生成相应的盐
2 3 3 4
D.FeO不稳定,在空气中加热迅速被氧化成Fe O
2 3
答案:D
解析:FeO不稳定,在空气中受热迅速被氧化成Fe O 。
3 4
4.有关铁的化合物的说法中,错误的是( )
A.Fe(OH) 是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色
2
B.由图示操作可制取Fe(OH)
2
C.Fe O 、Fe(OH) 都可以由化合反应制得
3 4 3
D.Fe(OH) 胶体呈红褐色、透明,能发生丁达尔效应
3
答案:A
解析:Fe(OH) 是一种白色固体,A错误;煤油能减少FeSO 溶液与氧气接触,可以避
2 4
免试管中部分氧气对氢氧化亚铁的氧化,B正确;铁在氧气中燃烧可生成Fe O ,可通过化合
3 4
反应:4Fe(OH) +2H O+O ===4Fe(OH) 制取Fe(OH) ,C正确;Fe(OH) 胶体呈
2 2 2 3 3 3
红褐色、透明,能发生丁达尔效应,D正确。
5.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸
气,就可以完成高温下“Fe与水蒸气反应的实验”。
11 / 14请回答该实验中的问题。
( 1 ) 实 验 前 必 须 对 整 套 装 置 进 行 气 密 性 的 检 查 , 操 作 方 法 是
_________________________。
( 2 ) 圆 底 烧 瓶 中 盛 装 的 是 水 , 该 装 置 受 热 后 的 主 要 作 用 是
___________________________ ; 烧 瓶 底 部 放 置 了 几 片 碎 瓷 片 , 碎 瓷 片 的 作 用 是
_______________________________________。
(3)酒精灯和酒精喷灯点燃的顺序是___________________________________________。
( 4 ) 干 燥 管 中 盛 装 的 物 质 可 以 是 ________ , 作 用 是
_________________________________。
(5)如果要在A的玻璃导管口处点燃该气体,则必须对该气体进行________,这一操作
的目的______________________________________________。
解析:(1)中学阶段检查装置气密性常用方法有两种:一种是利用热胀冷缩原理,另一
种是利用气压原理。气压原理一般只有涉及液体时才能用得到,这里显然是利用热胀冷缩原
理。利用热胀冷缩原理时要注意步骤一定要完整,既要证明“热胀”,也要证明“冷缩”。
(3)点燃加热仪器的顺序要考虑实验的安全性和对实验结果的影响,在本实验中为了防
止铁与空气中的氧气在加强热的条件下反应,应该先点燃酒精灯,产生水蒸气后,再点燃酒
精喷灯。(4)干燥管中盛装的物质可以是碱石灰,作用是除去反应产生的氢气中的水蒸气。
答案:(1)将干燥管末端的导管A浸入水中,用酒精灯火焰微热烧瓶底部,如果能观察
到浸入水中的玻璃导管口有气泡冒出,停止加热后,玻璃导管内有水柱上升,且较长时间不
会落,则表明该套装置的气密性良好
(2)为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气;防止暴沸
(3)先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯
(4)碱石灰;除去产物H 中的水蒸气
2
(5)验纯;防止H 不纯而发生爆炸
2
第二课时
12 / 141.下列关于Fe2+和Fe3+的叙述中,错误的是( )
A.Fe2+的水溶液为浅绿色
B.Fe3+的水溶液为黄色
C.Fe3+具有氧化性,Fe2+具有还原性
D.Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀
答案:D
解析:Fe3+溶液中滴入含SCN-的溶液,生成红色可溶性物质,不是红色沉淀。
2.下列离子方程式正确的是( )
A.将氨水滴入FeCl 溶液中:Fe3++3OH-===Fe(OH) ↓
3 3
B.氧化铁与盐酸反应:Fe O +6H+===2Fe3++3H O
2 3 2
C.向FeCl 溶液中加入铁粉:Fe+Fe3+===2Fe2+
3
D.向氯化亚铁溶液中通入:Cl Fe2++Cl ===Fe3++2Cl-
2 2
答案:B
解析:A项在书写离子方程式时,弱电解质NH ·H O不能拆写成离子的形式;C项离子
3 2
方程式中除遵循元素守恒外,电荷也必须守恒,正确的离子方程式应为 Fe+2Fe3+===3Fe2
+;D项只符合元素守恒,不符合电荷守恒,正确的离子方程式应为 2Fe2++Cl ===2Fe3++
2
2Cl-。
3.向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液
变成红色,则下列结论错误的是( )
A.该溶液中一定含有SCN-
B.氧化性:Fe3+>Cl
2
C.Fe2+与SCN-不能形成红色物质
D.Fe2+被氧化为Fe3+
答案:B
解析:溶液中的Fe2+与加入的新制氯水发生反应:2Fe2++Cl ===2Fe3++2Cl-,故氧化性:
2
Fe3+