文档内容
乙烯与有机高分子材料(2)
重难点 题型 分值
重点 有机物分子式的确定
选择和填空 3-5分
难点 实验式法确定有机物分子式
核心知识点一
一、有机物分子式的确定
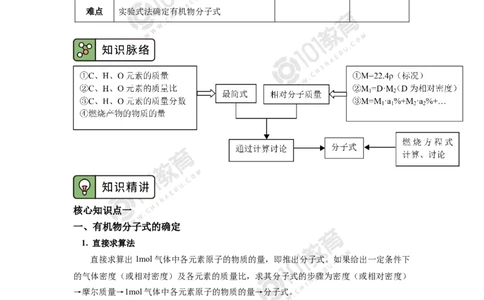
1. 直接求算法
直接求算出1mol气体中各元素原子的物质的量,即推出分子式。如果给出一定条件下
的气体密度(或相对密度)及各元素的质量比,求其分子式的步骤为密度(或相对密度)
→摩尔质量→1mol气体中各元素原子的物质的量→分子式。
2. 实验式法:
实验式(也叫最简式)是表示有机物分子中所含各元素的原子数目最简单整数比的式
子。用有机物的相对分子式质量除以其实验式的式量就可以确定其分子式。
①确定实验式的方法
a. 根据各种元素的质量之比:如某烃中m(C)∶m(H)=24∶5,则n(C)∶n
24 5
(H)= ∶ =2∶5,可知其实验式为C H。
12 1 2 5
b. 根据燃烧产物的量:如 1 mol 某烃完全燃烧生成 CO 和HO的物质的量之比为
2 2
1∶1.5,可知该烃的实验式为CH。
3
第1页②计算有机物的相对分子质量
a. 在标准状况下的气体,M=22.4L/mol·ρ(ρ的单位:g/L),M 与M数值相等。
r
b. 根据气体的相对密度,M D·M′(D为相对密度,M′为已知气体的相对分子质量)
r= r r
c. 平均相对分子质量 = M ×a% + M ×b% + …(M 、M …表示各组分气体的体积
r1 r2 r1 r2
分数)。
d. 根据公式计算:M = m/n(m:质量,n:物质的量)
③用相对分子质量除以实验式的式量,得到的整数倍数值,与实验式相乘,就得到了
分子式。如果实验式的式量等于其相对分子质量,那么实验式就是该化合物的分子式。
3. 余数法
用烃的相对分子质量除以14,看商数和余数。
其中商数为烃分子中的碳原子数。
根据烃类通式的特点:C H (烷烃)、C H (稀烃、环烷烃)、C H (炔烃、二
n 2n+2 n 2n n 2n-2
烯烃)、
C H (苯及其同系物),它们共同的特点是都有C H 部分,即有共同的式量14n,
n 2n-6 n 2n
因此可以用该烃的分子量除以14就可以得到该烃的CH 的数目,再根据余数确定分子式。
2
或者也可除以12可得C原子数目,再根据余数确定分子式。
例如:已知某烃的分子量为44,求其分子式?
44
=3余2,∴分子式为:C H ⇒C H
14 3 2×3+2 3 8
例如:已知某烃的分子量为78,求其分子式?
78
=6余6,∴分子式为:C H
12 6 6
若为烃的衍生物,则依商余法求出烃的分子式后,用烃分子中的一个 CH 代换一个O
4
(相对质量相等),如相对分子质量为44的烃,分子式为C H ,若为烃的衍生物则是
3 8
C HO。
2 4
4. 化学方程式法
利用燃烧的化学方程式求烃的分子式
用CH 表示烃的通式,则烃完全燃烧的化学方程式为:
x y
第2页y y
C H +(x+ )O ⃗点燃 xCO + H O
x y 4 2 2 2 2
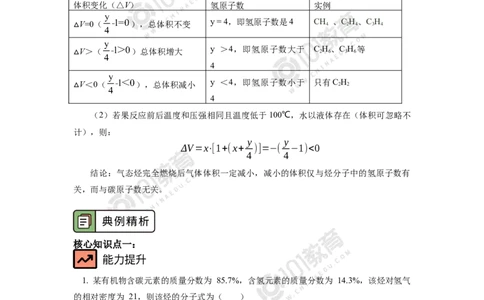
(1)气态烃的完全燃烧前后气体总体积的变化(△V)规律
①如果反应前后温度和压强相同且温度高于100℃,水以气体存在,则
y y y
ΔV=(x+ )−[1+(x+ )]= −1
2 4 4
结论:气体烃完全燃烧前后气体总体积的变化仅与烃分子中的氢原子数有关,而与碳
原子数无关,总体积可能不变,也可能增加或减少。
体积变化(△V) 氢原子数 实例
V=0( ),总体积不变 y = 4,即氢原子数是4 CH 4 、C 2 H 4 、C 3 H 4
△
V>( )总体积增大 y >4,即氢原子数大于 C 2 H 6 、C 3 H 6 等
4
△
V<0( ),总体积减小 y <4,即氢原子数小于 只有C 2 H 2
4
△
(2)若果反应前后温度和压强相同且温度低于100℃,水以液体存在(体积可忽略不
计),则:
y y
ΔV=x⋅[1+(x+ )]=−( −1)<0
4 4
结论:气态烃完全燃烧后气体体积一定减小,减小的体积仅与烃分子中的氢原子数有
关,而与碳原子数无关。
核心知识点一:
1. 某有机物含碳元素的质量分数为 85.7%,含氢元素的质量分数为 14.3%,该烃对氢气
的相对密度为 21,则该烃的分子式为( )
A. C H B. C H C. C H D. C H
2 4 3 6 4 8 2 6
【答案】B
【解析】根据已知条件知该烃的相对分子质量是 21×2=42,其中 C 原子的个数是
(42×85.7%)÷12=3,含有H原子的个数为(42×14.3%)÷1=6,所以分子式为C H。
3 6
2. 在标准状况下,某气态烃的密度是 1.34 g/L,一定量的该烃完全燃烧生成 8.8g CO
2
和 5.4 g H O,该烃的分子式为__________,其结构式为____________。
2
第3页【答案】C H
2 6
【解析】在标准状况下,某气态烃的密度为 1.34g/L,则气态烃的摩尔质量=1.34g/
L×22.4L/mol≈30 g/L,即该烃的相对分子质量为30。一定量的该烃完全燃烧生成水的物质
的量为 生成二氧化碳的物质的量为 则n(C)∶n
(H)=0.2mol∶0.6mol=1∶3,则该烃的最简式为CH,又知该烃的相对分子质量为30,所
3
以该烃的分子式为C H。
2 6
3. 某气态烃的分子式为 C H,相对分子质量为H 的39倍。它不能使酸性高锰酸钾溶液
m n 2
褪色,不能与溴水的四氯化碳溶液反应而使其褪色。在催化剂存在时,7.8 g 该烃能与 0.3
mol H 发生加成反应生成相应的饱和烃 C H 。则:
2 m p
(1)m、n、p 的值分别是 m = _____________,n = _____________,p =
_____________ 。
(2)C H 的结构简式是__________________。
m p
【点拨】解答本题可先由C H 的相对分子质量是H 的39倍,求出其相对分子质量,
m n 2
再由与H 加成推出不饱和键的情况。结合所学知识,可推断C H 的结构,然后结合苯的
2 m n
性质和结构得出答案。
【答案】(1)6 6 12 (2)
【解析】由题意知C H 的相对分子质量为39×2=78,C原子最大数目为
m n
C H 中含有6个碳原子,故分子式为C H。由于它不能与酸性高锰酸钾溶液和溴的四氯化
m n 6 6
碳溶液反应而使其褪色,且1mol C H 能与3molH 发生加成反应,根据所学知识,可知该
6 6 2
烃为苯。1mol苯能与3mol H 加成生成 。
2
1. 10 L某气态烃在 50 L 氧气里充分燃烧,得到液态水和体积为35L的混合气体(所有
气体体积都在同温同压下测定),该气态烃可是( )
A. 甲烷 B. 乙烷 C. 丙烷 D. 丙烯
【答案】BD
【解析】设该烃的分子式为CH,本题生成的水是液态,满足上述规律水是液态的情
x y
第4页况,列式可得 ,结合选项可知,该气态烃可能是乙烷或丙烯。
2. 在120 ℃时,1.5 L某气态烃在 a L O 中完全燃烧,得到相同条件下的气体(3 + a)
2
L,则该烃可能是 _____________。
【答案】C H、C H、C H、C H、C H、C H
3 8 4 8 5 8 6 8 7 8 8 8
【解析】该气态烃与O 在120℃时完全燃烧气体体积增大,且体积增大1.5L,满足上
2
述规律中水是气态情况,设该烃的分子式为C H,列式可得 ,所以y =
x y
8,只要氧气的量满足条件,在题给条件下,该烃可能是C H、C H、C H、C H、C H、
3 8 4 8 5 8 6 8 7 8
C H 中的任一种。
8 8
(答题时间:25分钟)
1. 验证某有机物属于烃,应完成的实验内容是( )
A. 只测定它的C、H比
B. 只要证明它完全燃烧后产物只有HO和CO
2 2
C. 只测定其燃烧产物中HO与CO 的物质的量的比值
2 2
D. 测定该试样的质量及试样完全燃烧后生成CO 和HO的质量
2 2
2. 某有机物在氧气中充分燃烧,生成的CO 和HO的物质的量之比为1∶2,则下列说
2 2
法中正确的是( )
A. 分子中C、H、O个数比为1∶2∶3
B. 分子中C、H个数比为1∶4
C. 分子中含有氧元素
D. 此有机物的最简式为CH
4
3. 下列实验式中,没有相对分子质量就可以确定分子式的是( )
①CH ②CH ③CH ④C H
3 2 2 5
A. ①② B. ③④
C. ②③ D. ①④
4. 定量有机物完全燃烧后,将燃烧产物通过足量的石灰水,过滤后得到白色沉淀10 g,
但称量滤液时只减少2.9 g,则此有机物不可能是( )
A. C HOH B. C HO
2 5 4 8 2
C. C H D. C HO
2 6 2 6 2
5. 25℃时,1L某气态烃在9L氧气中充分燃烧反应后的混合气体体积仍为10L(相同条
件下),则该烃可能是( )
第5页A. CH B. C H C. C H D.C H
4 2 4 2 2 6 6
6. 室温下,一气态烃与过量氧气混合完全燃烧,恢复到室温,使燃烧产物通过浓硫酸,
体积比反应前减少50mL,再通过NaOH溶液,体积又减少了40mL,原烃的分子式是(
)
A. CH B. C H C. C H D.C H
4 2 4 2 6 3 8
7. 2.3g某有机物A完全燃烧后,生成0.1molCO 和2.7gH O,测得该有机物的蒸气与空气
2 2
的相对密度是1.589,求该化合物的分子式。
第6页1.【答案】D
【解析】当CO 和HO中m(C)+m(H)=m(有机物)时,说明有机物中没有氧
2 2
元素。
2.【答案】B
【解析】由n(CO)∶n(HO)=1∶2仅能得出n(C)∶n(H)=1∶4,不能确定
2 2
是否含O。
3.【答案】D
【解析】由实验式的整数倍,即可得到有机物的分子式。据烷烃通式,当碳原子数为
n时,则氢原子数最多为2n+2。符合实验式为CH 的只有C H;符合实验式为CH的有
3 2 6
C H、C H 等;符合实验式为CH 的有C H、C H 等;符合实验式为C H 的只有C H 。
2 2 6 6 2 2 4 3 6 2 5 4 10
4.【答案】B
10g
【解析】n(CO)=n(CaCO )= =0.1 mol,则通入石灰水中的CO
2 3 100g⋅mol−1 2
的质量应是4.4 g,而产生的CaCO 的质量是10 g,若无其他物质进入,则石灰水质量应减
3
少5.6 g,题目中只减少2.9 g,故A燃烧时应同时生成2.7 g水,有机物中所含H元素的物
2.7g
质的量为n(H)= ×2=0.3 mol,所以此有机物中C、H元素物质的量之比是
18g⋅mol−1
1∶3,与含氧多少无关,故选项A、C、D均有可能,B选项符合题意。
5.【答案】A、B。
【解析】任意烃与一定量氧气充分燃烧的化学方程式:
y y
C x H y +(x+ 4 )O 2⃗点燃 xCO 2 + 2 H 2 O
当温度高于100℃时,生成的水为气体。若烃为气态烃,反应前后气体的体积不变,
即反应消耗的烃和O 与生成的二氧化碳和气态水的体积相等。
2
y y
∴1 + (x+ ) = x + y = 4
4 2
就是说气态烃充分燃烧时,当烃分子中氢原子数等于 4时(与碳原子数多少无关),
反应前后气体的体积不变(生成物中水为气态)。
6.【答案】C
【解析】烃在过量氧气中完全燃烧产物为CO 、HO及剩余O ,由于是恢复到室温,则
2 2 2
通过NaOH溶液后气体体积减少40mL为生成CO 体积。
2
y y
C x H y + (x+ 4 )O 2⃗点燃 xCO 2 + 2 H 2 O(g) ΔV
第7页y y
1 x+ x 1+
4 4
0.04 0.05
列式计算得:y=5x-4 当:
①x=1 y=1 ②x=2 y=6 ③x≥3 y≥11 只有②符合。(为什么?)
7.【解析】n(C)=n(CO )=0.1mol⇒m(C)=1.2g
2
n(H)=2n(H O)=0.15×2mol=0.3mol⇒m(H)=0.3g
2
n(O)=(2.3−1.2−0.3)/16=0.05mol
2.7
n(C):n(H):n(O)=0.1:( ×2):0.05=0.1:0.3:0.05=2:6:1
18
∴ 该有机物为C HO,即乙醇(C HOH)
2 6 2 5
第8页