一文读懂CRISPR Cas的编辑工具(Cas9, Cas12a, Cas12b, Cas12e, Cas13a, Cas13b, Cas13d)
从上一篇基因编辑文章中一口气聊一聊基因编辑(ZFN, TALEN, CRISPR Cas9),我们了解到ZFN、TALEN、CRISPR-Cas9等基因编辑工具其实离不开2大功能:一是特异性靶DNA的能力,另一个是切割靶DNA的能力。也就是定位靶目标核酸的部分,加上切割靶核酸的“剪刀”部分。对于CRISPR系统通过人为改造成基因编辑的工具,也是离不开对CRISPR系统在细菌抵御病毒的机制的研究。因此,想要熟悉基因编辑Cas系列的工具,正确的思路是“发现与特点-机制的研究和验证-性能优势突出”的过程。
一、Cas9
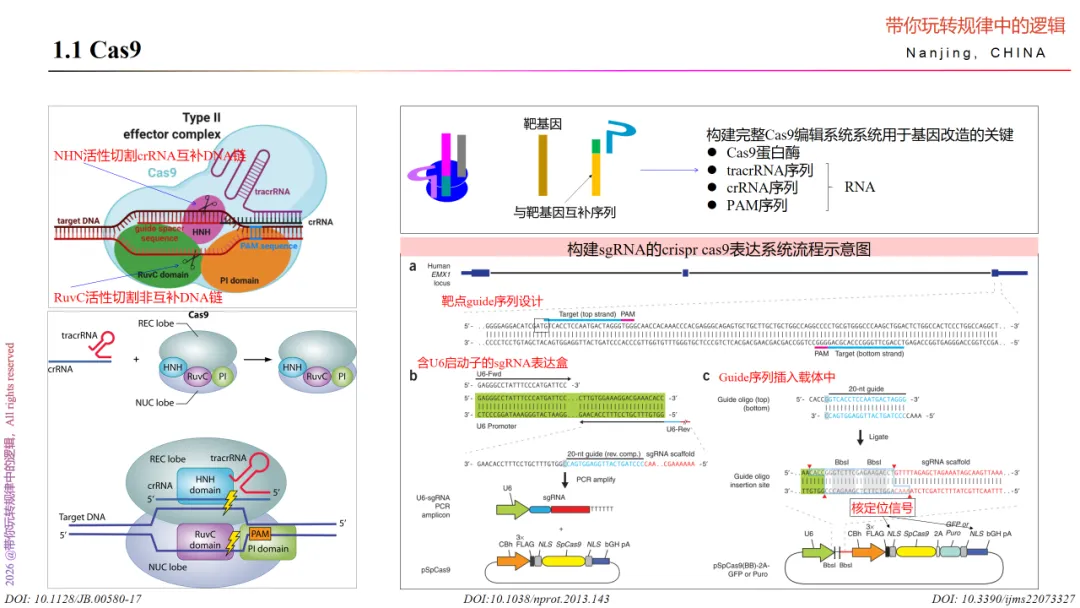
从原理中我们知道,CRISPR-Cas9抵御噬菌体病毒的机制是Cas9蛋白酶+tracrRNA+crRNA的“三元复合系统”协同作用的,因此,该系统要实现靶DNA切割功能时,需要具备两种能力,一种是与靶DNA互补的能力,一种是Cas9蛋白酶激活后的切割能力。对于与靶DNA互补的问题,解决“tracrRNA+crRNA”的序列即可。tracrRNA有一部分与crRNA互补,一部分行使支架作用—即scalfold序列,该序列决定了与Csa9蛋白酶的亲和力。那么,crRNA的序列则是关键。crRNA需要有20nt的序列与靶基因特异性配对,才能保证对特定DNA的识别。那么还有一个问题就是激活Cas9的切割活性了。Cas9有两个核酸酶活性,分别是HNH、RuvC。NHN活性切割crRNA互补DNA链、RuvC活性切割非互补DNA链。根据实验验证,增加PAM序列(Protospacer Adjacent Motif)序列是激活Cas9切割活性的前提,通常设计在靶基因的3’端。如来自S.pyogens菌的PAM序列通常为NGG。
因此,对Cas9系统的基因编辑的RNA结构设计,则应是“20nt crRNA(与靶基因配对) + PAM + scalfold(tracrRNA)”。
那么,对于构建Cas9系统,可以选择商业化的质粒或者自己构建,基本的方法就是分子克隆。鉴定构建好的Cas9系统,可以是通过WB、银染、或者对核酸大小的毛细管电泳检测。亦可是通过构建的质粒或含有报告基因的质粒转染细胞中,直接定量基因或者间接检测基因的表达水平的变化。
二、Cas12a
Cas12a是2015年由张锋团队首次鉴定和报道的。曾用名为Cpf1,因来自prevotella和francisella 1而得名。
Cas12a未结合靶DNA时是二元复合物,由“Cas12a+crRNA”组成,相较于Cas9省去了tracrRNA序列。因此,搞清楚Cas12a的作用机制和crRNA的序列特点,即可使用该工具。
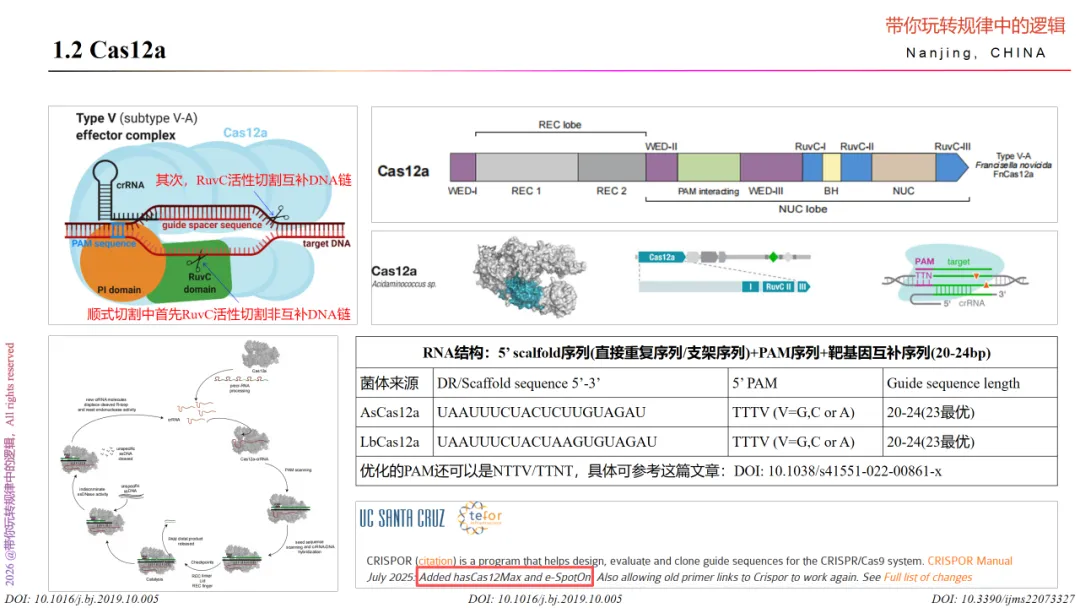
Cas12a由REC和Nuc组成双叶结构。Cas12a的切割能力位于Nuc上。Nuc则由RuvC结构域、PI结构域和WED结构域组成,WED结构域是Cas12a处理自身crRNA的RNase位点所在;Nuc和RuvC结构域之间的界面则是保证Cas12a切割DNA的DNase位点,并且Ruvc结构域含有催化中心,能够准确识别目标序列,在二价金属镁离子Mg2+的催化下精确地切割DNA产生粘性末端的双链DNA断裂。
具体的原理如下:在pre-crRNA转录后,Cas12a具有核糖核酸内切酶活性可直接将pre-crRNA直接加工成熟的crRNA,无需tracrRNA和RNaseⅢ的参与;当形成crRNA-Cas12a复合物时,RuvC结构域在距离PAM位点附近识别DNA非靶标链中特定的PAM序列,在PAM识别后,Cas12a解开靶DNA的局部双链结构,使crRNA的“spacer”区与靶DNA的互补链通过碱基配对形成R-loop复合物;Cas12a具有的RNA引导的DNase活性行使切割DNA靶标链行为,形成断裂的双链DNA分子并产生5’粘性末端双链DNA断裂。此外,R-loop形成也同时触发Cas12a的反式切割活性(trans-cleeavage)–非特异性切割周围的单链DNA分子。
上述中Cas12a通过识别富含T的PAM序列定位切割位点,常用的PAM序列的通式为(5’TTTN或5’TTN)。常用的Cas12a以来自氨基酸球菌属的BV3L6菌株(AsCas12a)和毛螺科细菌(LbCas12a)为主。其中AsCas12a和LbCas12a均偏好识别5’TTTN的PAM序列。
关于Cas12a的RNA序列设计,可参考下图表内容,亦可检索原始文献学习。
三、Cas12b
Cas12b,又称C2c1,是II由crRNA和tracrRNA共同介导(或融合体sgRNA单独介导)对特定核酸具有顺式和反式切割活性的核酸内切酶。即该系统可理解为“Cas12b+crRNA+tracrRNA”,既要了解Cas12b的酶切割活性,又要了解crRNA和tracrRNA的序列及与Cas13b的相互作用。最常用的Cas12b来源于嗜酸耐热菌 Alicyclobacillus acidoterrestris (AaCas12b)。
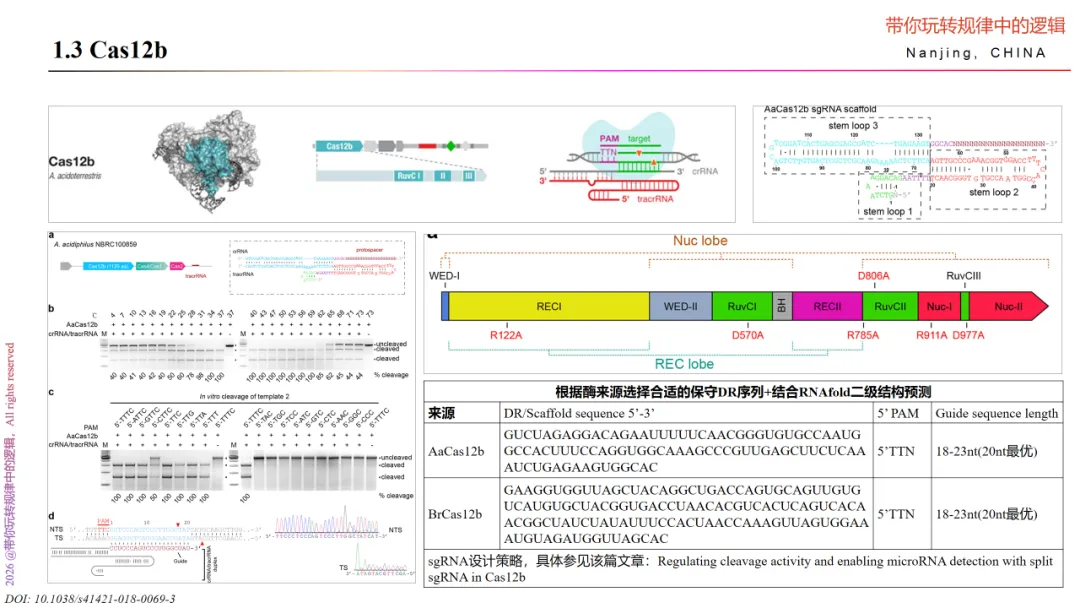
Cas12b是一个多功能蛋白,包含RNA结合域、单个RuvC核酸酶域(NUC叶和REC叶组成)和DNA结合域。
Cas12b能特异性识别并剪切带PAM(5’-TTN-3,5’-T rich)的dsDNA,使DNA双链断裂并生成黏性末端。这种切割能力离不开Cas12b与特定的crRNA结合后激活的切割酶活性。crRNA提供与靶DNA互补的序列,决定了其识别靶点。多个crRNA可以同时作用于一个Cas12b。Cas12b在结合crRNA前处于不活性状态。只有crRNA完全与靶DNA杂交后,其核酸酶域才被激活,内切DNA。激活的Cas12b会在crRNA结合位点产生双链断裂,切出一段DNA片段。然后会继续非专属性内切周围的DNA,产生短片段。因Cas12b在激活后活性逐渐减弱,也就限制了其作用于非专属性DNA内切的范围,但是在高DNA浓度条件下,该行为依旧可产生较大范围的非专属性切割。
此外,Cas12b特异性的剪切ssDNA靶标不依赖PAM序列–双链或单链DNA靶标均能激活AacCas12b的反式剪切活性(即旁路剪切活性/附属剪切活性),即当AaCas12b酶与sgRNA、靶标DNA结合形成三元复合物后,便会被激活针对非特异序列ssDNA的反式剪切活性,可无差别地剪切反应体系中任意序列的ssDNA。
对于Cas12b的RNA序列设计可参考下述图表内容,亦可查阅文献。
四、Cas12e/CasX
CasX系统是2016年由Jennifer Doudna研究团队发现的新型的CRISPR Cas系统,大小不到1000个氨基酸,是从一类纳古菌门的古菌中分离出来的,打破了CRISPR Cas编辑系统在细菌中的认知。
那么,CasX究竟是怎样的呢?
首先,CasX基因编辑系统包含CasX、tracrRNA、和crRNA,这和Cas12b很像,因此想要了解清楚,就需要研究明白这三部分的内容。
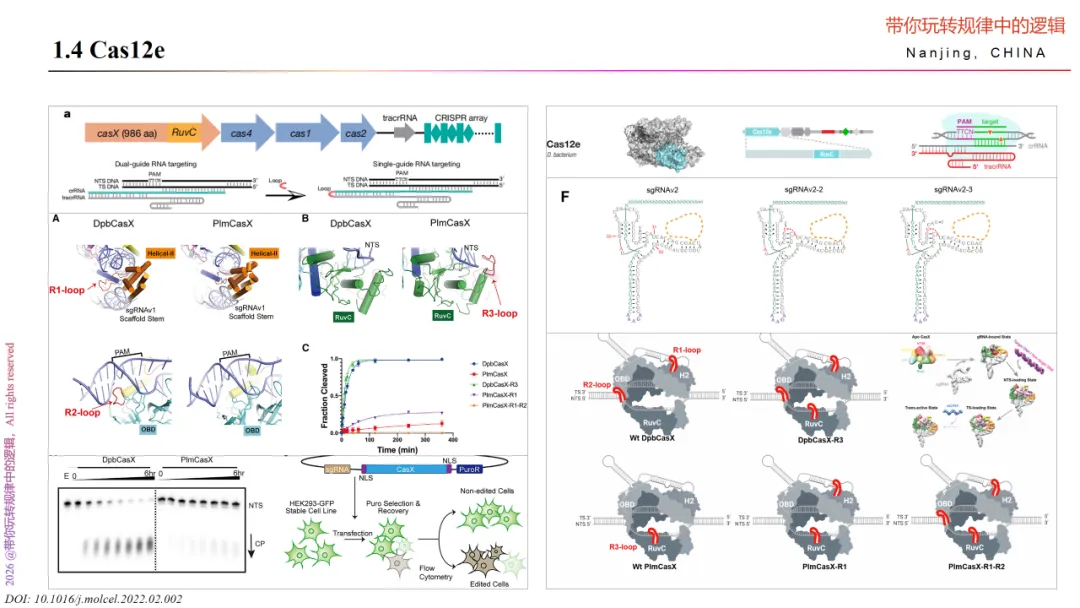
对于CasX,其结构域和其它的Cas蛋白有所不同,除了RuvC外,还包含Helical-I、Helical-II、OBD(寡聚结合结构域、RuvC 和 BH(桥螺旋)以及全NTS(非目标链结合)和目标链 (TS)。 NTS结构域包含一个四链β折叠,位于DNA的非目标链旁边。TS结构域位于与V 型 CRISPR Cas 系统的其他酶的Nuc结构域共同负责RuvC活性位点中的靶链位置。
其次,CasX的分子机制关键过程为:通过转录成成熟的crRNA与CasX蛋白结合,形成核糖核蛋白复合体,其中CasX的crRNA结合通道具有独特的双茎环结构;CasX通过识别5’TTCN(N为任意碱基)的PAM序列(原型间隔相邻基序),由其REC1/REC2结构域诱导局部DNA解旋,暴露出靶链,使crRNA的5’端10-12nt(种子区域)与靶DNA配对后触发构象变化,形成完整的R-loop结构,此时,CasX的NTS结构域(非靶链结合域)稳定非靶链,同时PI结构域(催化核心)被激活;在CasX的切割下,非靶链PAM上游12-14个核苷酸和靶链上PAM后的22-25个核苷酸被切割,产生长度约10个核苷酸的粘性末端产物。
另外,CasX蛋白的切割效率也离不开低盐的环境。根据文献,Cas12e在低浓度盐环境下更易形成R-loop和高切割活性,而高盐则会抑制其活性。因此,合适的盐环境对Cas12e的切割效率至关重要。
因此,设计CasX实验时,除了需要考虑crRNA的序列外,还应考虑整个反应条件的适配性。关于序列设计可以参考《CasX enzymes comprise a distinct family of RNA-guided genome editors》文章的设计思路,里面包含序列信息,合成后的序列通过T7体外转录的方式获得。当然,也可以选择其它文献,如《“X” marks the spot: Mining the gold in CasX for gene editing》。
五、Cas13a
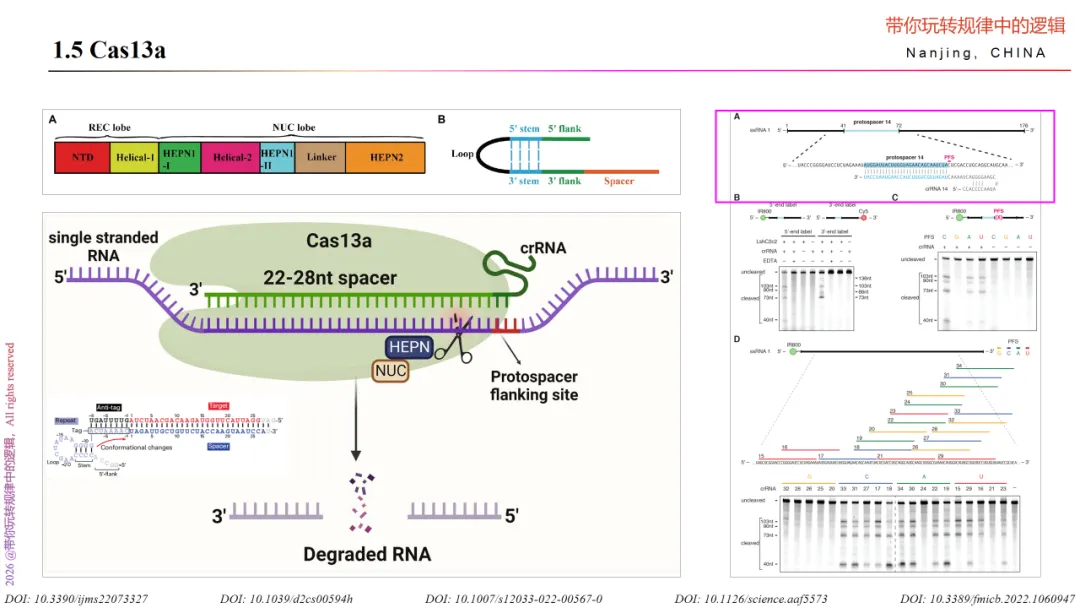
Cas13a是2016年被张锋教授团队利用来源于Leptotrichia shahii的Cas13a(LshCas13a)证实在哺乳动物细胞中具有靶向切割RNA活性的酶。相较于Cas12a,除了是单一crRNA与之结合外,即由Cas13a和crRNA的二元复合物与靶RNA形成三元结构,主要有3大关键点不同。
首先,Cas13a的蛋白结构域。cas13a蛋白由两个主要结构域组成,即REC和NUC叶片。其中REC包含NTD和Helical-1结构域,主要是负责识别并结合crRNA的;NUC包含2个HEPN结构域、Helical-2结构域、和连接两个HEPN结构域的连接结构域,其中HEPN域的激活被认为与靶RNA的识别有关,并进一步驱动蛋白构象的变化,产生复合的RNA酶活性位点,主要是负责切割RNA的。Cas13a在识别与crRNA间隔序列互补的目标序列(22–28 nt)后切割单链RNA(ssRNA)。
其次,Cas13a不需要在目标序列旁边的间隔邻近基序(Protospacer Adjacent Motif,PAM)才能行使内切酶活性,而是更倾向于位于3’间隔区侧翼位点(Protospacer Flanking Site,PFS)旁边的腺嘌呤、尿嘧啶或胞嘧啶。Cas13a只需要24个碱基的crRNA,它通过富含尿嘧啶的茎环结构与Cas13a分子相互作用,并通过Cas13a的一系列构象变化来促进目标的切割。当靶标RNA存在特定PFS序列时,crRNA与靶 RNA特定位点配对形成Cas13a+crRNA+靶 RNA的三元复合体,继而Cas13a的两个HEPN结构域发生构象变化,激活切割RNA的活性。此外,Cas13a 除了能精准切割靶RNA,还具有非特异性单链RNA反式切割活性,激活后能高效地切割体系中任意单链 RNA。
最后,来源菌体的Cas13a蛋白的gRNA设计时的DR序列的选择。DR(Direct Repeat)序列是与Cas13a蛋白特异性结合的关键区域,而且参与形成crRNA的茎环结构,对维持crRNA的二级结构的稳定性至关重要。DR序列的选择取决于所使用的Cas13a蛋白的来源菌株。常用的菌株有Leptotichia buccalis (Lbu)和Leptotrichia wadei (Lwa)。各自的DR专属序列分别为:Leptotichia buccalis (Lbu)菌株的DR为:GGACCACCCCAAAAAUGAAGGGGGACUAAAAC,Leptotrichia wadei(Lwa)菌株的DR序列为:GAUUUAGACUACCCCAAAAAACGAAGGGGACUAAAAC。
此外,Cas13a也能容忍crRNA与目标序列之间的单个错配,但错配若大于2个,则切割效率就会降低。它的PFS序列位于间隔区的3’端,由A、U 或C碱基组成。
了解了这些,Cas13a的crRNA就不难设计了,如果觉得难,不妨仔细阅读《C2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector》文章,涵盖序列分析。
六、Cas13b
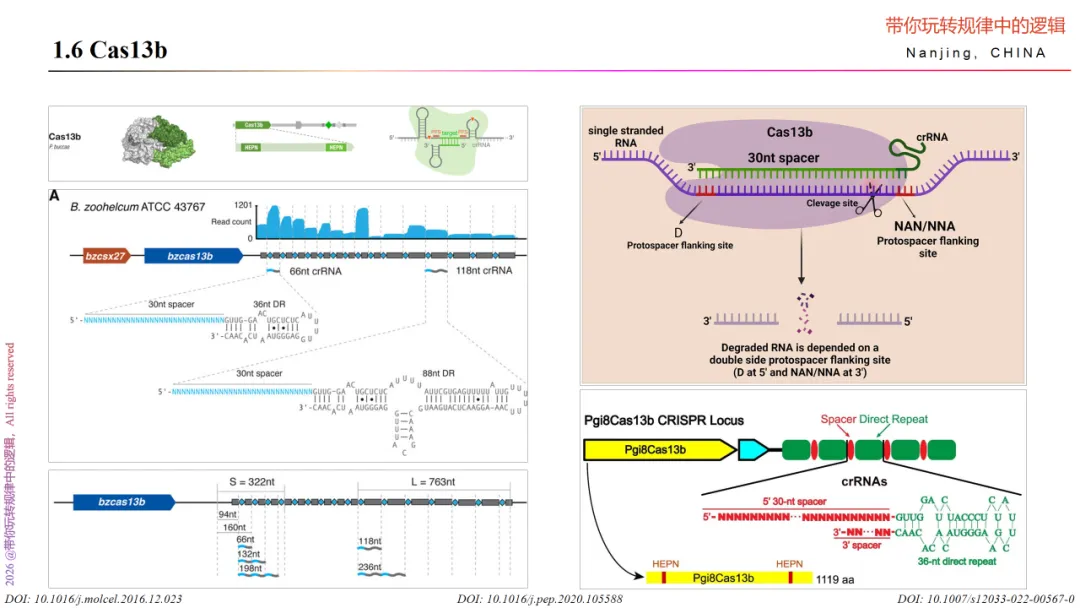
Cas13b和Cas13a在复合物上,也是由Cas13b+crRNA+Target RNA的三元结构。其拥有的两个HEPN结构域主要由α螺旋构成:HEPN1由12个线性连接的α螺旋组成,螺旋间通过柔性环连接。HEPN2包含9个α螺旋、若干短β链以及一个尖端带有带电残基的β发夹结构,该发夹尖端指向活性位点口袋。HEPN2位于HEPN1之上,使得活性位点残基,能够组装成一个典型的HEPN活性位点。 HEPN1结构域通过一个高度保守的结构域间连接肽(IDL)与Helical-1结构域相连,该连接肽横跨一个带正电荷的大型内部通道中心区域。
另外,与Cas13a相比,Cas13b在PFS上是有所不同的。要求5’端非C或者3’端通式NAN/NNA,这样有助于crRNA与Cas13b复合物的形成以及增强靶向的特异性。
对于crRNA序列的设计,可以遵循下图参考,亦可选择基因序列后在CHOPCHOP网站设计靶序列后,再加上DR序列,如选择来自Prevotella sp.菌的(PspCas 13b)DR序列:GUUGUGGAAGGUCCAGUUUUGAGGGGGCUAUUACAAC。
七、Cas13d
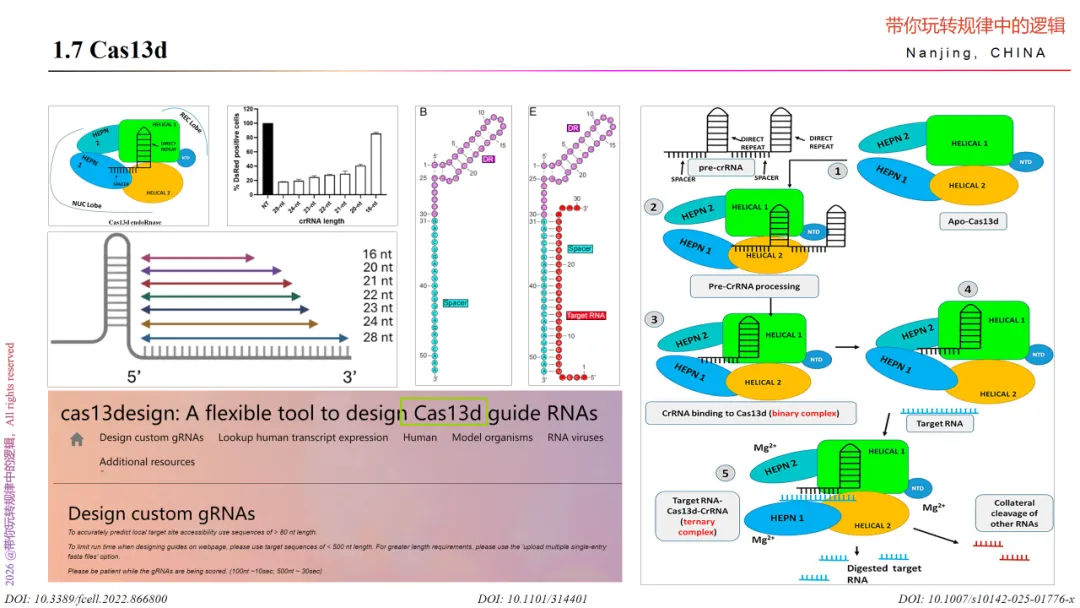
Cas13d同样是一种双叶效应蛋白,由一个crRNA”识别”叶(REC)和一个”核酸酶”叶(NUC)组成。REC叶包含两个结构域:N端结构域(NTD)和Helical-1结构域。NTD包含7条反平行β折叠和两个短α螺旋,而Helical-1结构域由8个α螺旋组成。NTD和Helical-1结构域的主要功能是识别并与crRNA的茎环重复序列和间隔区相互作用;两个HEPN结构域(HEPN1和HEPN2)和一个Helical-2结构域。HEPN1结构域由10个α螺旋组成,而HEPN2由11个α螺旋组成,它们通过HEPN1的α-3螺旋和HEPN2的α-28螺旋进一步相互作用。Helical-2结构域由8个α螺旋组成,最终包裹在HEPN2结构域的α-28螺旋周围。NUC叶的两个HEPN结构域和Helical-2结构域主要功能是稳定Cas13d-crRNA-靶RNA三元复合物的结合。
值得补充的是HEPN1结构域作为铰链,通过提供结构支架连接Cas13d的两个叶状结构;而HEPN2结构域不仅提供RNA切割的催化位点,还提供前体crRNA切割的催化位点。因此,Cas13d也是一种双功能核酸酶效应蛋白,能够像其他Cas13内切核糖核酸酶一样催化前体crRNA成熟并产生RNA切割活性。
那么,整个Cas13d的切割过程是怎样的呢?主要过程可分为三步。
第一步:crRNA与Cas13d的二元复合物的形成。Cas13d与前体crRNA组装,同时在crRNA内部切割形成成熟的crRNA,该成熟crRNA由30个核苷酸的5’端直接重复区(DR)和20个核苷酸的3’端间隔区(与靶标ssRNA互补)组成。在成熟crRNA生成后,Cas13d通过NTD和HEPN2结构域识别并钳制5’端crRNA柄/DR的前两个碱基对(bp),而3’端间隔区则被夹在螺旋-1和螺旋-2结构域之间。HEPN1结构域作为铰链,通过提供结构支架连接Cas13d的两个叶状结构,从而形成带正电荷的溶剂暴露RNA密度区。
第二步:稳定构象。crRNA与Cas13d结合后形成半开放蛤壳状的溶剂暴露二元复合物(又称”监视复合物”)。该Cas13d-crRNA复合物,已准备好主动搜索并识别互补的靶标ssRNA。3’端crRNA间隔区的三个U型转折及其与Cas13d的相互作用有助于进一步稳定二元复合物的构象,使其能够与靶标ssRNA结合。该Cas13d-crRNA二元复合物在结合靶标ssRNA前保持核酸酶失活状态。
第三步:靶标切割。当二元复合物找到靶标ssRNA后,间隔区与Cas13d之间的大部分相互作用被消除,使间隔区能与靶标ssRNA形成新的相互作用,构建双链A型RNA螺旋。同时,Cas13d的所有结构域会与crRNA间隔区和靶标ssRNA的糖-磷酸骨架形成新的相互作用(这些相互作用发生在由HEPN-1、螺旋-1和螺旋-2结构域界定的中央裂隙中),从而形成Cas13d-crRNA-靶标ssRNA三元复合物。该三元复合物又称”切割活性”复合物,因为带有两个R-X4-6-H基序的HEPN1和HEPN2结构域会形成催化性内切核糖核酸酶HEPN二聚体,从而产生双组分活性位点来介导靶标ssRNA和旁系ssRNA的水解。
在整个切割过程中,要保证Cas13d内切酶活性,需要特殊要求来满足。如HEPN核酸酶活性强烈依赖靶标ssRNA的碱基配对–与crRNA间隔区完全互补(>21个核苷酸)时Cas13d呈现完全构象激活和最佳切割活性;18-20个核苷酸互补时仅呈现半最大切割活性;在crRNA间隔区的两个特定区域(内部区域:间隔区核苷酸5-8;3’端区域:核苷酸13-22)与靶标ssRNA存在错配时,会完全消除ssRNA切割活性;Cas13d仅能切割结构可及的ssRNA序列,若靶标RNA存在二级结构则无法识别且RNA切割活性丧失;Cas13d对PFS限制的ssRNA切割没有偏好性,但对靶标ssRNA结构中的尿嘧啶碱基表现出明显偏好;Mg2+和辅助组件WYL结构域的存在可增强内切核糖核酸酶活性。这些特殊要求为设计Cas13d的实验提供了参考依据。
那么,该如何设计Cas13d的crRNA序列呢?因为Cas13d对PFS序列是非必须的,因此,设计时选择靶序列配对的长度和DR序列即可。根据已有文献支撑,靶序列长度为28nt结果最佳,DR序列依旧遵从来源的菌体,如Ruminococcus flavefaciens XPD3002的DR序列为CCCCUACCAACUGGUCGGGGUUU。当然,也可以通过软件设计,如Cas13 design在线工具。
全篇总结
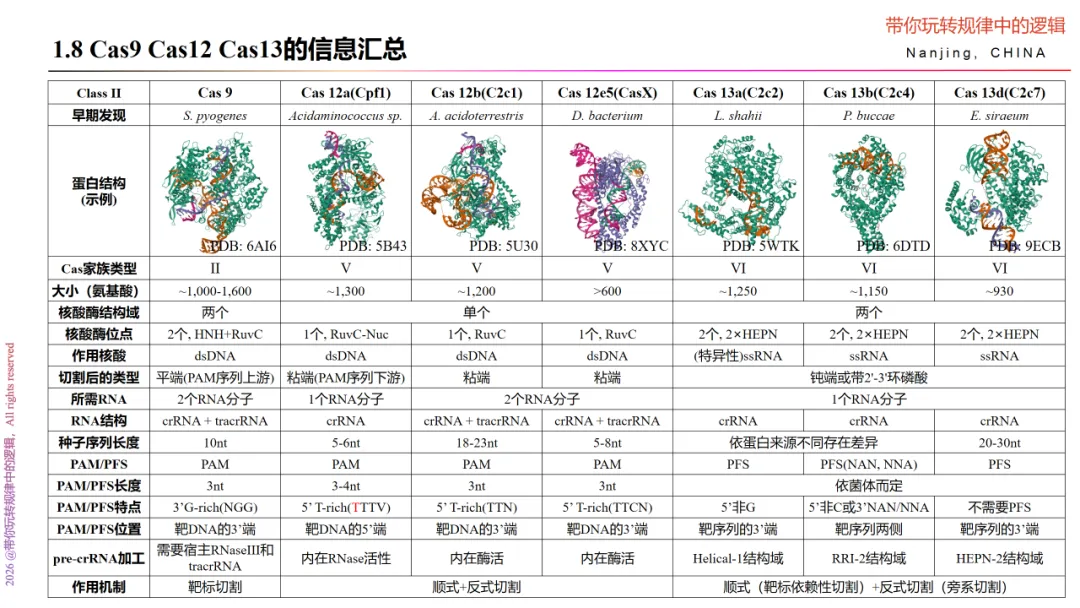
总的来说,Cas系列的基因编辑工具具有以下3大共性:(1)需要RNA结构稳定成二元或三元复合物;(2)crRNA序列的设计离不开Cas蛋白来源的菌体特异性识别的Scalfold序列或者DR序列,同时需要考虑PAM或PFS(Cas13系统特有)的问题;而且在设计时,可参考已有文献报道或者通过在线工具设计,最后经过二级结构预测避免非特异性;(3)拥有自己的核酸酶结构域,无论是1个还是2个,主要作用都是行使靶序列特异性识别下的位点切割。
此外,对于Cas13系列,反式切割活性高低,则是Cas13a > Cas13b > Cas13d。
 夜雨聆风
夜雨聆风




