QB沙龙总结 | AI-驱动分子科学中发现:以LUMI实验室为例
序
近年来,mRNA疗法在疫苗开发和基因治疗领域展现出巨大潜力,而高效、安全的递送系统仍是其临床应用的关键瓶颈。离子化脂质作为脂质纳米颗粒(lipid nanoparticles, LNPs)的核心组成部分,对mRNA的递送效率具有决定性作用。然而,传统的分子筛选流程依赖大量人工参与,包括分子设计、合成、纯化及功能表征,不仅耗时耗力,而且筛选效率有限。随着人工智能和自动化技术的发展,自驱实验室(Self-driving laboratory, SDL)逐渐成为加速材料与药物发现的重要工具。相较于仅能进行单次设计的开环模式,闭环SDL通过主动学习(Active learning)在“设计—合成—测试—再设计”的循环中不断优化候选分子,显著提升筛选效率和成功率。LUMI-lab正是这一新兴研究范式的代表性成果之一。
近日,来自加拿大多伦多大学的Bowen Li与Bo Wang团队在国际顶级期刊Cell上发表了题为LUMI-lab: A foundation model-driven autonomous platform enabling discovery of ionizable lipid designs for mRNA delivery的研究论文。该研究构建了一个由基础模型(Foundation Model)驱动的自驱实验室平台——LUMI-lab。研究团队以大规模无监督预训练模型LUMI作为系统的“决策大脑”,并整合机械臂与高通量自动化筛选平台,通过主动学习策略实现分子设计与实验验证的闭环优化。在10个迭代循环中,LUMI-lab系统性地评估了约1,700种可离子化脂质,最终筛选出性能优异的溴化脂质LUMI-6,其在小鼠肺上皮细胞中的体内基因编辑效率达到20.3%,显著优于现有递送体系。该研究充分展示了基础模型驱动的SDL在加速新型递送材料发现中的巨大潜力。

沙
龙
总
结

文章首先构建了LUMI-lab自驱实验室平台(图1),实现了从分子设计到体内功能验证的全流程自动化。该平台由三大核心模块组成:基础模型LUMI、自动化实验系统以及主动学习闭环。LUMI模型基于大规模化学结构数据进行无监督预训练,能够生成具有潜在高性能的离子化脂质结构;自动化实验系统通过机械臂和微流控装置完成LNP的制备与表征;主动学习模块则根据实验反馈不断优化分子设计策略,从而形成高效的闭环筛选流程。这一平台显著减少了人工干预,提高了实验的可重复性和筛选效率。
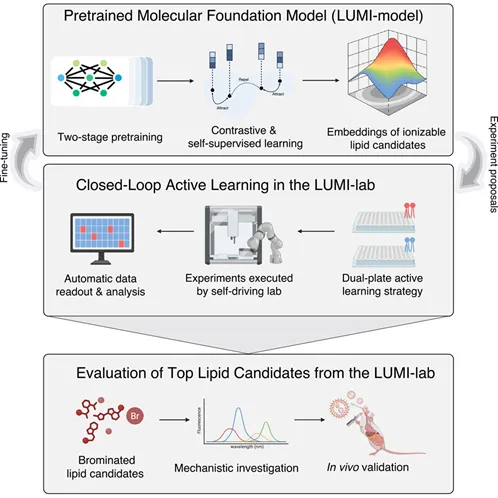
图1. LUMI-lab 研究概览
在模型层面,研究团队利用两阶段大规模小分子结构、离子化脂质相关数据对LUMI进行无监督预训练,使其能够学习分子结构与递送性能之间的潜在关联。随后,在第三阶段通过少量实验数据对模型进行微调,使其具备更准确的性能预测能力(图2)。结果表明,LUMI在候选分子的生成质量、多样性以及性能预测方面均优于传统机器学习方法,显示出基础模型在化学分子设计中的显著优势。此外,模型还能捕捉影响递送效率的关键结构特征,为理性分子设计提供理论依据。
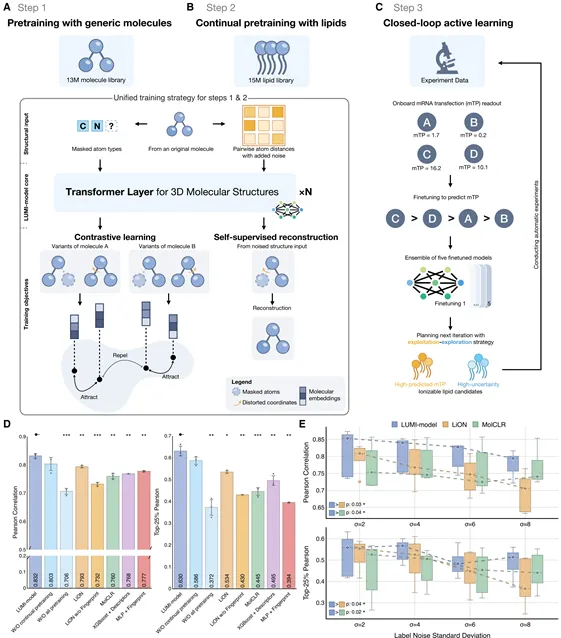
图2. LUMI模型预训练与基准测试
LUMI-lab通过主动学习策略实现了高效的闭环优化(图3)。在每一轮迭代中,模型根据已有实验数据选择效果最好与模型预测不确定性最高的候选分子以增强搜索深度和广度,随后自动完成脂质合成、LNP制备及体内外功能评估,并将实验结果反馈至模型以指导下一轮设计。通过10个迭代循环,系统共测试了约1,700种离子化脂质,筛选效率显著高于传统方法。这一结果充分证明了闭环SDL在复杂生物材料发现中的高效性与可行性。
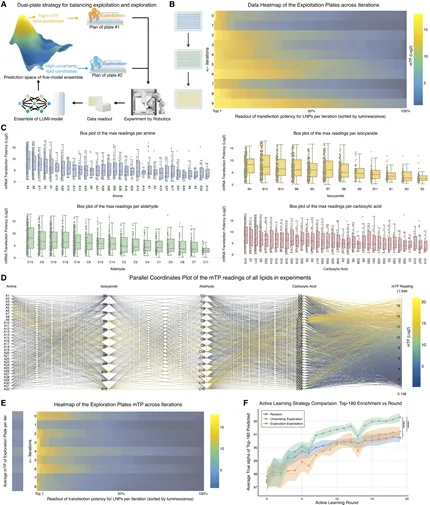
图3. LUMI-lab 主动学习轨迹
在多轮迭代优化后,研究团队成功鉴定出性能最优的候选分子LUMI-6。该溴化离子化脂质在小鼠肺上皮细胞中的体内基因编辑效率达到20.3%,显著优于现有主流离子化脂质材料。同时,LUMI-6在生物相容性和递送稳定性方面也表现出良好的综合性能,验证了LUMI-lab在发现高效mRNA递送材料方面的强大能力(图4)。
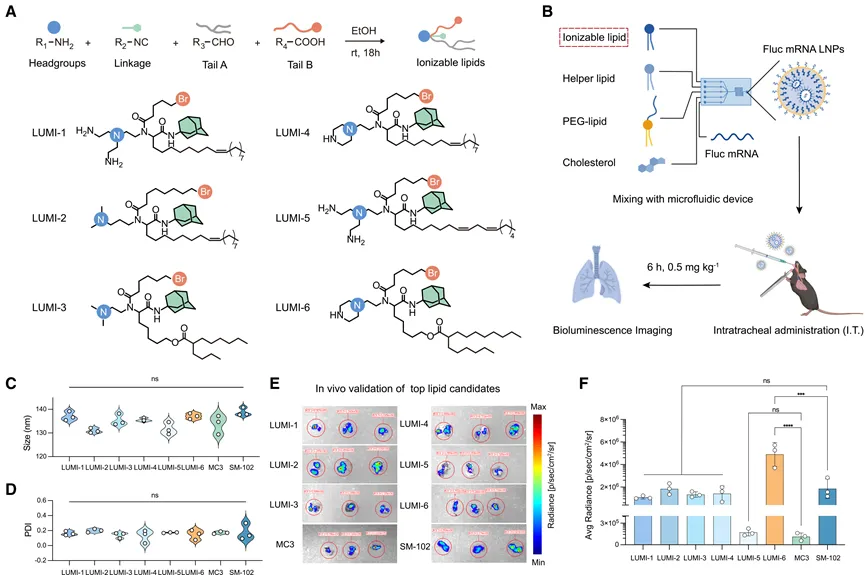
图4. 体内验证 LUMI-lab 设计的分子
为了进一步理解模型的设计逻辑,研究团队对LUMI生成的高性能脂质进行了结构分析(图5)。结果显示,头基的电离特性、疏水尾链的长度与支化程度以及连接基团的化学性质均对递送效率产生重要影响。这些发现不仅验证了模型预测的可靠性,也为未来离子化脂质的理性设计提供了重要指导,体现了基础模型在化学与生物医学研究中的可解释性价值。
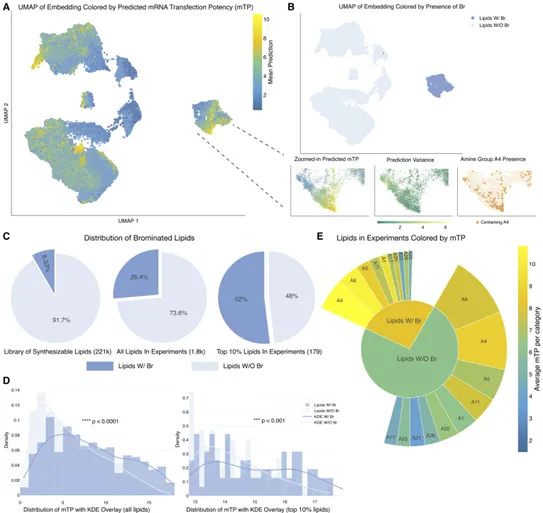
图5. 高性能离子化脂质表征
总结与讨论
综上所述,该研究首次将基础模型(Foundation Model)深度融入自驱实验室(Self-Driving Laboratory, SDL)体系,提出了“Foundation Model + SDL”的创新研究范式,实现了离子化脂质从分子设计到体内功能验证的全流程自动化与智能化。通过主动学习驱动的闭环优化,LUMI-lab在短时间内系统筛选了约1,700种候选分子,并成功发现高性能离子化脂质LUMI-6,显著提升了mRNA递送效率,展示了人工智能与自动化实验深度融合在生物医药材料发现中的巨大潜力。
尽管如此,该研究仍存在一些值得关注的局限性。首先,SDL在涉及小鼠等动物实验时面临标准化和规模化的挑战。与体外高通量筛选不同,动物实验易受到个体差异、操作流程、伦理审批以及实验环境等多重因素的影响,这些变量增加了实验结果的不确定性,也限制了SDL在体内研究中的自动化与可重复性。此外,动物实验的成本和周期较高,使得闭环迭代的效率在一定程度上受到制约,未来亟需发展更加标准化的操作流程或替代模型(如类器官与微生理系统)以提升SDL的适用性和可扩展性。
其次,文章中所探索的可离子化脂质的化学合成路线相对简单,主要集中于模块化结构的组合与修饰。这种设计策略虽然有利于高通量合成和自动化筛选,但在一定程度上限制了化学空间的多样性,可能导致所发现分子的结构新颖性不足。更复杂或具有挑战性的合成路线尚未被充分纳入SDL体系,这提示未来研究需要将自动化合成技术与更广泛的有机化学反应相结合,以进一步拓展可探索的分子结构范围。
此外,平台建设和运行成本也是需要考虑的现实问题。LUMI-lab依赖于先进的机器人系统、高通量筛选设备以及计算资源,这在一定程度上限制了其在普通实验室中的普及应用。同时,基础模型在跨领域任务中的泛化能力及其决策过程的可解释性仍有待进一步提升。
展望未来,LUMI-lab所代表的研究范式为智能化科研提供了重要方向。随着自动化实验技术、人工智能算法以及替代生物模型的不断发展,SDL有望在药物递送系统、蛋白质工程、小分子药物设计及功能材料发现等多个领域发挥更大的作用。特别是通过引入类器官、器官芯片(organ-on-a-chip)等新型体外模型,可以在提高实验标准化程度的同时减少对动物实验的依赖,从而进一步提升闭环优化的效率与伦理可接受性。
在讨论层面,该研究也引发了若干值得关注的科学问题:例如,如何在保证自动化效率的同时提升化学空间的探索深度;如何实现体内实验的标准化与可扩展性;以及基础模型在分子设计中的可解释性与可靠性等。这些问题的深入探讨将为SDL技术的进一步发展提供重要启示。

QB期刊介绍
Quantitative Biology (QB)期刊是由清华大学、北京大学、高等教育出版社联合创办的全英文学术期刊。由高等教育出版社和Wiley双平台出版和发行。QB主要刊登生物信息学、计算生物学、系统生物学、理论生物学和合成生物学的最新研究成果和前沿进展,并为生命科学与计算机、数学、物理等交叉研究领域打造一个学术水平高、可读性强、具有全球影响力的交叉学科期刊品牌。
QB期刊目前已被ESCI, PMC,Scopus, CSCD等国内外重要数据库收录。
 夜雨聆风
夜雨聆风




