文档内容
专练 46 滴定曲线的综合应用
授课提示:对应学生用书91页
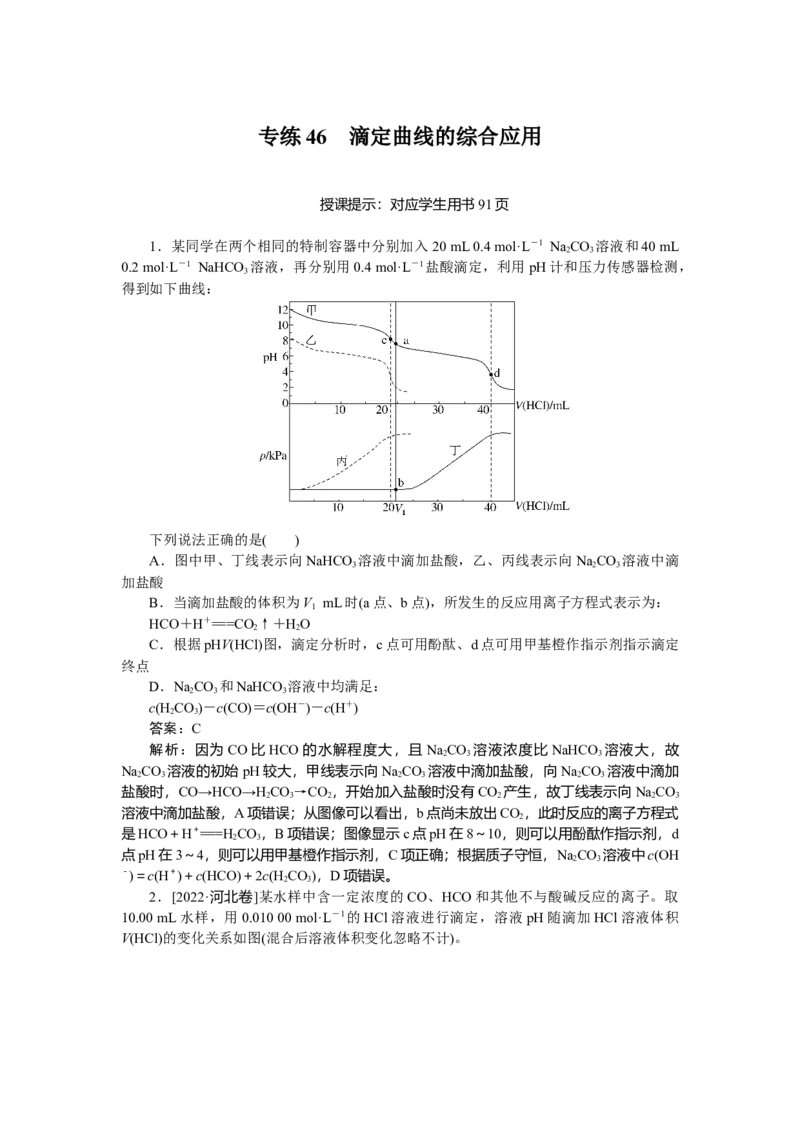
1.某同学在两个相同的特制容器中分别加入 20 mL 0.4 mol·L-1 Na CO 溶液和40 mL
2 3
0.2 mol·L-1 NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,利用pH计和压力传感器检测,
3
得到如下曲线:
下列说法正确的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴
3 2 3
加盐酸
B.当滴加盐酸的体积为V mL时(a点、b点),所发生的反应用离子方程式表示为:
1
HCO+H+===CO ↑+HO
2 2
C.根据pHV(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定
终点
D.NaCO 和NaHCO 溶液中均满足:
2 3 3
c(H CO)-c(CO)=c(OH-)-c(H+)
2 3
答案:C
解析:因为CO比HCO的水解程度大,且 NaCO 溶液浓度比NaHCO 溶液大,故
2 3 3
NaCO 溶液的初始pH较大,甲线表示向NaCO 溶液中滴加盐酸,向NaCO 溶液中滴加
2 3 2 3 2 3
盐酸时,CO→HCO→H CO→CO ,开始加入盐酸时没有CO 产生,故丁线表示向NaCO
2 3 2 2 2 3
溶液中滴加盐酸,A项错误;从图像可以看出,b点尚未放出CO,此时反应的离子方程式
2
是HCO+H+===H CO,B项错误;图像显示c点pH在8~10,则可以用酚酞作指示剂,d
2 3
点pH在3~4,则可以用甲基橙作指示剂,C项正确;根据质子守恒,NaCO 溶液中c(OH
2 3
-)=c(H+)+c(HCO)+2c(H CO),D项错误。
2 3
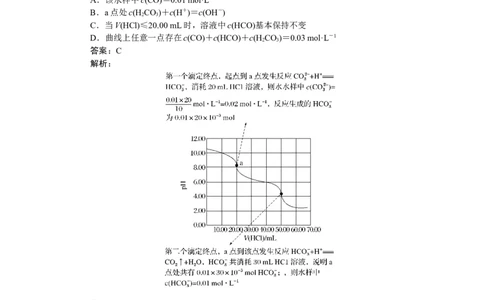
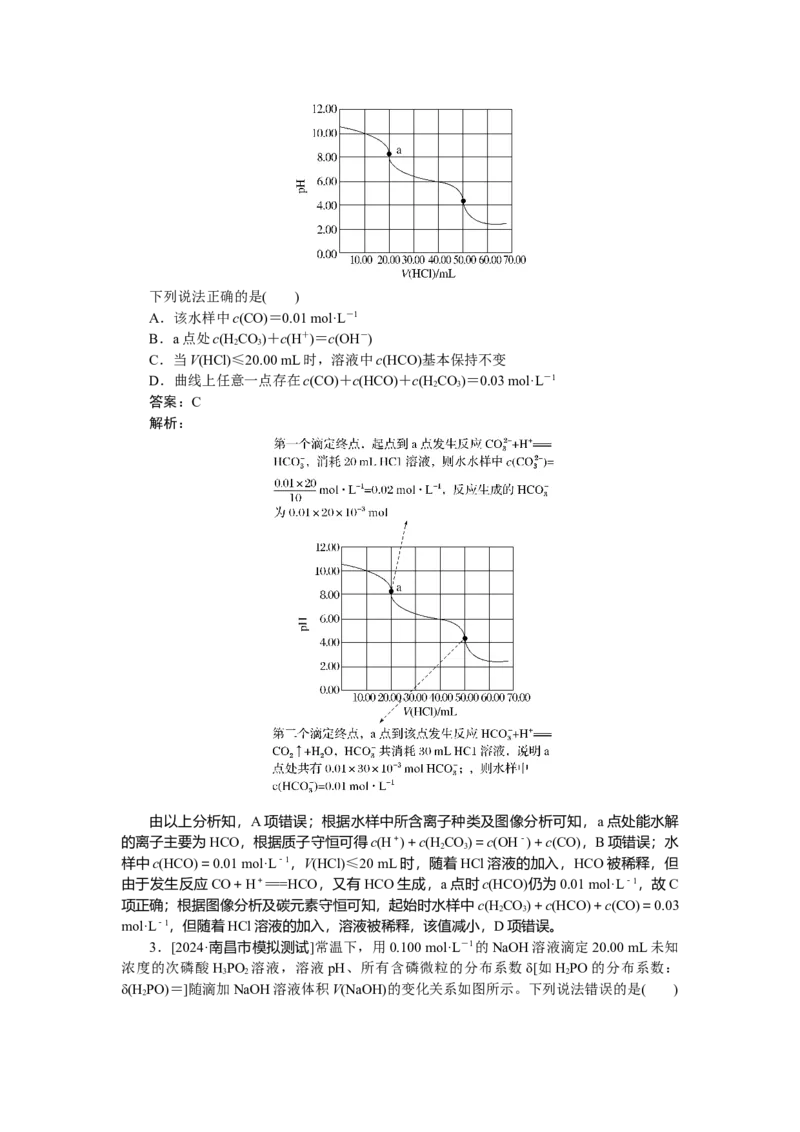
2.[2022·河北卷]某水样中含一定浓度的CO、HCO和其他不与酸碱反应的离子。取
10.00 mL水样,用0.010 00 mol·L-1的HCl溶液进行滴定,溶液pH随滴加HCl溶液体积
V(HCl)的变化关系如图(混合后溶液体积变化忽略不计)。下列说法正确的是( )
A.该水样中c(CO)=0.01 mol·L-1
B.a点处c(H CO)+c(H+)=c(OH-)
2 3
C.当V(HCl)≤20.00 mL时,溶液中c(HCO)基本保持不变
D.曲线上任意一点存在c(CO)+c(HCO)+c(H CO)=0.03 mol·L-1
2 3
答案:C
解析:
由以上分析知,A项错误;根据水样中所含离子种类及图像分析可知,a点处能水解
的离子主要为HCO,根据质子守恒可得c(H+)+c(H CO)=c(OH-)+c(CO),B项错误;水
2 3
样中c(HCO)=0.01 mol·L-1,V(HCl)≤20 mL时,随着HCl溶液的加入,HCO被稀释,但
由于发生反应CO+H+===HCO,又有HCO生成,a点时c(HCO)仍为0.01 mol·L-1,故C
项正确;根据图像分析及碳元素守恒可知,起始时水样中 c(H CO)+c(HCO)+c(CO)=0.03
2 3
mol·L-1,但随着HCl溶液的加入,溶液被稀释,该值减小,D项错误。
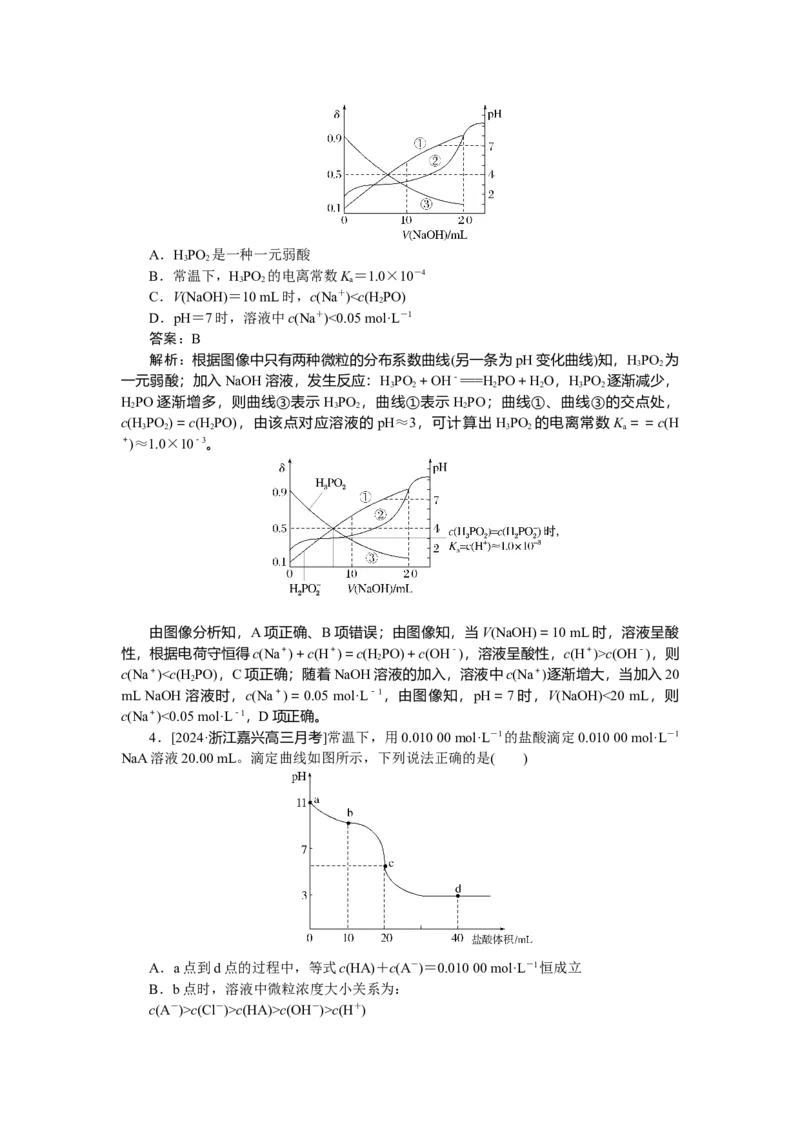
3.[2024·南昌市模拟测试]常温下,用0.100 mol·L-1的NaOH溶液滴定20.00 mL未知
浓度的次磷酸HPO 溶液,溶液pH、所有含磷微粒的分布系数δ[如HPO的分布系数:
3 2 2
δ(H PO)=]随滴加NaOH溶液体积V(NaOH)的变化关系如图所示。下列说法错误的是( )
2A.HPO 是一种一元弱酸
3 2
B.常温下,HPO 的电离常数K=1.0×10-4
3 2 a
C.V(NaOH)=10 mL时,c(Na+)c(OH-),则
2
c(Na+)c(Cl-)>c(HA)>c(OH-)>c(H+)C.c点时,溶液中微粒浓度存在关系:
c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-)
D.d点时,溶液中微粒浓度存在关系:
c(OH-)+c(A-)=c(H+)
答案:C
解析:根据物料守恒,开始时c(HA)+c(A-)=0.010 00 mol·L-1,但随着盐酸滴定,溶
液的体积增大,c(HA)+c(A-)<0.010 00 mol·L-1,故A错误;加入盐酸的体积为10 mL,
此时反应后溶质为NaA、HA、NaCl,且NaA、HA物质的量相同,此时溶液显碱性,说明
A-的水解大于HA的电离,即微粒浓度大小顺序是 c(HA)>c(Cl-)>c(A-)>c(OH-)>c(H+),
故B错误;两者恰好完全反应,溶质为NaCl和HA,两者物质的量相等,根据电荷守恒,
因此有c(Na+)+c(H+)=c(OH-)+c(A-)+c(Cl-),根据物料守恒,c(Cl-)=c(HA)+c(A-),
因此有:c(Na+)+c(H+)=c(HA)+c(OH-)+2c(A-),故C正确;d点时,溶质为HCl、
NaCl、HA,且物质的量相等,根据电荷守恒,c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(A-),
故D错误。
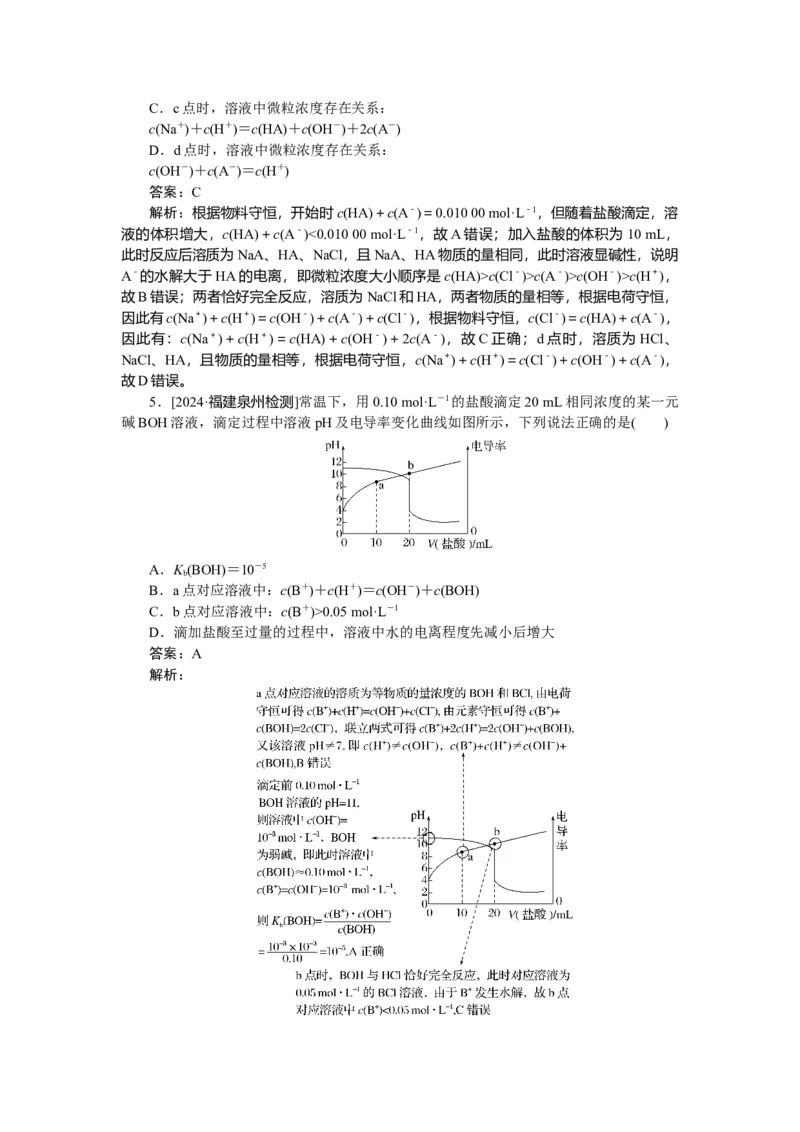
5.[2024·福建泉州检测]常温下,用0.10 mol·L-1的盐酸滴定20 mL相同浓度的某一元
碱BOH溶液,滴定过程中溶液pH及电导率变化曲线如图所示,下列说法正确的是( )
A.K (BOH)=10-5
b
B.a点对应溶液中:c(B+)+c(H+)=c(OH-)+c(BOH)
C.b点对应溶液中:c(B+)>0.05 mol·L-1
D.滴加盐酸至过量的过程中,溶液中水的电离程度先减小后增大
答案:A
解析:BOH和HCl均抑制水的电离,BCl水解促进水的电离,滴加盐酸的过程中,BOH的浓
度逐渐减小,从滴定开始至BOH恰好完全转化为BCl的过程中,水的电离程度逐渐增大,
随后HCl过量,水的电离程度逐渐减小,则滴加盐酸至过量的过程中水的电离程度先增大
后减小,D错误。
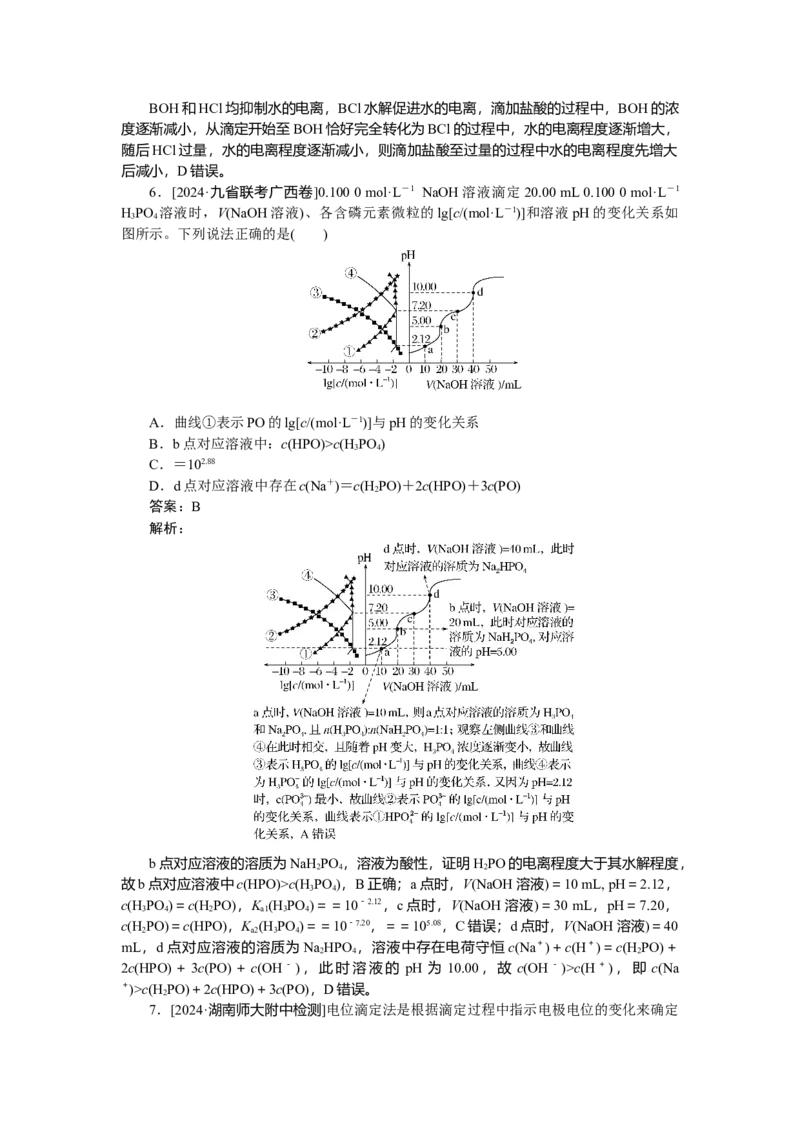
6.[2024·九省联考广西卷]0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1
HPO 溶液时,V(NaOH溶液)、各含磷元素微粒的lg[c/(mol·L-1)]和溶液pH的变化关系如
3 4
图所示。下列说法正确的是( )
A.曲线①表示PO的lg[c/(mol·L-1)]与pH的变化关系
B.b点对应溶液中:c(HPO)>c(H PO )
3 4
C.=102.88
D.d点对应溶液中存在c(Na+)=c(H PO)+2c(HPO)+3c(PO)
2
答案:B
解析:
b点对应溶液的溶质为NaH PO ,溶液为酸性,证明HPO的电离程度大于其水解程度,
2 4 2
故b点对应溶液中c(HPO)>c(H PO ),B正确;a点时,V(NaOH溶液)=10 mL, pH=2.12,
3 4
c(H PO )=c(H PO),K (H PO )==10-2.12,c点时,V(NaOH溶液)=30 mL,pH=7.20,
3 4 2 a1 3 4
c(H PO)=c(HPO),K (H PO )==10-7.20,==105.08,C错误;d点时,V(NaOH溶液)=40
2 a2 3 4
mL,d点对应溶液的溶质为NaHPO ,溶液中存在电荷守恒c(Na+)+c(H+)=c(H PO)+
2 4 2
2c(HPO)+3c(PO)+c(OH-),此时溶液的 pH 为 10.00,故 c(OH-)>c(H+),即 c(Na
+)>c(HPO)+2c(HPO)+3c(PO),D错误。
2
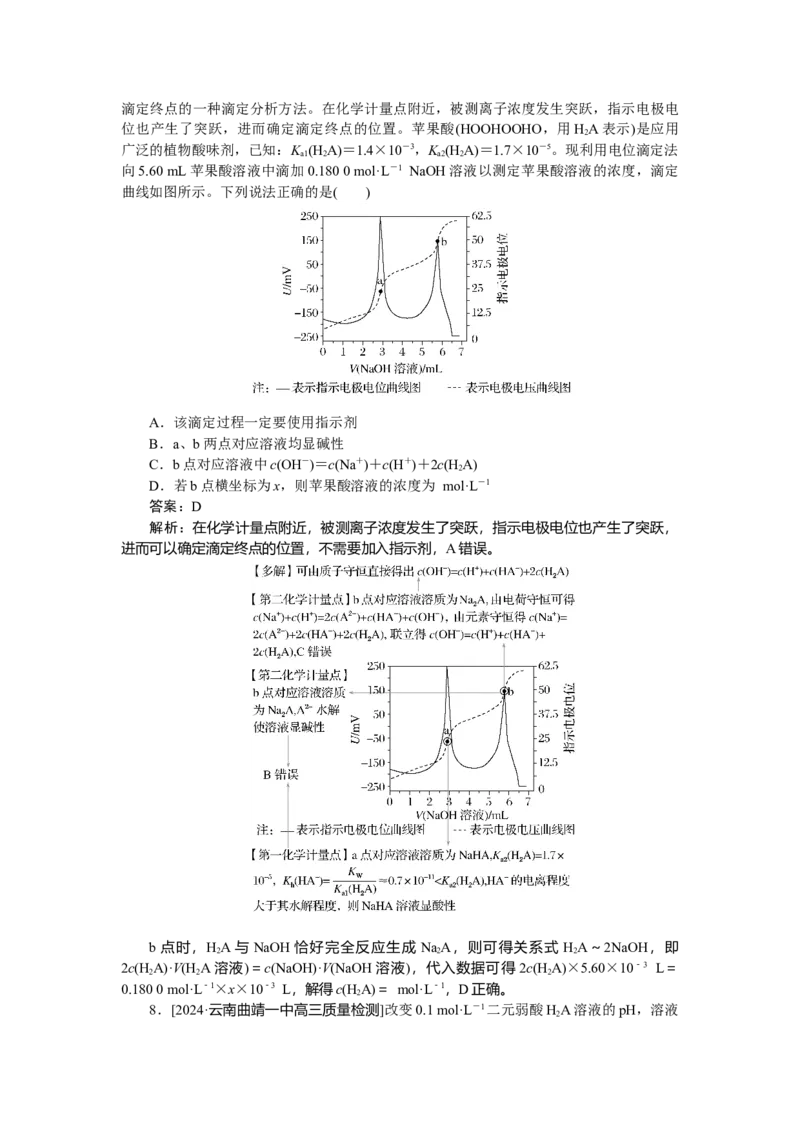
7.[2024·湖南师大附中检测]电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电
位也产生了突跃,进而确定滴定终点的位置。苹果酸(HOOHOOHO,用HA表示)是应用
2
广泛的植物酸味剂,已知:K (H A)=1.4×10-3,K (H A)=1.7×10-5。现利用电位滴定法
a1 2 a2 2
向5.60 mL苹果酸溶液中滴加0.180 0 mol·L-1 NaOH溶液以测定苹果酸溶液的浓度,滴定
曲线如图所示。下列说法正确的是( )
A.该滴定过程一定要使用指示剂
B.a、b两点对应溶液均显碱性
C.b点对应溶液中c(OH-)=c(Na+)+c(H+)+2c(H A)
2
D.若b点横坐标为x,则苹果酸溶液的浓度为 mol·L-1
答案:D
解析:在化学计量点附近,被测离子浓度发生了突跃,指示电极电位也产生了突跃,
进而可以确定滴定终点的位置,不需要加入指示剂,A错误。
b 点时,HA 与 NaOH 恰好完全反应生成 NaA,则可得关系式 HA~2NaOH,即
2 2 2
2c(H A)·V(H A溶液)=c(NaOH)·V(NaOH溶液),代入数据可得 2c(H A)×5.60×10-3 L=
2 2 2
0.180 0 mol·L-1×x×10-3 L,解得c(H A)= mol·L-1,D正确。
2
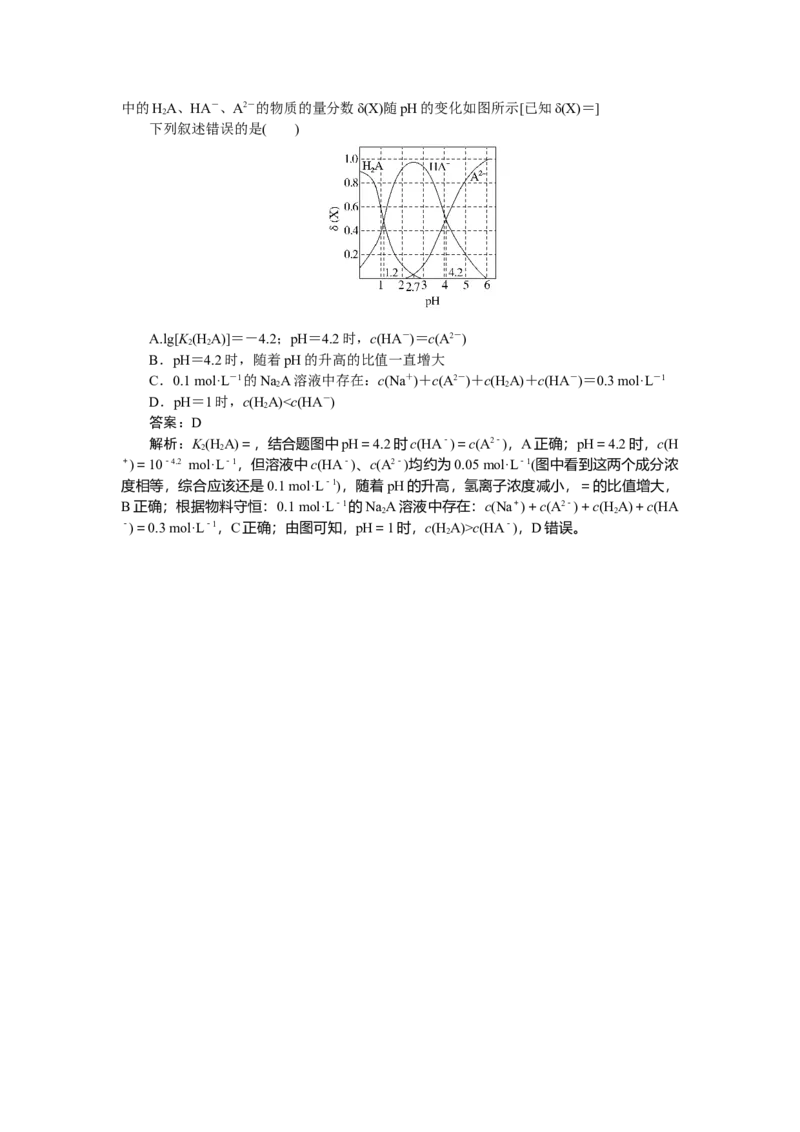
8.[2024·云南曲靖一中高三质量检测]改变0.1 mol·L-1二元弱酸HA溶液的pH,溶液
2中的HA、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=]
2
下列叙述错误的是( )
A.lg[K (H A)]=-4.2;pH=4.2时,c(HA-)=c(A2-)
2 2
B.pH=4.2时,随着pH的升高的比值一直增大
C.0.1 mol·L-1的NaA溶液中存在:c(Na+)+c(A2-)+c(H A)+c(HA-)=0.3 mol·L-1
2 2
D.pH=1时,c(H A)c(HA-),D错误。
2