文档内容
点石联考9月高三联考 化学
2025—2026学年度上学期高三年级9月份联合考试 化学(B版)
说明:
本解答给出的非选择题答案仅供参考,若考生的回答与本答案不同,但只要合理,可参照评
分标准酌情给分。
一、选择题:本题共 15 分,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C A A B B C D C D B C A C D B
二、非选择题:本题共 4 小题,共 55 分。
16.(14分)
(1)平面三角形(1分)
(2)4(2分)
(3)s(1分)
(4)b(2分)
(5)① (2分)
②O(2分)
(6)①sp3(2分)
②1∶1(2分)
17.(14分)
(1)①CaC +2H O―→CH≡CH↑+Ca(OH) (2分)
2 2 2
△
②CH =CH—CHO+2[Ag(NH ) ]OH――→2Ag↓+CH =CH—COONH +3NH +H O(2分)
2 3 2 2 4 3 2
(2)① (2分)
答案第 1 页 共 10 页点石联考9月高三联考 化学
②3-甲基-1-丁烯(2分)
③abd(2分)
④8(2分)
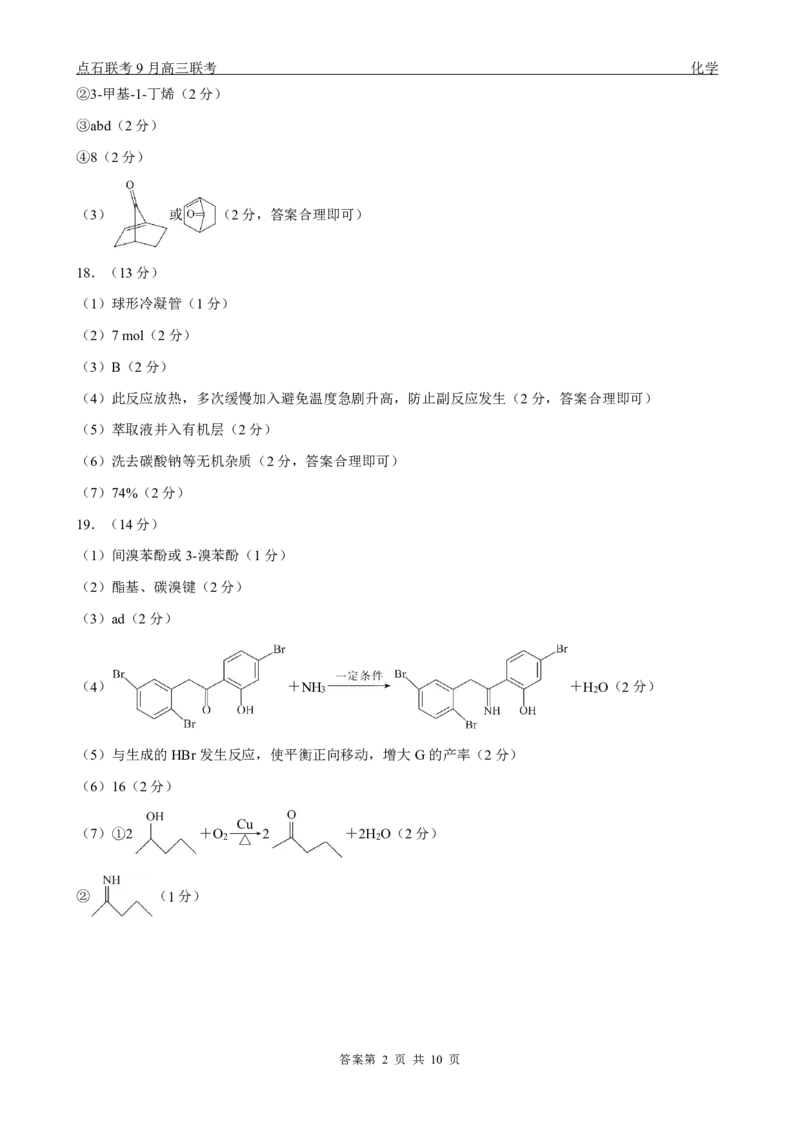
(3) 或 (2分,答案合理即可)
18.(13分)
(1)球形冷凝管(1分)
(2)7mol(2分)
(3)B(2分)
(4)此反应放热,多次缓慢加入避免温度急剧升高,防止副反应发生(2分,答案合理即可)
(5)萃取液并入有机层(2分)
(6)洗去碳酸钠等无机杂质(2分,答案合理即可)
(7)74%(2分)
19.(14分)
(1)间溴苯酚或3-溴苯酚(1分)
(2)酯基、碳溴键(2分)
(3)ad(2分)
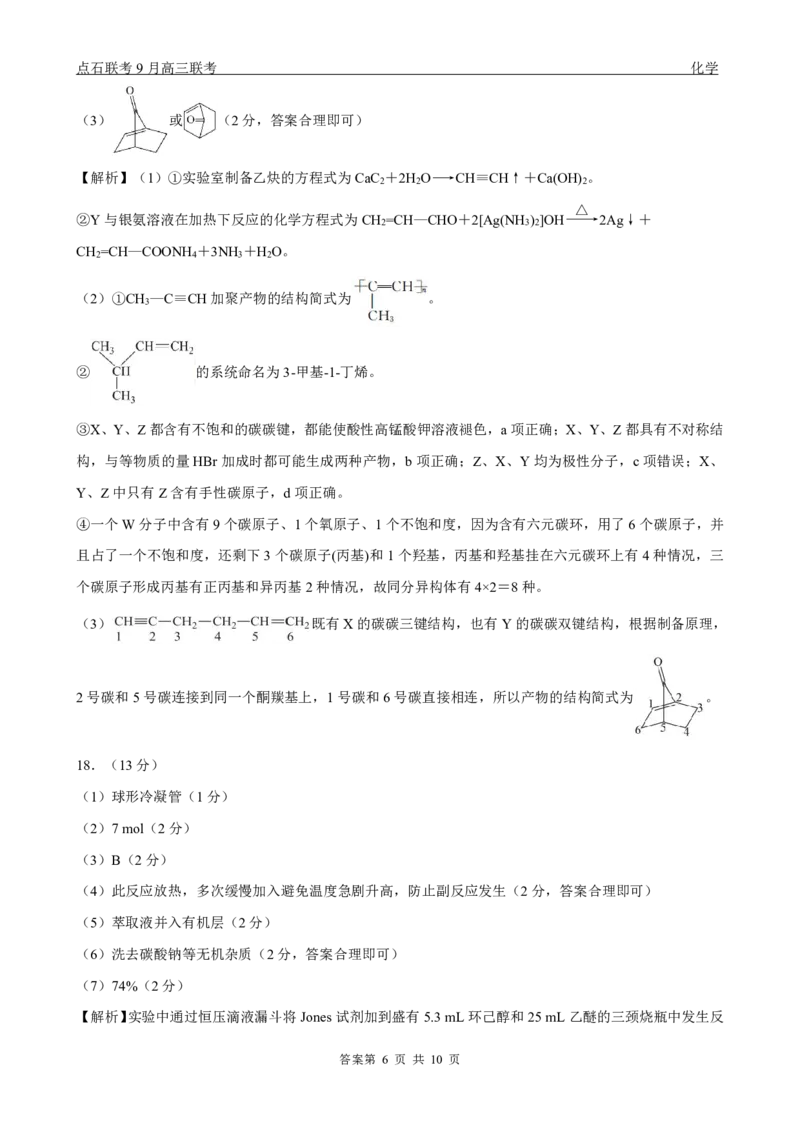
(4) +NH +H O(2分)
3 2
(5)与生成的HBr发生反应,使平衡正向移动,增大G的产率(2分)
(6)16(2分)
Cu
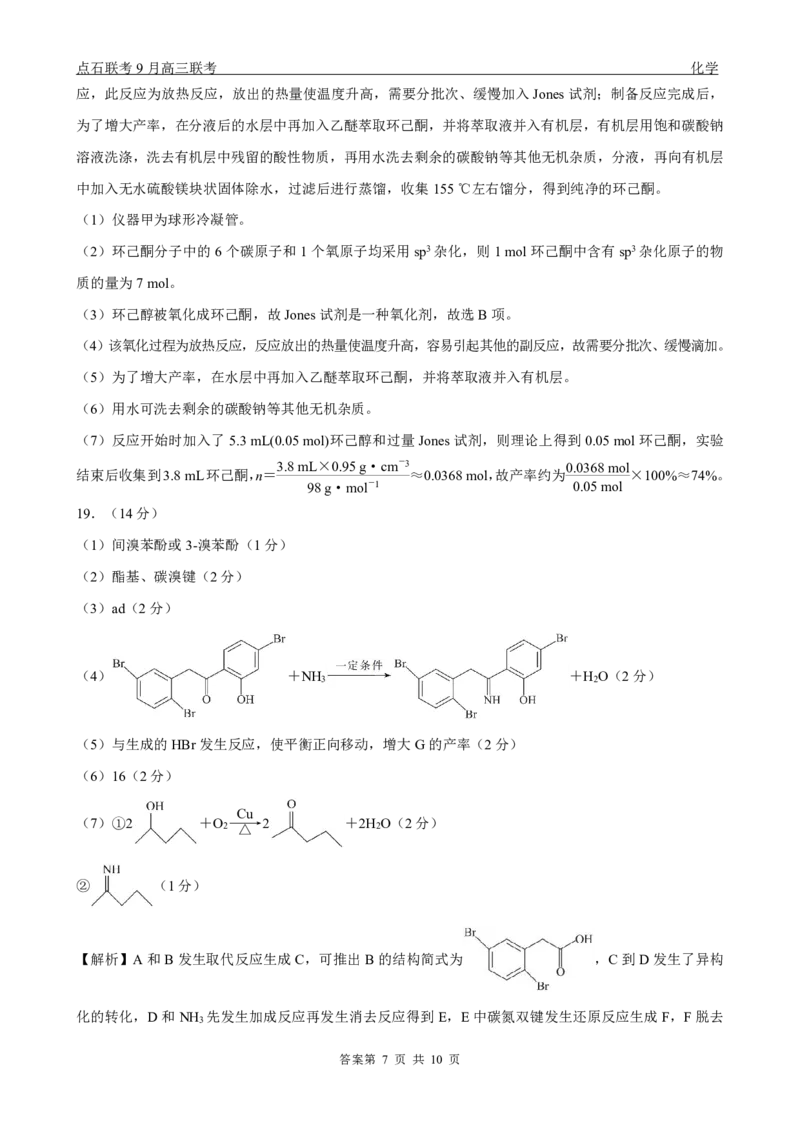
(7)①2 +O ――→2 +2H O(2分)
2 △ 2
② (1分)
答案第 2 页 共 10 页点石联考9月高三联考 化学
2025—2026 学年度上学期高三年级 9月份联合考试 化学(B 版)
一、选择题
1.C【解析】合成纤维为混合物,A项错误;油脂水解生成甘油(丙三醇),B项错误;日光灯灯管内含有
等离子体,C项正确;汽油属于烃类,D项错误。
2.A【解析】基态Se原子M能层的电子排布式为3s23p63d10,A项正确;PBr 中心P原子采取sp3杂化,
3
但题目中给出的杂化轨道图为sp2杂化,B项错误;高密度聚乙烯支链较少,C项错误;丙酸的分子式为
C H O ,D项错误。
3 6 2
3.A【解析】Cl—C键的极性大于H—C键的极性,ClCH COOH的酸性大于CH COOH,符合强酸制弱
2 3
酸原理,A项正确;碳溴键在热NaOH溶液中会发生水解反应,B项错误;Cu2+与少量氨水反应生成Cu(OH) ,
2
C项错误;甲酸与过量碳酸钾溶液反应生成碳酸氢钾,D项错误。
4.B【解析】F和K的电负性差值大于Br和K的电负性差值,KF离子键成分的百分数更大,A项正确;
正丁烷碳原子的个数小于2-甲基丁烷,沸点较低,B项错误;甲烷键角约为109°28′,白磷键角为60°,
C项正确;CsCl中铯离子的配位数为8,NaCl中钠离子的配位数为6,D项正确。
5.B【解析】乙二酸可以使酸性高锰酸钾溶液褪色,A项错误;Mg和Li在元素周期表中处于对角线的位
置,性质相似,在氧气中燃烧只生成正常的氧化物,不生成其他复杂的氧化物,B项正确;H 中的s-sσ
2
键无方向性,C项错误;甲苯只与液溴反应,不与溴水反应,D项错误。
6.C【解析】热的碳酸钠溶液可以促进油脂水解,A项正确;酸性高锰酸钾溶液可以除去硫化氢和乙烯,
但会生成二氧化碳,碱石灰除去二氧化碳和带出的水,天然气得到净化,B项正确;实验室制备乙酸乙酯
时,乙醇、乙酸易被饱和碳酸钠溶液吸收,需要防倒吸,导管不能插入饱和碳酸钠溶液中,C项错误;乙
醇能降低溶剂的极性,使极性较大的[Cu(NH ) ]SO ·H O析出,D项错误。
3 4 4 2
7.D【解析】葡萄糖在酶的作用下分解生成乙醇,不属于水解反应,A项错误;DNA分子两条链上的碱
基之间主要是氢键的作用,氢键不属于化学键,B项错误;溴苯为液体,分离水和溴苯的方法为分液,C
项错误;晶体具有自范性的本质是晶体粒子在微观空间里自发呈周期性有序排列,D项正确。
8.C【解析】氰基在酸性溶液中加热水解生成羧酸,A项正确;酯化反应中浓硫酸作催化剂和吸水剂,B
项正确;丙酮能与水互溶,不能用于萃取溴水中的溴,C项错误;苯环和氰基都可以与氢气发生加成反应,
故1mol苯氰最多与5mol氢气发生加成反应,D项正确。
答案第 3 页 共 10 页点石联考9月高三联考 化学
9.D【解析】一个该分子中含有4个氮原子,故分子中含有氢原子的个数为偶数,A项正确;利巴韦林中
含有羟基,可以与甲醇的羟基形成分子间氢键,B项正确;利巴韦林中含有酰胺基,既可以在酸性条件下
发生水解反应,也可以在碱性条件下发生水解反应,C项正确;醇在浓硫酸、加热条件下发生消去反应,
D项错误。
10.B【解析】过程①得反应类型为加成反应,A项正确;由过程②可知,a中O—H键容易断裂,故极性
较大,B项错误;离子键无方向性和饱和性,C项正确;乙醛生成的b溶于水、不溶于乙醚,水和乙醚不
互溶,会分层,再利用分液的方法可以获得不含乙醛的乙醚,D项正确。
11.C【解析】Birch反应是一个加氢的反应,为还原反应,A项正确;1,4-环己二烯含有碳碳双键,可
以发生加聚反应,B项正确;氨气中的氮原子为sp3杂化,N的sp3杂化轨道和H的1s轨道形成sp3-s类型
的σ键,C项错误;加氢时需要氢原子,有可能是醇来提供,D项正确。
12.A【解析】甲基为推电子定位基,根据题目的信息:发生Birch反应时,若苯环上连有推电子基团,
则双键碳带有更多取代基的产物为主产物,结合苯的还原反应可得主产物为 。故选A项。
13.C【解析】根据Y的基态原子核外的s能级和p能级上的电子数相等,可推出Y为O,可假定阴离子
得到的2个电子被O所得,O正好满足8电子稳定结构,X与O形成的应该是配位键,X提供空轨道,则
X为B,Z形成一条共价键,并且原子序数比O的大,比M的小,则Z为F,M为Na。O原子采取sp3
杂化,4个B原子不可能处于同一平面,A项错误;BF 分子中B原子最外层不满足8电子稳定结构,B
3
项错误;电负性:F>O>B>Na,C项正确;Na [O(BF ) ]中的阴离子半径较大,离子键较弱,熔点较低(类
2 3 4
比离子液体),D项错误。
14.D【解析】每个二价铁周围有2个NH 和4个氯,但每个氯被2个二价铁共用,故化学式为Fe(NH ) Cl (也
3 3 2 2
可以用均摊法),A、C项正确;根据化合物存在多条无限伸展的链状结构,链和链之间存在范德华力,可
知该化合物为混合晶体,B项正确;该晶体中NH 的N原子参与配位,已经没有孤电子对,不能形成氢键,
3
D项错误。
15.B【解析】正丁胺存在分子间氢键,故沸点比与它相对分子质量接近的正戊烷的大,A项正确;第(3)
步中氢气与碳氮双键进行加成,C的电负性较小,带正电荷,故带负电荷的H原子与C原子连接,B项错
误;物质K为乙醇,可以使酸性高锰酸钾溶液褪色,C项正确;根据机理第(1)步,羰基上的氧原子进
入到水中,由整个机理可知,最终有机产物中的氧原子来自酯基中双键上的氧原子,D项正确。
答案第 4 页 共 10 页点石联考9月高三联考 化学
二、非选择题
16.(14分)
(1)平面三角形(1分)
(2)4(2分)
(3)s(1分)
(4)b(2分)
(5)① (2分)
②O(2分)
(6)①sp3(2分)
②1∶1(2分)
【解析】(1)SO 中心S原子的价层电子对数为3,故VSEPR模型为平面三角形。
2
(2)氯元素的基态原子最外层电子占据1个3s轨道和3个sp轨道,共4中不同空间运动状态的电子。
(3)漂白粉中所含的金属元素为钙元素,处于元素周期表的s区。
(4)过氧化氢为极性分子;过氧化氢中的氧原子上有孤电子对,可以与金属阳离子形成配合物;BaO 与
2
硫酸反应时元素化合价没有变化,为非氧化还原反应;反应H +O H O 中,1molO 参加反
2 2 2 2 2
应,转移2mol电子。故选b项。
(5)①在碳酸根电子式的基础上,碳原子和氧原子之间插入氧原子即可。
②此反应生成的正盐为Na CO ,起所含的三种元素中,第一电离能最大的为O元素。
2 3
(6)①S O 2-中S的杂化方式与SO 2-相同,为sp3杂化。
2 4 3
②1mol靛蓝转化为靛白转移了2mol电子(把靛白的—O-补成—OH,相当于多了2mol氢原子),1mol连
二亚硫酸钠反应也转移2mol电子,故两者的物质的量之比为1∶1。
17.(14分)
(1)①CaC +2H O―→CH≡CH↑+Ca(OH) (2分)
2 2 2
△
②CH =CH—CHO+2[Ag(NH ) ]OH――→2Ag↓+CH =CH—COONH +3NH +H O(2分)
2 3 2 2 4 3 2
(2)① (2分)
②3-甲基-1-丁烯(2分)
③abd(2分)
④8(2分)
答案第 5 页 共 10 页点石联考9月高三联考 化学
(3) 或 (2分,答案合理即可)
【解析】(1)①实验室制备乙炔的方程式为CaC +2H O―→CH≡CH↑+Ca(OH) 。
2 2 2
△
②Y与银氨溶液在加热下反应的化学方程式为CH =CH—CHO+2[Ag(NH ) ]OH――→2Ag↓+
2 3 2
CH =CH—COONH +3NH +H O。
2 4 3 2
(2)①CH —C≡CH加聚产物的结构简式为 。
3
② 的系统命名为3-甲基-1-丁烯。
③X、Y、Z都含有不饱和的碳碳键,都能使酸性高锰酸钾溶液褪色,a项正确;X、Y、Z都具有不对称结
构,与等物质的量HBr加成时都可能生成两种产物,b项正确;Z、X、Y均为极性分子,c项错误;X、
Y、Z中只有Z含有手性碳原子,d项正确。
④一个W分子中含有9个碳原子、1个氧原子、1个不饱和度,因为含有六元碳环,用了6个碳原子,并
且占了一个不饱和度,还剩下3个碳原子(丙基)和1个羟基,丙基和羟基挂在六元碳环上有4种情况,三
个碳原子形成丙基有正丙基和异丙基2种情况,故同分异构体有4×2=8种。
(3) 既有X的碳碳三键结构,也有Y的碳碳双键结构,根据制备原理,
2号碳和5号碳连接到同一个酮羰基上,1号碳和6号碳直接相连,所以产物的结构简式为 。
18.(13分)
(1)球形冷凝管(1分)
(2)7mol(2分)
(3)B(2分)
(4)此反应放热,多次缓慢加入避免温度急剧升高,防止副反应发生(2分,答案合理即可)
(5)萃取液并入有机层(2分)
(6)洗去碳酸钠等无机杂质(2分,答案合理即可)
(7)74%(2分)
【解析】实验中通过恒压滴液漏斗将Jones试剂加到盛有5.3mL环己醇和25mL乙醚的三颈烧瓶中发生反
答案第 6 页 共 10 页点石联考9月高三联考 化学
应,此反应为放热反应,放出的热量使温度升高,需要分批次、缓慢加入Jones试剂;制备反应完成后,
为了增大产率,在分液后的水层中再加入乙醚萃取环己酮,并将萃取液并入有机层,有机层用饱和碳酸钠
溶液洗涤,洗去有机层中残留的酸性物质,再用水洗去剩余的碳酸钠等其他无机杂质,分液,再向有机层
中加入无水硫酸镁块状固体除水,过滤后进行蒸馏,收集155℃左右馏分,得到纯净的环己酮。
(1)仪器甲为球形冷凝管。
(2)环己酮分子中的6个碳原子和1个氧原子均采用sp3杂化,则1mol环己酮中含有sp3杂化原子的物
质的量为7mol。
(3)环己醇被氧化成环己酮,故Jones试剂是一种氧化剂,故选B项。
(4)该氧化过程为放热反应,反应放出的热量使温度升高,容易引起其他的副反应,故需要分批次、缓慢滴加。
(5)为了增大产率,在水层中再加入乙醚萃取环己酮,并将萃取液并入有机层。
(6)用水可洗去剩余的碳酸钠等其他无机杂质。
(7)反应开始时加入了5.3mL(0.05mol)环己醇和过量Jones试剂,则理论上得到0.05mol环己酮,实验
3.8mL×0.95g·cm-3
0.0368mol
结束后收集到3.8mL环己酮,n= ≈0.0368mol,故产率约为 ×100%≈74%。
98g·mol-1 0.05mol
19.(14分)
(1)间溴苯酚或3-溴苯酚(1分)
(2)酯基、碳溴键(2分)
(3)ad(2分)
(4) +NH +H O(2分)
3 2
(5)与生成的HBr发生反应,使平衡正向移动,增大G的产率(2分)
(6)16(2分)
Cu
(7)①2 +O ――→2 +2H O(2分)
2 △ 2
② (1分)
【解析】A和B发生取代反应生成C,可推出B的结构简式为 ,C到D发生了异构
化的转化,D和NH 先发生加成反应再发生消去反应得到E,E中碳氮双键发生还原反应生成F,F脱去
3
答案第 7 页 共 10 页点石联考9月高三联考 化学
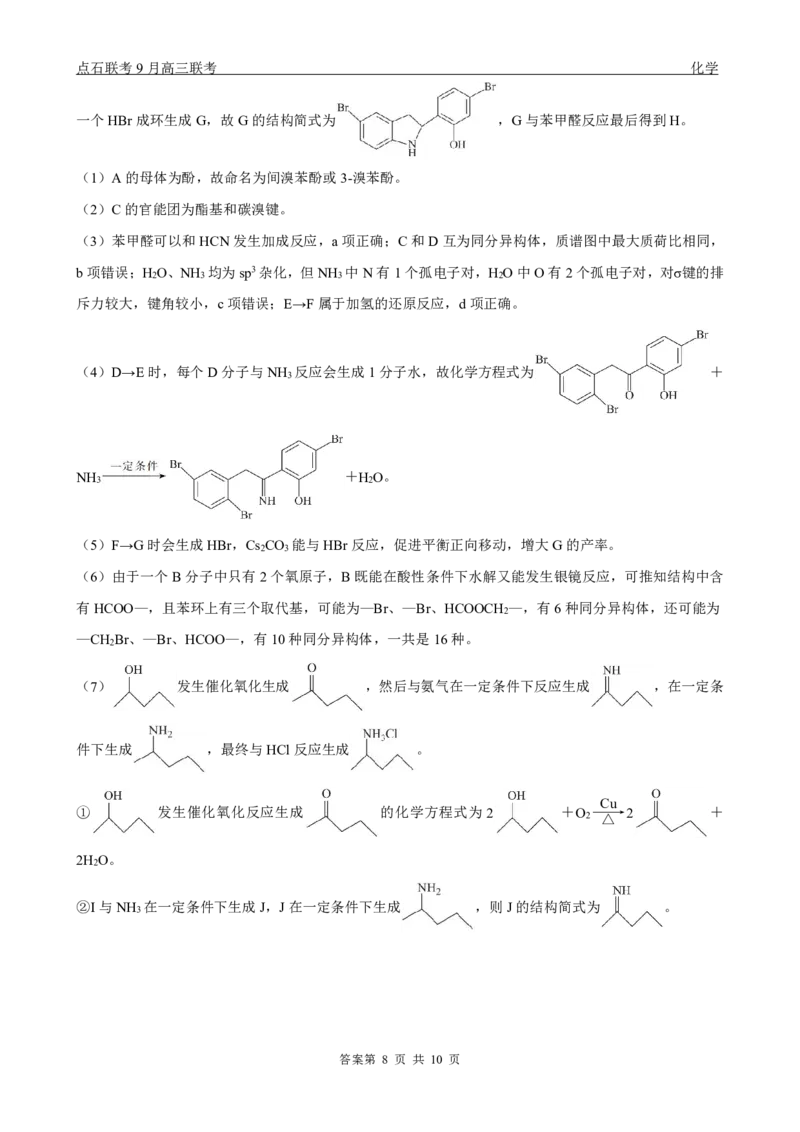
一个HBr成环生成G,故G的结构简式为 ,G与苯甲醛反应最后得到H。
(1)A的母体为酚,故命名为间溴苯酚或3-溴苯酚。
(2)C的官能团为酯基和碳溴键。
(3)苯甲醛可以和HCN发生加成反应,a项正确;C和D互为同分异构体,质谱图中最大质荷比相同,
b项错误;H O、NH 均为sp3杂化,但NH 中N有1个孤电子对,H O中O有2个孤电子对,对σ键的排
2 3 3 2
斥力较大,键角较小,c项错误;E→F属于加氢的还原反应,d项正确。
(4)D→E时,每个D分子与NH 反应会生成1分子水,故化学方程式为 +
3
NH +H O。
3 2
(5)F→G时会生成HBr,Cs CO 能与HBr反应,促进平衡正向移动,增大G的产率。
2 3
(6)由于一个B分子中只有2个氧原子,B既能在酸性条件下水解又能发生银镜反应,可推知结构中含
有HCOO—,且苯环上有三个取代基,可能为—Br、—Br、HCOOCH —,有6种同分异构体,还可能为
2
—CH Br、—Br、HCOO—,有10种同分异构体,一共是16种。
2
(7) 发生催化氧化生成 ,然后与氨气在一定条件下反应生成 ,在一定条
件下生成 ,最终与HCl反应生成 。
Cu
① 发生催化氧化反应生成 的化学方程式为 2 +O ――→2 +
2 △
2H O。
2
②I与NH 在一定条件下生成J,J在一定条件下生成 ,则J的结构简式为 。
3
答案第 8 页 共 10 页点石联考9月高三联考 化学
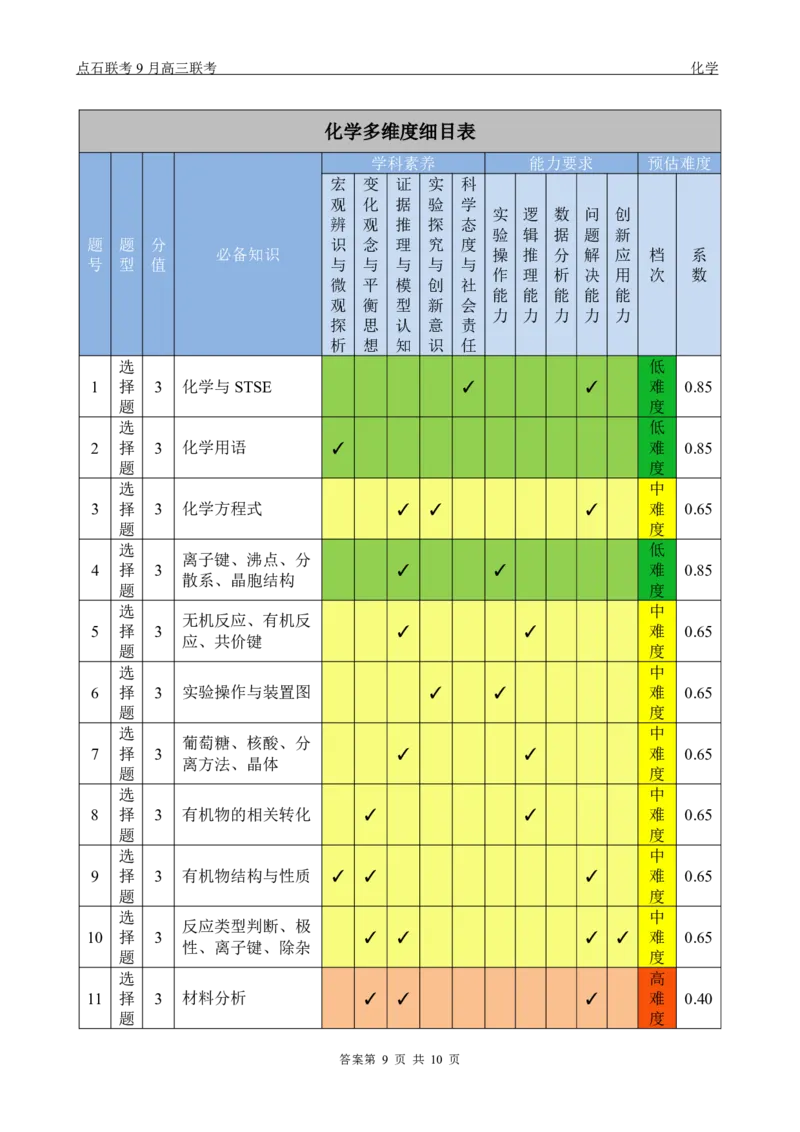
化学多维度细目表
学科素养 能力要求 预估难度
宏 变 证 实 科
观 化 据 验 学
实 逻 数 问 创
辨 观 推 探 态
验 辑 据 题 新
题 题 分 识 念 理 究 度
必备知识 操 推 分 解 应 档 系
号 型 值 与 与 与 与 与
作 理 析 决 用 次 数
微 平 模 创 社
能 能 能 能 能
观 衡 型 新 会
力 力 力 力 力
探 思 认 意 责
析 想 知 识 任
选 低
1 择 3 化学与STSE ✓ ✓ 难 0.85
题 度
选 低
2 择 3 化学用语 ✓ 难 0.85
题 度
选 中
3 择 3 化学方程式 ✓ ✓ ✓ 难 0.65
题 度
选 低
离子键、沸点、分
4 择 3 ✓ ✓ 难 0.85
散系、晶胞结构
题 度
选 中
无机反应、有机反
5 择 3 ✓ ✓ 难 0.65
应、共价键
题 度
选 中
6 择 3 实验操作与装置图 ✓ ✓ 难 0.65
题 度
选 中
葡萄糖、核酸、分
7 择 3 ✓ ✓ 难 0.65
离方法、晶体
题 度
选 中
8 择 3 有机物的相关转化 ✓ ✓ 难 0.65
题 度
选 中
9 择 3 有机物结构与性质 ✓ ✓ ✓ 难 0.65
题 度
选 中
反应类型判断、极
10 择 3 ✓ ✓ ✓ ✓ 难 0.65
性、离子键、除杂
题 度
选 高
11 择 3 材料分析 ✓ ✓ ✓ 难 0.40
题 度
答案第 9 页 共 10 页点石联考9月高三联考 化学
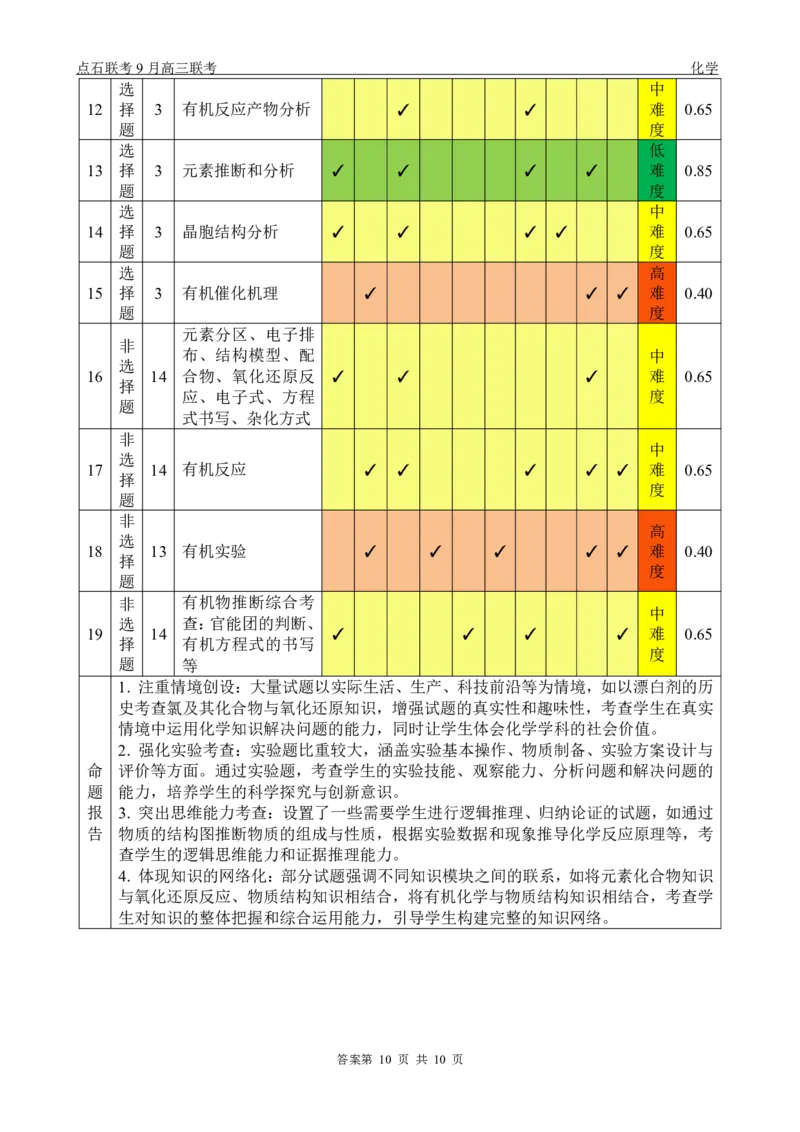
选 中
12 择 3 有机反应产物分析 ✓ ✓ 难 0.65
题 度
选 低
13 择 3 元素推断和分析 ✓ ✓ ✓ ✓ 难 0.85
题 度
选 中
14 择 3 晶胞结构分析 ✓ ✓ ✓ ✓ 难 0.65
题 度
选 高
15 择 3 有机催化机理 ✓ ✓ ✓ 难 0.40
题 度
元素分区、电子排
非
布、结构模型、配 中
选
16 14 合物、氧化还原反 ✓ ✓ ✓ 难 0.65
择
应、电子式、方程 度
题
式书写、杂化方式
非
中
选
17 14 有机反应 ✓ ✓ ✓ ✓ ✓ 难 0.65
择
度
题
非
高
选
18 13 有机实验 ✓ ✓ ✓ ✓ ✓ 难 0.40
择
度
题
非 有机物推断综合考
中
选 查:官能团的判断、
19 14 ✓ ✓ ✓ ✓ 难 0.65
择 有机方程式的书写
度
题 等
1. 注重情境创设:大量试题以实际生活、生产、科技前沿等为情境,如以漂白剂的历
史考查氯及其化合物与氧化还原知识,增强试题的真实性和趣味性,考查学生在真实
情境中运用化学知识解决问题的能力,同时让学生体会化学学科的社会价值。
2. 强化实验考查:实验题比重较大,涵盖实验基本操作、物质制备、实验方案设计与
命 评价等方面。通过实验题,考查学生的实验技能、观察能力、分析问题和解决问题的
题 能力,培养学生的科学探究与创新意识。
报 3. 突出思维能力考查:设置了一些需要学生进行逻辑推理、归纳论证的试题,如通过
告 物质的结构图推断物质的组成与性质,根据实验数据和现象推导化学反应原理等,考
查学生的逻辑思维能力和证据推理能力。
4. 体现知识的网络化:部分试题强调不同知识模块之间的联系,如将元素化合物知识
与氧化还原反应、物质结构知识相结合,将有机化学与物质结构知识相结合,考查学
生对知识的整体把握和综合运用能力,引导学生构建完整的知识网络。
答案第 10 页 共 10 页