文档内容
厦门市 2023 届高三毕业班第二次质量检测
化 学 试 题
本试卷共6页.总分 100分.考试时间 75分钟.
可能用到的相对原子质量:H 1 C 12 O 16 Ce 140
一、选择题:本题共 14小题,每小题 3分,共42分.每小题只有一个选项符合题目要求.
1.厦门大学设计具有高催化活性与稳定性Pt FeCoC纳米催化剂用于质子交换膜氢氧燃料电池.下列说法
3
错误的是( )
A.Pt、Fe、Co均属于过渡元素 B.催化剂通过降低活化能提高电池工作效率
C.纳米Pt FeCoC催化剂属于胶体 D.正极电极反应式为O 4e 4H 2H O
3 2 2
2.下列食品添加剂不属于电解质的是( )
A.二氧化硫B.亚硝酸钠 C.葡萄糖酸 D.山梨酸钾
3.我国科学家利用Zn(NO ) 和AgNO 在十八胺(C H NH )中金属阳离子氧化性不同,分别制得纳米晶
3 2 3 18 37 2
体材料ZnO和Ag.下列说法错误的是( )
A.第一电离能:NOC B.十八胺中碳原子杂化类型均为sp3
C.氧化性:Zn2 Ag D.熔点:十八烷十八胺
4.生物大分子血红蛋白分子链的部分结构及载氧示意如图.下列说法错误的是( )
A.构成血红蛋分子链的多肽链之间存在氢键作用
B.血红素中Fe2提供空轨道形成配位键
C.CO与血红素中Fe2配位能力强于O
2
D.用酸性丙酮提取血红蛋白中血红素时仅发生物理变化
5.一种对乙酰氨基酚的合成路线如下.下列说法错误的是( )
A.a至少有12个原子共平面 B.bc的反应类型为取代反应
学科网(北京)股份有限公司C.c苯环上的一氯代物有2种 D.1 mol d最多能与2 mol NaOH反应
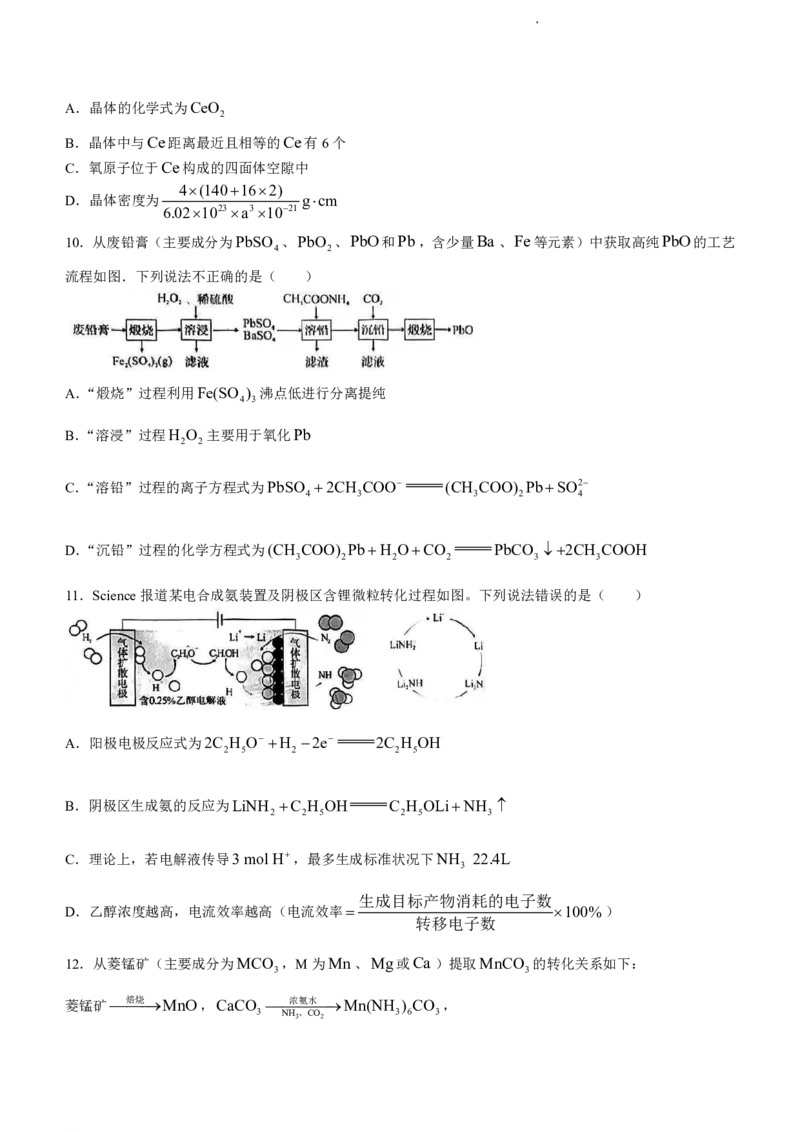
6.下列实验操作正确且能达到实验目的的是( )
2mL 0.5 molL1CuCl 溶 液
2
Cu(H O)2 4Cl CuCl2 +4H O
2 4 4 2
A.模拟侯氏制碱 B.用NaOH溶液滴 C.探究温度对化学平衡的影响 D.探究苯酚和碳酸
法 获 得 定未知浓度的醋酸溶 酸性强弱
液
NaHC O ,
4 3
7.W、R、X、Y、Z为原子序数依次增大的短周期元素.RW 、XW和ZW 三种微粒的空间构型相同,Y
4 4 4
原子的电子层数等于最外层电子数.以下说法错误的是( )
A.氢化物稳定性:ZR X B.最高价氧化物对应水化物酸性:R ZY
C.电负性:X R Y D.原子晶体ZR 中Z的配位数为4
8.一种复合膨松剂的工作原理为H R3NaHCO Na R3CO 3H O,其中H R结构如图。N
3 3 3 2 2 3 A
是阿伏加德罗常数的值,下列说法不正确的是( )
CH COOH
2
|
HO—C—COOH
|
CH COOH
2
A.标准状况下,2.24 L CO 中氧原子数为0.2N
2 A
B.1 L 0.1 molL1 NaHCO 溶液中HCO和CO2微粒总数为0.1N
3 3 3 A
C.0.1 mol Na R固体中离子数为0.4N
3 A
D.19.2 g H R 中键数为0.3N
3 A
9.一种光催化材料的晶胞如图,属于立方晶系,其晶胞参数为a nm。下列说法错误的是( )
学科网(北京)股份有限公司A.晶体的化学式为CeO
2
B.晶体中与Ce距离最近且相等的Ce有6个
C.氧原子位于Ce构成的四面体空隙中
4(140162)
D.晶体密度为 gcm
6.021023a31021
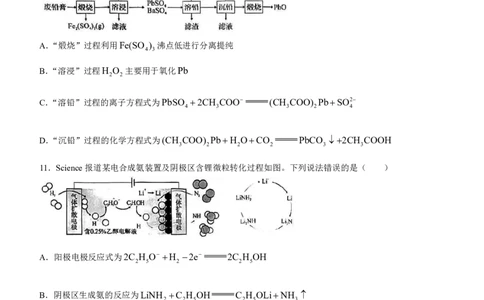
10.从废铅膏(主要成分为PbSO 、PbO 、PbO和Pb,含少量Ba、Fe等元素)中获取高纯PbO的工艺
4 2
流程如图.下列说法不正确的是( )
A.“煅烧”过程利用Fe(SO ) 沸点低进行分离提纯
4 3
B.“溶浸”过程H O 主要用于氧化Pb
2 2
C.“溶铅”过程的离子方程式为PbSO 2CH COO (CH COO) PbSO2
4 3 3 2 4
D.“沉铅”过程的化学方程式为(CH COO) PbH OCO PbCO 2CH COOH
3 2 2 2 3 3
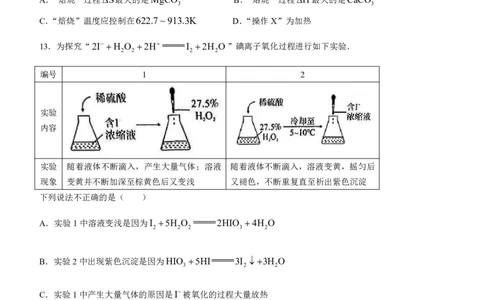
11.Science报道某电合成氨装置及阴极区含锂微粒转化过程如图。下列说法错误的是( )
A.阳极电极反应式为2C H O H 2e 2C H OH
2 5 2 2 5
B.阴极区生成氨的反应为LiNH C H OH C H OLiNH
2 2 5 2 5 3
C.理论上,若电解液传导3 mol H,最多生成标准状况下NH 22.4L
3
生成目标产物消耗的电子数
D.乙醇浓度越高,电流效率越高(电流效率 100%)
转移电子数
12.从菱锰矿(主要成分为MCO ,M为Mn、Mg或Ca)提取MnCO 的转化关系如下:
3 3
菱锰矿焙烧MnO,CaCO 浓氨水Mn(NH ) CO ,
3 NH、CO 3 6 3
3 2
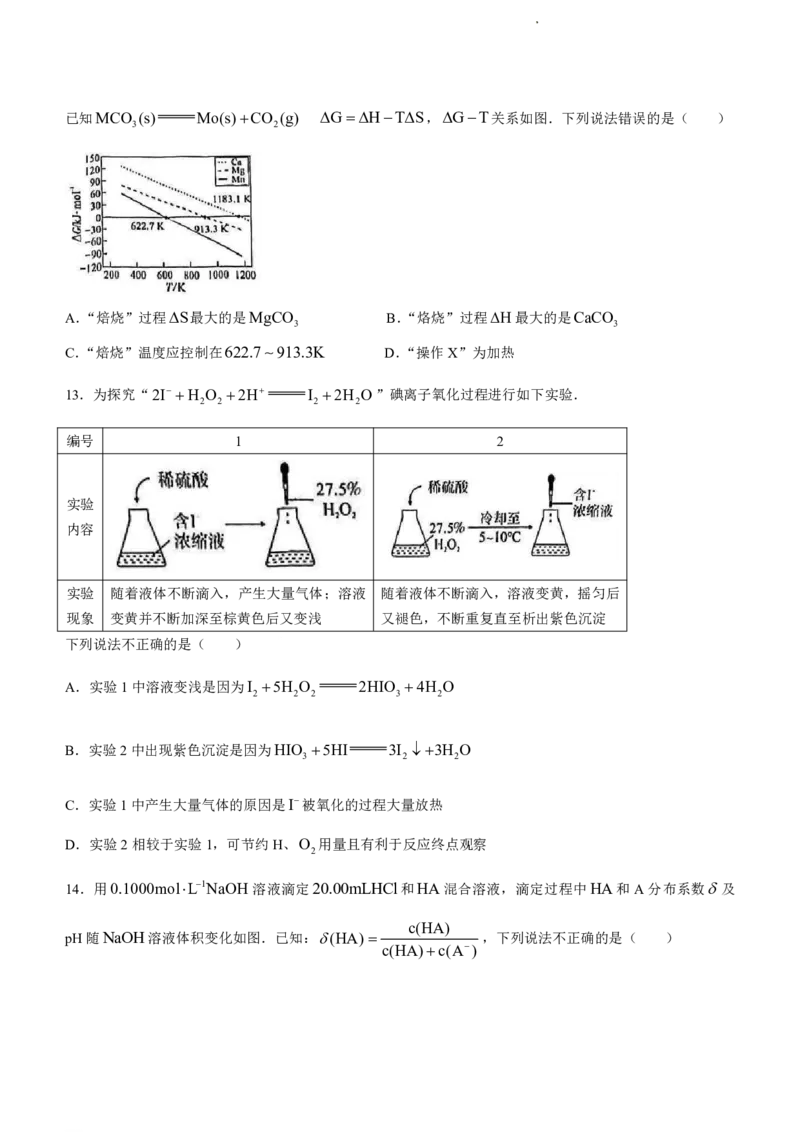
学科网(北京)股份有限公司已知MCO (s) Mo(s)CO (g) GHTS,GT关系如图.下列说法错误的是( )
3 2
A.“焙烧”过程S最大的是MgCO B.“烙烧”过程H最大的是CaCO
3 3
C.“焙烧”温度应控制在622.7913.3K D.“操作X”为加热
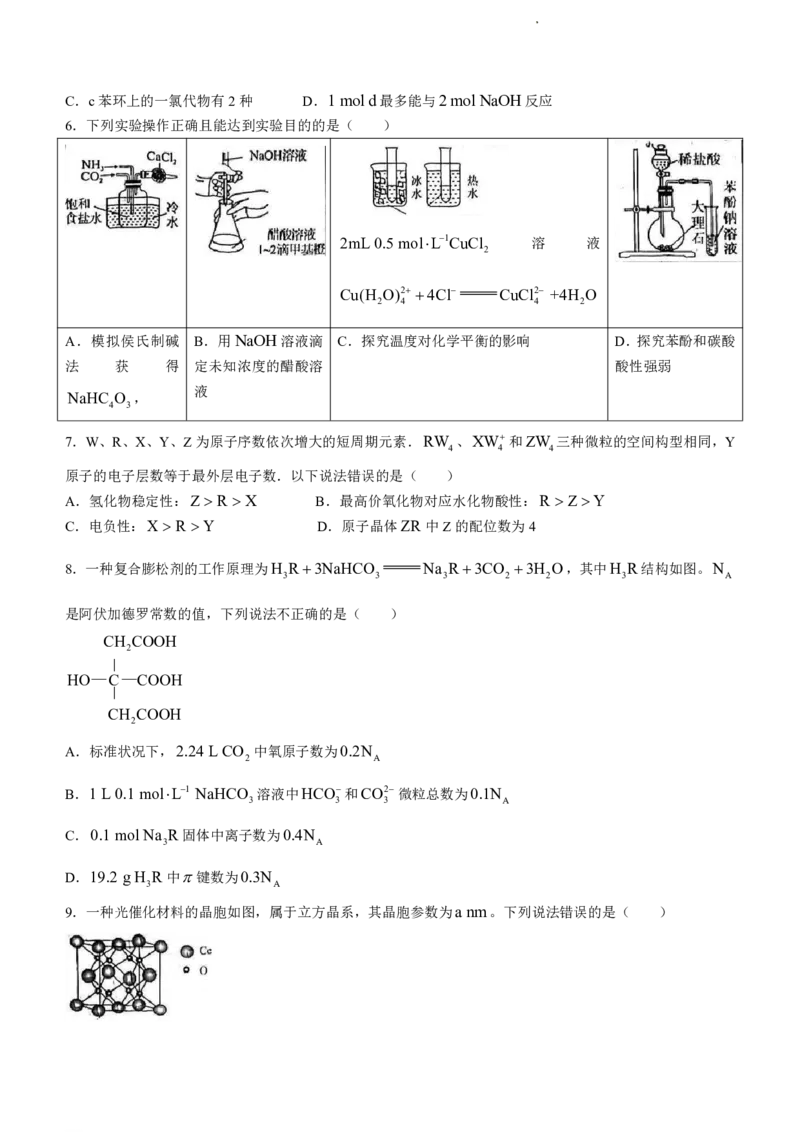
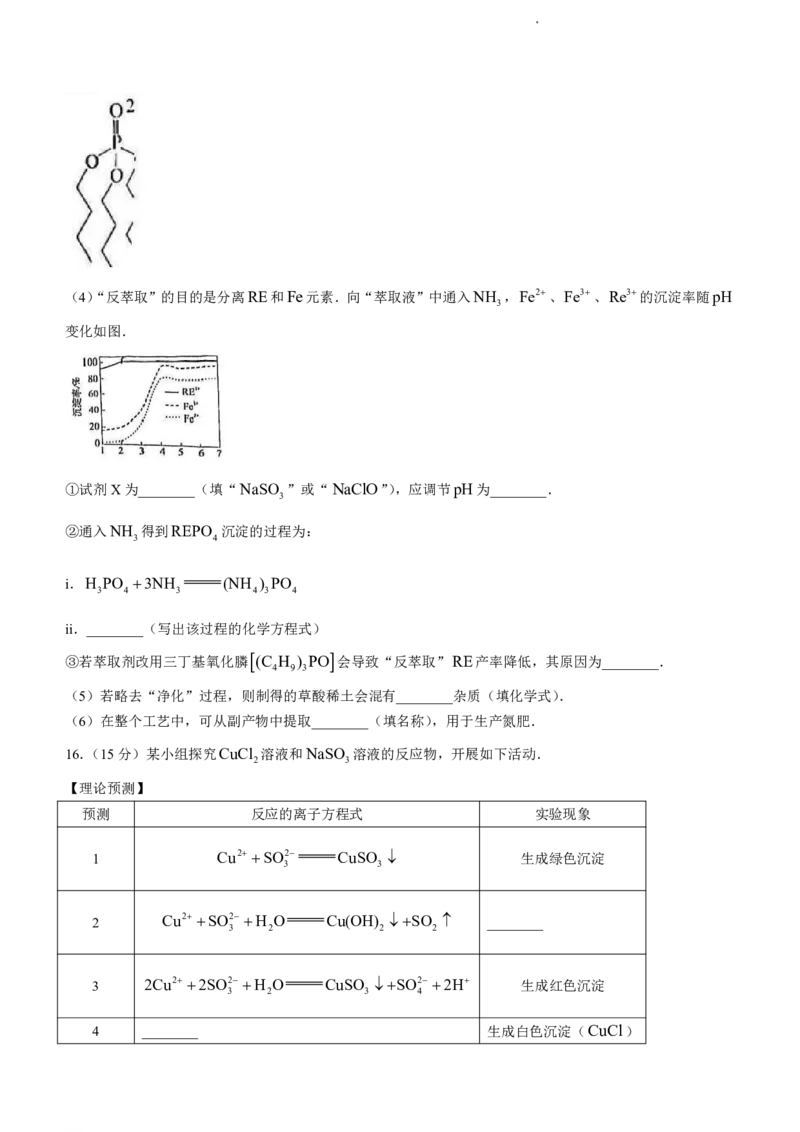
13.为探究“2I H O 2H I 2H O”碘离子氧化过程进行如下实验.
2 2 2 2
编号 1 2
实验
内容
实验 随着液体不断滴入,产生大量气体;溶液 随着液体不断滴入,溶液变黄,摇匀后
现象 变黄并不断加深至棕黄色后又变浅 又褪色,不断重复直至析出紫色沉淀
下列说法不正确的是( )
A.实验1中溶液变浅是因为I 5H O 2HIO 4H O
2 2 2 3 2
B.实验2中出现紫色沉淀是因为HIO 5HI 3I 3H O
3 2 2
C.实验1中产生大量气体的原因是I被氧化的过程大量放热
D.实验2相较于实验1,可节约H、O 用量且有利于反应终点观察
2
14.用0.1000molL1NaOH溶液滴定20.00mLHCl和HA混合溶液,滴定过程中HA和A分布系数及
c(HA)
pH随NaOH溶液体积变化如图.已知:(HA) ,下列说法不正确的是( )
c(HA)c( A)
学科网(北京)股份有限公司A.K (HA)104.76
a
B.pH7时,c(Na)c(A)c(Cl)c(H)c(OH)
C.V(NaOH)40.0mL时,滴定过程中水的电离程度不断增大
D.可利用甲基紫(变色范围为2.03.0)确定第一滴定终点
二、非选择题:本题共4小题,共 58分.
15.(14分)磷精矿主要成分为Ca F(PO ) ,含少量REPO 、FeO、Fe O 、SiO ,其中RE代表稀土元
5 4 3 4 2 3 2
素.从磷精矿分离稀土元素的工业流程如下.
(1)RE属于IIIB族,其中Sc的基态原子核外电子排布式为________.
(2)“酸浸”过程HNO 与Ca F(PQ ) 反应的化学方程式如下,请补充完整.
3 5 4 3
Ca F PO HNO Ca(NO ) ________HF
5 4 3 3 3 2
(3)“萃取”的目的是富集RE,但其余元素也会按一定比例进入萃取剂中。
①通过3ROHPOCl (RO) PO3HCl制得有机磷萃取剂(RO) PO ,其中1代表烃基,R 对
3 3 3
(RO) PO产率的影响如下表。
3
R CH CH CH CH CH CH CH CH CH
2 3 2 2 3 2 2 2 3
(RO) PO产率/% 82 62 20
3
由表可知,随着碳原子数增加,烃基________(填“推电子”或“吸电子”)能力增强,OH键更难断裂,
(RO) PO产率降低.
3
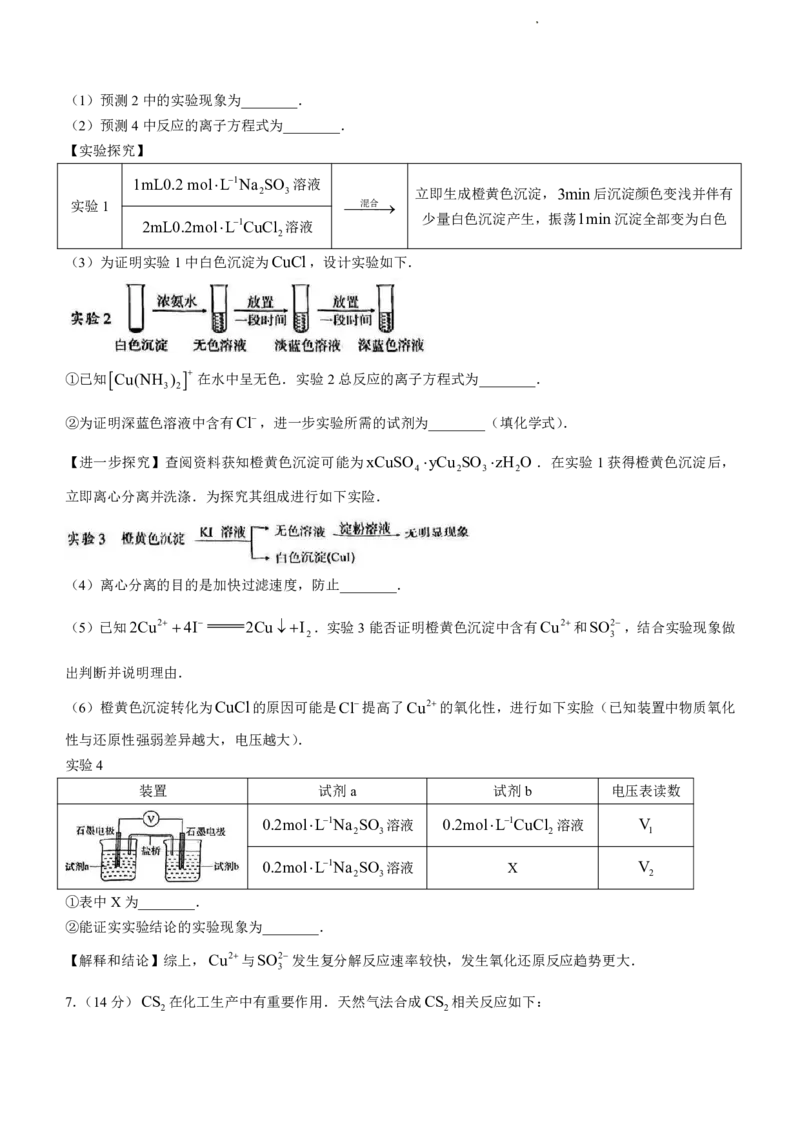
(2)“萃取”过程使用的萃取剂(C H O) PO的结构如图.与RE3配位的能力:1号O原子________2号O
4 9 3
原子(填“”“”或“”).
学科网(北京)股份有限公司(4)“反萃取”的目的是分离RE和Fe元素.向“萃取液”中通入NH ,Fe2、Fe3、Re3的沉淀率随pH
3
变化如图.
①试剂X为________(填“NaSO ”或“NaClO”),应调节pH为________.
3
②通入NH 得到REPO 沉淀的过程为:
3 4
i.H PO 3NH (NH ) PO
3 4 3 4 3 4
ii.________(写出该过程的化学方程式)
③若萃取剂改用三丁基氧化膦 (C H ) PO 会导致“反萃取”RE产率降低,其原因为________.
4 9 3
(5)若略去“净化”过程,则制得的草酸稀土会混有________杂质(填化学式).
(6)在整个工艺中,可从副产物中提取________(填名称),用于生产氮肥.
16.(15分)某小组探究CuCl 溶液和NaSO 溶液的反应物,开展如下活动.
2 3
【理论预测】
预测 反应的离子方程式 实验现象
1 Cu2 SO2 CuSO 生成绿色沉淀
3 3
2 Cu2 SO2 H O Cu(OH) SO ________
3 2 2 2
3 2Cu2 2SO2 H O CuSO SO2 2H 生成红色沉淀
3 2 3 4
4 ________ 生成白色沉淀(CuCl)
学科网(北京)股份有限公司(1)预测2中的实验现象为________.
(2)预测4中反应的离子方程式为________.
【实验探究】
1mL0.2 molL1Na SO 溶液
2 3 立即生成橙黄色沉淀,3min后沉淀颜色变浅并伴有
实验1 混合
少量白色沉淀产生,振荡1min沉淀全部变为白色
2mL0.2molL1CuCl 溶液
2
(3)为证明实验1中白色沉淀为CuCl,设计实验如下.
①已知 Cu(NH ) 在水中呈无色.实验2总反应的离子方程式为________.
3 2
②为证明深蓝色溶液中含有Cl,进一步实验所需的试剂为________(填化学式).
【进一步探究】查阅资料获知橙黄色沉淀可能为xCuSO yCu SO zH O .在实验1获得橙黄色沉淀后,
4 2 3 2
立即离心分离并洗涤.为探究其组成进行如下实险.
(4)离心分离的目的是加快过滤速度,防止________.
(5)已知2Cu2 4I 2CuI .实验3能否证明橙黄色沉淀中含有Cu2和SO2,结合实验现象做
2 3
出判断并说明理由.
(6)橙黄色沉淀转化为CuCl的原因可能是Cl提高了Cu2的氧化性,进行如下实脸(已知装置中物质氧化
性与还原性强弱差异越大,电压越大).
实验4
装置 试剂a 试剂b 电压表读数
0.2molL1Na SO 溶液 0.2molL1CuCl 溶液 V
2 3 2 1
0.2molL1Na SO 溶液 X V
2 3 2
①表中X为________.
②能证实实验结论的实验现象为________.
【解释和结论】综上,Cu2与SO2发生复分解反应速率较快,发生氧化还原反应趋势更大.
3
7.(14分)CS 在化工生产中有重要作用.天然气法合成CS 相关反应如下:
2 2
学科网(北京)股份有限公司反应I CH (g)2S (g) CS (g)2H S(g) H 104.71kJmol
4 2 2 2 1
2CH (g)S (g) 2CS (g)4H S(g) H 201.73kJmol1
4 g 2 2 2
n(S )
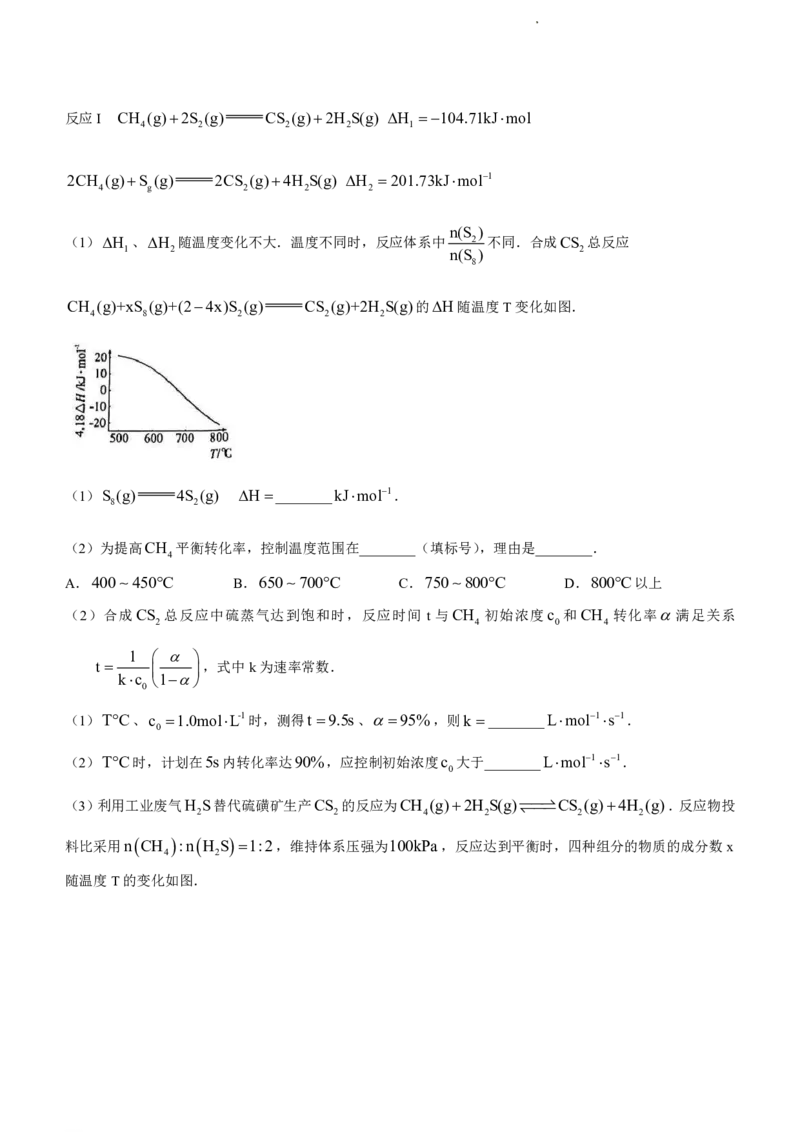
(1)H 、H 随温度变化不大.温度不同时,反应体系中 2 不同.合成CS 总反应
1 2 n(S ) 2
8
CH (g)+xS (g)+(24x)S (g) CS (g)+2H S(g)的H随温度T变化如图.
4 8 2 2 2
(1)S (g) 4S (g) H ________kJmol1.
8 2
(2)为提高CH 平衡转化率,控制温度范围在________(填标号),理由是________.
4
A.400450C B.650700C C.750800C D.800C以上
(2)合成CS 总反应中硫蒸气达到饱和时,反应时间 t 与CH 初始浓度c 和CH 转化率满足关系
2 4 0 4
1
t ,式中k为速率常数.
kc 1
0
(1)TC、c 1.0molL-1时,测得t 9.5s、95%,则k ________Lmol1s1.
0
(2)TC时,计划在5s内转化率达90%,应控制初始浓度c 大于________Lmol1s1.
0
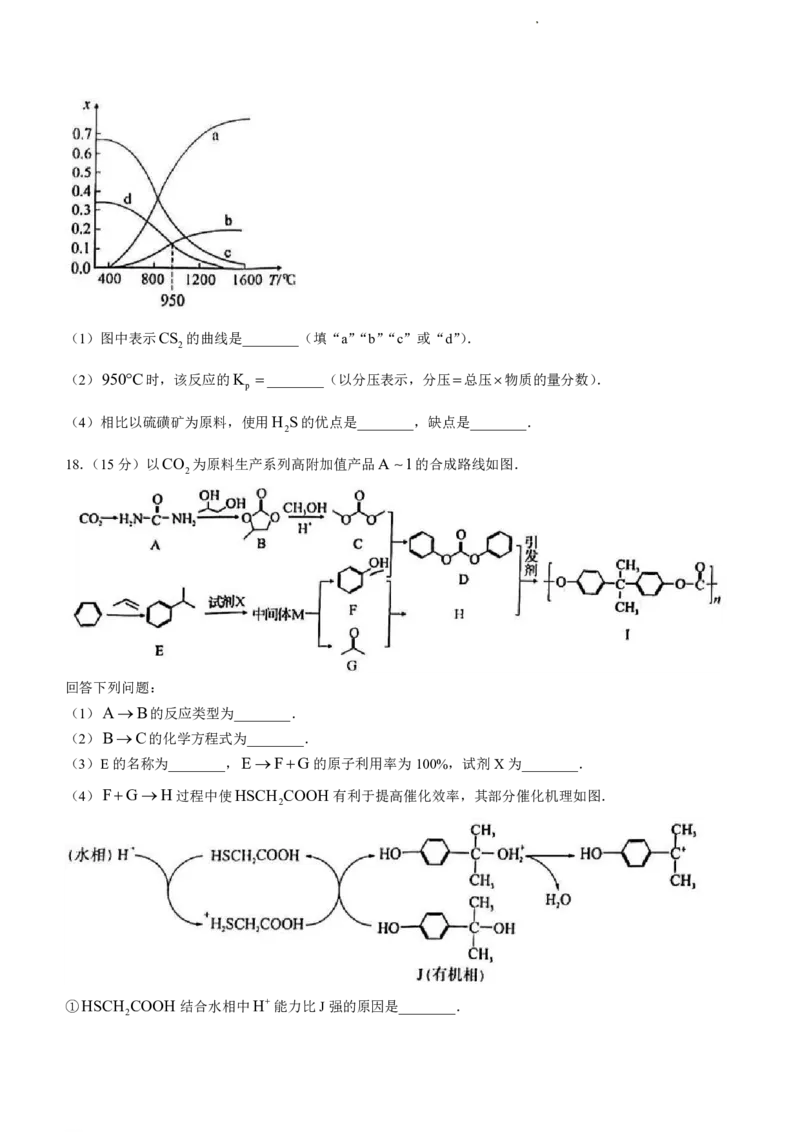
(3)利用工业废气H S替代硫磺矿生产CS 的反应为CH (g)2H S(g) CS (g)4H (g).反应物投
2 2 4 2 2 2
料比采用n CH :n H S 1:2,维持体系压强为100kPa,反应达到平衡时,四种组分的物质的成分数x
4 2
随温度T的变化如图.
学科网(北京)股份有限公司(1)图中表示CS 的曲线是________(填“a”“b”“c”或“d”).
2
(2)950C时,该反应的K ________(以分压表示,分压总压物质的量分数).
p
(4)相比以硫磺矿为原料,使用H S的优点是________,缺点是________.
2
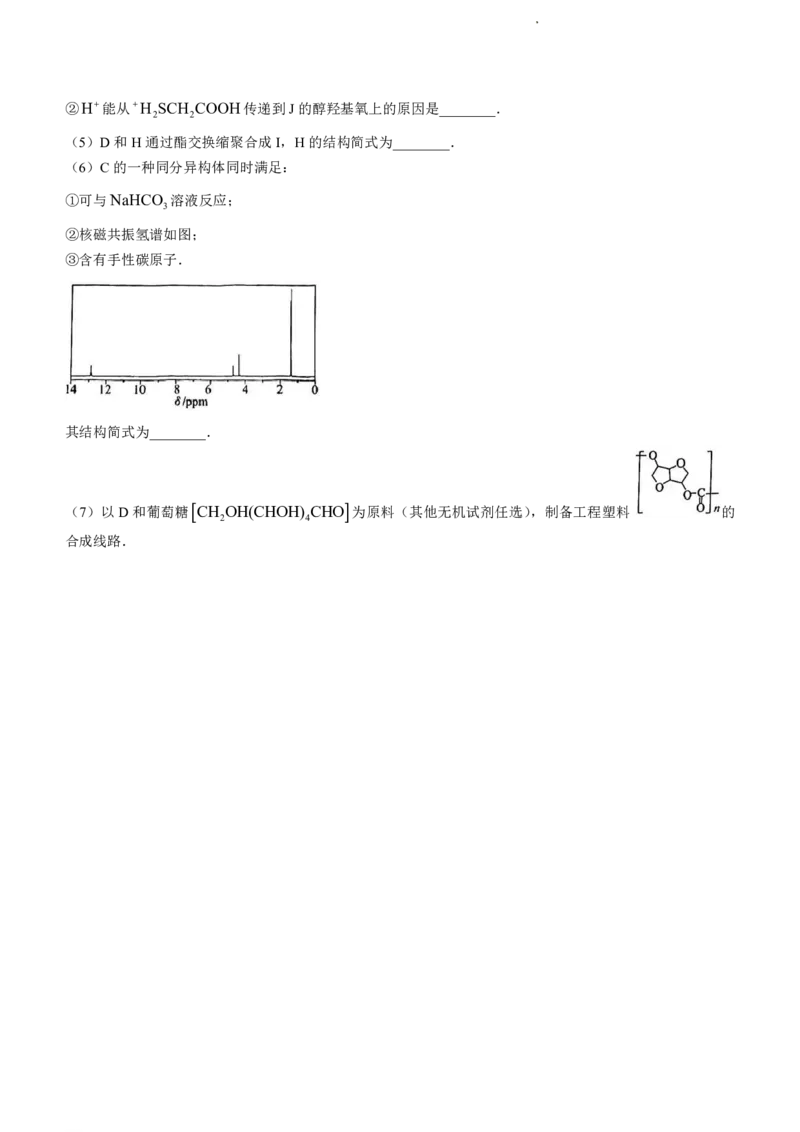
18.(15分)以CO 为原料生产系列高附加值产品A 1的合成路线如图.
2
回答下列问题:
(1)AB的反应类型为________.
(2)BC的化学方程式为________.
(3)E的名称为________,EFG的原子利用率为100%,试剂X为________.
(4)FGH过程中使HSCH COOH 有利于提高催化效率,其部分催化机理如图.
2
①HSCH COOH 结合水相中H能力比J强的原因是________.
2
学科网(北京)股份有限公司②H能从H SCH COOH传递到J的醇羟基氧上的原因是________.
2 2
(5)D和H通过酯交换缩聚合成I,H的结构简式为________.
(6)C的一种同分异构体同时满足:
①可与NaHCO 溶液反应;
3
②核磁共振氢谱如图;
③含有手性碳原子.
其结构简式为________.
(7)以D和葡萄糖 CH OH(CHOH) CHO 为原料(其他无机试剂任选),制备工程塑料 的
2 4
合成线路.
学科网(北京)股份有限公司学科网(北京)股份有限公司