文档内容
课时作业
A篇·知识对点训练
知识点1 乙酸的分子结构及酸性
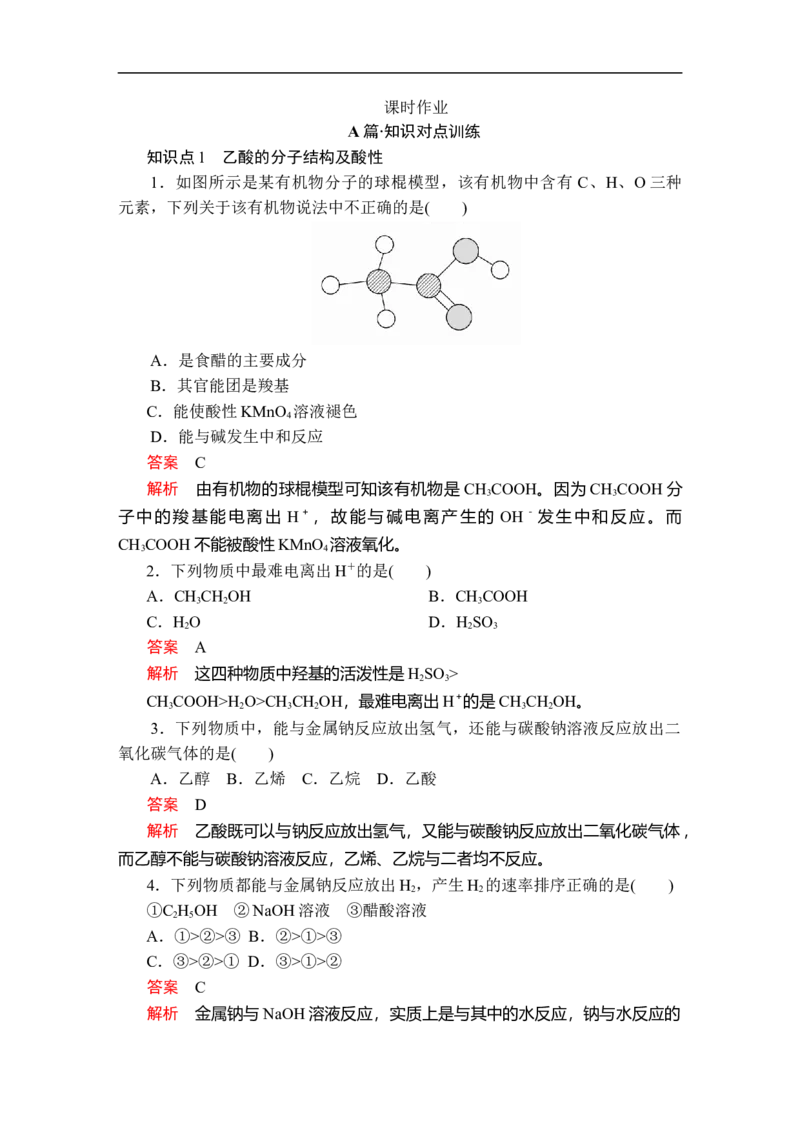
1.如图所示是某有机物分子的球棍模型,该有机物中含有 C、H、O三种
元素,下列关于该有机物说法中不正确的是( )
A.是食醋的主要成分
B.其官能团是羧基
C.能使酸性KMnO 溶液褪色
4
D.能与碱发生中和反应
答案 C
解析 由有机物的球棍模型可知该有机物是 CH COOH。因为CH COOH分
3 3
子中的羧基能电离出 H+,故能与碱电离产生的 OH-发生中和反应。而
CH COOH不能被酸性KMnO 溶液氧化。
3 4
2.下列物质中最难电离出H+的是( )
A.CH CH OH B.CH COOH
3 2 3
C.H O D.H SO
2 2 3
答案 A
解析 这四种物质中羟基的活泼性是H SO >
2 3
CH COOH>H O>CH CH OH,最难电离出H+的是CH CH OH。
3 2 3 2 3 2
3.下列物质中,能与金属钠反应放出氢气,还能与碳酸钠溶液反应放出二
氧化碳气体的是( )
A.乙醇 B.乙烯 C.乙烷 D.乙酸
答案 D
解析 乙酸既可以与钠反应放出氢气,又能与碳酸钠反应放出二氧化碳气体,
而乙醇不能与碳酸钠溶液反应,乙烯、乙烷与二者均不反应。
4.下列物质都能与金属钠反应放出H ,产生H 的速率排序正确的是( )
2 2
①C H OH ②NaOH溶液 ③醋酸溶液
2 5
A.①>②>③ B.②>①>③
C.③>②>① D.③>①>②
答案 C
解析 金属钠与NaOH溶液反应,实质上是与其中的水反应,钠与水反应的速率比乙醇快;醋酸溶液中H+浓度更大,与钠反应速率更快。
知识点2 酯化反应
5.下列说法正确的是( )
A.酯化反应的实质是酸与醇反应生成水,与中和反应相似
B.醇与所有酸发生的反应都是酯化反应
C.酯化反应是可逆反应
D.两个羟基去掉一分子水的反应就是酯化反应
答案 C
解析 酯化反应是指醇与酸作用生成酯和水的反应,该反应是分子之间的反
应,与中和反应(离子间的反应)有明显的差异性,A、D两项错误;无机含氧酸
与醇也能发生酯化反应生成酯和水,但无氧酸如 HBr与醇不能发生酯化反应,B
项错误。
6.羧酸和醇反应生成的酯的相对分子质量为 90,该反应的反应物可能是(
)
A.①② B.③④ C.②④ D.②③
答案 C7.下列有机物中,既能跟金属钠反应放出氢气,又能发生酯化反应,还能
发生催化氧化反应的是( )
A.乙酸 B.乙醇
C.乙酸乙酯 D.水
答案 B
解析 乙酸不能发生催化氧化反应,乙酸乙酯不能发生题中所说的任何反应,
水只能与金属钠反应,只有乙醇既能跟金属钠反应放出氢气,又能发生酯化反应,
还能发生催化氧化反应生成乙醛。
8.实验室用乙酸、乙醇、浓硫酸制取乙酸乙酯,加热蒸馏后,在饱和
Na CO 溶液的液面上得到无色油状液体,当振荡混合物时,有气泡产生,主要
2 3
原因可能是( )A.有部分H SO 被蒸馏出来
2 4
B.有部分未反应的乙醇被蒸馏出来
C.有部分未反应的乙酸被蒸馏出来
D.有部分乙酸乙酯与碳酸钠反应
答案 C
解析 制取乙酸乙酯时,加热挥发的乙酸会随蒸气进入碳酸钠溶液中,而乙
酸的酸性比碳酸强,所以会有二氧化碳生成。
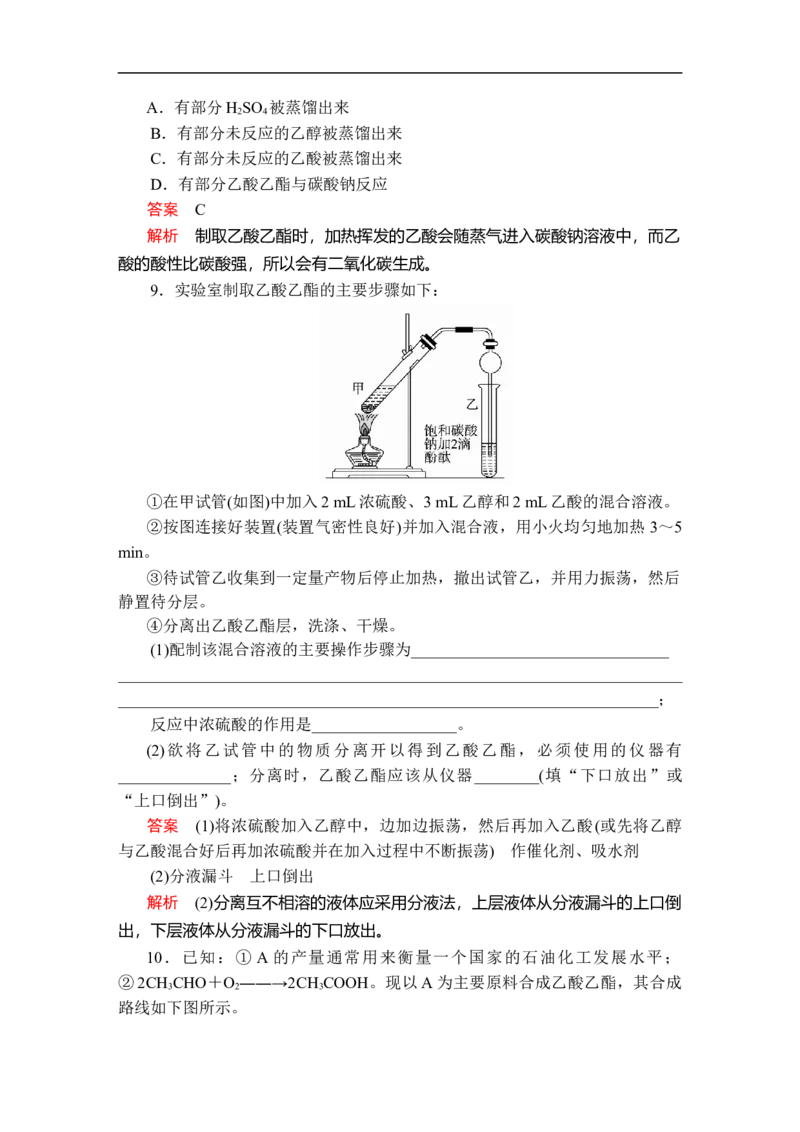
9.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热 3~5
min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后
静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)配制该混合溶液的主要操作步骤为________________________________
______________________________________________________________________
___________________________________________________________________;
反应中浓硫酸的作用是__________________。
(2)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有
______________;分离时,乙酸乙酯应该从仪器________(填“下口放出”或
“上口倒出”)。
答案 (1)将浓硫酸加入乙醇中,边加边振荡,然后再加入乙酸(或先将乙醇
与乙酸混合好后再加浓硫酸并在加入过程中不断振荡) 作催化剂、吸水剂
(2)分液漏斗 上口倒出
解析 (2)分离互不相溶的液体应采用分液法,上层液体从分液漏斗的上口倒
出,下层液体从分液漏斗的下口放出。
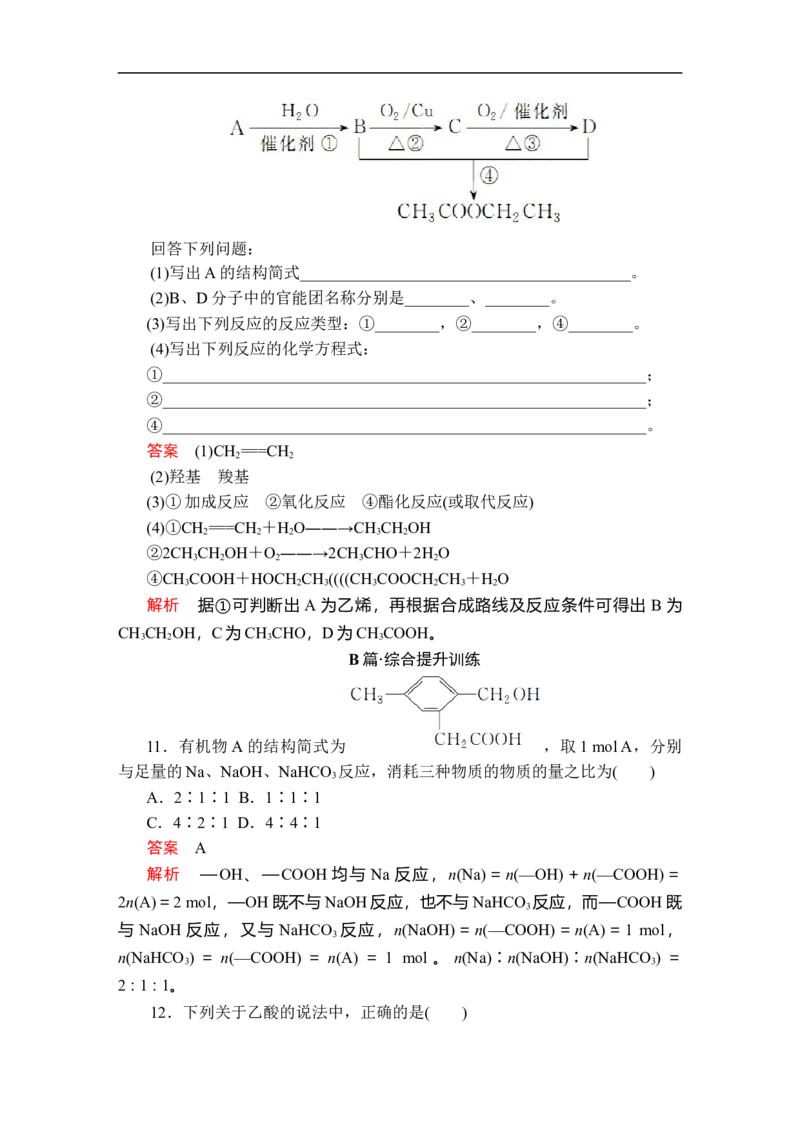
10.已知:① A 的产量通常用来衡量一个国家的石油化工发展水平;
②2CH CHO+O ――→2CH COOH。现以A为主要原料合成乙酸乙酯,其合成
3 2 3
路线如下图所示。回答下列问题:
(1)写出A的结构简式_________________________________________。
(2)B、D分子中的官能团名称分别是________、________。
(3)写出下列反应的反应类型:①________,②________,④________。
(4)写出下列反应的化学方程式:
①____________________________________________________________;
②____________________________________________________________;
④____________________________________________________________。
答案 (1)CH ===CH
2 2
(2)羟基 羧基
(3)①加成反应 ②氧化反应 ④酯化反应(或取代反应)
(4)①CH ===CH +H O――→CH CH OH
2 2 2 3 2
②2CH CH OH+O ――→2CH CHO+2H O
3 2 2 3 2
④CH COOH+HOCH CH ((((CH COOCH CH +H O
3 2 3 3 2 3 2
解析 据①可判断出 A 为乙烯,再根据合成路线及反应条件可得出 B 为
CH CH OH,C为CH CHO,D为CH COOH。
3 2 3 3
B篇·综合提升训练
11.有机物A的结构简式为 ,取1 mol A,分别
与足量的Na、NaOH、NaHCO 反应,消耗三种物质的物质的量之比为( )
3
A.2∶1∶1 B.1∶1∶1
C.4∶2∶1 D.4∶4∶1
答案 A
解析 —OH、—COOH 均与 Na 反应,n(Na)=n(—OH)+n(—COOH)=
2n(A)=2 mol,—OH既不与NaOH反应,也不与NaHCO 反应,而—COOH既
3
与 NaOH 反应,又与 NaHCO 反应,n(NaOH)=n(—COOH)=n(A)=1 mol,
3
n(NaHCO ) = n(—COOH) = n(A) = 1 mol 。 n(Na)∶n(NaOH)∶n(NaHCO ) =
3 3
2∶1∶1。
12.下列关于乙酸的说法中,正确的是( )①乙酸易溶于水和乙醇,其水溶液能导电
②无水乙酸又称为冰醋酸,它是纯净物
③乙酸分子里有四个氢原子,所以它不是一元酸
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤1 mol乙酸与足量乙醇在浓硫酸作用下可生成88 g乙酸乙酯
⑥食醋中含有乙酸,乙酸可由乙醇氧化得到
A.①②③④ B.①②③⑥
C.①②④⑥ D.②④⑤⑥
答案 C
解析 ①乙酸易溶于水和乙醇,是弱酸,其水溶液能导电,正确;②无水乙
酸在低于16.6 ℃时会凝结成冰一样的晶体,无水乙酸又称为冰醋酸,属于纯净
物,正确;③乙酸属于一元酸,错误;④乙酸在常温下是有刺激性气味的液体,
正确;⑤乙酸的酯化反应是可逆反应,不能进行到底,错误;⑥食醋中含有乙酸,
乙醇会被酸性 KMnO 溶液氧化成乙酸,正确。
4
13.巴豆酸的结构简式为CH —CH===CH—COOH。现有①氯化氢、②溴水、
3
③纯碱溶液、④乙醇、⑤酸性高锰酸钾溶液,判断在一定条件下,能与巴豆酸反
应的物质是( )
A.只有②④⑤ B.只有①③④
C.只有①②③④ D.全部
答案 D
解析 根据巴豆酸的结构简式可知,该分子中含有的官能团是碳碳双键和羧
基,碳碳双键能与HCl、溴水发生加成反应,能与酸性高锰酸钾溶液发生氧化反
应,羧基能与纯碱反应生成CO ,能与乙醇发生酯化反应,所以①~⑤的物质都
2
能发生反应。
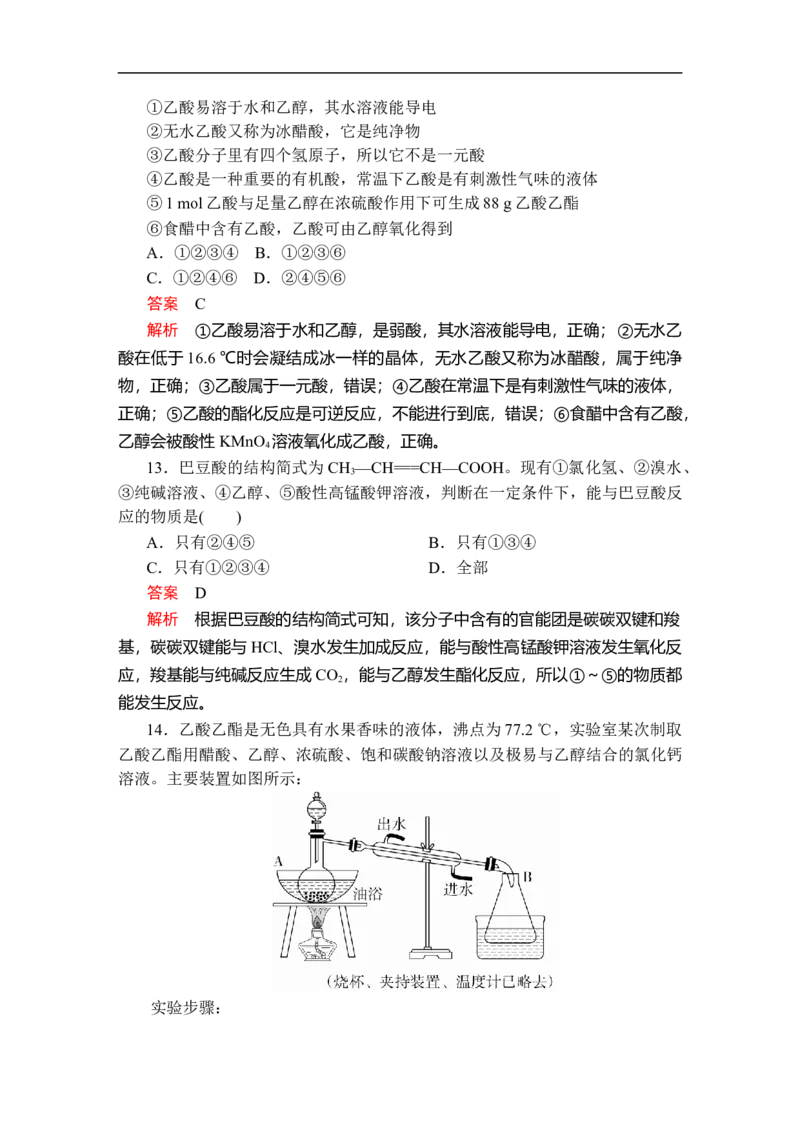
14.乙酸乙酯是无色具有水果香味的液体,沸点为77.2 ℃,实验室某次制取
乙酸乙酯用醋酸、乙醇、浓硫酸、饱和碳酸钠溶液以及极易与乙醇结合的氯化钙
溶液。主要装置如图所示:
实验步骤:①先向A中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙
醇和冰醋酸注入分液漏斗里待用。这时分液漏斗里醋酸和乙醇的物质的量之比约
为5∶7。
②加热油浴保温。
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加入速率,使蒸出酯的速
率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下B中的锥形瓶,将一定量饱和Na CO 溶液分批少量多次地加到馏出
2 3
液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物用分液漏斗分液,弃去水层。
⑦将饱和CaCl 溶液(适量)加入分液漏斗中,振荡一段时间后静置,放出水
2
层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
试回答:
(1)实验中浓硫酸的主要作用是______________。
(2)用饱和Na CO 溶液洗涤粗酯的目的是___________________________。
2 3
如果用NaOH溶液代替Na CO 溶液将引起的后果是
2 3
____________________________________________________________。
(3)用饱和CaCl 溶液洗涤粗酯的目的是____________。
2
(4)在步骤⑧所得的粗酯里还含有的杂质是____________。
答案 (1)作催化剂和吸水剂
(2)中和乙酸、溶解乙醇,降低乙酸乙酯的溶解度 使乙酸乙酯水解而使实
验失败
(3)除去乙醇
(4)水
解析 (1)浓硫酸在酯化反应中起到催化剂与吸水剂的作用。
(2)用饱和Na CO 溶液洗涤粗酯的目的是中和挥发出来的乙酸,使之转化为
2 3
乙酸钠溶于水中;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分
层得到酯。氢氧化钠是强碱,如果用 NaOH溶液代替Na CO 溶液将会使乙酸乙
2 3
酯水解。
(3)饱和CaCl 溶液可以吸收乙酸乙酯中可能残留的乙醇。
2
(4)饱和碳酸钠溶液除掉了乙酸和乙醇,饱和 CaCl 溶液可以吸收乙酸乙酯中
2
可能残留的乙醇,这样分离出的粗酯中还含有杂质水。