文档内容
2024 级校际联考(五)化学试题
可能用到的相对原子质量: 1 12 14 16 32 64 65
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1. 化学与生产生活密切相关,以下说法错误的是( )
A. 运用盐类水解的原理,可以用热碱去油污
B. 工业合成氨气,不能使用过高温度,原因之一是防止催化剂中毒
C. 将含有较多氯化镁的海水溶液蒸干并灼烧用于得到氯化镁固体粗产品
D. 焊接钢材时,分别用饱和NaCO 和NH Cl溶液处理焊接点
2 3 4
2. 下列事实不能用勒夏特列原理解释的是( )
A.工业合成氨中,将氨气液化分离
B. 平衡中加入少量KSCN固体,溶液颜色加深
C. A、B两支试管中分别加入等体积5%的HO 溶液,在B试管中加入2~3滴CuSO 溶液,B中试管中
2 2 4
产生气泡快
D.向氯水中加碳酸钙,可提高溶液中HClO的浓度
3. 下列说法不正确的是( )
A.已知2O(g)= 3O(g)的ΔH<0、ΔS>0,则该反应在任何温度下都能自发进行
3 2
B.“冰,水为之,而寒于水”,相同质量的水和冰,水具有的能量高
C.干冰(CO)升华过程中ΔS>0
2
D.碳酸钙在高温下才能分解,因此碳酸钙的分解反应不属于自发反应
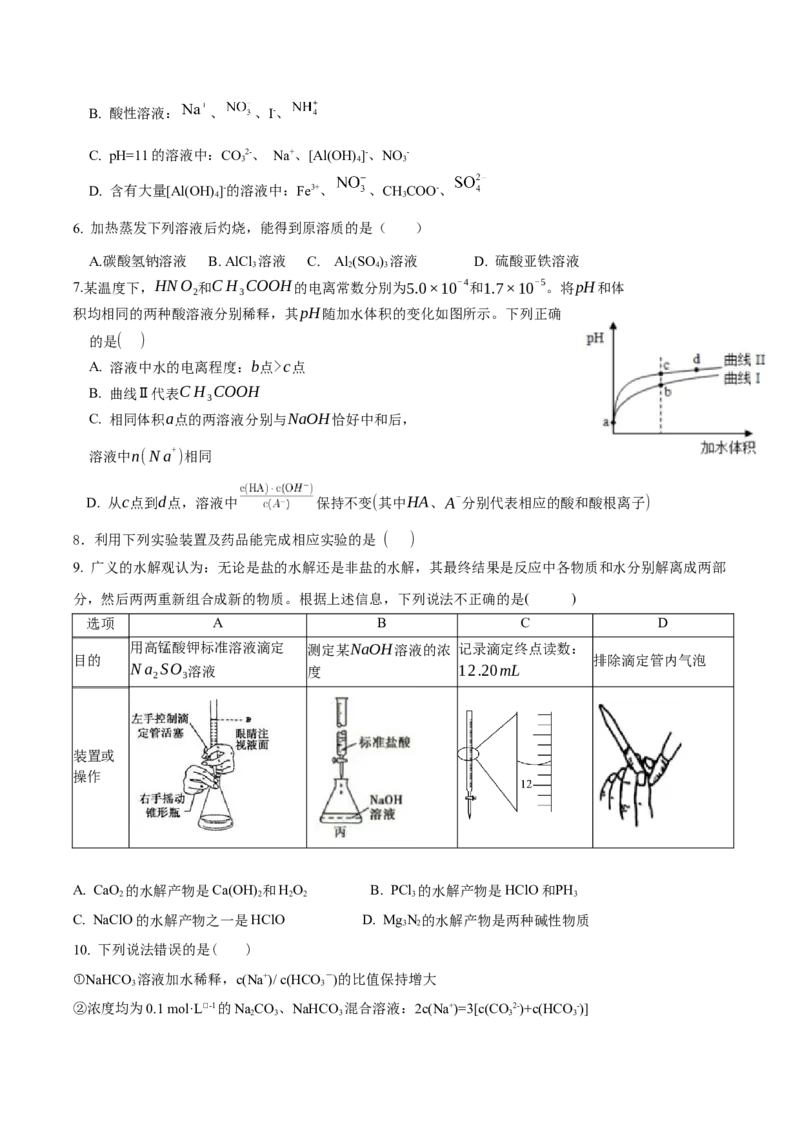
4. 下列图示与对应的叙述不相符合的是( )
A. 图甲表示燃料燃烧反应的能量变化
B.图乙表示酶催化反应的反应速率随反应温度的变化
C.图丙表示弱电解质在水中建立电离平衡的过程
D.图丁表示强碱滴定强酸的滴定曲线
5. 在室温下的下列环境中,可能大量共存的离子组是( )
的溶液: 、 、Cl-、
A.B. 酸性溶液: 、 、I-、
C. pH=11的溶液中:CO2-、 Na+、[Al(OH) ]-、NO -
3 4 3
D. 含有大量[Al(OH) ]-的溶液中:Fe3+、 、CHCOO-、
4 3
6. 加热蒸发下列溶液后灼烧,能得到原溶质的是( )
A.碳酸氢钠溶液 B. AlCl 溶液 C. Al (SO ) 溶液 D. 硫酸亚铁溶液
3 2 4 3
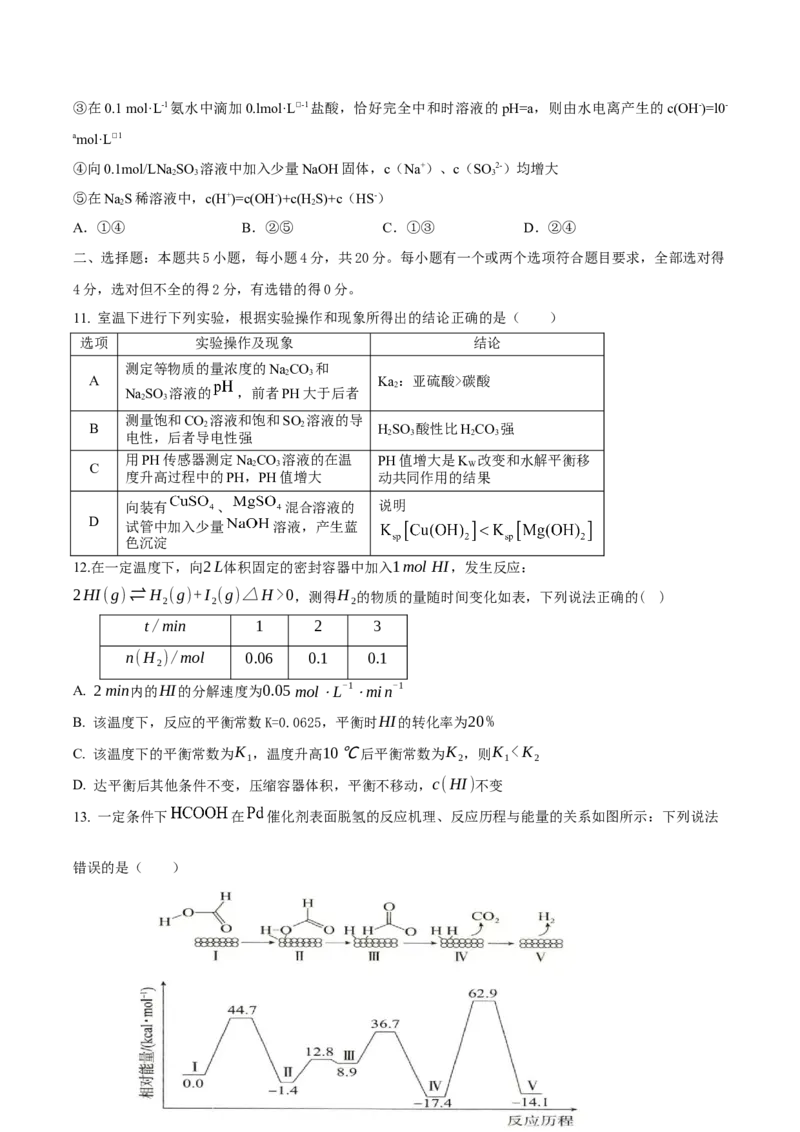
7.某温度下,HNO 和CH COOH的电离常数分別为5.0×10-4和1.7×10-5。将pH和体
2 3
积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列正确
的是( )
A. 溶液中水的电离程度:b点>c点
B. 曲线Ⅱ代表CH COOH
3
C. 相同体积a点的两溶液分别与NaOH恰好中和后,
溶液中n(Na+
)相同
D. 从c点到d点,溶液中 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
8.利用下列实验装置及药品能完成相应实验的是 ( )
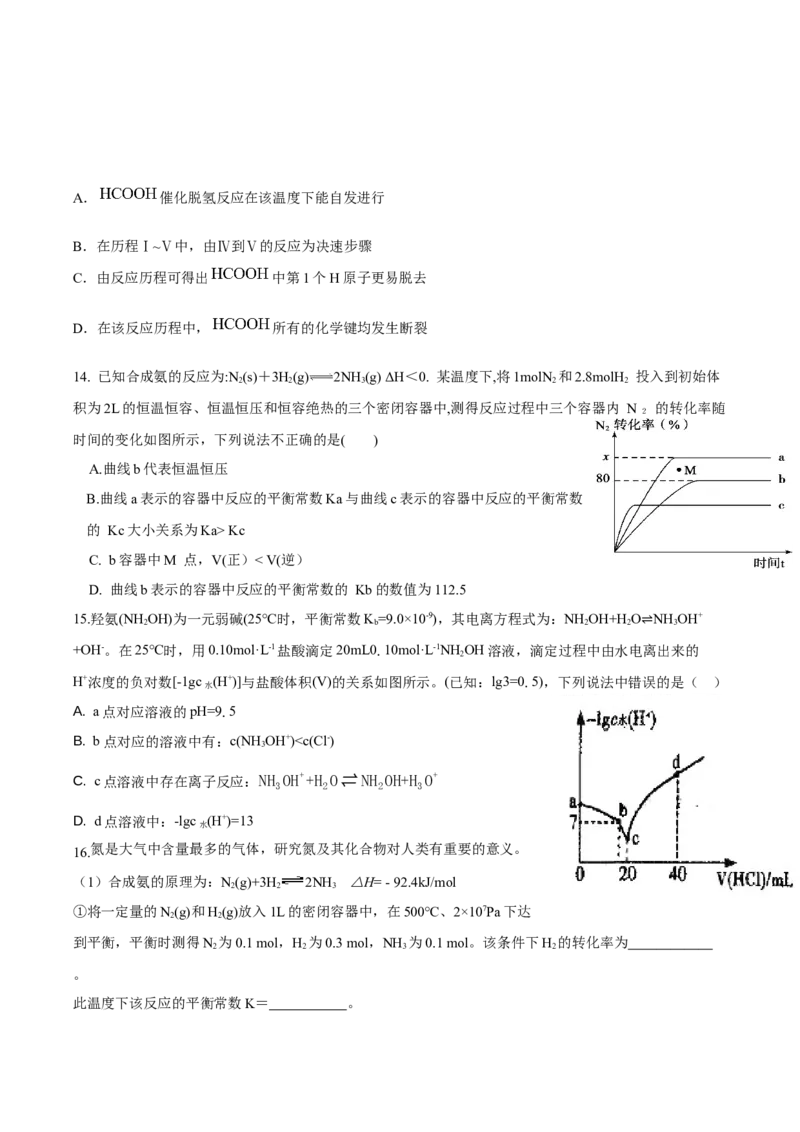
9. 广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部
分,然后两两重新组合成新的物质。根据上述信息,下列说法不正确的是( )
选项 A B C D
用高锰酸钾标准溶液滴定 测定某NaOH溶液的浓 记录滴定终点读数:
目的 排除滴定管内气泡
Na SO 溶液 度 12.20mL
2 3
装置或
操作
A. CaO 的水解产物是Ca(OH) 和HO B. PCl 的水解产物是HClO和PH
2 2 2 2 3 3
C. NaClO的水解产物之一是HClO D. MgN的水解产物是两种碱性物质
3 2
10. 下列说法错误的是( )
①NaHCO 溶液加水稀释,c(Na+)/ c(HCO -)的比值保持增大
3 3
②浓度均为0.1 mol·L-1的NaCO、NaHCO 混合溶液:2c(Na+)=3[c(CO 2-)+c(HCO-)]
2 3 3 3 3③在0.1 mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-
amol·L1
④向0.1mol/LNa SO 溶液中加入少量NaOH固体,c(Na+)、c(SO 2-)均增大
2 3 3
⑤在NaS稀溶液中,c(H+)=c(OH-)+c(HS)+c(HS-)
2 2
A.①④ B.②⑤ C.①③ D.②④
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得
4分,选对但不全的得2分,有选错的得0分。
11. 室温下进行下列实验,根据实验操作和现象所得出的结论正确的是( )
选项 实验操作及现象 结论
测定等物质的量浓度的NaCO 和
2 3
A Ka:亚硫酸>碳酸
2
NaSO 溶液的 ,前者PH大于后者
2 3
测量饱和CO 溶液和饱和SO 溶液的导
B 2 2 HSO 酸性比HCO 强
电性,后者导电性强 2 3 2 3
用PH传感器测定NaCO 溶液的在温 PH值增大是K 改变和水解平衡移
C 2 3 W
度升高过程中的PH,PH值增大 动共同作用的结果
向装有 、 混合溶液的 说明
D
试管中加入少量 溶液,产生蓝
色沉淀
12.在一定温度下,向2L体积固定的密封容器中加入1mol HI,发生反应:
2HI(g)⇌H (g)+I (g)△H>0,测得H 的物质的量随时间变化如表,下列说法正确的( )
2 2 2
t/min 1 2 3
n(H )/mol 0.06 0.1 0.1
2
A. 2 min内的HI的分解速度为0.05 mol⋅L-1 ⋅min-1
B. 该温度下,反应的平衡常数K=0.0625,平衡时HI的转化率为20%
C. 该温度下的平衡常数为K ,温度升高10℃后平衡常数为K ,则K Kc
C. b容器中M 点,V(正)< V(逆)
D. 曲线b表示的容器中反应的平衡常数的 Kb的数值为112.5
15.羟氨(NH OH)为一元弱碱(25℃时,平衡常数K=9.0×10-9),其电离方程式为:NH OH+H O NH OH+
2 b 2 2 3
+OH-。在25℃时,用0.10mol·L-1盐酸滴定20mL0.10mol·L-1NH OH溶液,滴定过程中由水电⇌离出来的
2
H+浓度的负对数[-1gc (H+)]与盐酸体积(V)的关系如图所示。(已知:lg3=0.5),下列说法中错误的是( )
水
A. a点对应溶液的pH=9.5
B. b点对应的溶液中有:c(NH OH+)T)、其他条件相同时,下列图像正确的是______(填代号)。
2 1
17. I. 已知1mol/L (NH )SO 溶液测得溶液PH值为4,1mol/L 的NaCO 溶液
4 2 4 2 3
测得溶液PH值为11,回答下列问题:
(1)1mol/L 的NaCO 溶液中各种离子浓度由大到小关系 ;
2 3
(2)1mol/L (NH )SO 溶液中由水电离的c(H+) 1mol/L 的NaCO 溶液由水电离的c(H+);
4 2 4 2 3
(填“>”“<”或“=”)
(3)取1mol/L (NH )SO 溶液加蒸馏水稀释,在稀释过程中,下列表达式变小的是 ;
4 2 4
A.c(H+) B.c (NH+)/c(H+) C.c(H+)·c(OH-) D.c(OH-)/c(H+)
4
(4)取1mol/L (NH )SO 溶液1L,通入NH 的物质的量为a摩尔时溶液的PH值恰好
4 2 4 3
为7,已知NH •H O的电离常数为2×10-5(mol/L)2,则a= 。(溶液温度体积不变)
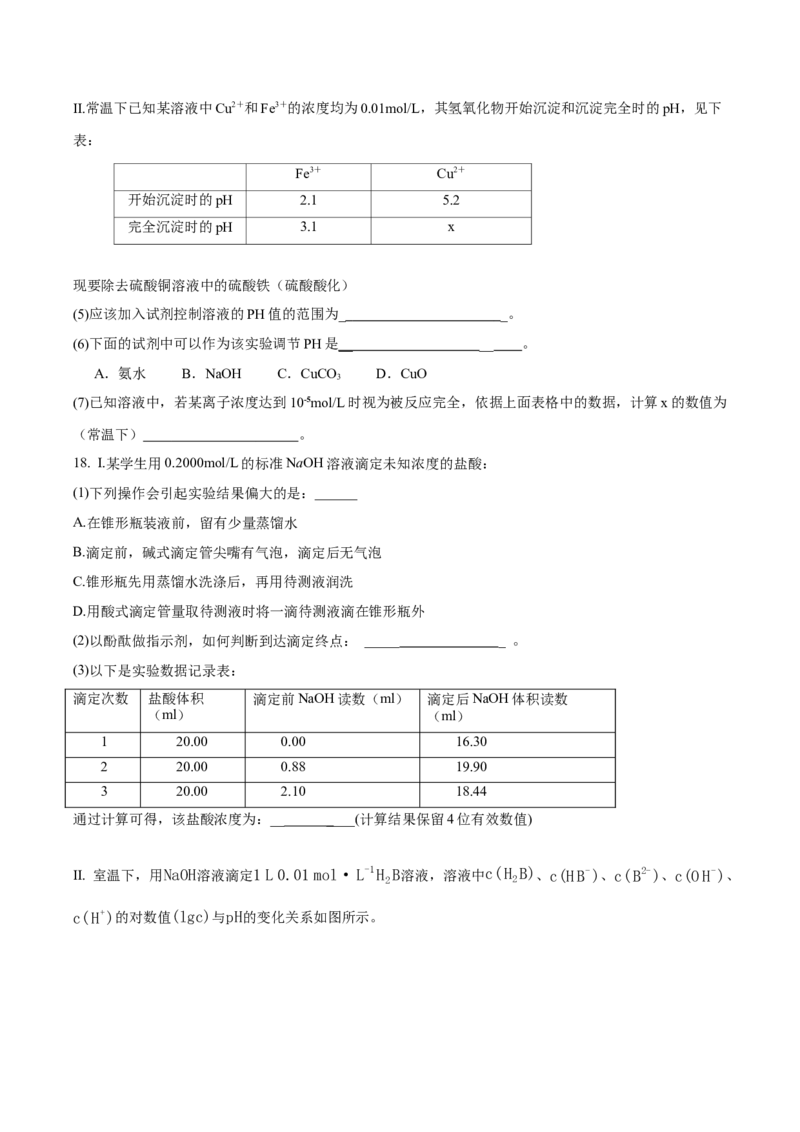
3 2II.常温下已知某溶液中Cu2+和Fe3+的浓度均为0.01mol/L,其氢氧化物开始沉淀和沉淀完全时的pH,见下
表:
Fe3+ Cu2+
开始沉淀时的pH 2.1 5.2
完全沉淀时的pH 3.1 x
现要除去硫酸铜溶液中的硫酸铁(硫酸酸化)
(5)应该加入试剂控制溶液的PH值的范围为_ _。
(6)下面的试剂中可以作为该实验调节PH是 __ __ 。
A.氨水 B.NaOH C.CuCO D.CuO
3
(7)已知溶液中,若某离子浓度达到10-5mol/L时视为被反应完全,依据上面表格中的数据,计算x的数值为
(常温下) 。
18. I.某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸:
(1)下列操作会引起实验结果偏大的是:______
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,碱式滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,再用待测液润洗
D.用酸式滴定管量取待测液时将一滴待测液滴在锥形瓶外
(2)以酚酞做指示剂,如何判断到达滴定终点: _____ _ 。
(3)以下是实验数据记录表:
滴定次数 盐酸体积 滴定前NaOH读数(ml) 滴定后NaOH体积读数
(ml) (ml)
1 20.00 0.00 16.30
2 20.00 0.88 19.90
3 20.00 2.10 18.44
通过计算可得,该盐酸浓度为:__ ____(计算结果保留4位有效数值)
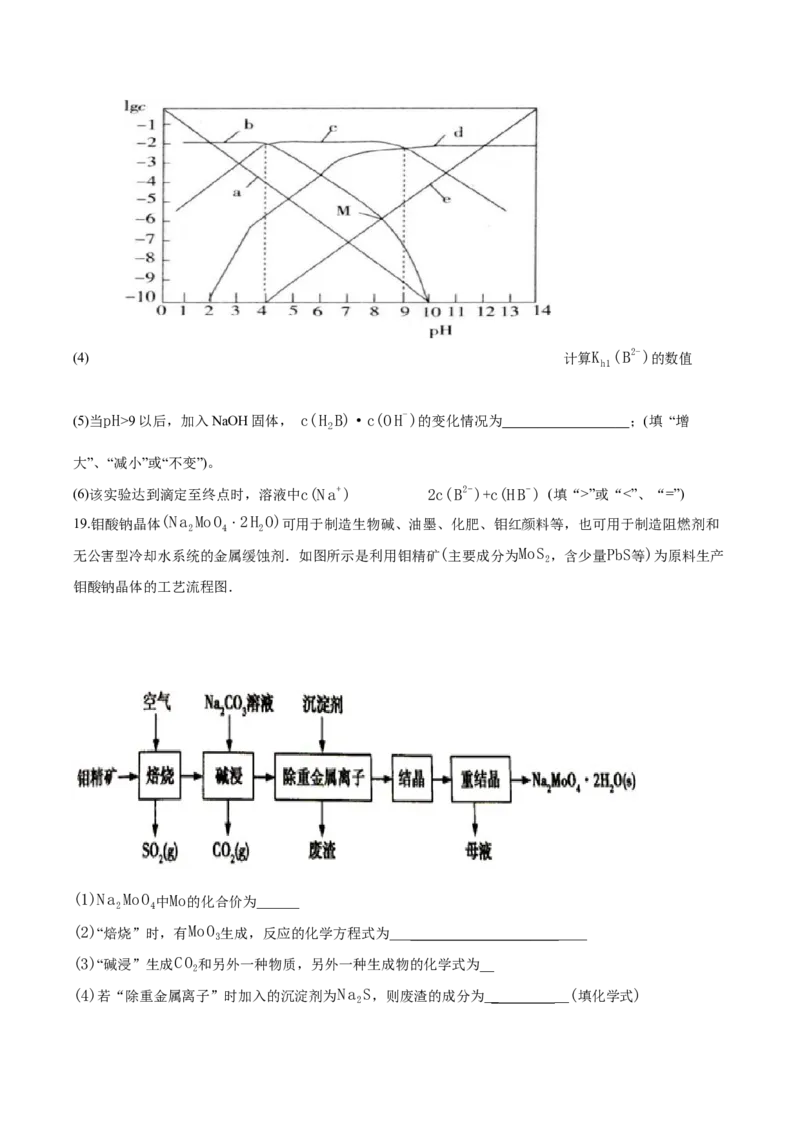
II. 室温下,用NaOH溶液滴定1 L 0.01 mol·L-1H B溶液,溶液中c(H B)、c(HB-)、c(B2-)、c(OH-)、
2 2
c(H+)的对数值(lgc)与pH的变化关系如图所示。(4) 计算K (B2-)的数值
h1
(5)当pH>9以后,加入NaOH固体, c(H B)·c(OH-)的变化情况为 ;(填 “增
2
大”、“减小”或“不变”)。
(6)该实验达到滴定至终点时,溶液中c(Na+) 2c(B2-)+c(HB-) (填“>”或“<”、“=”)
19.钼酸钠晶体(Na MoO ⋅2H O)可用于制造生物碱、油墨、化肥、钼红颜料等,也可用于制造阻燃剂和
2 4 2
无公害型冷却水系统的金属缓蚀剂.如图所示是利用钼精矿(主要成分为MoS ,含少量PbS等)为原料生产
2
钼酸钠晶体的工艺流程图.
(1)Na MoO 中Mo的化合价为______
2 4
(2)“焙烧”时,有MoO 生成,反应的化学方程式为___ _ ____ ____
3
(3)“碱浸”生成CO 和另外一种物质,另外一种生成物的化学式为__
2
(4)若“除重金属离子”时加入的沉淀剂为Na S,则废渣的成分为_ _ __(填化学式)
2(5)测得“除重金属离子”中部分离子的浓度:c(MoO2-)=0.40mol⋅L-1 ,c(SO2-)=0.04mol⋅L-1.“结
4 4
晶”前应先除去SO2- ,方法是加入Ba(OH) 固体.假设加入Ba(OH) 固体后溶液体积不变,当BaMoO 开
4 2 2 4
始沉淀时,去除的SO2- 的质量分数为 %.(保留小数点后一位数字)〔已知
4
K (BaSO )=1.1×10-10 ,K (BaMoO )=4.0×10-8〕
sp 4 sp 4
(6)在碱性条件下,将钼精矿加入NaClO溶液中,也可以制备钼酸钠.该反应的离子方程式为_ __
__ _ .
20. 以CO 为碳源选择性加氢合成甲醇一直是研究的热点,涉及的主要反应如下:
2
i. CO (g) +3H (g) CHOH(g) +HOg) ΔH<0
2 2 3 2 1
ii. CO (g) +H (g) CO(g) +H O(g) ΔH >0
2 2 2 2
的
(1)在一定温度下,由最稳定单质生成1mol某物质 焓变叫做该物质的标准摩尔生成焓,下表为298K
时几种物质的标准摩尔生成焓。则△H =___________kJ·mol-1。
2
物质 H(g) O(g) CO(g) CO(g) HO(g)
2 2 2 2
(kJ ·mol-1) 0 0 - 110.5 - 393.5 -241.8
(2)反应ii的反应速率v=v -v =k c(CO)c(H)-k cm (CO)cn (H O),其中k 、k 分别为正、逆反应
正 逆 正 2 2 逆 2 正 逆
速率常数。该反应的平衡常数 ,则m=___________,升高温度时k -k ___________ (填 “增
正 逆
大”、“减小”或“不变”)。
(3)在一定温度下,向1L密闭容器中通入1mol CO (g) 和a mol H (g) 发生上述反应,起始总压强为
2 2
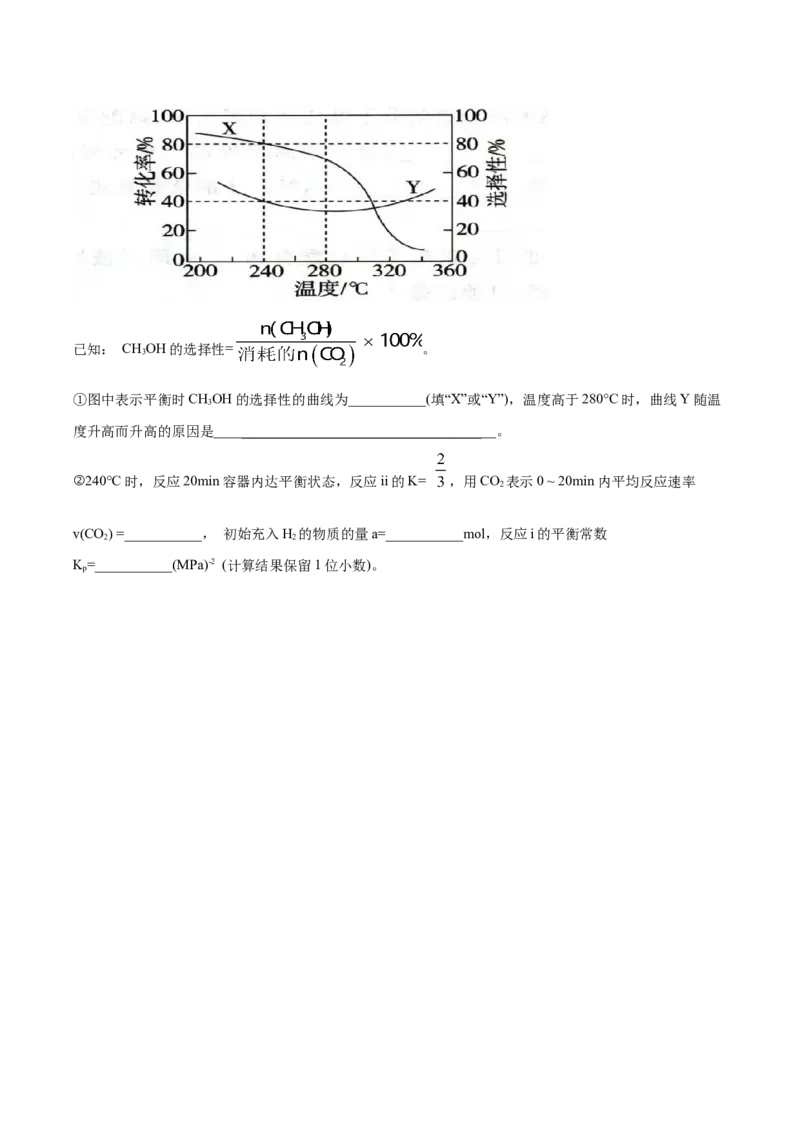
21.2MPa。实验测得CO 的平衡转化率和平衡时CHOH的选择性随温度变化如图所示:
2 3已知: CHOH的选择性= 。
3
①图中表示平衡时CHOH的选择性的曲线为___________(填“X”或“Y”),温度高于280°C时,曲线Y随温
3
度升高而升高的原因是____ _ ____ __。
②240°C时,反应20min容器内达平衡状态,反应ii的K= ,用CO 表示0 ~ 20min内平均反应速率
2
v(CO) =___________, 初始充入H 的物质的量a=___________mol,反应i的平衡常数
2 2
K=___________(MPa)-2 (计算结果保留1位小数)。
p一、单项选择题:本题包括10个小题,每小题2分,共20分,每小题只有1个选项符合题意。
1. C 2. C 3. D 4. A 5. C 6.C 7.D 8.D 9. B 10. B
二、选择题:本题包括5个小题,共20分。每小题有一个或两个选项符合题意,全部选对的
得4分,选对但不全的得2分,有选错的得0分。
11. AC 12. AC 13. D 14. AD 15.BD
三、非选择题:本题共5小题,共60分。
16.(12分) 除标注外,每空2分
(1)33.3% (1分) 100/27(1分) ad
(2)0.0015mol/(L·s) bc c (3) 乙
17.(12分) 除标注外,每空2分
I、(1) C(Na+)>C(CO 2-)>C(OH-)>C(HCO -)>C(H+) (1分) (2) < (1分)
3 3
(3)AB (4) 0.01
II、(5) [3.1,5.2) (6) CD (7) 6.7
18.(12分)
(1) BC (2)当滴入最后半滴标准溶液时,锥形瓶中溶液由无色变为浅红色,并且在半分钟内
颜色不再变化。 (3)0.1632 mol/L
(4)10-5 (5)减小 (6)>
19.(10分) 除标注外,每空2分
.(1)+6;(1分) (2)2MoS +7O 2MoO +4SO ;
2 2 3 2
(3) Na MoO ;(1分) (4)PbS;
2 4
(5)97.3; (6)MoS +9ClO-+6OH-=MoO2-+9Cl-+2SO2-+3H O
2 4 4 2
或者 MoS +3ClO-+2OH-=MoO2-+3Cl-+2S+H O
2 4 2
20(14分) 除标注外,每空2分
(1)+41.2
(2) 1 增大 (1分)
(3) X (1分) 高于280℃时,以反应ii为主,反应ii为吸热反应,温度升高,平衡
正向移动,CO 的平衡转化率增大
20.02mol/(L·min) 1.12 4.2