文档内容
点石联考10月高二联考 化学
2025—2026 学年度上学期高二年级 10 月份联合考试 化学
说明:
本解答给出的非选择题答案仅供参考,若考生的回答与本答案不同,但只要合理,可参照评
分标准酌情给分。
一、选择题:本题共 15 分,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合
题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C A B D B B A C D A C B C C B
严肃认真 高度负责 公平公正
给分有理 扣分有据 宽严适度
二、非选择题:本题共 4 小题,共 55 分。
16.(每空2分)
题号 参考答案 评分细则
N (g)+O (g)===2NO(g) ∆H=+180.5 kJ·mol-1 或 完全正确得2分,方程式错(配平错误、不写状态)
2 2
1 1 扣1分,方程式对反应热错(数值错误、不写单位)
N (g)+ O (g)===NO(g) ∆H=+90.25kJ·mol-1
2 2
2 2
(1) 扣1分,方程式错反应热对不得分;===用
或
表示、反应热不写“+”号不扣分
①SnO ①此空写化学名称扣1分
2
(2) ②不是 ②此空答案唯一,错字、漏字、多字均不得分
③B ③此空答案唯一
①> < ①>(此空写汉字扣1分,下同) <
(3)
②BD ②完全正确得2分,少选得1分,错选不得分
17.(除特殊标注外,每空2分)
题号 参考答案 评分细则
第一个空:完全正确得2分,配平错误、不写条
高温
SiO 2 +2C Si+2CO↑ 件、不写箭头扣1分,条件写加热、△扣1分
(1) 第二个空:答案合理即可,其中加反应物增大接
将焦炭粉碎后与石英砂混合均匀 触面积得2分,加反应物增大浓度不得分,只写
加反应物得1分
吸收(1分) 此空答案唯一,错字、漏字、多字均不得分
(2) 19.5(1分) 此空本次阅卷多写单位(kJ)不扣分
不变 此空答案唯一,错字、漏字、多字均不得分
点石联考 高二10月化学试题参考答案 第 1 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
(3) L (1分) 此空答案唯一,多写不得分
1
abc或a>b>c 完全正确得2分,有错、有漏不得分
此空写化学名称不扣分
(4) H 、HCl(共2分)
2 少写给1分,有写错的此空不得分
18.(每空2分)
题号 参考答案 评分细则
此空任写其中一个,完全正确得2分,配平错误、
S O2+2H+===SO ↑+S↓+H O
2 3 2 2 不写箭头、写化学方程式扣1分
(1)
或S O2+2H+===H SO +S↓
2 3 2 3
生成的SO 易溶于水,导致容器内压强变化不明显 此空答到SO 易溶于水即给满分
2 2
13 此空答案唯一,错、漏、多字均不得分
(2) H+浓度 此空答H+浓度或反应物浓度、H SO 浓度均可给
2 4
分
1
(3) 此空“数值对但未化简”扣1分
1750
随着c(KMnO )的增大,反应速率的增大不能抵消 此空答案表述不唯一,合理表述即可,但表达意
(4) 4
n(KMnO )增大带来的影响,总反应时长增加 思正确,内容表述不顺畅,可酌情扣1分
4
(5) Mn2+ 此空答案唯一
19.(每空2分)
题号 参考答案 评分细则
高温 此空答案唯一,错字、漏字、多字均不得分。
(1) +49 此空不写“+”号不扣分,此空本次阅卷多写单
位(kJ·mol-1)不扣分
AD 此空完全正确得2分,少选得1分,错选不得分
增大水醇比,有利于反应 此空答案表述不唯一,合理表述即可,如“增大
(2)
水醇比,水蒸气浓度增大,促使积碳与水蒸气反
C(s)+H2O(g) CO(g)+H2(g)正向进行,消除积碳
应,将积碳转化为气体产物而消除”等也可。
1 此空本次阅卷多写单位不扣分
(3) 16 此空“数值对但未化简”扣1分
49V2
(4) 4×10-4 此空本次阅卷多写单位(cm3·s-1)不扣分
严肃认真 高度负责 公平公正
给分有理 扣分有据 宽严适度
请化学老师上课讲评试卷时,提醒学生认真审题、规范作答。
及时纠正学生此次答题上所存在的一些小问题!
点石联考 高二10月化学试题参考答案 第 2 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
2025—2026 学年度上学期高二年级 10 月份联合考试 化学
一、选择题
1.【点石答案】C
1.【素材来源】人教版高中化学教材选择性必修1第二章第一节化学反应速率相关内容。
1.【点石立意】本题以生活情境为背景,考查学生对化学反应速率调控的理解。体现科学精神与社会责任
等学科素养。
1.【点石解析】用菜窖储存大白菜主要是为了减缓大白菜腐败速率,A项不符合题意;哈尔滨红肠中按国
家标准添加适量亚硝酸钠是利用亚硝酸钠作防腐剂,减慢红肠腐败速率,B项不符合题意;腊月制作东北
大酱时在温热的环境下发酵是为了适当升高温度,加快发酵速率,C项符合题意;东北大铁锅洗干净后擦
干水分是为了减缓铁锅生锈速率,D项不符合题意。
2.【点石答案】A
1.【素材来源】人教版高中化学教材选择性必修1第一章第一节反应热相关内容。
1.【点石解析】本题以基本概念为载体进行考查,考查学生对化学反应与能量变化、吸放热反应的判断、
焓变的理解。体现宏观辨识与微观探析等学科素养。题以生活情境为背景,考查学生对化学反应速率调控
的考查。体现科学精神与社会责任等学科素养。
【点石思路】甲烷燃烧时,化学能转化为光能和热能,A项错误。
3.【点石答案】B
1.【素材来源】人教版高中化学教材选择性必修1第三章第一节电离平衡相关内容。
1.【点石立意】本题以弱电解质判断方法为载体进行考查,考查学生对弱电解质本质的理解。体现宏观辨
识与微观探析等学科素养。
1.【点石解析】未说明溶液浓度,氨水导电能力弱不能说明NH ·H O为弱电解质,A项不符合题意;稀氨
3 2
水中存在NH和NH ·H O,说明NH ·H O部分电离,NH ·H O为弱电解质,B项符合题意;氨水能与硫
4 3 2 3 2 3 2
酸发生反应不能说明NH ·H O为弱电解质,C项不符合题意;常温下,氨水pH大于7说明溶液呈碱性,
3 2
不能说明NH ·H O为弱电解质,D项不符合题意。
3 2
4.【点石答案】D
1.【素材来源】人教版高中化学教材选择性必修1第一章反应热、第二章第二节化学平衡、第二章第三节
化学反应的方向关内容。
1.【点石立意】本题以硫转化过程的物质转化和能量变化为载体进行考查,考查学生燃烧热的理解、可逆
反应特点掌握。体现宏观辨识与微观探析、变化观念与平衡思想等学科素养。
1.【点石解析】未说明温度和压强,11.2LH S气体的物质的量无法计算,A项错误;1molSO 与足量
2 2
O 置于密闭容器中发生的是可逆反应,生成SO 的分子数小于N ,B项错误;1molH S(g)完全燃烧生成
2 3 A 2
SO (g)和H O(l)所放出的热量为H S的燃烧热,C项错误;SO (g)+H O(l)===H SO (l)为放热反应,反应过
2 2 2 3 2 2 4
程中气体分子数目减少,∆H与∆S均小于零,D项正确。
5.【点石答案】B
1.【素材来源】人教版高中化学教材选择性必修1第一章反应热、第三章第一节电离平衡相关内容。
1.【点石立意】本题以化学符号表征、化学图像分析为载体进行考查,考查学生盖斯定律的应用、弱电解
质电离本质、弱电解质稀释过程分析、不同状态物质转化过程中的能量变化。体现宏观辨识与微观探析、
变化观念与平衡思想、证据推理与模型认知等学科素养。
1.【点石解析】HCl为强电解质,在水溶液中能全部电离生成Cl-和H O+,A项正确;根据盖斯定律可知
3
点石联考 高二10月化学试题参考答案 第 3 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
2Cu(s)+O (g)===2CuO(s) ∆H =-315kJ·mol-1,B项错误;纯净的醋酸不导电,加水后溶液导电能力增强,
2 1
当加水过多,溶液中导电离子浓度减小,导电能力减弱,C项正确;H O(s)→H O(l)→H O(g)的每一步均为
2 2 2
吸热过程,D项正确。
6.【点石答案】B
1.【素材来源】人教版高中化学教材选择性必修1第三章第一节电离平衡相关内容。
1.【点石立意】本题以弱电解质电离平衡常数的理解和应用为载体进行考查,考查学生对弱电解质电离过
程的掌握、酸性强弱判断。体现宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知等学科
素养。
1.【点石解析】H CO 的K 大于HCN 的K ,故H CO 的酸性强于 HCN,A项正确;少量草酸与足量
2 3 a1 a 2 3
Na CO 溶液反应的离子方程式为H C O +2CO2===C O2+2HCO,B项错误;向HCN溶液中加入NaOH
2 3 2 2 4 3 2 4 3
c(CN) K
固体,c(H+)减小而K 不变,故 = a 的值增大,C项正确;多元弱酸溶液的酸性主要是由弱酸
a
c(HCN) c(H)
的第一步电离决定的,D项正确。
7.【点石答案】A
1.【素材来源】人教版高中化学教材选择性必修1第一章第二节反应热的计算相关内容。
1.【点石立意】本题以NaHCO 物质变化过程中的能量变化为情境进行考查,考查学生对盖斯定律的理解
3
和应用。体现变化观念与平衡思想等学科素养。
1.【点石解析】根据盖斯定律可知∆H =-∆H +∆H +∆H =-(+37.6kJ·mol-1)+(+92.3kJ·mol-1)+(-16.4kJ·mol-1)=
4 1 3 2
+38.3kJ·mol-1,A项正确;∆H =+92.3kJ·mol-1,则2NaHCO (s)===Na CO (s)+CO (g)+H O(l)的正反应活化
3 3 2 3 2 2
能比逆反应活化能大92.3kJ·mol-1,B项错误;H O(l)===H O(g) ∆H>0,∆H =∆H +∆H,故∆H >∆H ,
2 2 5 3 5 3
C项错误;NaHCO 固体溶解在水中不属于化学反应,D项错误。
3
8.【点石答案】C
1.【素材来源】人教版高中化学教材选择性必修1第二章第二节化学平衡、第三章第一节电离平衡相关内
容。
1.【点石立意】本题以氯水中的平衡、NO 与N O 转化平衡、可逆反应的判断、温度对弱电解质电离平
2 2 4
衡影响为情境进行考查,考查学生对平衡移动的理解和应用。体现变化观念与平衡思想、证据推理与模型
认知等学科素养。
1.【点石解析】光照时,HClO分解,c(HClO)减小,Cl 2 +H 2 O HCl+HClO平衡正向移动,c(Cl 2 )减小,
溶液黄绿色褪去,A项正确;压缩封装有NO 和N O 混合气体的注射器,开始c(NO )增大,混合气体的
2 2 4 2
颜色先变深,然后2NO 2 (g) N 2 O 4 (g)平衡正向移动,混合气体颜色又逐渐变浅,B项正确;Fe3+过量,
不能判断Fe3+与I-的反应为可逆反应,C项错误;磷酸电离吸热,温度升高,促进电离平衡正向移动,磷
酸溶液酸性增强,D项正确。
9.【点石答案】D
1.【素材来源】人教版高中化学教材选择性必修1第二章第一节化学反应速率相关内容。
1.【点石立意】本题以在一定条件下,1-苯基丙炔与氯化氢反应历程分析为情境,考查学生对活化能的理
解、化学反应的调控。体现了证据推理与模型认知等学科素养。
1.【点石解析】反应前期,产物A的生成速率更快,则生成产物A的活化能更小,故A为 、
B为 ,A项正确,C项正确;与 相比较, 能量更低,更稳定,B项
点石联考 高二10月化学试题参考答案 第 4 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
正确;反应前期,主要生成 ,随着反应时间的延长,产物会逐渐由 转变为
,欲获得较多的产物 ,反应时间控制为20min左右为宜,D项错误。
10.【点石答案】A
11.【素材来源】人教版高中化学教材选择性必修1第二章第一节化学反应速率,第二章化学平衡相关内
容。
11.【点石立意】本题以碳酸钙分解为情境,考查学生对平衡状态判断、反应速率计算、平衡移动判断、
平衡常数的理解。体现了变化观念和平衡思想、证据推理与模型认知等学科素养。
11.【点石解析】反应过程中,固体转化为气体,气体密度不变时,反应到达平衡状态,A项正确;K=c
平
(CO ),温度不变,K值不变,平衡时CO 物质的量浓度不变,c =c ,B、D项错误;t min内,容器乙中
衡 2 2 1 2 2
c
的平均反应速率v(CO )= 2 mol·L-1·min-1,C项错误。
2
t
2
11.【点石答案】C
11.【素材来源】人教版高中化学教材选择性必修1第一章第一节反应热相关内容。
11.【点石立意】本题以中和反应反应热测定实验为情境,考查学生对中和反应反应热测量实验相关要点
的理解和掌握。体现了科学探究与创新意识等学科素养。
11.【点石解析】用铜质搅拌器代替玻璃搅拌器,会有热量散失,该反应为放热反应,∆H<0,故测得∆H
会偏大,A项错误;实验过程中,盐酸和NaOH溶液要快速、一次性混合,以减少热量散失,B项错误;
生成0.025molH O(l)放出100g×3.2℃×4.18J·g-1·℃-1×10-3kJ·J-1=1.3376kJ热量,则生成1molH O(l)放
2 2
1.3376
出热量为 kJ≈53.5kJ,C项正确;分别测量NaOH溶液和盐酸的初始温度,二者的平均值
5010 30.5
为反应前的初始温度,D项错误。
12.【点石答案】B
11.【素材来源】人教版高中化学教材选择性必修1第二章第一节化学反应速率相关内容。
11.【点石立意】本题以HCOOH脱氢的科技情境为载体,考查学生对活化能的理解、化学反应的调控。体
现了证据推理与模型认知等学科素养。
11.【点石解析】在催化剂a的作用下,反应的活化能更小,反应速率更快,A项错误;由图可知,两种
催化剂作用下,HCOO*+H*===COO*+2H*的活化能均最大,故为反应的决速步,B项正确;催化剂降低了
反应的活化能,但不能改变反应的焓变,C项错误;催化剂不能增大HCOOH的平衡转化率,D项错误。
13.【点石答案】C
11.【素材来源】人教版高中化学教材选择性必修1第一章化学反应的热效应,第二章第一节化学反应速
率相关内容。
11.【点石立意】本题以O 分解的不同路径为载体,考查学生对活化能的理解、盖斯定律的应用、焓变的
3
计算。体现了宏观辨识与微观探析、证据推理与模型认知等学科素养。
11.【点石解析】Cl(g)的相对能量为akJ·mol-1=(d-c)kJ·mol-1,A项正确;O (g)+ClO(g)===O (g)+Cl(g)为吸
2 3
热过程,∆H=+(d-b)kJ·mol-1,B项正确;O 的相对能量为0,Cl(g)的相对能量为(a-0)kJ·mol-1,故2molCl(g)
2
形成1molCl (g)分子时需要释放的能量为2akJ,C项错误;由图可知路径Ⅰ正反应的活化能为(e-c)kJ·mol-1,
2
D项正确。
14.【点石答案】C
11.【素材来源】人教版高中化学教材选择性必修1第二章第二节化学化学平衡相关内容。
点石联考 高二10月化学试题参考答案 第 5 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
11.【点石立意】本题以平衡图像分析为载体,考查学生对化学平衡移动的应用、图像分析能量。体现了
证据推理与模型认知等核心素养。
11.【点石解析】T 温度下的反应速率更快,故T >T ,A项正确;T 温度下,反应开始至到达平衡状态
1 1 2 2
时,A和B的物质的量变化之比为(9-3)∶3=2∶1,故x=1,B项正确;T 温度下到达平衡,消耗4molA(g),
1
生成2molB(g)和4molC(g),列出三段式:
2A(g) B(g) + 2C(g)
初始/mol 9 0 0
改变/mol 4 2 4
平衡/mol 5 2 4
4 2
( )2
2 2 16
平衡常数K= = ,C项错误;T 温度下,反应达到平衡状态时,容器内有3molA(g)、3molB(g)
2
5 25
( )2
2
和6molC(g),混合气体中C的体积分数为50%,D项正确。
15.【点石答案】B
11.【素材来源】人教版高中化学教材选择性必修1第三章第一节电离平衡相关内容。
11.【点石立意】本题以H S电离平衡为载体,考查学生对电离平衡移动、电离平衡常数的理解和掌握。体
2
现了宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知等学科素养。
11.【点石解析】电离平衡时,溶液中c(H+)≈c(HS-),c(H S)≈0.1mol·L-1,根据K =9×10-8可求出c(H+)
2 a1
3104.5
≈c(HS-)≈3×10-4.5mol·L-1,H S的电离程度α≈ ×100%,A项错误;升高温度,溶液电离程度增大,
2
0.1
c(S2) c(S2)c(HS)c(H)c(H) K K 91023
K 和K 增大,B项正确; = = a1 a2 = ,C项错误;溶
a1 a2
c(H S) c(H S)c(HS)c(H)c(H) c2(H) c2(H)
2 2
液中存在关系:c(H S)>c(HS-)>c(S2-),D项错误。
2
二、非选择题
16.(14分)
【点石答案】
1 1
(1)N (g)+O (g)===2NO(g) ∆H=+180.5kJ·mol-1或 N (g)+ O (g)===NO(g) ∆H=+90.25kJ·mol-(1 2分)
2 2 2 2
2 2
(2)①SnO (2分) ②不是(2分) ③B(2分)
2
(3)①>(2分) <(2分)
(2)②BD(2分)
【点石立意】本题以生活中氮氧化物处理为情境,考查学生对热化学方程式的书写、催化效率判断、化学
反应速率调控、化学平衡等。体现了变化观念与平衡思想、证据推理与模型认知、科学精神与社会责任等
学科素养。
【点石解析】
(1)N 与O 反应生成1molNO需要吸收90.25kJ能量,则生成2molNO需要吸收180.5kJ能量,热化
2 2
1 1
学方程式为N (g)+O (g)===2NO(g) ∆H=+180.5kJ·mol-1或 N (g)+ O (g)===NO(g) ∆H=
2 2 2 2
2 2
+90.25kJ·mol-1。
(2)
①由图可知,tmin内,在SnO 催化作用下NO的转化率最低,反应速率最慢,反应活化能最大。
2
②2CO(g)+2NO(g) 2CO 2 (g)+N 2 (g)为放热反应,若a点处于平衡状态,则温度升高,NO的转化率会
点石联考 高二10月化学试题参考答案 第 6 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
下降,与图像不符,故a点不是处于平衡状态。
③反应放热,升高温度,平衡逆向移动,NO平衡转化率下降,A项不符合题意;缩小容器的体积,平衡
正向移动且反应速率加快,B项符合题意;增加NO的浓度,NO的平衡转化率下降,C项不符合题意;
及时分离出CO 不能加快反应速率,D项不符合题意。
2
(3)
①压强增大,反应4NO(g)+4NH 3 (g)+O 2 (g) 4N 2 (g)+6H 2 O(g)逆向移动,NO平衡转化率降低,故p 1 >
p ;根据图像信息可知,温度升高,NO平衡转化率降低,故该反应为放热反应,∆H<0。
2
②NO和NH 的投料比等于化学计量数之比,无论反应是否到达平衡状态,二者的转化率始终相等,A项
3
n(NH ) n(NH )
不符合题意;反应未到达平衡状态时, 3 的值会发生改变,当 3 的值不再改变时,可判断反
n(N ) n(N )
2 2
应到达平衡状态,B项符合题意;消耗nmolNO的同时生成nmolN ,无法用于比较正、逆反应速率的大
2
m
小,C项不符合题意;混合气体的平均摩尔质量M = ,反应未到达平衡状态,m不变,n会改变,故M
n
不再改变时,能判断反应到达平衡状态,D项符合题意。
17.(13分)
【点石答案】
高温
(1)SiO +2C Si+2CO↑(2分) 将焦炭粉碎后与石英砂混合均匀(2分,答案合理即可)
2
(2)吸收(1分) 19.5(1分) 不变(2分)
(3)L (1分) abc或a>b>c(2分)
1
(4)H 、HCl(2分)
2
【点石立意】本题以改良西门子法制粗硅为情境,考查学生对热化学方程式的书写、化学反应速率调控、
化学平衡、活化分子的理解等。体现了宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、
科学精神与社会责任等学科素养。
【点石解析】
高温
(1)工业制粗硅会生成Si和CO,反应的化学方程式为SiO +2C Si+2CO↑;将焦炭粉碎后与石英
2
砂混合均匀或反应过程中搅拌等均能加快反应速率。
(2)∆H>0,消耗1molSi(s)吸收39kJ能量,则消耗0.5mol(14g)Si(s),会吸收19.5kJ能量;增大反应
物浓度,单位体积内活化分子数增大,但活化分子百分数不变。
n(H ) n(H )
(3)其他条件相同、n(SiHCl )一定时,投料比 2 的值越大,SiHCl 的平衡转化率越大,故 2
3 3
n(SiHCl ) n(SiHCl )
3 3
的值最大的是L;温度相同时,a点SiHCl 的平衡转化率最大,起始n(SiHCl )相同,则a点生成物浓度最大,
1 3 3
逆反应速率最快,平衡时正反应速率等于逆反应速率,则a点正反应速率也最快,可推知平衡时正反应速率由大
到小的顺序为abc。
(4)“合成SiHCl ”时生成了H ,“还原”时生成了HCl,二者均可循环利用。
3 2
【点石点评】该题以工业制备高纯硅为背景,综合考查化学反应原理与工业流程分析,既注重基础知识的
巩固,又突出对学生综合分析能力、图像解读能力和工业思维的考查,符合新课标“应用性”和“综合性”
的要求,是一道优质的高考模拟题。
点石联考 高二10月化学试题参考答案 第 7 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
18.(14分)
【点石答案】
Ⅰ.(1)S O2+2H+===SO ↑+S↓+H O或S O2+2H+===H SO +S↓(2分) 生成的SO 易溶于水,导
2 3 2 2 2 3 2 3 2
致容器内压强变化不明显(2分,答到SO 易溶于水即给满分)
2
Ⅱ.(2)13(2分) H+浓度(或反应物浓度、H SO 浓度)(2分)
2 4
1
Ⅲ.(3) (2分)
1750
(4)随着c(KMnO )的增大,反应速率的增大不能抵消n(KMnO )增大带来的影响,总反应时长增加(2
4 4
分,合理表述即可)
(5)Mn2+(2分)
【点石立意】本题以探究Na S O 与稀硫酸反应速率、草酸与酸性KMnO 反应速率为情境,考查学生对
2 2 3 4
控制变量思想、化学反应速率计算、速率图像分析、催化剂本质理解等。体现了宏观辨识与微观探析、变
化观念与平衡思想、证据推理与模型认知、科学探究与创新意识等学科素养。
【点石解析】
Ⅰ.(1)Na S O 与H SO 发生反应生成Na SO 、SO 、S和H O,离子方程式为S O2+2H+===
2 2 3 2 4 2 4 2 2 2 3
SO ↑+S↓+H O或S O2+2H+===H SO +S↓;生成的SO 易溶于水,导致容器内压强变化不明显,故注
2 2 2 3 2 3 2
射器2活塞外推不明显。
Ⅱ.(2)根据控制变量的思想可知,实验时,三组实验溶液总体积需相同,故a=13;该组实验是探究反应
物浓度对反应速率的影响。
0.00504 1
Ⅲ.(3)v(KMnO )= mol·L-1·min-1= mol·L-1·min-1。
4
(241)5 1750
(4)随着c(KMnO )的增大,反应速率的增大不能抵消n(KMnO )增大带来的影响,总反应时长增加。
4 4
(5)催化剂要参与反应且最后要能复原,根据反应机理图像,可知催化剂为Mn2+。
19.(14分)
【点石答案】
(1)高温(2分) +49(2分)
(2)AD(2分) 增大水醇比,有利于反应C(s)+H 2 O(g) CO(g)+H 2 (g)正向进行,消除积碳(2分)
16
(3)1(2分) (2分)
49V2
(4)4×10-4(2分)
【点石立意】本题生产H 为情境,考查盖斯定律的应用、反应进行方向判断和焓变判断、多重平衡体系
2
中的计算、化学反应速率计算、常见反应的热效应。体现了变化观念与平衡思想、证据推理与模型认知、
科学精神与社会责任等学科素养。
【点石解析】
(1)反应④为熵增焓增的反应,在高温下能自发进行;
1
(1)根据盖斯定律可知∆H = (∆H +∆H -2∆H )=+49kJ·mol-1。
2 1 3 4
2
(2)C(s)+H 2 O(g) CO(g)+H 2 (g)为吸热反应,氯化铵晶体与Ba(OH) 2 ·8H 2 O的反应为吸热反应,甲烷
燃烧为放热反应,Na与H O的反应放热,H O分解生成H 和O 为吸热反应,AD项符合题意;乙醇制氢
2 2 2 2
点石联考 高二10月化学试题参考答案 第 8 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
气时易生成积碳,增大水醇比,有利于C(s)+H 2 O(g) CO(g)+H 2 (g)正向进行,有效消除积碳。
(3)700K 下到达平衡时,n(CO )=n(CH ),n(H O)=7 mol,n(H )=2 mol,根据 H 原子守恒可知平衡时
2 4 2 2
16827222
n(CO )=n(CH )= mol=1mol,根据C原子守恒可知平衡时n(CO)=(1×2-1-1)mol=
2 4
4
2 1
( )4
c4(H )c(CO ) V V 16
0mol;该温度下,反应④的浓度平衡常数K= 2 2 = = 。
c(CH )c2(H O) 1 7 49V2
4 2 ( )2
V V
4
(4)当水醇比为4时,H O的平均反应速率为(0.005cm3·s-1× ×10%)=4×10-4cm3·s-1。
2
41
【点石点评】本题以“乙醇制氢气”为背景,融合了热化学、化学平衡、反应速率等核心知识点,以真实
情境为载体,贴近实际,全面考查学生对热化学、平衡原理、速率计算的掌握程度,同时注重信息提取与
综合应用能力。题目难度梯度合理,区分度高,既落实了基础知识,又体现了核心素养(如“变化观念与
平衡思想”“证据推理与模型认知”)的考查要求,对高中化学教学具有良好的导向作用,是一道较为优
质的化学联考题。
点石联考 高二10月化学试题参考答案 第 9 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}点石联考10月高二联考 化学
【注】本答案设计形式、排版风格为点石联考独家原创。
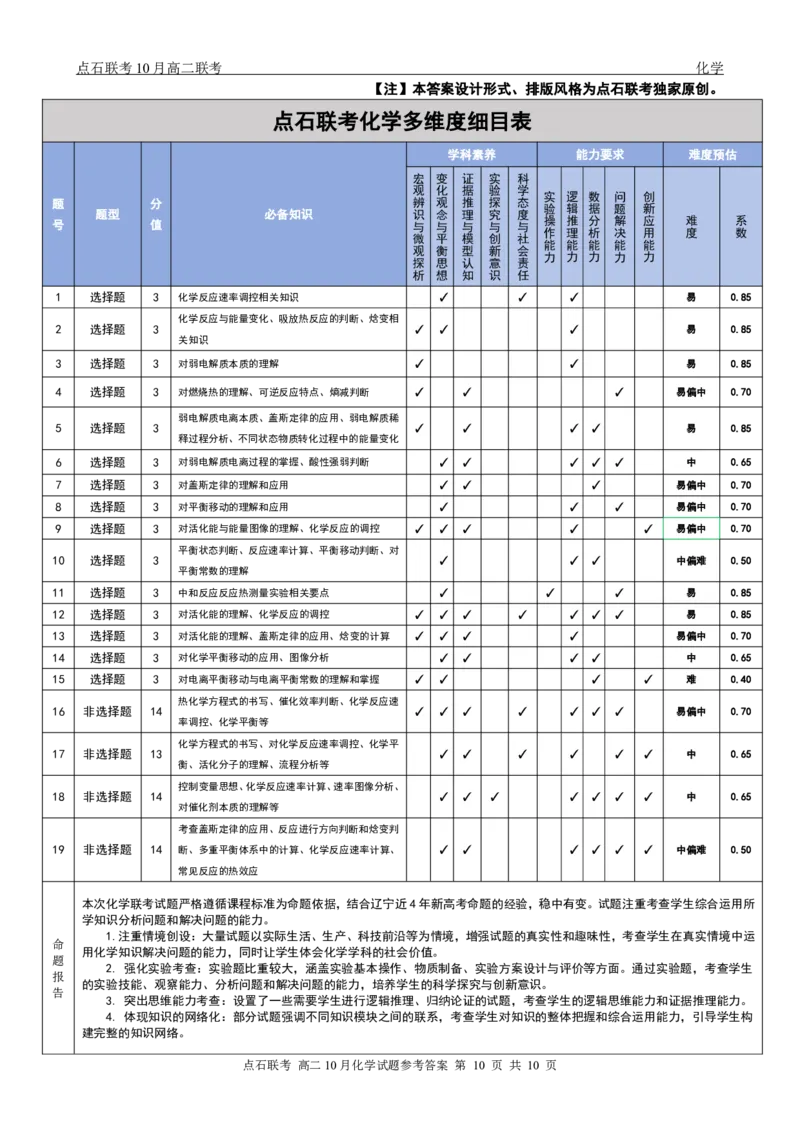
点石联考化学多维度细目表
学科素养 能力要求 难度预估
宏 变 证 实 科
观 化 据 验 学
实 逻 数 问 创
题 分 辨 观 推 探 态 验 辑 据 题 新
题型 必备知识 识 念 理 究 度
操 推 分 解 应 难 系
号 值 与 与 与 与 与
作 理 析 决 用 度 数
微 平 模 创 社
能 能 能 能 能
观 衡 型 新 会
力 力 力 力 力
探 思 认 意 责
析 想 知 识 任
1 选择题 3 化学反应速率调控相关知识 ✓ ✓ ✓ 易 0.85
化学反应与能量变化、吸放热反应的判断、焓变相
2 选择题 3 ✓ ✓ ✓ 易 0.85
关知识
3 选择题 3 对弱电解质本质的理解 ✓ ✓ 易 0.85
4 选择题 3 对燃烧热的理解、可逆反应特点、熵减判断 ✓ ✓ ✓ 易偏中 0.70
弱电解质电离本质、盖斯定律的应用、弱电解质稀
5 选择题 3 ✓ ✓ ✓ ✓ 易 0.85
释过程分析、不同状态物质转化过程中的能量变化
6 选择题 3 对弱电解质电离过程的掌握、酸性强弱判断 ✓ ✓ ✓ ✓ ✓ 中 0.65
7 选择题 3 对盖斯定律的理解和应用 ✓ ✓ ✓ 易偏中 0.70
8 选择题 3 对平衡移动的理解和应用 ✓ ✓ ✓ 易偏中 0.70
9 选择题 3 对活化能与能量图像的理解、化学反应的调控 ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
平衡状态判断、反应速率计算、平衡移动判断、对
10 选择题 3 ✓ ✓ ✓ 中偏难 0.50
平衡常数的理解
11 选择题 3 中和反应反应热测量实验相关要点 ✓ ✓ ✓ 易 0.85
12 选择题 3 对活化能的理解、化学反应的调控 ✓ ✓ ✓ ✓ ✓ ✓ ✓ 易 0.85
13 选择题 3 对活化能的理解、盖斯定律的应用、焓变的计算 ✓ ✓ ✓ ✓ 易偏中 0.70
14 选择题 3 对化学平衡移动的应用、图像分析 ✓ ✓ ✓ ✓ 中 0.65
15 选择题 3 对电离平衡移动与电离平衡常数的理解和掌握 ✓ ✓ ✓ ✓ 难 0.40
热化学方程式的书写、催化效率判断、化学反应速
16 非选择题 14 ✓ ✓ ✓ ✓ ✓ ✓ ✓ 易偏中 0.70
率调控、化学平衡等
化学方程式的书写、对化学反应速率调控、化学平
17 非选择题 13 ✓ ✓ ✓ ✓ ✓ ✓ 中 0.65
衡、活化分子的理解、流程分析等
控制变量思想、化学反应速率计算、速率图像分析、
18 非选择题 14 ✓ ✓ ✓ ✓ ✓ ✓ ✓ 中 0.65
对催化剂本质的理解等
考查盖斯定律的应用、反应进行方向判断和焓变判
19 非选择题 14 断、多重平衡体系中的计算、化学反应速率计算、 ✓ ✓ ✓ ✓ ✓ ✓ 中偏难 0.50
常见反应的热效应
本次化学联考试题严格遵循课程标准为命题依据,结合辽宁近4年新高考命题的经验,稳中有变。试题注重考查学生综合运用所
学知识分析问题和解决问题的能力。
1.注重情境创设:大量试题以实际生活、生产、科技前沿等为情境,增强试题的真实性和趣味性,考查学生在真实情境中运
命
用化学知识解决问题的能力,同时让学生体会化学学科的社会价值。
题
2. 强化实验考查:实验题比重较大,涵盖实验基本操作、物质制备、实验方案设计与评价等方面。通过实验题,考查学生
报
的实验技能、观察能力、分析问题和解决问题的能力,培养学生的科学探究与创新意识。
告
3. 突出思维能力考查:设置了一些需要学生进行逻辑推理、归纳论证的试题,考查学生的逻辑思维能力和证据推理能力。
4. 体现知识的网络化:部分试题强调不同知识模块之间的联系,考查学生对知识的整体把握和综合运用能力,引导学生构
建完整的知识网络。
点石联考 高二10月化学试题参考答案 第 10 页 共 10 页
{#{QQABYYqw4gqwgJSACR5qEQHWCUgQkJGjLYoMwUARKAQCiBFIFIA=}#}