文档内容
绝密★启用前
辽西重点高中 2025-2026 学年度上学期高二 10 月联考
化学试题
考生注意
1.本试卷本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分100分,考
试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔
把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签
字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试
题卷、草稿纸上作答无效。
3.可能用到的相对原子质量:H 1 C 12 O 16 N 14 CL 35 B 11
第Ⅰ卷(选择题,共45分)
一、选择题(共45分,每题只有一个正确答案)
1.设 为阿伏加德罗常数的值,下列说法正确的是
A.常温下, 中,所含的电子总数为
B. 的 溶液中,所含的 数目为
C.一定条件下, 与足量的 反应,可生成
D.标准状况下, 中,所含的原子总数为
2.由稻壳制备纳米 的流程如图所示。下列说法正确的是
稻壳 纳米 纳米 纳米
A. 属于碱性氧化物 B.稀盐酸不属于电解质
C.光纤通信材料的主要成分为高纯 D.工业上,常采用电解熔融的 来获得单质
3.稀盐酸与碳酸氢钠的反应为吸热反应,下列相关说法错误的是
A.该反应的能量变化如图所示
B.碳酸氢钠固体溶于水的过程为吸热过程
C.理论上,该反应可设计成原电池
D. 与 反应生成 的能量变化趋势与该反应能量变化趋势相一致
4.对于反应 ,在不同条件下的化学反应速率如下,
其中反应速率最快的是
A. B.
C. D.
5.下列化学用语说法正确的是
A.丙烷分子球棍模型:
B.次氯酸的结构式:
C.氮气的电子式:
D.用电子式表示 的形成过程为:
6.石油中含有的多种烷烃是重要的有机化工原料,下列有关说法错误的是
A.重油裂解得到的丙烯(CH=CH—CH)中所有碳原子都处于同一平面
2 3
B.沸点:正庚烷>正己烷>正丁烷
C.1 mol烷烃C H 中含共价键(3n+1) mol
n 2n+2
D.含有4个甲基的己烷的同分异构体有3种7.下列类比正确的是
选
所学知识 类比
项
A 乙烯能使酸性高锰酸钾溶液褪色 丙烯能使酸性高锰酸钾溶液褪色
向硝酸钡溶液中通入 ,溶液中产生 向氯化钡溶液中通入 ,溶液中产生白
B
白色沉淀 色沉淀
碳在氧气不足时燃烧生成 ,在足量 硫在氧气不足时燃烧生成 ,在足量氧
C
氧气中燃烧生成 气中燃烧生成
向乙醇中加入灼热的氧化铜,氧化铜变 向 中加入灼热的氧化铜,氧
D
红色
化铜变红色
A.A B.B C.C D.D
8.下列相关方程式书写错误的是
A. 通入足量的水中:
B.二氧化硅与足量碳在高温下反应:
C.淀粉水解生成葡萄糖:
D.向稀碳酸氢铵溶液中滴加足量氢氧化钠溶液:
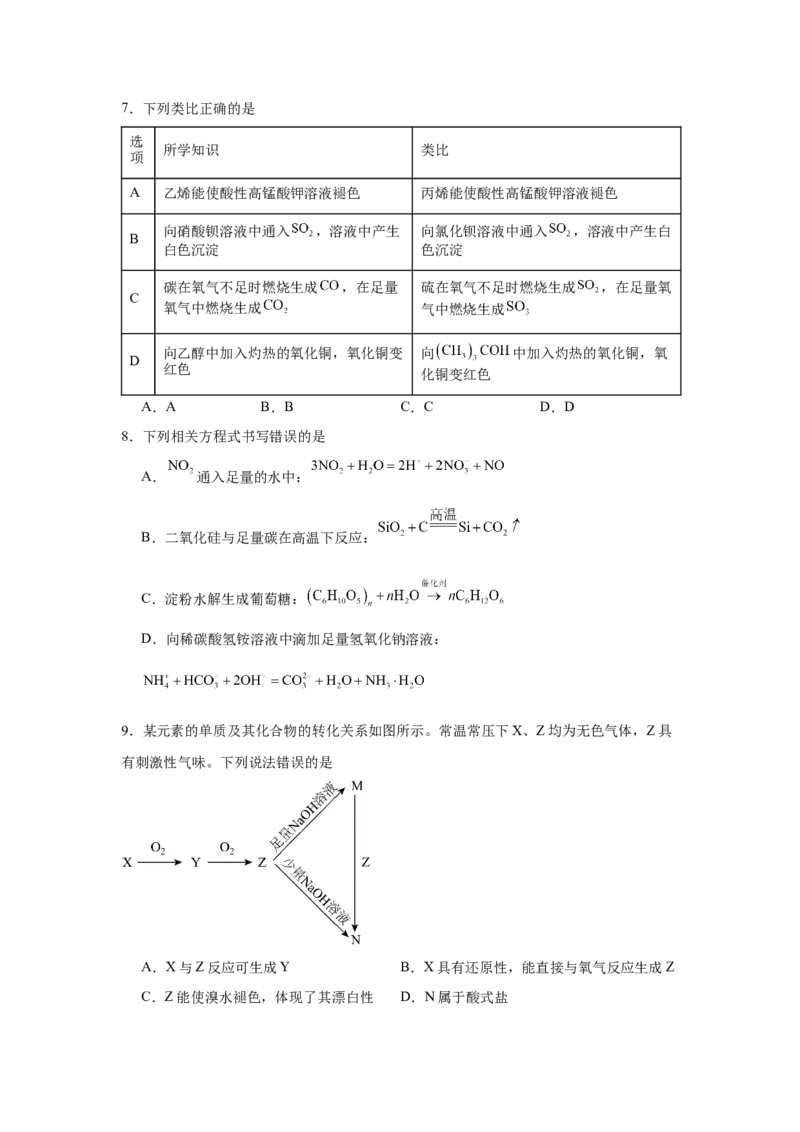
9.某元素的单质及其化合物的转化关系如图所示。常温常压下X、Z均为无色气体,Z具
有刺激性气味。下列说法错误的是
A.X与Z反应可生成Y B.X具有还原性,能直接与氧气反应生成Z
C.Z能使溴水褪色,体现了其漂白性 D.N属于酸式盐10.化学与生活、环境密切相关,下列说法不正确的是
A.华为Mate 60手机使用了麒麟芯片,其主要成分是硅单质
B.提倡采用新技术不断开采煤、石油和天然气,以满足经济发展的需要
C.硅胶可作食品包装中的干燥剂
D.高铁列车使用的大丝束碳纤维被称为“新材料之王”,属于新型无机非金属材料
11.下列说法正确的是
A. ,则碳的燃烧热
B.若改变条件,反应物的转化率增大,则平衡常数一定增大
C. ,则不论在何种条件下都不可能自发进行
D. 与NaOH中和反应的 和HCl与NaOH中和反应的 相比,
12.下列关于化学反应与能量的说法正确的是
A.已知正丁烷的燃烧热为2878 ,则表示正丁烷燃烧热的热化学方程式为
B.已知在一定条件下,2 mol 与1 mol 充分反应后,释放出98 kJ的热量,则
其热化学方程式为
C.已知稀盐酸与稀NaOH溶液反应生成1 mol水时,放出的热量为57.3 kJ,则表示稀
硫酸与稀NaOH溶液反应的热化学方程式为
D.已知C(石墨,s)=C(金刚石,s) ,则金刚石比石墨稳定
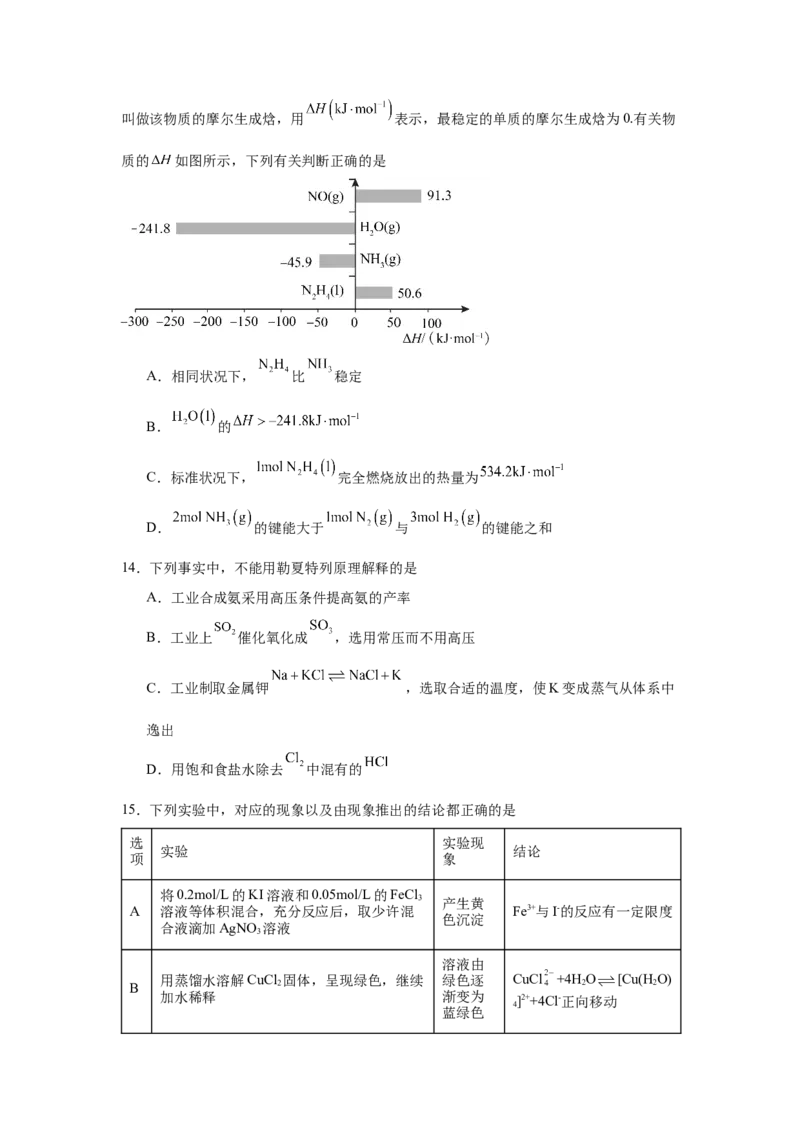
13.已知:在标准压强( )、 下,由最稳定的单质合成 某物质的反应焓变叫做该物质的摩尔生成焓,用 表示,最稳定的单质的摩尔生成焓为0.有关物
质的 如图所示,下列有关判断正确的是
A.相同状况下, 比 稳定
B. 的
C.标准状况下, 完全燃烧放出的热量为
D. 的键能大于 与 的键能之和
14.下列事实中,不能用勒夏特列原理解释的是
A.工业合成氨采用高压条件提高氨的产率
B.工业上 催化氧化成 ,选用常压而不用高压
C.工业制取金属钾 ,选取合适的温度,使K变成蒸气从体系中
逸出
D.用饱和食盐水除去 中混有的
15.下列实验中,对应的现象以及由现象推出的结论都正确的是
选 实验现
实验 结论
项 象
将0.2mol/L的KI溶液和0.05mol/L的FeCl
3 产生黄
A 溶液等体积混合,充分反应后,取少许混 Fe3+与I-的反应有一定限度
色沉淀
合液滴加AgNO 溶液
3
溶液由
用蒸馏水溶解CuCl 固体,呈现绿色,继续 绿色逐 CuCl +4H O [Cu(H O)
B 2 2 2
加水稀释 渐变为 ]2++4Cl-正向移动
4
蓝绿色热水中
将装有NO 的密闭烧瓶分别浸泡在热水和 颜色深 探究温度对反应速率的影
C 2
冰水中2NO (g) NO(g) ΔH<0 冰水中 响
2 2 4
颜色浅
向稀硫酸中滴加等浓度等体积的Ba(OH) 溶 电导率
D 2 说明BaSO 为弱电解质
液,同时测定溶液电导率变化 下降 4
A.A B.B C.C D.D
第Ⅱ卷(选择题,共55分)
二、非选择题(本题共4小题,共55分,考生根据要求做答。)
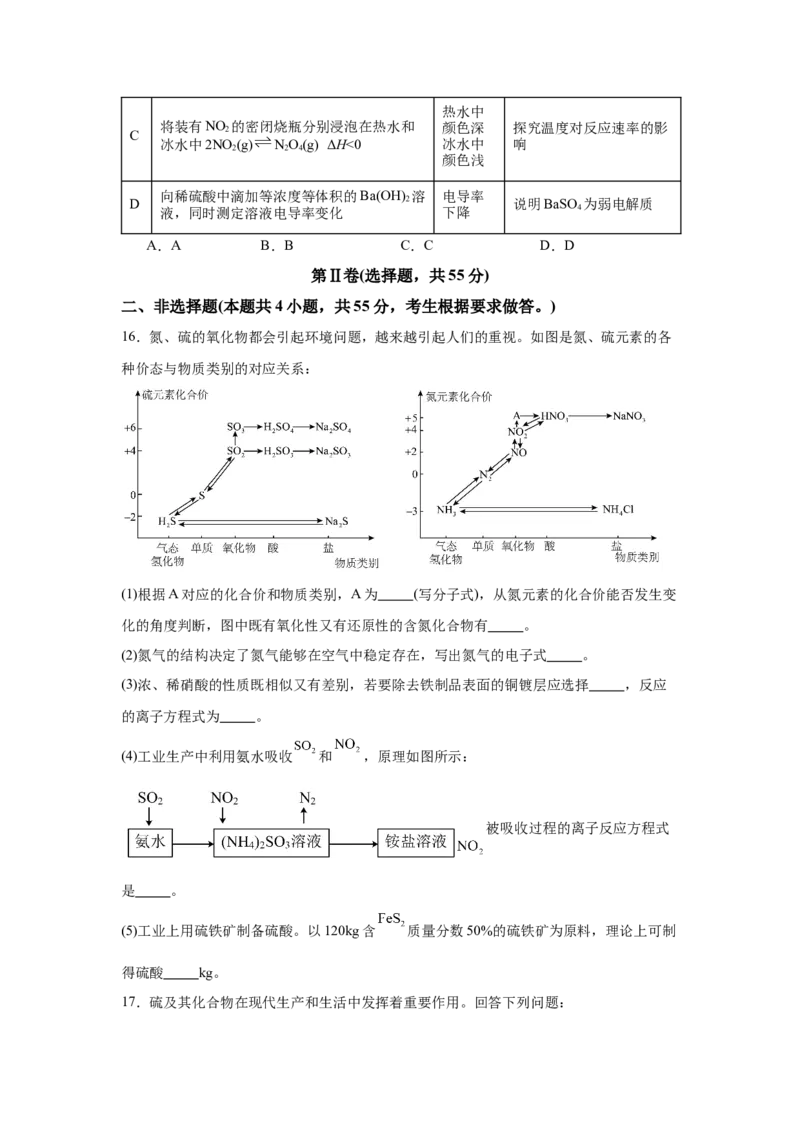
16.氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各
种价态与物质类别的对应关系:
(1)根据A对应的化合价和物质类别,A为 (写分子式),从氮元素的化合价能否发生变
化的角度判断,图中既有氧化性又有还原性的含氮化合物有 。
(2)氮气的结构决定了氮气能够在空气中稳定存在,写出氮气的电子式 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择 ,反应
的离子方程式为 。
(4)工业生产中利用氨水吸收 和 ,原理如图所示:
被吸收过程的离子反应方程式
是 。
(5)工业上用硫铁矿制备硫酸。以120kg含 质量分数50%的硫铁矿为原料,理论上可制
得硫酸 kg。
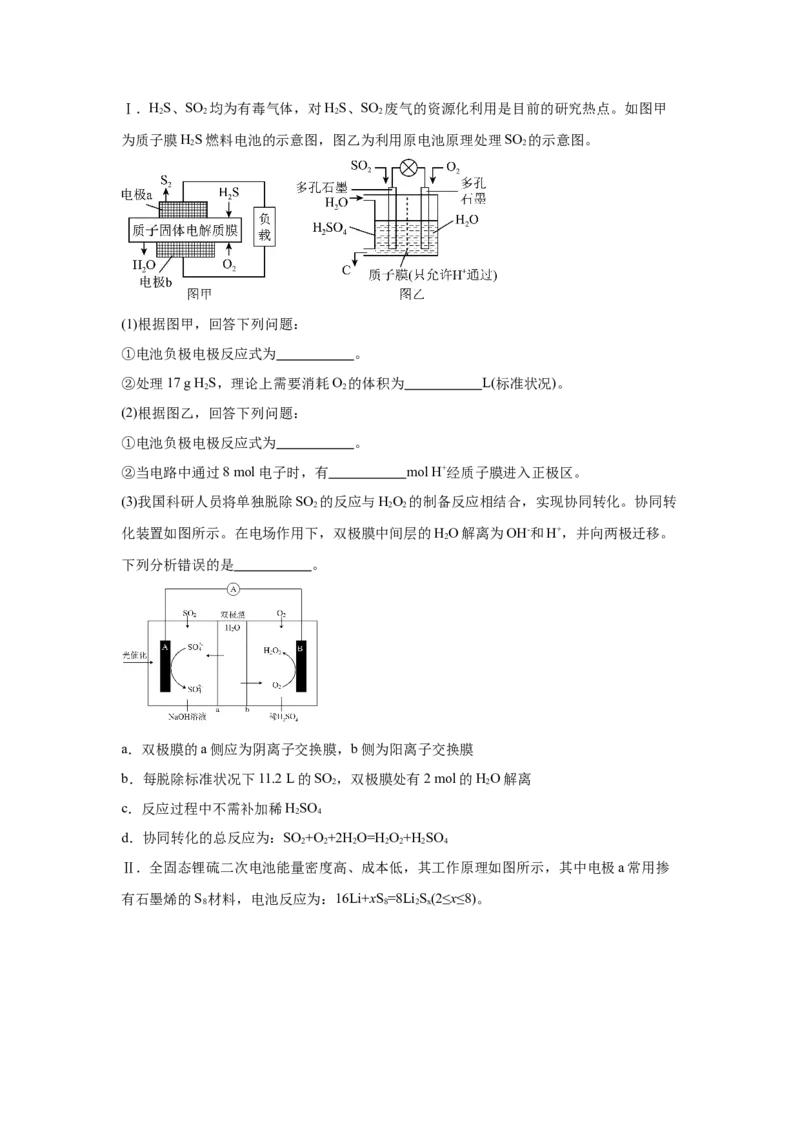
17.硫及其化合物在现代生产和生活中发挥着重要作用。回答下列问题:Ⅰ.HS、SO 均为有毒气体,对HS、SO 废气的资源化利用是目前的研究热点。如图甲
2 2 2 2
为质子膜HS燃料电池的示意图,图乙为利用原电池原理处理SO 的示意图。
2 2
(1)根据图甲,回答下列问题:
①电池负极电极反应式为 。
②处理17 g HS,理论上需要消耗O 的体积为 L(标准状况)。
2 2
(2)根据图乙,回答下列问题:
①电池负极电极反应式为 。
②当电路中通过8 mol电子时,有 mol H+经质子膜进入正极区。
(3)我国科研人员将单独脱除SO 的反应与HO 的制备反应相结合,实现协同转化。协同转
2 2 2
化装置如图所示。在电场作用下,双极膜中间层的HO解离为OH-和H+,并向两极迁移。
2
下列分析错误的是 。
a.双极膜的a侧应为阴离子交换膜,b侧为阳离子交换膜
b.每脱除标准状况下11.2 L的SO ,双极膜处有2 mol的HO解离
2 2
c.反应过程中不需补加稀HSO
2 4
d.协同转化的总反应为:SO +O +2H O=HO+H SO
2 2 2 2 2 2 4
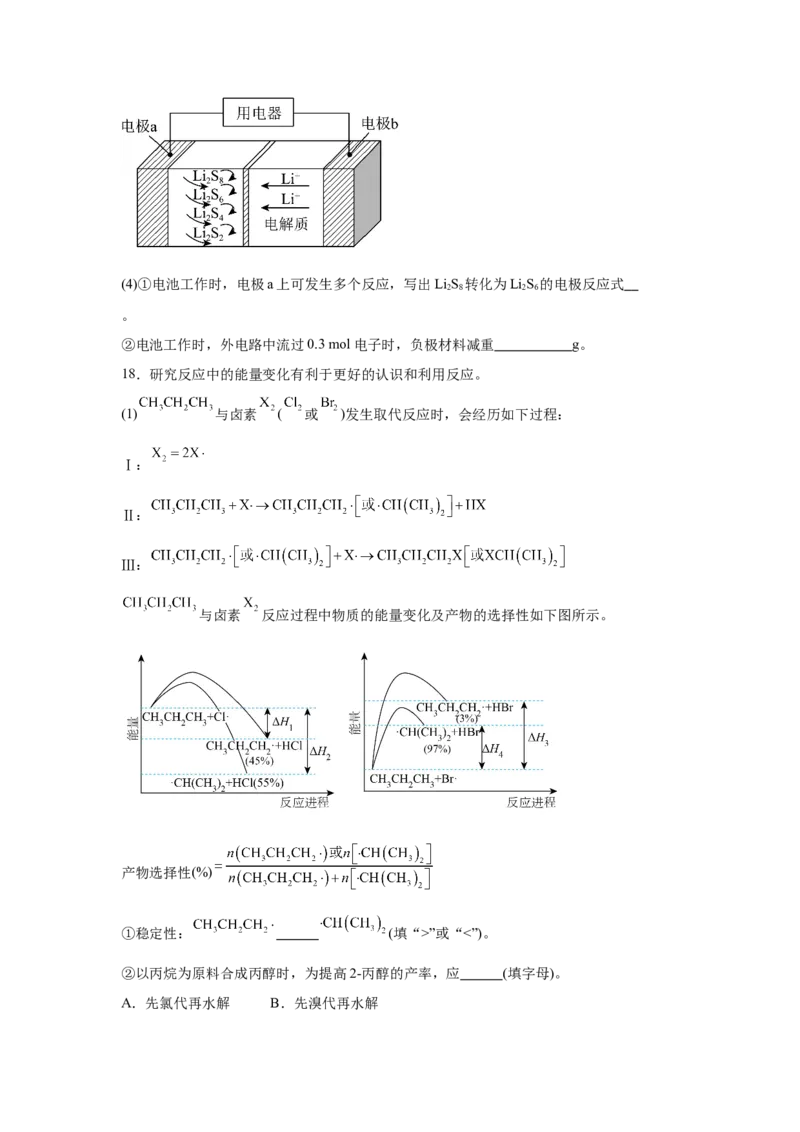
Ⅱ.全固态锂硫二次电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺
有石墨烯的S 材料,电池反应为:16Li+xS=8Li S(2≤x≤8)。
8 8 2 x(4)①电池工作时,电极a上可发生多个反应,写出LiS 转化为LiS 的电极反应式
2 8 2 6
。
②电池工作时,外电路中流过0.3 mol电子时,负极材料减重 g。
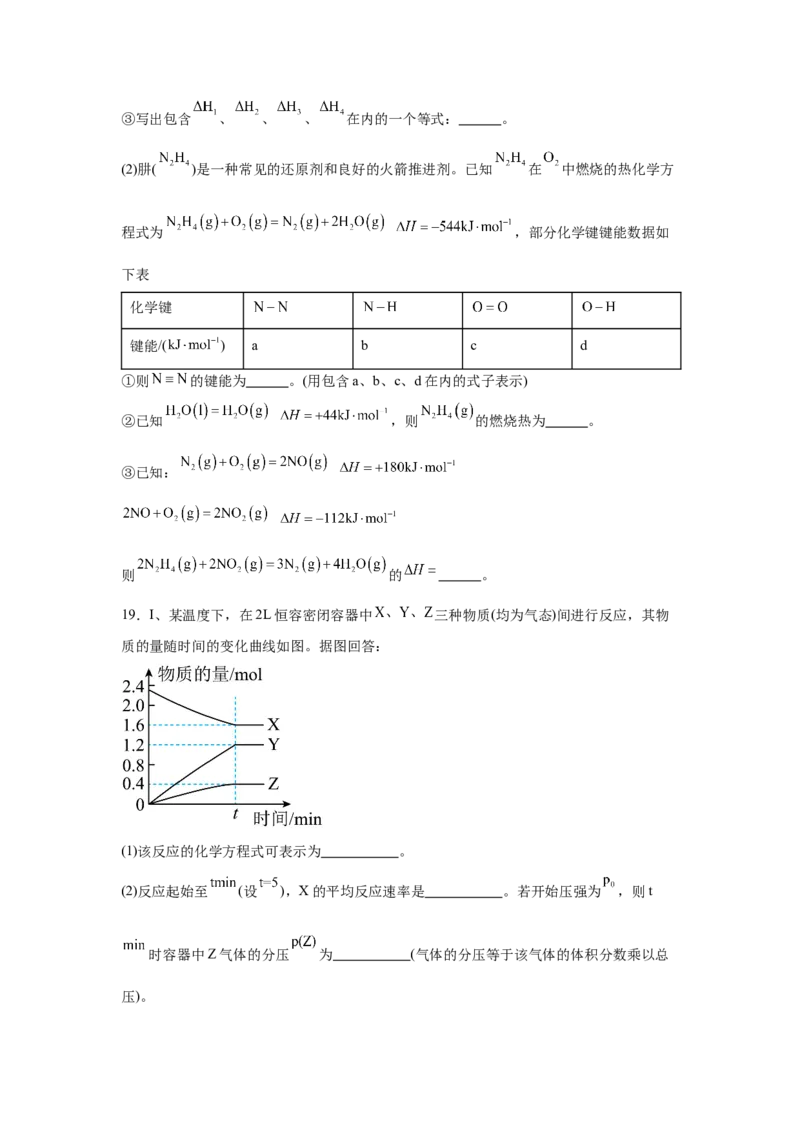
18.研究反应中的能量变化有利于更好的认识和利用反应。
(1) 与卤素 ( 或 )发生取代反应时,会经历如下过程:
Ⅰ:
Ⅱ:
Ⅲ:
与卤素 反应过程中物质的能量变化及产物的选择性如下图所示。
产物选择性(%)
①稳定性: (填“>”或“<”)。
②以丙烷为原料合成丙醇时,为提高2-丙醇的产率,应 (填字母)。
A.先氯代再水解 B.先溴代再水解③写出包含 、 、 、 在内的一个等式: 。
(2)肼( )是一种常见的还原剂和良好的火箭推进剂。已知 在 中燃烧的热化学方
程式为 ,部分化学键键能数据如
下表
化学键
键能/( ) a b c d
①则 的键能为 。(用包含a、b、c、d在内的式子表示)
②已知 ,则 的燃烧热为 。
③已知:
则 的 。
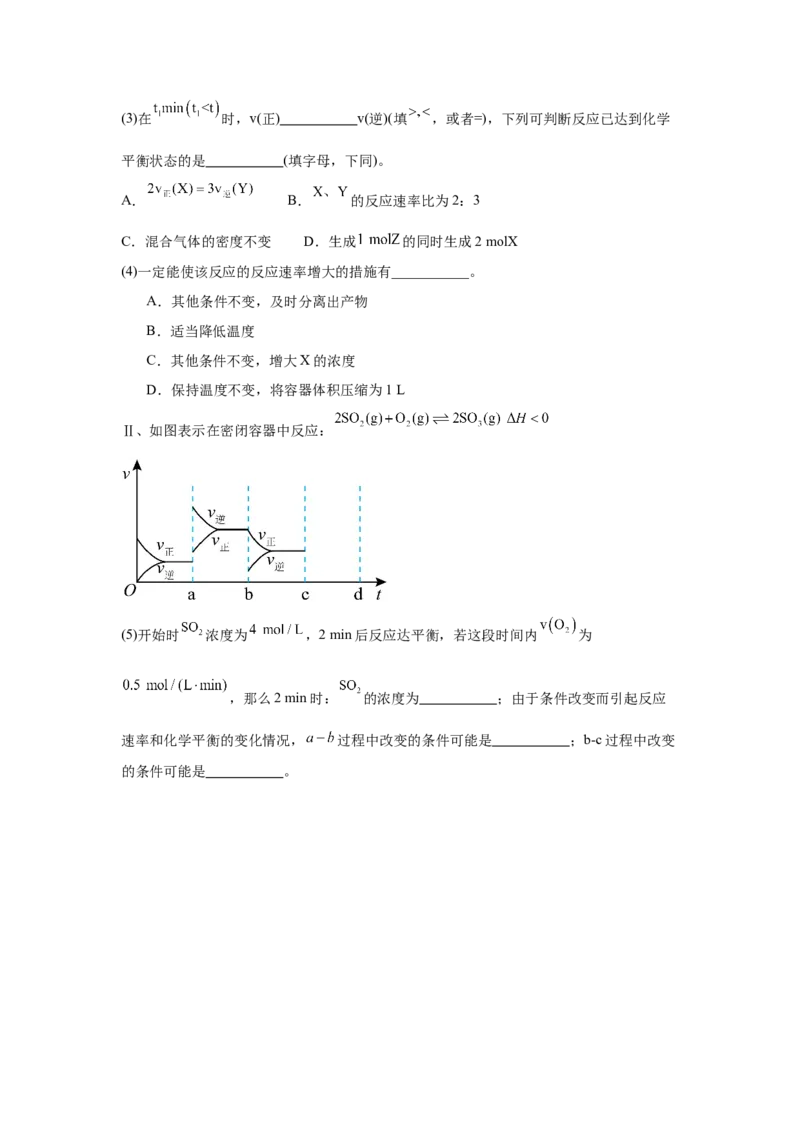
19.I、某温度下,在2L恒容密闭容器中 三种物质(均为气态)间进行反应,其物
质的量随时间的变化曲线如图。据图回答:
(1)该反应的化学方程式可表示为 。
(2)反应起始至 (设 ),X的平均反应速率是 。若开始压强为 ,则t
时容器中Z气体的分压 为 (气体的分压等于该气体的体积分数乘以总
压)。(3)在 时,v(正) v(逆)(填 ,或者=),下列可判断反应已达到化学
平衡状态的是 (填字母,下同)。
A. B. 的反应速率比为2:3
C.混合气体的密度不变 D.生成 的同时生成2 molX
(4)一定能使该反应的反应速率增大的措施有___________。
A.其他条件不变,及时分离出产物
B.适当降低温度
C.其他条件不变,增大X的浓度
D.保持温度不变,将容器体积压缩为1 L
Ⅱ、如图表示在密闭容器中反应:
(5)开始时 浓度为 ,2 min后反应达平衡,若这段时间内 为
,那么2 min时: 的浓度为 ;由于条件改变而引起反应
速率和化学平衡的变化情况, 过程中改变的条件可能是 ;b-c过程中改变
的条件可能是 。