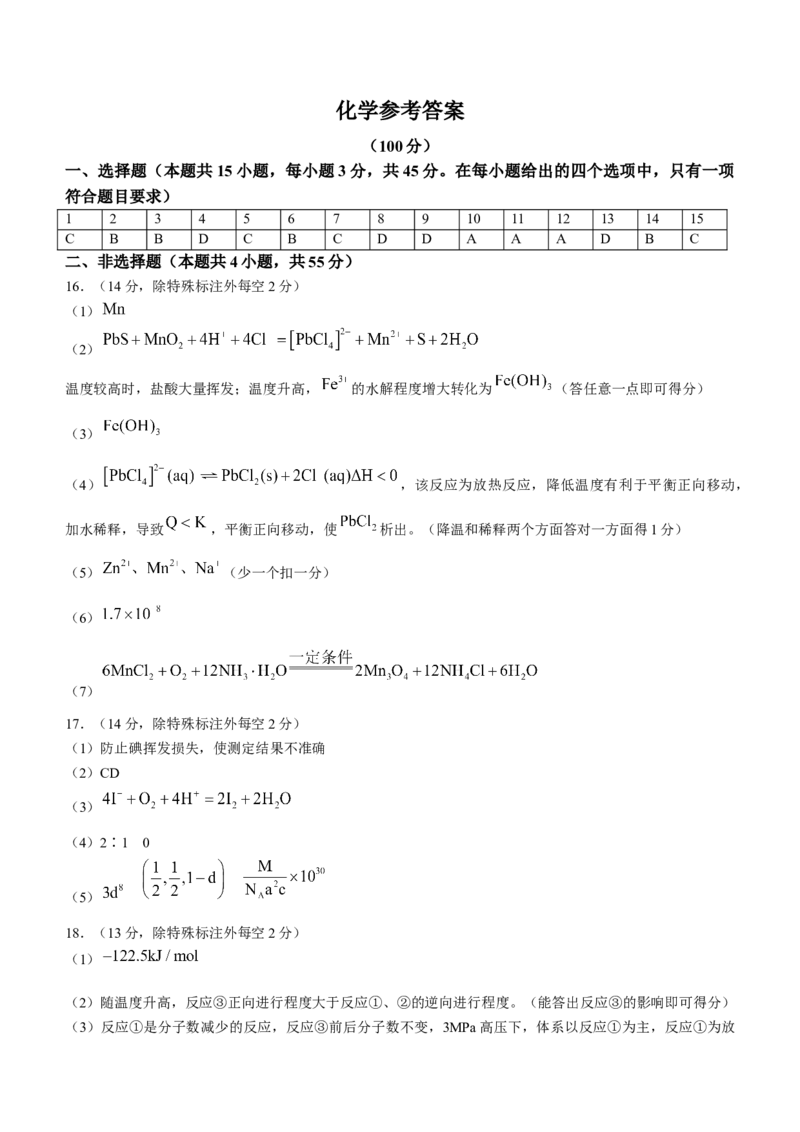文档内容
黑龙江省“六校联盟”高三年级联合适应性测试
化学试卷
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷
上无效。
3.考试结束后,将本试卷和答题卡一并交回.
4.可能用到的相对原子质量:H-1 B-11 C-12 N-14 O-16 Na-23 S-32 Fe-56 Ba-137
Cu-64 Y-89
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.推进美丽中国建设,促进人与自然和谐共生,下列说法正确的是( )
A.明矾可用于水体的净化和杀菌消毒
B.采用聚乙烯塑料代替聚乳酸塑料,有利于减少白色污染
C.汽车尾气系统安装催化转化器,有助于减少汽车尾气污染
D.煤的气化和液化处理有利于减少二氧化碳排放,提前实现“碳达峰”
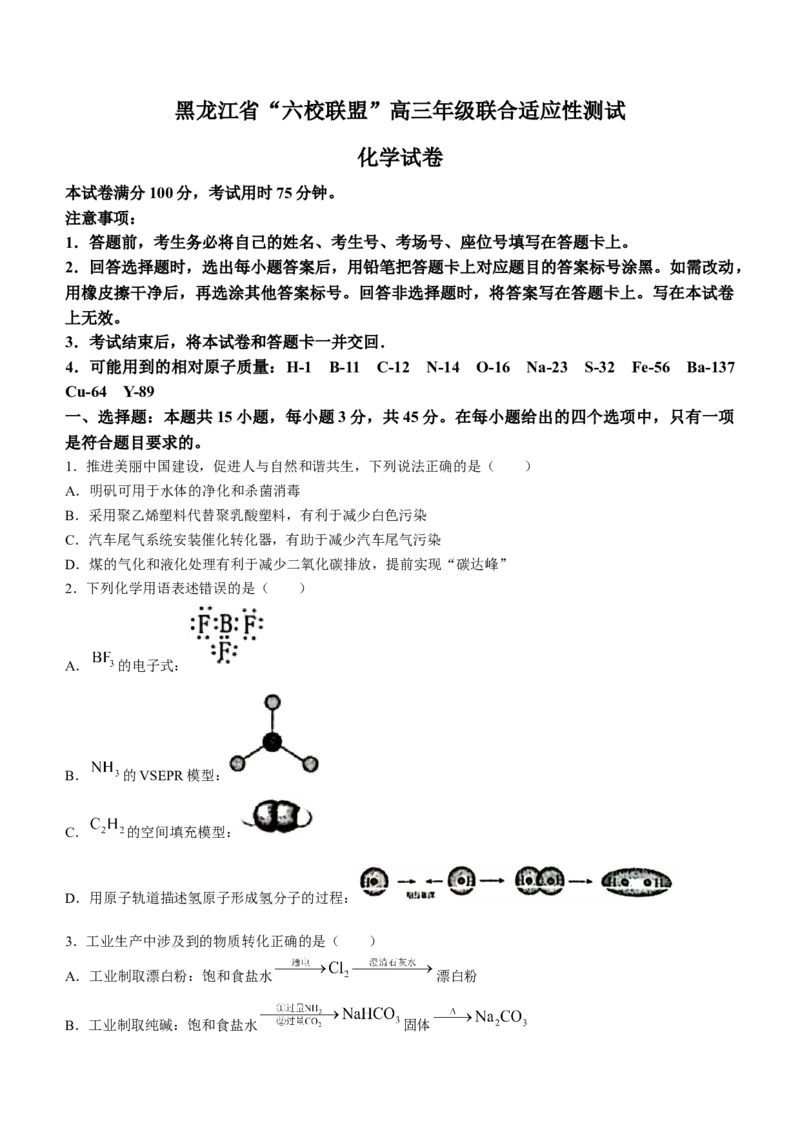
2.下列化学用语表述错误的是( )
A. 的电子式:
B. 的VSEPR模型:
C. 的空间填充模型:
D.用原子轨道描述氢原子形成氢分子的过程:
3.工业生产中涉及到的物质转化正确的是( )
A.工业制取漂白粉:饱和食盐水 漂白粉
B.工业制取纯碱:饱和食盐水 固体
学科网(北京)股份有限公司C.工业制取镁: 溶液 无水
D.工业制取硫酸:
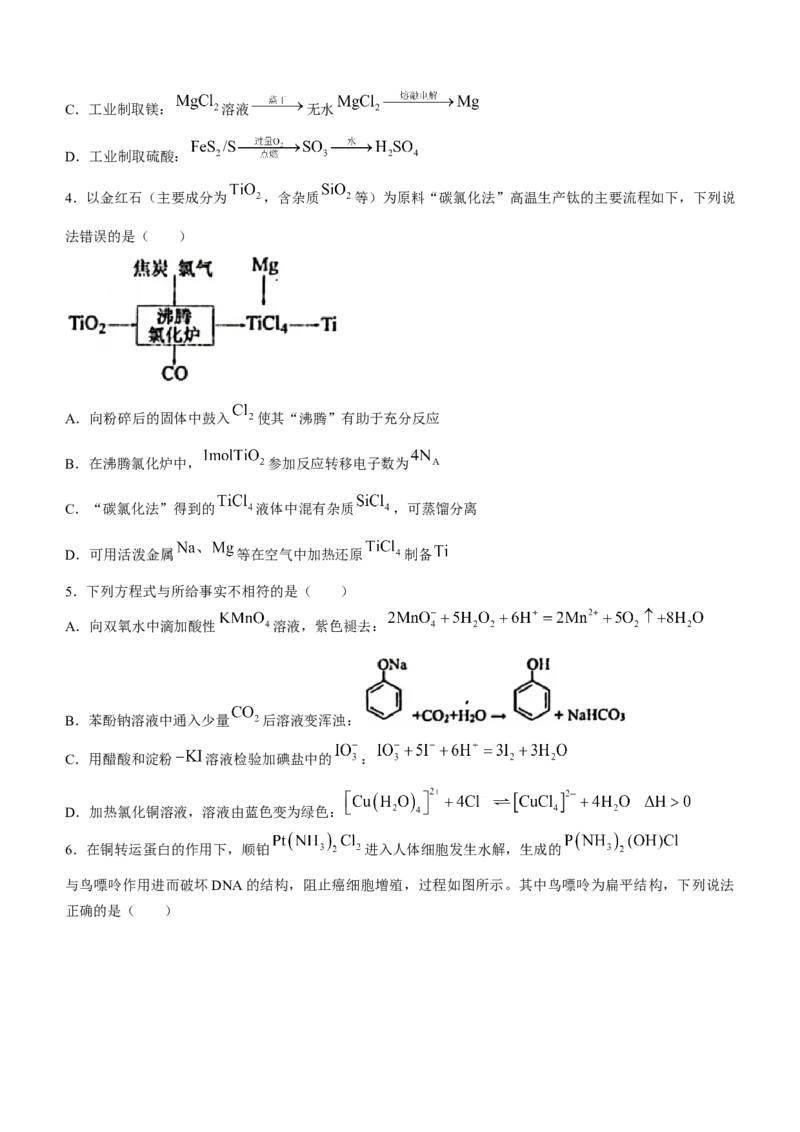
4.以金红石(主要成分为 ,含杂质 等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说
法错误的是( )
A.向粉碎后的固体中鼓入 使其“沸腾”有助于充分反应
B.在沸腾氯化炉中, 参加反应转移电子数为
C.“碳氯化法”得到的 液体中混有杂质 ,可蒸馏分离
D.可用活泼金属 等在空气中加热还原 制备
5.下列方程式与所给事实不相符的是( )
A.向双氧水中滴加酸性 溶液,紫色褪去:
B.苯酚钠溶液中通入少量 后溶液变浑浊:
C.用醋酸和淀粉 溶液检验加碘盐中的 :
D.加热氯化铜溶液,溶液由蓝色变为绿色:
6.在铜转运蛋白的作用下,顺铂 进入人体细胞发生水解,生成的
与鸟嘌呤作用进而破坏DNA的结构,阻止癌细胞增殖,过程如图所示。其中鸟嘌呤为扁平结构,下列说法
正确的是( )
学科网(北京)股份有限公司A.鸟嘌呤和 中N原子的杂化方式完全相同
B.在水溶液中的溶解性B强于A
C.鸟嘌呤中的原子电负性:
D.(C)结构中化学键包括:共价键、配位键、氢键
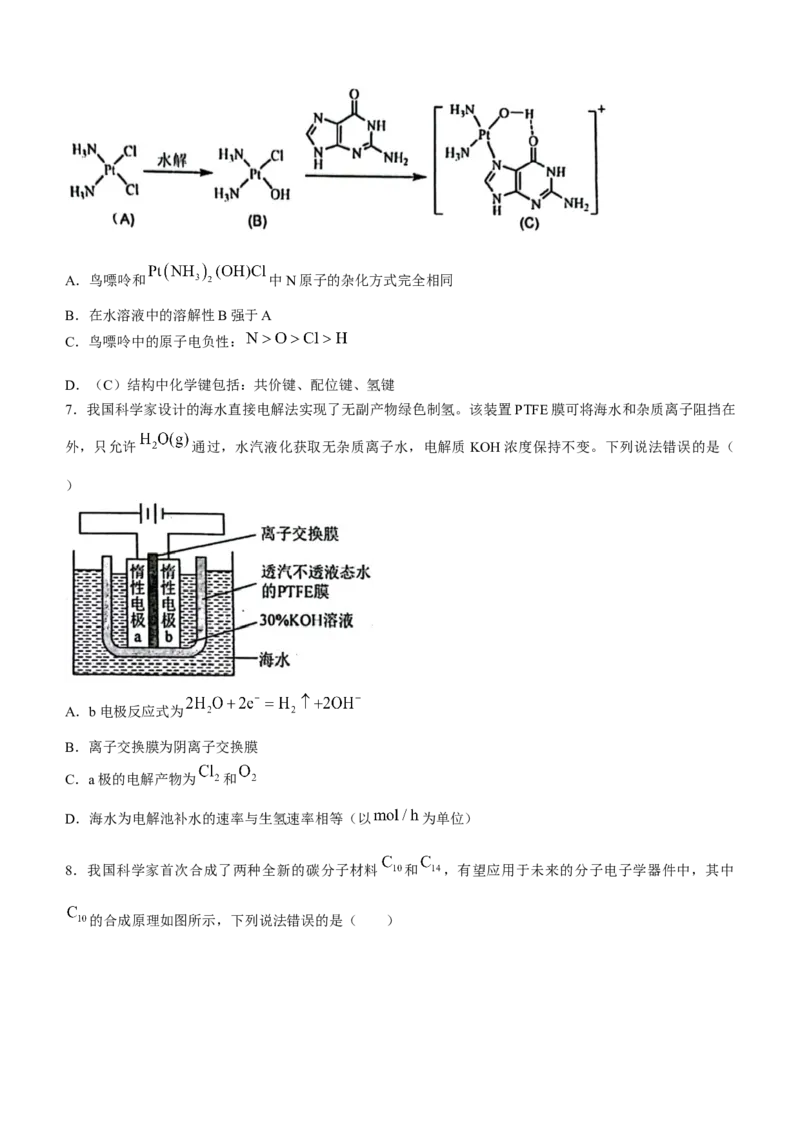
7.我国科学家设计的海水直接电解法实现了无副产物绿色制氢。该装置PTFE膜可将海水和杂质离子阻挡在
外,只允许 通过,水汽液化获取无杂质离子水,电解质 KOH浓度保持不变。下列说法错误的是(
)
A.b电极反应式为
B.离子交换膜为阴离子交换膜
C.a极的电解产物为 和
D.海水为电解池补水的速率与生氢速率相等(以 为单位)
8.我国科学家首次合成了两种全新的碳分子材料 和 ,有望应用于未来的分子电子学器件中,其中
的合成原理如图所示,下列说法错误的是( )
学科网(北京)股份有限公司A. 中所有原子均处于同一平面
B. 与足量 溶液反应,最多消耗
C. 与金刚石、石墨互为同素异形体
D. 中所有碳原子均采用 杂化
9.X、Y、Z、M为分布在三个短周期的主族元素,原子序数依次增大,X、Z两种元素可组成10电子和18
电子化合物,基态Y原子的s能级电子数为p能级电子数的4倍。Z、M同主族,M的原子序数为Z的2倍。
下列说法正确的是( )
A.基态原子的第一电离能:
B.Y的最高价含氧酸为强酸
C.M的单质在过量 燃烧所得产物为非极性分子
D.简单氢化物的沸点:
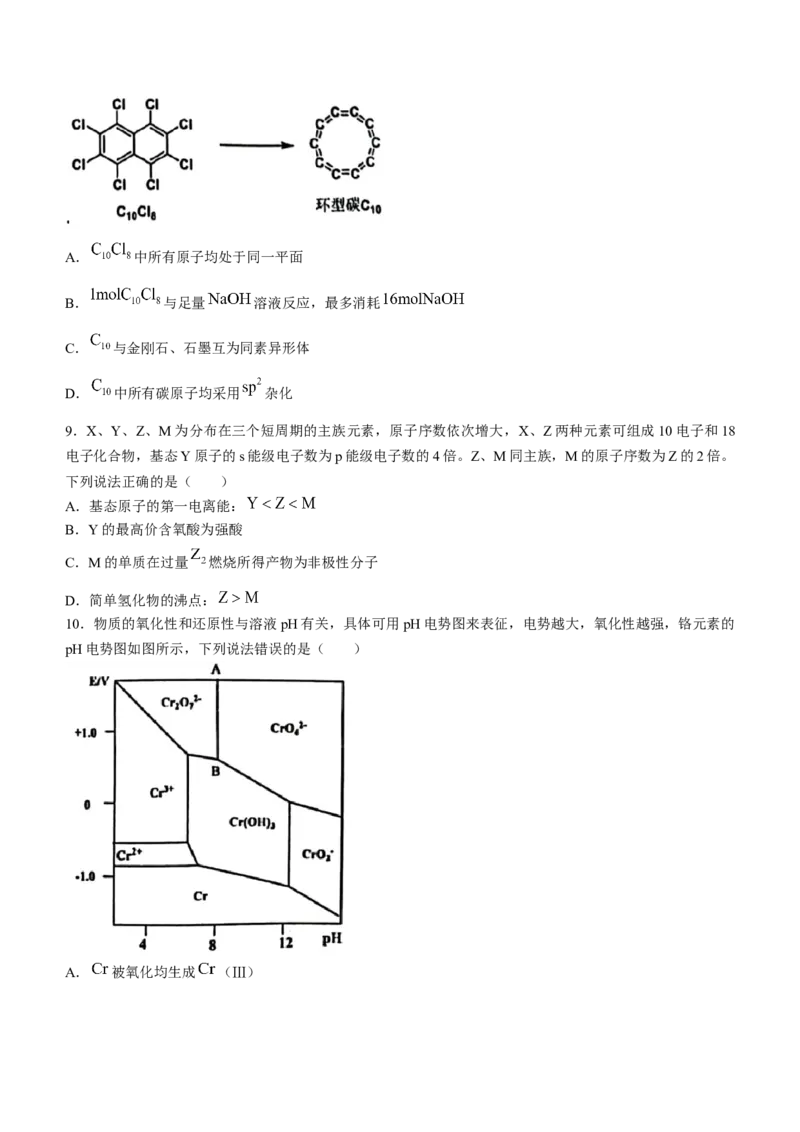
10.物质的氧化性和还原性与溶液pH有关,具体可用pH电势图来表征,电势越大,氧化性越强,铬元素的
pH电势图如图所示,下列说法错误的是( )
A. 被氧化均生成 (Ⅲ)
学科网(北京)股份有限公司B.AB线的反应为:
C.pH值越大 越容易被氧化
D. 时, 可与 反应生成
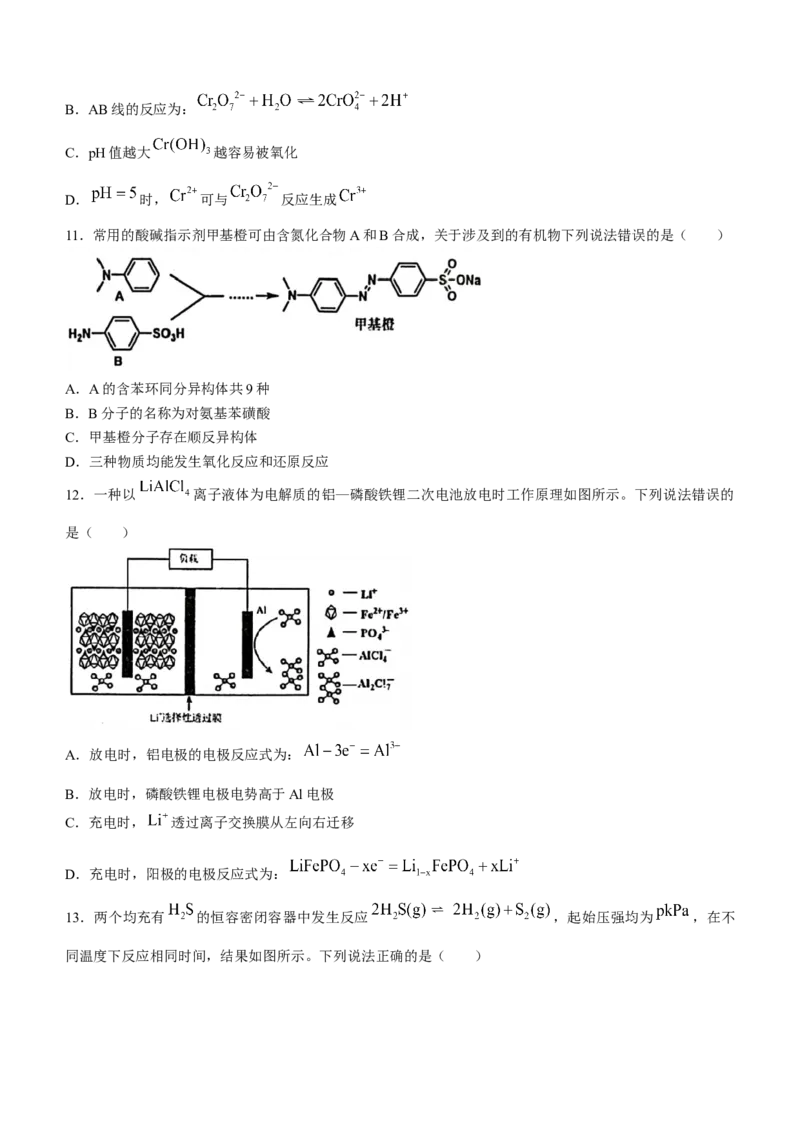
11.常用的酸碱指示剂甲基橙可由含氮化合物A和B合成,关于涉及到的有机物下列说法错误的是( )
A.A的含苯环同分异构体共9种
B.B分子的名称为对氨基苯磺酸
C.甲基橙分子存在顺反异构体
D.三种物质均能发生氧化反应和还原反应
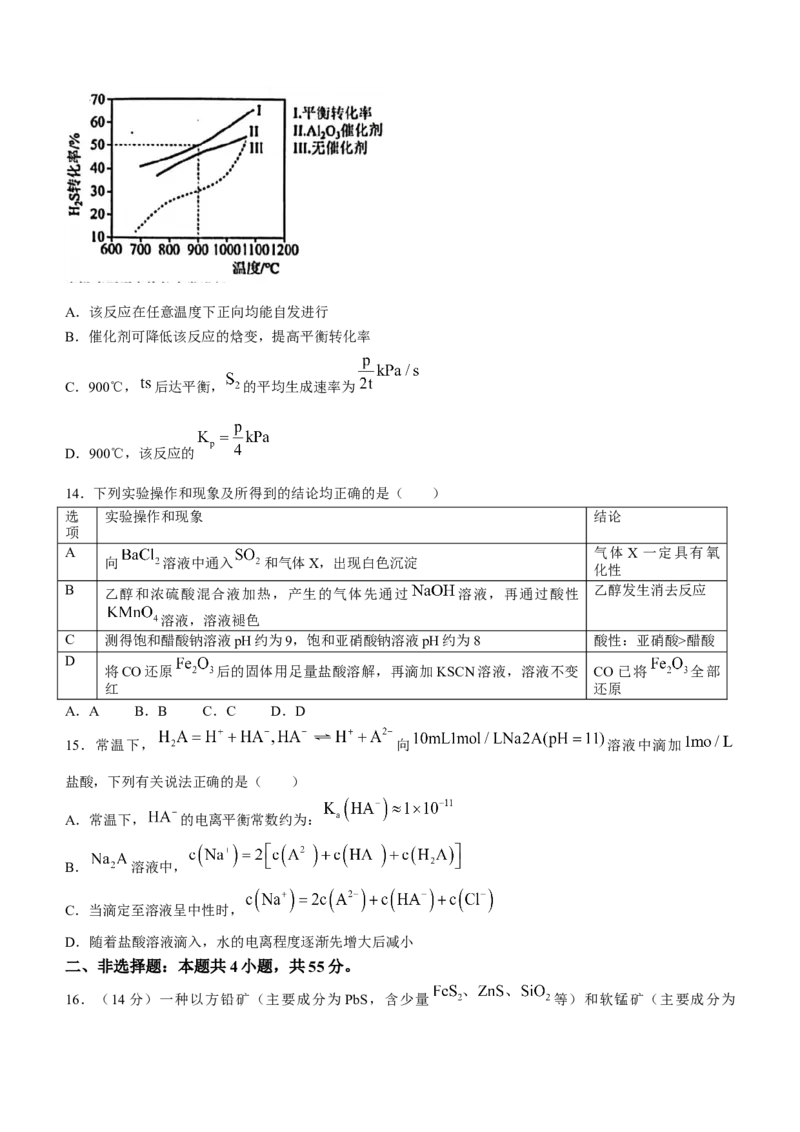
12.一种以 离子液体为电解质的铝—磷酸铁锂二次电池放电时工作原理如图所示。下列说法错误的
是( )
A.放电时,铝电极的电极反应式为:
B.放电时,磷酸铁锂电极电势高于Al电极
C.充电时, 透过离子交换膜从左向右迁移
D.充电时,阳极的电极反应式为:
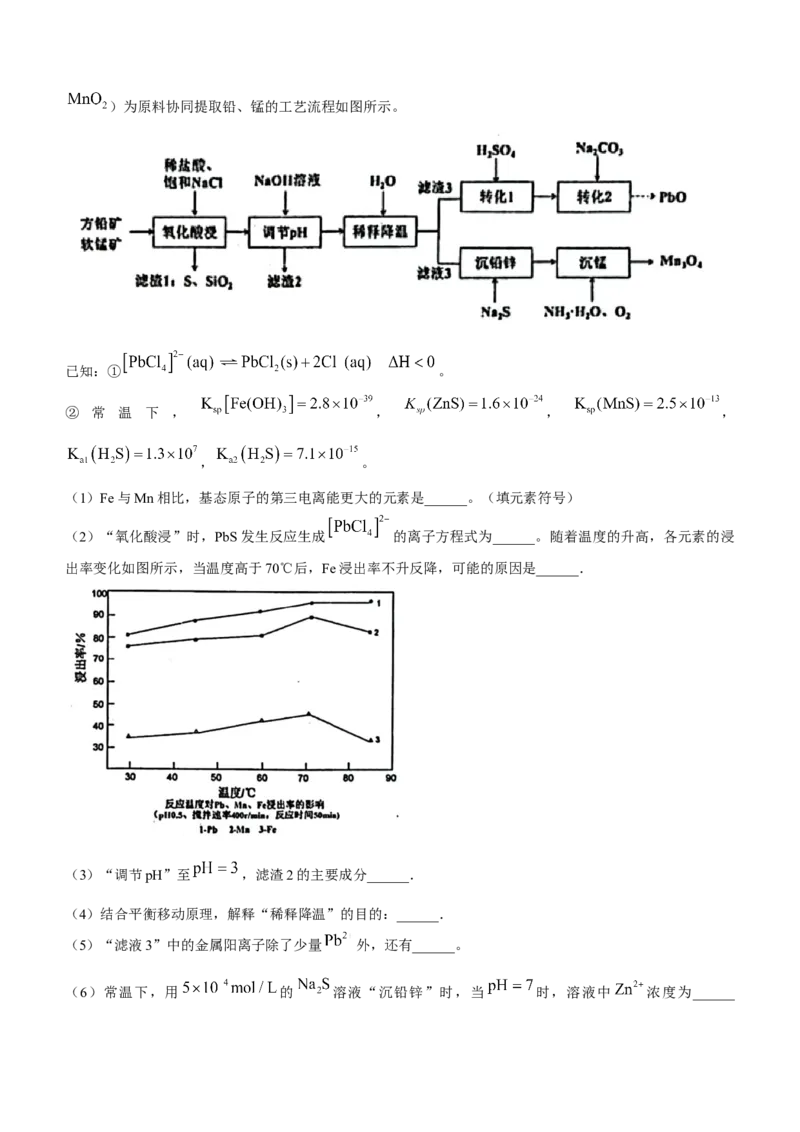
13.两个均充有 的恒容密闭容器中发生反应 ,起始压强均为 ,在不
同温度下反应相同时间,结果如图所示。下列说法正确的是( )
学科网(北京)股份有限公司A.该反应在任意温度下正向均能自发进行
B.催化剂可降低该反应的焓变,提高平衡转化率
C.900℃, 后达平衡, 的平均生成速率为
D.900℃,该反应的
14.下列实验操作和现象及所得到的结论均正确的是( )
选 实验操作和现象 结论
项
A 气体 X 一定具有氧
向 溶液中通入 和气体X,出现白色沉淀
化性
B 乙醇和浓硫酸混合液加热,产生的气体先通过 溶液,再通过酸性 乙醇发生消去反应
溶液,溶液褪色
C 测得饱和醋酸钠溶液pH约为9,饱和亚硝酸钠溶液pH约为8 酸性:亚硝酸>醋酸
D
将CO还原 后的固体用足量盐酸溶解,再滴加KSCN溶液,溶液不变 CO 已将 全部
红 还原
A.A B.B C.C D.D
15.常温下, 向 溶液中滴加
盐酸,下列有关说法正确的是( )
A.常温下, 的电离平衡常数约为:
B. 溶液中,
C.当滴定至溶液呈中性时,
D.随着盐酸溶液滴入,水的电离程度逐渐先增大后减小
二、非选择题:本题共4小题,共55分。
16.(14分)一种以方铅矿(主要成分为 PbS,含少量 等)和软锰矿(主要成分为
学科网(北京)股份有限公司)为原料协同提取铅、锰的工艺流程如图所示。
已知:① 。
② 常 温 下 , , , ,
, 。
(1)Fe与Mn相比,基态原子的第三电离能更大的元素是______。(填元素符号)
(2)“氧化酸浸”时,PbS发生反应生成 的离子方程式为______。随着温度的升高,各元素的浸
出率变化如图所示,当温度高于70℃后,Fe浸出率不升反降,可能的原因是______.
(3)“调节pH”至 ,滤渣2的主要成分______.
(4)结合平衡移动原理,解释“稀释降温”的目的:______.
(5)“滤液3”中的金属阳离子除了少量 外,还有______。
(6)常温下,用 的 溶液“沉铅锌”时,当 时,溶液中 浓度为______
学科网(北京)股份有限公司(设 的平衡浓度为 )。
(7)一定条件下,写出“沉锰”制备 的化学方程式______.
17.(14 分)钇钡铜氧晶体是一种新型节能高温超导材料。对钇钡铜氧材料分析表明,组成为
,其中Y元素为 价,铜元素以Cu(Ⅱ)和罕见的Cu(Ⅲ)形式存在,将该材料溶于稀酸
之后,Cu(III)将全部被还原为Cu(II)。现通过以下实验确定Cu(II)和Cu(III)的比例。
实验步骤:
a.称取 样品溶于稀酸,充分反应后加入过量碘化钾,配制250mL待测溶液。
b.取 25.00mL 待测溶液,以淀粉为指示剂,用 0.0100mol/L 的 标准溶液滴定,消耗标准液
23.04mL。
c.再次称取0.5000g样品溶于过量碘化钾溶液充分反应后,配制250mL待测溶液。取25.00mL反应后溶液,
用 标准液滴定至终点,消耗标准液30.55mL。
d.做空白实验,消耗 标准溶液0.50mL。
已知:
回答下列问题:
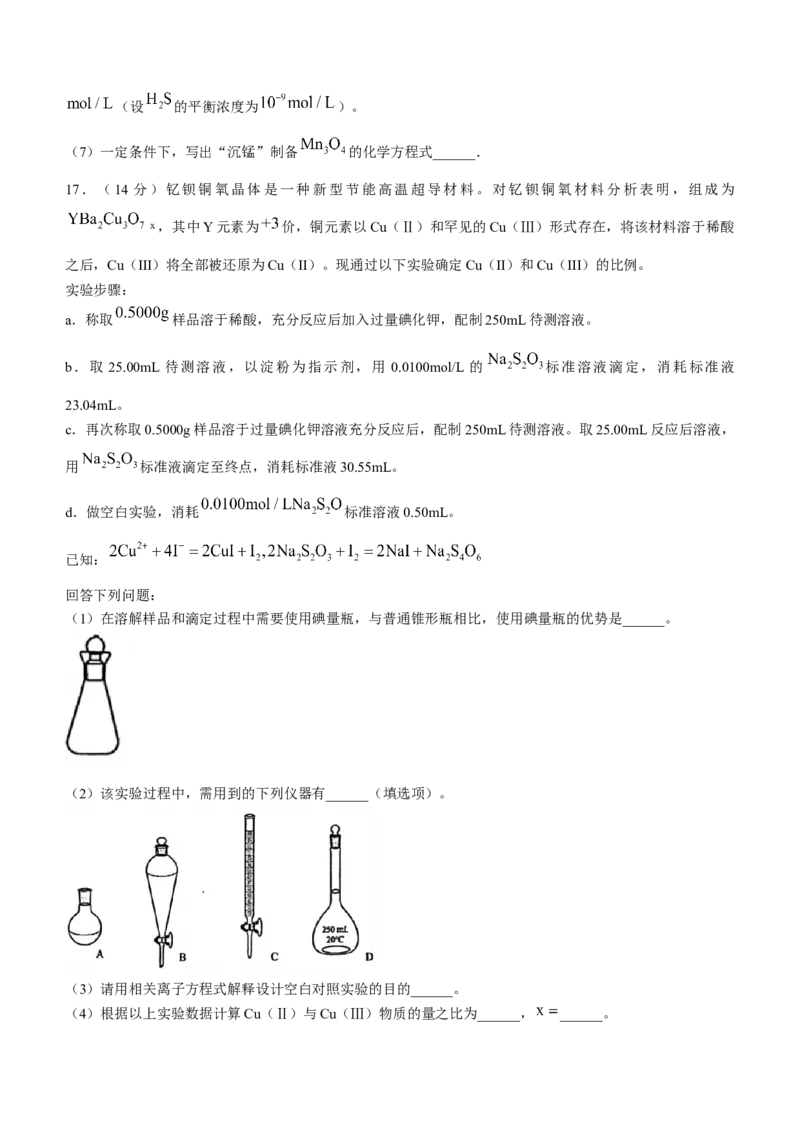
(1)在溶解样品和滴定过程中需要使用碘量瓶,与普通锥形瓶相比,使用碘量瓶的优势是______。
(2)该实验过程中,需用到的下列仪器有______(填选项)。
(3)请用相关离子方程式解释设计空白对照实验的目的______。
(4)根据以上实验数据计算Cu(Ⅱ)与Cu(Ⅲ)物质的量之比为______, ______。
学科网(北京)股份有限公司(5)某种钇钡铜氧晶体属于四方晶系晶胞,参数如图所示。晶胞夹角均为90°,基态三价Cu价层电子排布
式为______.
图中D原子的分数坐标为 ,则C原子的分数坐标为______.
钇钡铜氧晶体的摩尔质量为Mg/mol。则该晶体的密度为______ (列出计算式, 为阿伏伽德罗常
数)。
18.(13分)大气中二氧化碳 导致全球变暖和海洋酸化等问题愈发严重。基于功能催化剂将 氢
化和甲苯甲基化过程耦合直接合成二甲苯(X)等高价值化学品的过程也展现出巨大潜力。
相关主要反应有:
①
②
③
④
⑤
回答下列问题:
(1)通过 与 和 直接甲基化得二甲苯(X)的 ______.
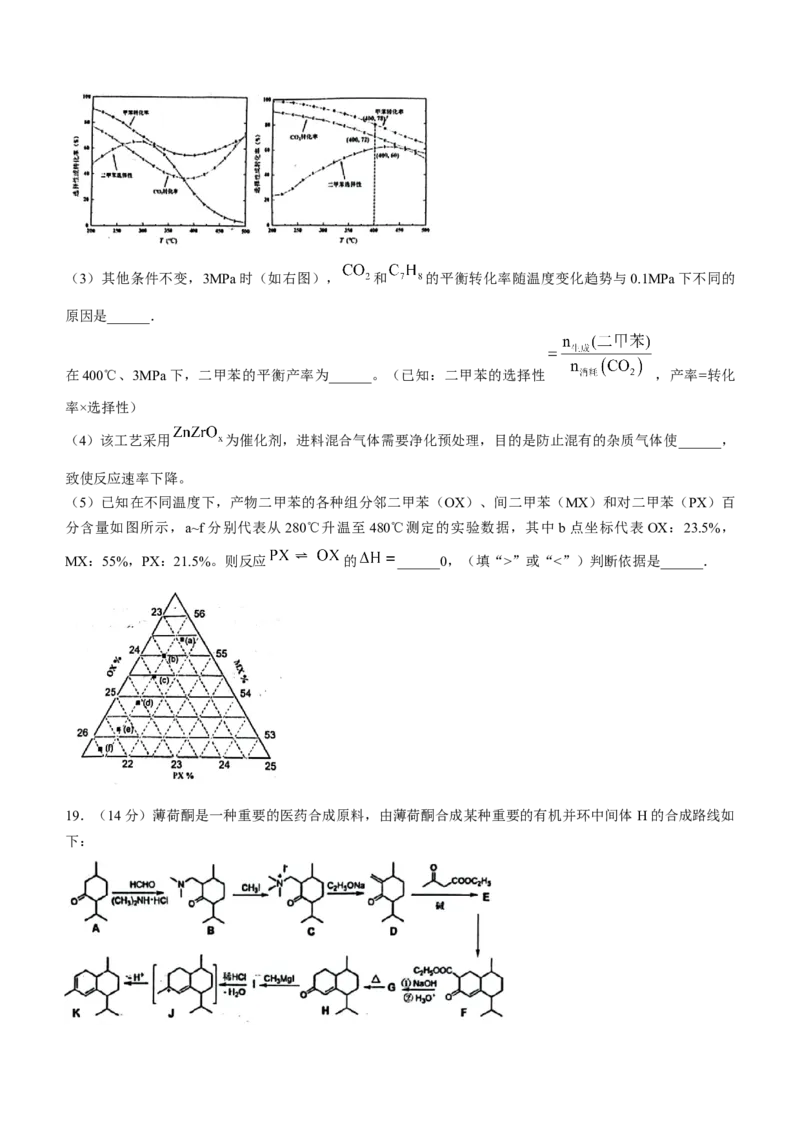
(2)下图显示了在 下,进料组成为 时的平衡产物分布
(如左图), 后 的转化率升高的原因是______.
学科网(北京)股份有限公司(3)其他条件不变,3MPa时(如右图), 和 的平衡转化率随温度变化趋势与0.1MPa下不同的
原因是______.
在400℃、3MPa下,二甲苯的平衡产率为______。(已知:二甲苯的选择性 ,产率=转化
率×选择性)
(4)该工艺采用 为催化剂,进料混合气体需要净化预处理,目的是防止混有的杂质气体使______,
致使反应速率下降。
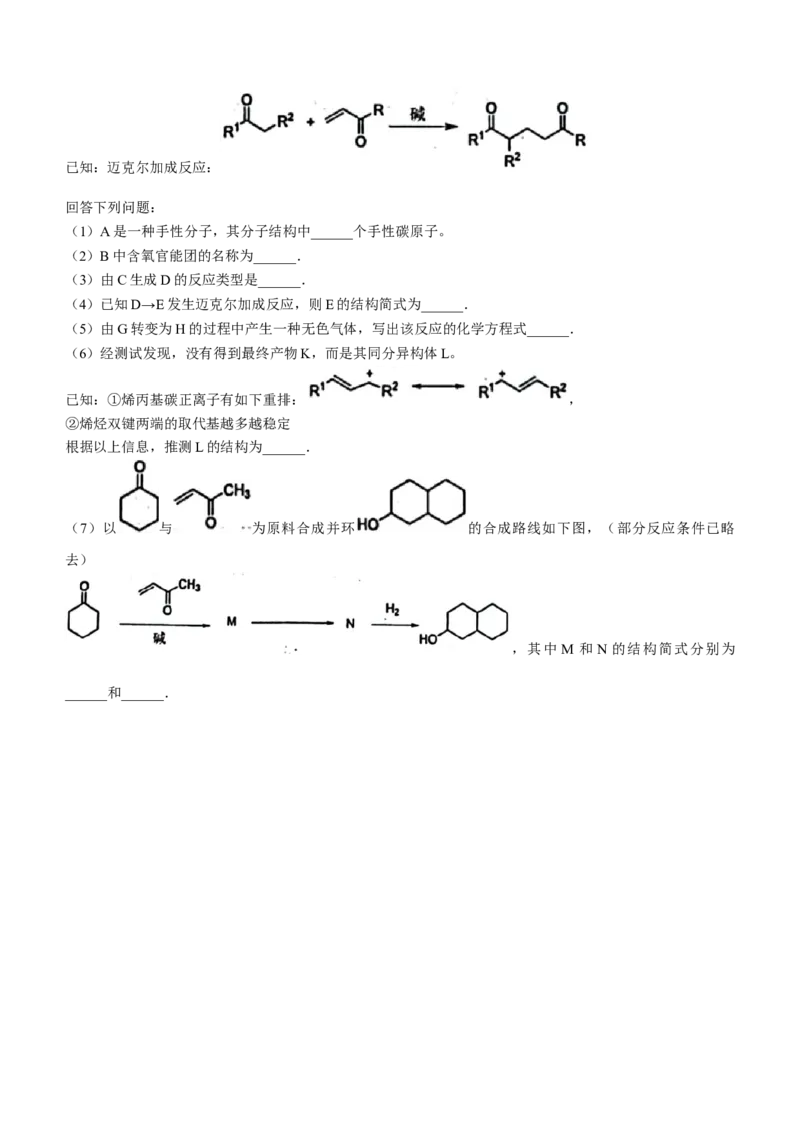
(5)已知在不同温度下,产物二甲苯的各种组分邻二甲苯(OX)、间二甲苯(MX)和对二甲苯(PX)百
分含量如图所示,a~f分别代表从280℃升温至480℃测定的实验数据,其中 b点坐标代表OX:23.5%,
MX:55%,PX:21.5%。则反应 的 ______0,(填“>”或“<”)判断依据是______.
19.(14分)薄荷酮是一种重要的医药合成原料,由薄荷酮合成某种重要的有机并环中间体 H的合成路线如
下:
学科网(北京)股份有限公司已知:迈克尔加成反应:
回答下列问题:
(1)A是一种手性分子,其分子结构中______个手性碳原子。
(2)B中含氧官能团的名称为______.
(3)由C生成D的反应类型是______.
(4)已知D→E发生迈克尔加成反应,则E的结构简式为______.
(5)由G转变为H的过程中产生一种无色气体,写出该反应的化学方程式______.
(6)经测试发现,没有得到最终产物K,而是其同分异构体L。
已知:①烯丙基碳正离子有如下重排: ,
②烯烃双键两端的取代基越多越稳定
根据以上信息,推测L的结构为______.
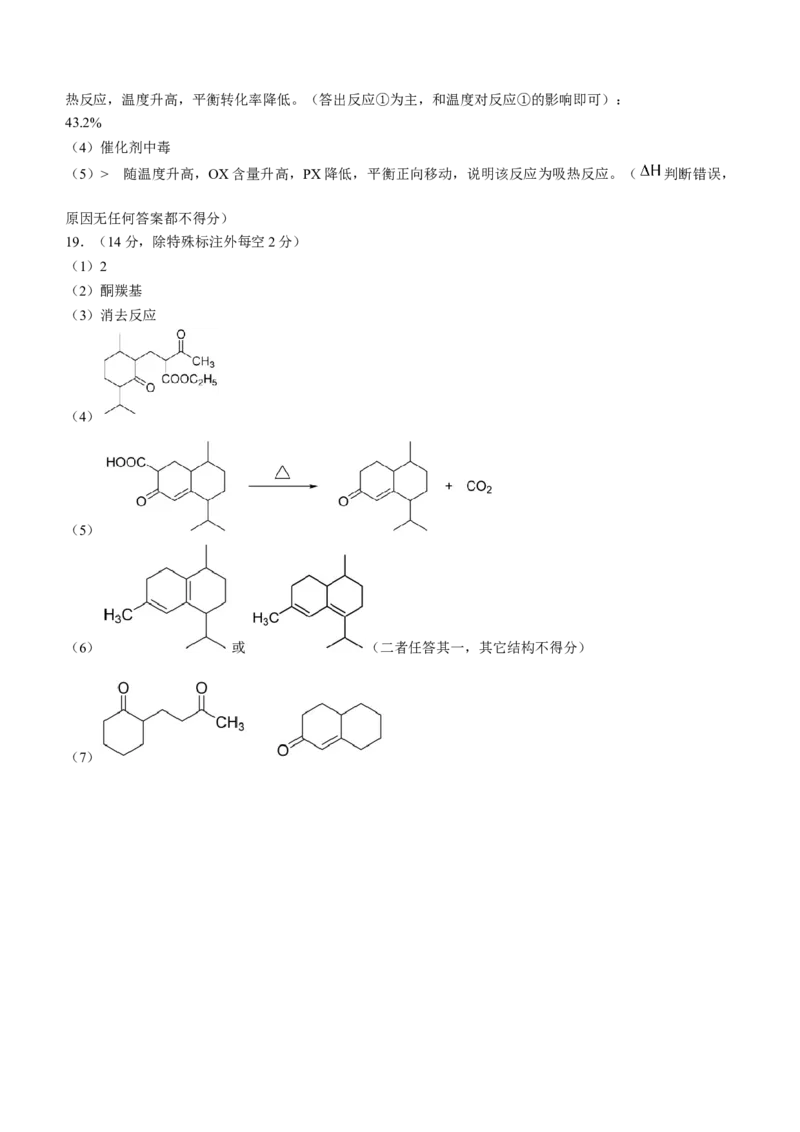
(7)以 与 为原料合成并环 的合成路线如下图,(部分反应条件已略
去)
,其中 M 和 N 的结构简式分别为
______和______.
学科网(北京)股份有限公司化学参考答案
(100分)
一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项
符合题目要求)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C B B D C B C D D A A A D B C
二、非选择题(本题共4小题,共55分)
16.(14分,除特殊标注外每空2分)
(1)
(2)
温度较高时,盐酸大量挥发;温度升高, 的水解程度增大转化为 (答任意一点即可得分)
(3)
(4) ,该反应为放热反应,降低温度有利于平衡正向移动,
加水稀释,导致 ,平衡正向移动,使 析出。(降温和稀释两个方面答对一方面得1分)
(5) (少一个扣一分)
(6)
(7)
17.(14分,除特殊标注外每空2分)
(1)防止碘挥发损失,使测定结果不准确
(2)CD
(3)
(4)2∶1 0
(5)
18.(13分,除特殊标注外每空2分)
(1)
(2)随温度升高,反应③正向进行程度大于反应①、②的逆向进行程度。(能答出反应③的影响即可得分)
(3)反应①是分子数减少的反应,反应③前后分子数不变,3MPa高压下,体系以反应①为主,反应①为放
学科网(北京)股份有限公司热反应,温度升高,平衡转化率降低。(答出反应①为主,和温度对反应①的影响即可):
43.2%
(4)催化剂中毒
(5)> 随温度升高,OX含量升高,PX降低,平衡正向移动,说明该反应为吸热反应。( 判断错误,
原因无任何答案都不得分)
19.(14分,除特殊标注外每空2分)
(1)2
(2)酮羰基
(3)消去反应
(4)
(5)
(6) 或 (二者任答其一,其它结构不得分)
(7)
学科网(北京)股份有限公司