文档内容
2019年湖南省株洲市中考化学试卷(教师版)
一、选择题(每题2分,总共40分)
1.(2分)下列过程中一定发生了化学变化的是( )
A.干冰气化 B.塑料降解 C.铁水铸成锅 D.汽油除油污
【考点】E3:化学变化和物理变化的判别.
菁优网版权所有
【分析】有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化,干冰气
化、铁水铸成锅、汽油除油污都属于物理变化。化学变化的特征是:有新物质生成。判
断物理变化和化学变化的依据是:是否有新物质生成。
【解答】解:A、干冰气化没有新物质生成,属于物理变化;故选项错误;
B、塑料降解生成新物质,属于化学变化;故选项正确;
C、铁水铸成锅没有新物质生成,属于物理变化;故选项错误;
D、汽油除油污没有新物质生成,属于物理变化;故选项错误;
故选:B。
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:
是否有新物质生成,问题就很容易解决。本考点主要出现在选择题和填空题中。
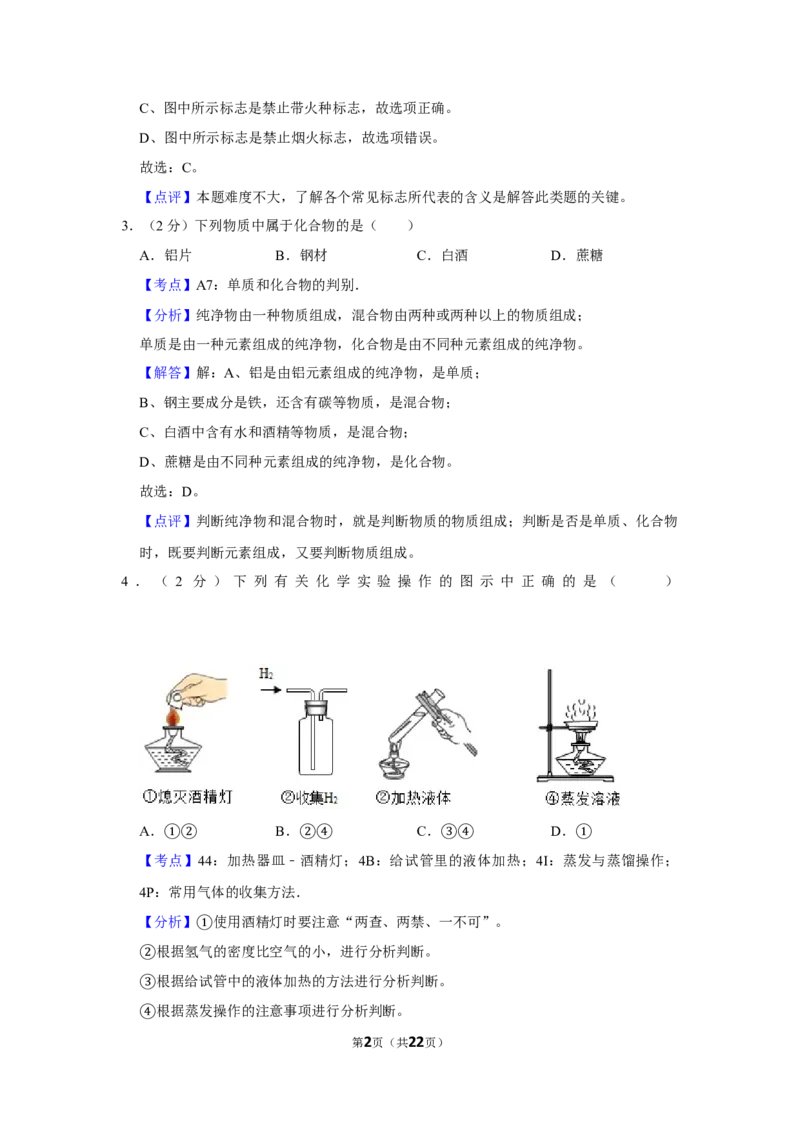
2.(2分)下列与燃烧和爆炸有关的图标中不正确的是( )
A. 禁止吸烟 B. 禁止燃放鞭炮
C. 禁止放易燃物 D. 禁止烟火
【考点】HH:几种常见的与化学有关的图标.
菁优网版权所有
【分析】根据图中常见标志的含义及题目的要求进行分析判断即可。
【解答】解:A、图中所示标志是禁止吸烟标志,故选项错误。
B、图中所示标志是禁止燃放鞭炮标志,故选项错误。
第1页(共22页)C、图中所示标志是禁止带火种标志,故选项正确。
D、图中所示标志是禁止烟火标志,故选项错误。
故选:C。
【点评】本题难度不大,了解各个常见标志所代表的含义是解答此类题的关键。
3.(2分)下列物质中属于化合物的是( )
A.铝片 B.钢材 C.白酒 D.蔗糖
【考点】A7:单质和化合物的判别.
菁优网版权所有
【分析】纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
【解答】解:A、铝是由铝元素组成的纯净物,是单质;
B、钢主要成分是铁,还含有碳等物质,是混合物;
C、白酒中含有水和酒精等物质,是混合物;
D、蔗糖是由不同种元素组成的纯净物,是化合物。
故选:D。
【点评】判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物
时,既要判断元素组成,又要判断物质组成。
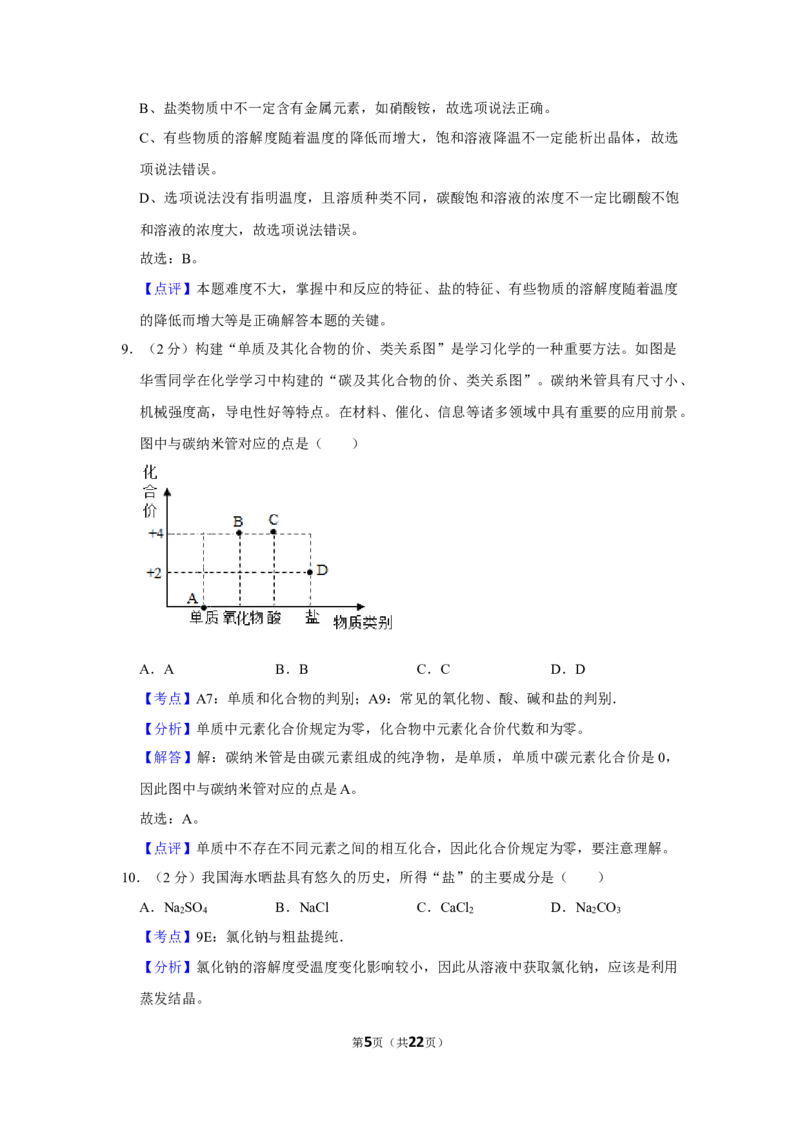
4 . ( 2 分 ) 下 列 有 关 化 学 实 验 操 作 的 图 示 中 正 确 的 是 ( )
A. B. C. D.
【考①点②】44:加热器皿﹣②酒精④灯;4B:给试管里③的④液体加热;4I:蒸①发与蒸馏操作;
4P:常用气体的收集方法.
菁优网版权所有
【分析】 使用酒精灯时要注意“两查、两禁、一不可”。
根据氢①气的密度比空气的小,进行分析判断。
②根据给试管中的液体加热的方法进行分析判断。
③根据蒸发操作的注意事项进行分析判断。
④ 第2页(共22页)【解答】解: 使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时,不能用
嘴吹灭酒精灯,①应用灯帽盖灭,图中所示操作正确。
氢气的密度比空气的小,应从短导管通入,将空气从长导管排出,图中所示操作错误。
②给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试
③
管容积的 ,图中液体超过试管容积的 ,图中所示操作错误。
蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作
④错误。
故选:D。
【点评】本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作
的注意事项是解答此类试题的关键。
5.(2分)某小孩食欲不振、生长迟缓、发育不良,下列适合改善该小孩症状的食品是(
)
A.高钙奶 B.补铁剂 C.补锌剂 D.海带汤
【考点】J1:人体的元素组成与元素对人体健康的重要作用.
菁优网版权所有
【分析】根据缺少营养素对身体的影响进行分析。
【解答】解:小孩食欲不振、生长迟缓、发育不良,主要是由于缺锌引起的,需要合理
补锌。
A.高钙奶的营养成分主要是钙元素,故A错误;
B.补铁剂的营养成分主要是铁元素,故B错误;
C.补锌剂的营养成分主要是锌元素,故C正确;
D.海带汤的营养成分主要是碘元素,故D错误。
故选:C。
【点评】六大营养素与人体的健康有密切的关系,也是中考的热点之一,特别是六大营
养素包括的种类、生理功能、食物来源、缺乏症,摄入时的注意事项等内容。
6.(2分)取用粉末状固体化学药品时,应使用的仪器是( )
A.滴管 B.研钵 C.药匙 D.镊子
【考点】48:固体药品的取用.
菁优网版权所有
【分析】根据粉末状固体药品取用的方法进行分析。
【解答】解:取用粉末状药品时可以用药匙。
故选:C。
第3页(共22页)【点评】需要熟练掌握实验室常见仪器的名称以及其用途,并熟练掌握各种实验仪器的
使用方法与注意事项。
7.(2分)2019年是“国际化学元素周期表年”。制出第一张元素周期表的科学家的是(
)
A.舍勒 B.道尔顿 C.门捷列夫 D.阿伏伽德罗
【考点】51:化学的历史发展过程.
菁优网版权所有
【分析】根据科学家们各自在科学上做出的贡献,进行分析解答本题。
【解答】解:A、舍勒通过实验测定了空气的组成,但受传统学说的影响,错过了发现
空气组成的机会,故选项错误。
B、道尔顿在化学上的主要贡献是提出了原子学说,故选项错误。
C、门捷列夫在化学上的主要贡献是发现了元素周期律,并编制出元素周期表,故选项
正确。
D、阿伏伽德罗在化学上的主要贡献是提出了分子的概念,并创立了分子学说,故选项
错误。
故选:C。
【点评】本题难度不大,了解化学的发展历史,关注化学学科成就,有利于激发学习化
学的兴趣,培养社会责任感。
8.(2分)下列说法中正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.盐类物质中不一定含有金属元素
C.饱和溶液降温一定能析出晶体
D.碳酸饱和溶液的浓度比硼酸不饱和溶液的浓度大
【考点】7P:晶体和结晶的概念与现象;7R:溶质的质量分数;97:中和反应及其应用;
A8:氧化物、酸、碱和盐的概念.
菁优网版权所有
【分析】A、中和反应是酸与碱作用生成盐和水的反应,反应物是酸和碱,生成物是盐
和水,进行分析判断。
B、盐是由金属离子(或铵根离子)和酸根离子组成的化合物。
C、根据有些物质的溶解度随着温度的降低而增大,进行分析判断。
D、根据选项说法没有指明温度,且溶质种类不同,进行分析判断。
【解答】解:A、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应,如
CO +2NaOH═Na CO +H O,故选项推理错误。
2 2 3 2
第4页(共22页)B、盐类物质中不一定含有金属元素,如硝酸铵,故选项说法正确。
C、有些物质的溶解度随着温度的降低而增大,饱和溶液降温不一定能析出晶体,故选
项说法错误。
D、选项说法没有指明温度,且溶质种类不同,碳酸饱和溶液的浓度不一定比硼酸不饱
和溶液的浓度大,故选项说法错误。
故选:B。
【点评】本题难度不大,掌握中和反应的特征、盐的特征、有些物质的溶解度随着温度
的降低而增大等是正确解答本题的关键。
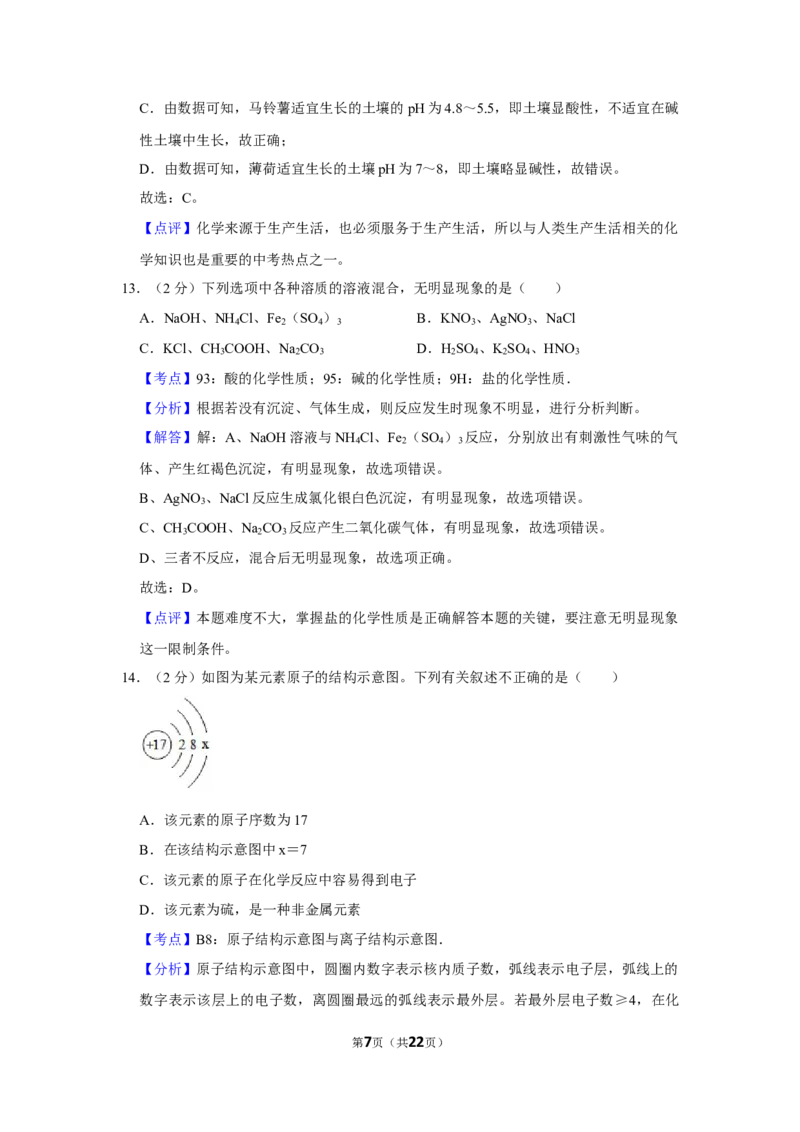
9.(2分)构建“单质及其化合物的价、类关系图”是学习化学的一种重要方法。如图是
华雪同学在化学学习中构建的“碳及其化合物的价、类关系图”。碳纳米管具有尺寸小、
机械强度高,导电性好等特点。在材料、催化、信息等诸多领域中具有重要的应用前景。
图中与碳纳米管对应的点是( )
A.A B.B C.C D.D
【考点】A7:单质和化合物的判别;A9:常见的氧化物、酸、碱和盐的判别.
菁优网版权所有
【分析】单质中元素化合价规定为零,化合物中元素化合价代数和为零。
【解答】解:碳纳米管是由碳元素组成的纯净物,是单质,单质中碳元素化合价是0,
因此图中与碳纳米管对应的点是A。
故选:A。
【点评】单质中不存在不同元素之间的相互化合,因此化合价规定为零,要注意理解。
10.(2分)我国海水晒盐具有悠久的历史,所得“盐”的主要成分是( )
A.Na SO B.NaCl C.CaCl D.Na CO
2 4 2 2 3
【考点】9E:氯化钠与粗盐提纯.
菁优网版权所有
【分析】氯化钠的溶解度受温度变化影响较小,因此从溶液中获取氯化钠,应该是利用
蒸发结晶。
第5页(共22页)【解答】解:我国海水晒盐具有悠久的历史,所得“盐”的主要成分是氯化钠。
故选:B。
【点评】海水中含有较多的氯化钠,海水晒盐所得“盐”的主要成分是氯化钠。
11.(2分)将石油加热炼制,不可能得到的产品是( )
A.煤焦油 B.润滑油 C.柴油 D.煤油
【考点】H9:石油加工的产物.
菁优网版权所有
【分析】石油中含有多种成分,这些成分的沸点不同,根据沸点不同将它们加热分离可
得到汽油、煤油、柴油、润滑油、石蜡、溶剂油、沥青等产品;根据石油分馏的产品进
行分析判断即可。
【解答】解:石油属于混合物,它是由汽油、煤油、柴油、润滑油、机油等沸点不同物
质混合而成的,石油通过分馏即可得到上述物质。将煤隔绝空气加强热,可生成焦炭、
煤焦油、煤气、焦炉气等产物,煤气、煤焦油、焦炉气均属于煤加工的产品。
A.煤焦油属于煤加工的产品,故选项符合题意。
B.润滑油属于石油加工的产品,故选项不合题意。
C.柴油属于石油加工的产品,故选项不合题意。
D.煤油属于石油加工的产品,故选项不合题意。
故选:A。
【点评】本题难度不大,了解石油加热炼制得到的产品是正确解答本题的关键。
12.(2分)一些重要作物最适宜生长的土壤的pH范围如下:
作物 水稻 马铃薯 草莓 薄荷
pH 6~7 4.8~5.5 5~7.5 7~8
下列说法中正确的是( )
A.水稻和薄荷生长都适宜酸性土壤
B.草莓生长只适宜酸性土壤
C.马铃薯生长不适宜碱性土壤
D.以上作物都不适宜碱性土壤
【考点】99:溶液的酸碱性与pH值的关系.
菁优网版权所有
【分析】根据土壤的酸碱性与pH的关系来分析解答。
【解答】解:溶液的pH>7,溶液显碱性;pH=7,溶液显中性;pH<7,溶液显酸性。
A.由数据可知,薄荷适宜生长的土壤pH为7~8,即土壤略显碱性,故错误;
B.由数据可知,草莓适宜生长的土壤的pH为5~7.5,即土壤略显碱性,故错误;
第6页(共22页)C.由数据可知,马铃薯适宜生长的土壤的pH为4.8~5.5,即土壤显酸性,不适宜在碱
性土壤中生长,故正确;
D.由数据可知,薄荷适宜生长的土壤pH为7~8,即土壤略显碱性,故错误。
故选:C。
【点评】化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化
学知识也是重要的中考热点之一。
13.(2分)下列选项中各种溶质的溶液混合,无明显现象的是( )
A.NaOH、NH Cl、Fe (SO ) B.KNO 、AgNO 、NaCl
4 2 4 3 3 3
C.KCl、CH COOH、Na CO D.H SO 、K SO 、HNO
3 2 3 2 4 2 4 3
【考点】93:酸的化学性质;95:碱的化学性质;9H:盐的化学性质.
菁优网版权所有
【分析】根据若没有沉淀、气体生成,则反应发生时现象不明显,进行分析判断。
【解答】解:A、NaOH溶液与NH Cl、Fe (SO ) 反应,分别放出有刺激性气味的气
4 2 4 3
体、产生红褐色沉淀,有明显现象,故选项错误。
B、AgNO 、NaCl反应生成氯化银白色沉淀,有明显现象,故选项错误。
3
C、CH COOH、Na CO 反应产生二氧化碳气体,有明显现象,故选项错误。
3 2 3
D、三者不反应,混合后无明显现象,故选项正确。
故选:D。
【点评】本题难度不大,掌握盐的化学性质是正确解答本题的关键,要注意无明显现象
这一限制条件。
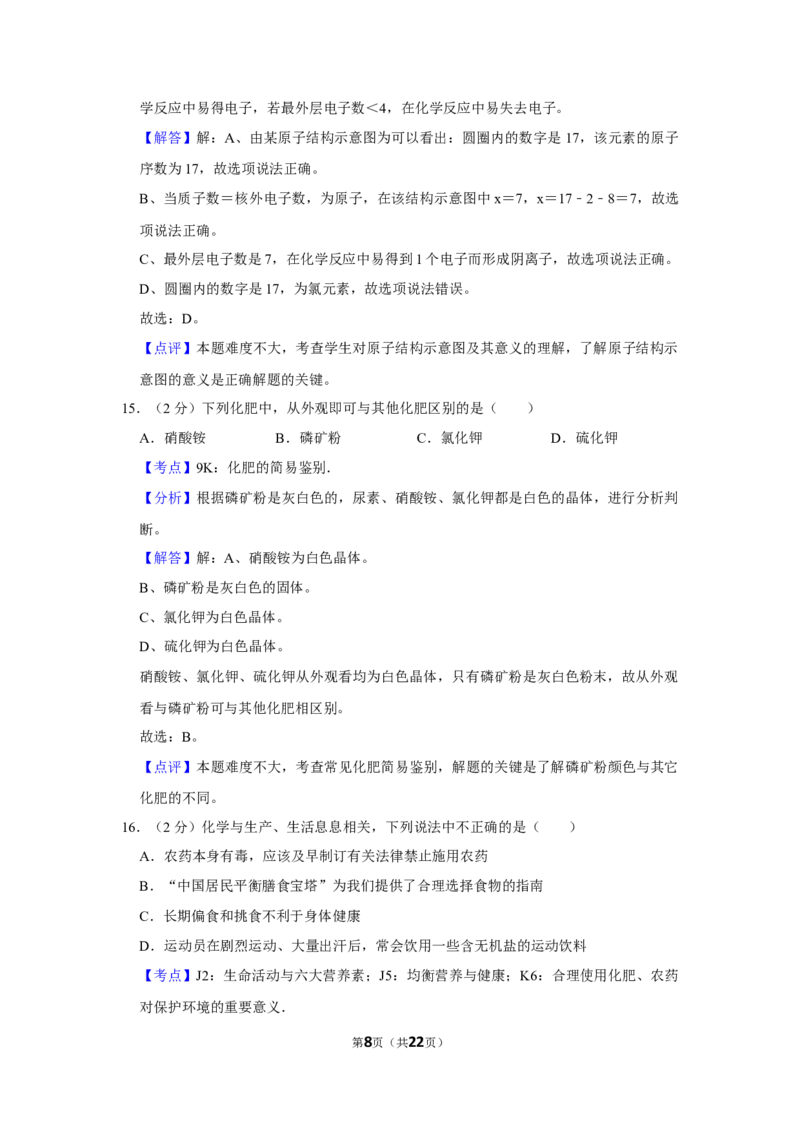
14.(2分)如图为某元素原子的结构示意图。下列有关叙述不正确的是( )
A.该元素的原子序数为17
B.在该结构示意图中x=7
C.该元素的原子在化学反应中容易得到电子
D.该元素为硫,是一种非金属元素
【考点】B8:原子结构示意图与离子结构示意图.
菁优网版权所有
【分析】原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的
数字表示该层上的电子数,离圆圈最远的弧线表示最外层。若最外层电子数≥4,在化
第7页(共22页)学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子。
【解答】解:A、由某原子结构示意图为可以看出:圆圈内的数字是 17,该元素的原子
序数为17,故选项说法正确。
B、当质子数=核外电子数,为原子,在该结构示意图中x=7,x=17﹣2﹣8=7,故选
项说法正确。
C、最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法正确。
D、圆圈内的数字是17,为氯元素,故选项说法错误。
故选:D。
【点评】本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示
意图的意义是正确解题的关键。
15.(2分)下列化肥中,从外观即可与其他化肥区别的是( )
A.硝酸铵 B.磷矿粉 C.氯化钾 D.硫化钾
【考点】9K:化肥的简易鉴别.
菁优网版权所有
【分析】根据磷矿粉是灰白色的,尿素、硝酸铵、氯化钾都是白色的晶体,进行分析判
断。
【解答】解:A、硝酸铵为白色晶体。
B、磷矿粉是灰白色的固体。
C、氯化钾为白色晶体。
D、硫化钾为白色晶体。
硝酸铵、氯化钾、硫化钾从外观看均为白色晶体,只有磷矿粉是灰白色粉末,故从外观
看与磷矿粉可与其他化肥相区别。
故选:B。
【点评】本题难度不大,考查常见化肥简易鉴别,解题的关键是了解磷矿粉颜色与其它
化肥的不同。
16.(2分)化学与生产、生活息息相关,下列说法中不正确的是( )
A.农药本身有毒,应该及早制订有关法律禁止施用农药
B.“中国居民平衡膳食宝塔”为我们提供了合理选择食物的指南
C.长期偏食和挑食不利于身体健康
D.运动员在剧烈运动、大量出汗后,常会饮用一些含无机盐的运动饮料
【考点】J2:生命活动与六大营养素;J5:均衡营养与健康;K6:合理使用化肥、农药
对保护环境的重要意义.
菁优网版权所有
第8页(共22页)【分析】A.根据农药的作用进行分析;
B.根据合理膳食进行分析;
C.根据青少年长期偏食、挑食不利于身体健康进行分手;
D.根据汗液的组成进行分析。
【解答】解:A.农药有毒,应该及早制订有关法合理施用农药,故A错误;
B.“平衡膳食宝塔”是根据平衡膳食的原则转化成各类食物的大致比例,并以直观的
宝塔形式表示出来,为我们提供了合理选择食物的指南,故B正确;
C.青青少年长期偏食、挑食会导致营养不良,不利于身体健康,要合理膳食,故 C正
确;
D.因为汗的成分是水、无机盐、尿素,故大量出汗后,应该饮用一些含无机盐的运动
原料,故D正确。
故选:A。
【点评】化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化
学知识也是重要的中考热点之一。
17.(2分)下列说法不正确的是( )
A.空气的成分按体积计算大约是:氮气78%,氧气21%,其他成分1%
B.地球上的水储量是丰富的,但可供利用的淡水资源是有限的
C.棉花、羊毛、蚕丝、涤纶、尼伦和腈纶等都是合成纤维
D.基本营养素包括蛋白质、糖类、油脂、维生素、无机盐和水六大类
【考点】61:空气的成分及各成分的体积分数;78:水资源状况;I4:合成纤维及其应
用;J2:生命活动与六大营养素.
菁优网版权所有
【分析】A.根据空气的组成来分析;
B.根据淡水资源的储量来分析;
C.根据纤维的分类来分析;
D.根据人体所需营养素来分析。
【解答】解:A.空气的成分按体积计算大约是:氮气 78%,氧气21%,其他成分
1%,故正确;
B.地球上的水储量是丰富的,但可供利用的淡水资源是有限的,故正确;
C.棉花、羊毛、蚕丝属于天然纤维;涤纶、尼伦和腈纶属于合成纤维,故错误;
D.人体所需的基本营养素包括蛋白质、糖类、油脂、维生素、无机盐和水六大类,故
正确。
第9页(共22页)故选:C。
【点评】本题考查了的知识点较多,但是均属于进出知识的考查,难度不大。
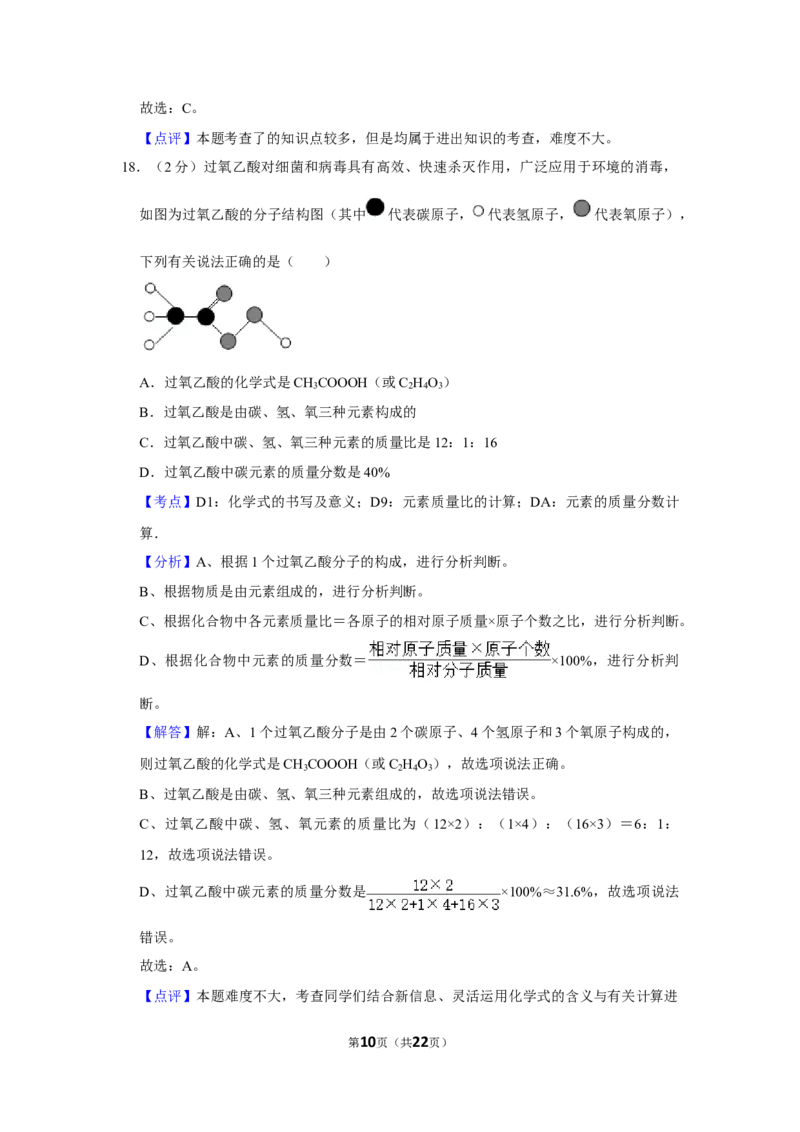
18.(2分)过氧乙酸对细菌和病毒具有高效、快速杀灭作用,广泛应用于环境的消毒,
如图为过氧乙酸的分子结构图(其中 代表碳原子, 代表氢原子, 代表氧原子),
下列有关说法正确的是( )
A.过氧乙酸的化学式是CH COOOH(或C H O )
3 2 4 3
B.过氧乙酸是由碳、氢、氧三种元素构成的
C.过氧乙酸中碳、氢、氧三种元素的质量比是12:1:16
D.过氧乙酸中碳元素的质量分数是40%
【考点】D1:化学式的书写及意义;D9:元素质量比的计算;DA:元素的质量分数计
算.
菁优网版权所有
【分析】A、根据1个过氧乙酸分子的构成,进行分析判断。
B、根据物质是由元素组成的,进行分析判断。
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断。
D、根据化合物中元素的质量分数= ×100%,进行分析判
断。
【解答】解:A、1个过氧乙酸分子是由2个碳原子、4个氢原子和3个氧原子构成的,
则过氧乙酸的化学式是CH COOOH(或C H O ),故选项说法正确。
3 2 4 3
B、过氧乙酸是由碳、氢、氧三种元素组成的,故选项说法错误。
C、过氧乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×3)=6:1:
12,故选项说法错误。
D、过氧乙酸中碳元素的质量分数是 ×100%≈31.6%,故选项说法
错误。
故选:A。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进
第10页(共22页)行分析问题、解决问题的能力。
19.(2分)造纸是我国古代四大发明之一。早期的纸张生产中,常常用纸表面涂敷某种
物质的工艺,但存在副作用,该物质易导致纸张发生酸性腐蚀,使纸张变脆易破损,该
物质是( )
A.烧碱 B.明矾 C.草木灰 D.熟石灰
【考点】94:常见碱的特性和用途;9G:常用盐的用途.
菁优网版权所有
【分析】根据已有的物质的性质和用途的关系进行分析解答即可。
【解答】解:早期的纸张生产中,常在纸表面涂敷明矾的工艺,利用的是明矾水解出氢
离子,溶液呈酸性,在酸性环境下,纤维素水解,使高分子链断裂,从而使纸张变脆易
破裂;
故选:B。
【点评】掌握物质的性质和用途的关系是正确解答本题的关键。
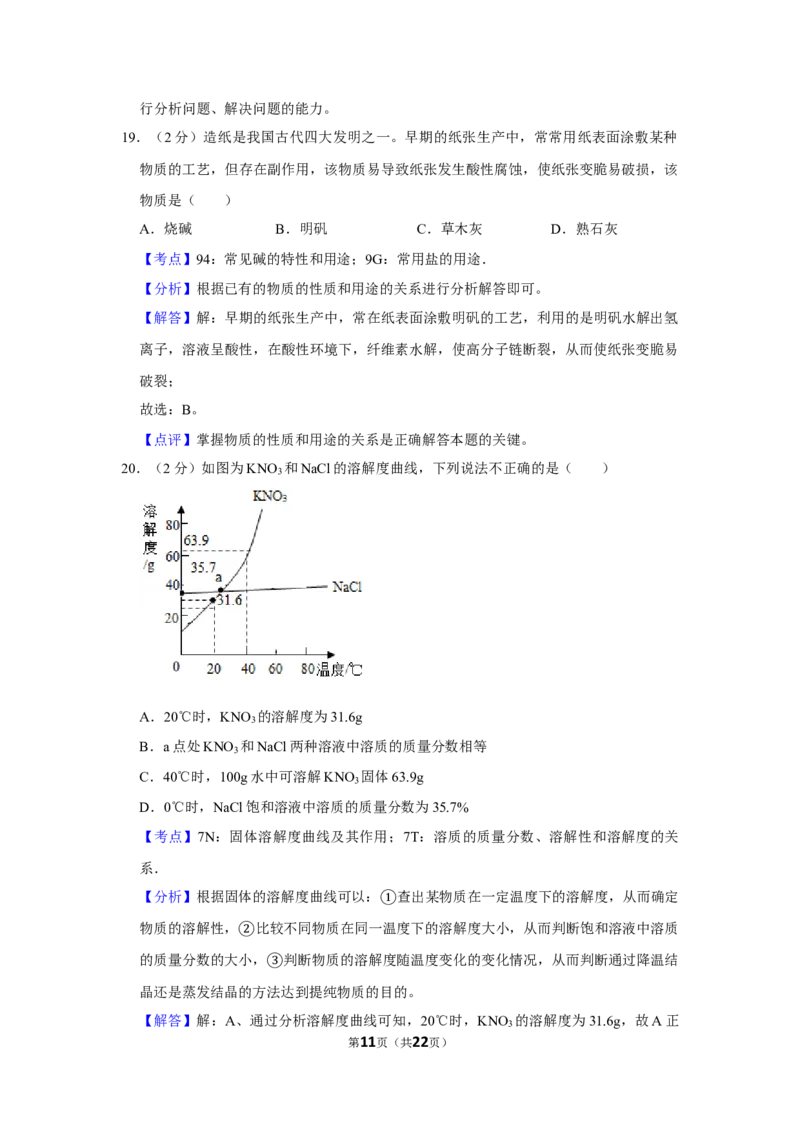
20.(2分)如图为KNO 和NaCl的溶解度曲线,下列说法不正确的是( )
3
A.20℃时,KNO 的溶解度为31.6g
3
B.a点处KNO 和NaCl两种溶液中溶质的质量分数相等
3
C.40℃时,100g水中可溶解KNO 固体63.9g
3
D.0℃时,NaCl饱和溶液中溶质的质量分数为35.7%
【考点】7N:固体溶解度曲线及其作用;7T:溶质的质量分数、溶解性和溶解度的关
系.
菁优网版权所有
【分析】根据固体的溶解度曲线可以: 查出某物质在一定温度下的溶解度,从而确定
物质的溶解性, 比较不同物质在同一①温度下的溶解度大小,从而判断饱和溶液中溶质
的质量分数的大小②, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结
晶还是蒸发结晶的方法③达到提纯物质的目的。
【解答】解:A、通过分析溶解度曲线可知,20℃时,KNO 的溶解度为31.6g,故A正
3
第11页(共22页)确;
B、a点处KNO 和NaCl两种物质的溶解度相等,所以a点处溶液中溶质的质量分数相
3
等,故B正确;
C、40℃时,硝酸钾的溶解度是63.9g,所以100g水中可溶解KNO 固体63.9g,故C正
3
确;
D、0℃时,氯化钠的溶解度是35.7g,所以NaCl饱和溶液中溶质的质量分数为
×100%≠35.7%,故D错误。
故选:D。
【点评】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体
的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
二、解答题(共3小题,满分8分)
21.(3分)纯净的二氧化硅是现代光学及光纤制品的基本原料。请回答下列问题:
(1)二氧化硅的化学性质很不活泼,氢氟酸(HF)是唯一可以与之发生反应的酸(生
成物为水和四氟化硅气体),该反应的化学方程式为 SiO +4HF = SiF ↑ +2H O 。
2 4 2
(2)二氧化硅与碳酸钙在高温下反应生成硅酸钙( CaSiO )和二氧化碳:在物质的分
3
类 单质 化合物 氧化物 酸 碱 盐中,硅酸钙属于 (填序号)。
【①考点】A②7:单质和③化合物的④判别⑤;A⑥9:常见的氧化物、酸、②碱⑥和盐的判别;G5:书
写化学方程式、文字表达式、电离方程式.
菁优网版权所有
【分析】(1)根据反应物和生成物书写化学方程式;
(2)根据物质的分类进行分析。
【解答】解:(1)二氧化硅和氢氟酸反应生成水和四氟化硅,化学方程式为:
SiO +4HF=SiF ↑+2H O;
2 4 2
(2)硅酸钙( CaSiO )由钙元素、硅元素和氧元素组成属于化合物;由钙离子和硅酸
3
根离子构成,属于盐。
故答案为:
(1)SiO +4HF=SiF ↑+2H O;
2 4 2
(2) 。
【点评②】⑥本题通过给出的信息,考查了化学方程式的书写和物质的分类,熟练掌握相应
的知识是解答此类题目的关键。
22.在探究金属活动性顺序时,华雪同学把两根绕成螺旋状的洁净铜丝分别浸入硫酸铝溶
第12页(共22页)液、硝酸银溶液中,过一会儿取出:
(1)铜丝浸入硫酸铝溶液中,可观察到的现象是: 无现象 。
(2)铜丝浸入硝酸银溶液中,可观察到铜丝上有 银白 色物质生成,溶液逐渐变成
蓝色。
(3)铜丝浸入硝酸银溶液中,离子数目减少的是 A g + ,离子数目增加的是 C u 2 +
。
(4)根据上述实验所观察到的现象,华雪同学 能 (填“能”或者“不能”)证明
铝、铜、银的金属活动性顺序Al>Cu>Ag
【考点】86:金属活动性顺序及其应用.
菁优网版权所有
【分析】根据金属活动性顺序的运用分析:在金属活动性顺序中,氢前的金属能与酸发
生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来。
【解答】解:(1)由于金属活动性铝大于铜,若把铜丝浸入硫酸铝溶液中,观察到无
明显现象,说明铜的金属活动性比铝弱;
在金属活动性顺序中,铜位于氢的后面,铜不能与稀硫酸发生置换反应;
(2)由于金属活动性铜大于银,将铜丝浸入硝酸银溶液中,生成硝酸铜溶液和银,铜
丝表面覆盖一层银白色物质,溶液由无色逐渐变成蓝色,
(3)铜丝浸入硝酸银溶液中,生成硝酸铜溶液和银,其中银离子得到电子转化为银原
子,铜原子失去电子转换为铜离子;
(4)根据铜丝浸入硫酸铝溶液中,无明显现象,说明金属活动性铝大于铜,铜丝浸入
硝酸银溶液中,铜丝表面覆盖一层银白色物质,溶液由无色逐渐变成蓝色,说明金属活
动性铜大于银,可得铝、铜、银的金属活动性顺序Al>Cu>Ag。
故答案为:(1)无现象;(2)银白;(3)Ag+;Cu2+;(4)能。
【点评】本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意
义以及金属活动性顺序进行。
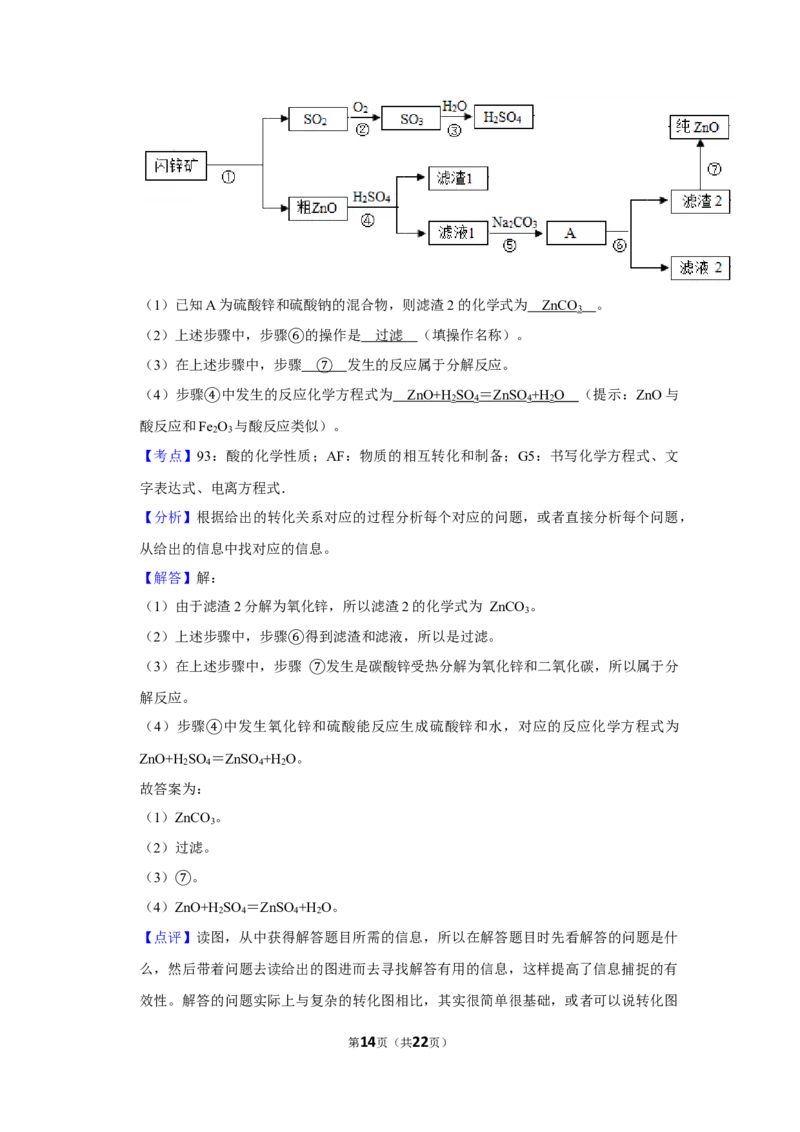
23.(5分)氧化锌软膏可用于急性或亚急性皮炎、湿疹、痱子及轻度、小面积的皮肤溃
疡。闪锌矿(主要成分为ZnS)是含锌的主要矿物质之一,高温煅烧闪锌矿生成氧化锌
和SO ,以氧化锌产品为原料制备纯氧化锌的生产工艺流程如图:
2
第13页(共22页)(1)已知A为硫酸锌和硫酸钠的混合物,则滤渣2的化学式为 ZnCO 。
3
(2)上述步骤中,步骤 的操作是 过滤 (填操作名称)。
(3)在上述步骤中,步⑥骤 发生的反应属于分解反应。
(4)步骤 中发生的反应化⑦学方程式为 ZnO+H
2
SO
4
= ZnSO
4
+H
2
O (提示:ZnO与
酸反应和F④e O 与酸反应类似)。
2 3
【考点】93:酸的化学性质;AF:物质的相互转化和制备;G5:书写化学方程式、文
字表达式、电离方程式.
菁优网版权所有
【分析】根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,
从给出的信息中找对应的信息。
【解答】解:
(1)由于滤渣2分解为氧化锌,所以滤渣2的化学式为 ZnCO 。
3
(2)上述步骤中,步骤 得到滤渣和滤液,所以是过滤。
(3)在上述步骤中,步⑥骤 发生是碳酸锌受热分解为氧化锌和二氧化碳,所以属于分
解反应。 ⑦
(4)步骤 中发生氧化锌和硫酸能反应生成硫酸锌和水,对应的反应化学方程式为
ZnO+H SO④=ZnSO +H O。
2 4 4 2
故答案为:
(1)ZnCO 。
3
(2)过滤。
(3) 。
(4)⑦ZnO+H
2
SO
4
=ZnSO
4
+H
2
O。
【点评】读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什
么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息捕捉的有
效性。解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图
第14页(共22页)提供的是情境,考查基本知识。
三、解答题(2小题,共10分)
24.(4分)请用所学的知识回答下列问题:
(1)量取液体时,如果视线没有与量筒内无色液体凹液面的最低处保持水平,而是采
用俯视的方法,将会对读数产生什么影响?
(2)为什么菜刀、镰刀、锤子等用铁制而不是铝制?
【考点】42:测量容器﹣量筒;82:金属的物理性质及用途.
菁优网版权所有
【分析】根据已有的量筒的使用方法以及金属的性质进行分析解答即可。
【解答】解:(1)量取液体时,如果视线没有与量筒内无色液体凹液面的最低处保持
水平,而是采用俯视的方法,则会使读数偏大,故填:偏大;
(2)菜刀、镰刀、锤子等用铁制而不是铝制,是因为铁的硬度大于铝,故填:铁的硬
度比铝大。
【点评】本题考查的是常见的仪器的使用以及金属的性质,完成此题,可以依据已有的
知识进行。
25.(6分)在汽油中加入适量的乙醇(C H OH)作为汽车燃料(车用乙醇汽油),可适
2 5
当节省石油资源,并在一定程度上减少汽车尾气的污染。请回答下列问题:
(1)乙醇完全燃烧的化学方程式为 C H OH+3O 2CO +3H O 。
2 5 2 2 2
(2)二氧化碳和水在一定条件下可发生反应,若反应属于化合反应,则在反应后的溶
液中滴加紫色石蕊溶液,溶液呈 红 色:若反应生成了葡萄糖,则反应条件为 光照
。
(3)C H OH在物质的分类上属于 AD 。
2 5
A.化合物 B.氧化物 C.碱 D.有机物
(4)甲醇(CH OH)与乙醇 不属于 (填“属于”或“不属于”)同一种物质。
3
【考点】A7:单质和化合物的判别;A9:常见的氧化物、酸、碱和盐的判别;AB:甲
烷、乙醇等常见有机物的性质和用途;AC:有机物与无机物的区别;G5:书写化学方
程式、文字表达式、电离方程式.
菁优网版权所有
【分析】(1)根据乙醇完全燃烧生成二氧化碳和水进行解答;
(2)根据二氧化碳和水在不同条件下的反应分析;
(3)根据有机物的概念分析;
(4)根据物质的构成分析。
第15页(共22页)【解答】解:(1)乙醇完全燃烧生成二氧化碳和水,反应的化学方程式为:
C H OH+3O 2CO +3H O;
2 5 2 2 2
(2)常温下,二氧化碳和水可以化合生成碳酸,碳酸溶液显酸性,可使紫色石蕊溶液
变红色;同时绿色植物也可以在光照下,利用二氧化碳和水合成葡萄糖同时放出氧气;
(3)C H OH是含碳的化合物,属于有机物;
2 5
(4)甲醇(CH OH)与乙醇,用不同化学式表示,其构成不同,属于不同物质。
3
故答案为:(1)C H OH+3O 2CO +3H O;(2)红;光照;(3)AD;(4)
2 5 2 2 2
不属于。
【点评】此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基
础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力。解题时需要认真
分析题目给出的条件,联系实际,逐一分析推断。
四、实验探究题(2小题,共18分)
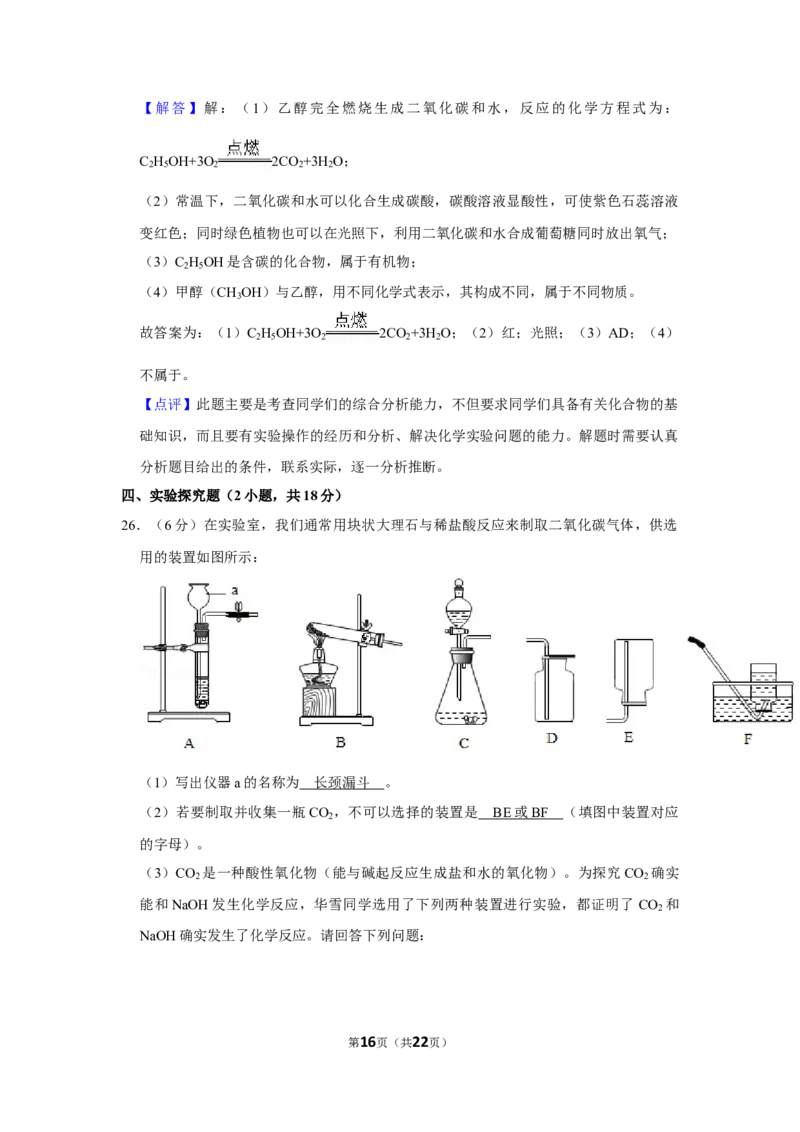
26.(6分)在实验室,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选
用的装置如图所示:
(1)写出仪器a的名称为 长颈漏斗 。
(2)若要制取并收集一瓶CO ,不可以选择的装置是 BE 或 BF (填图中装置对应
2
的字母)。
(3)CO 是一种酸性氧化物(能与碱起反应生成盐和水的氧化物)。为探究CO 确实
2 2
能和NaOH发生化学反应,华雪同学选用了下列两种装置进行实验,都证明了 CO 和
2
NaOH确实发生了化学反应。请回答下列问题:
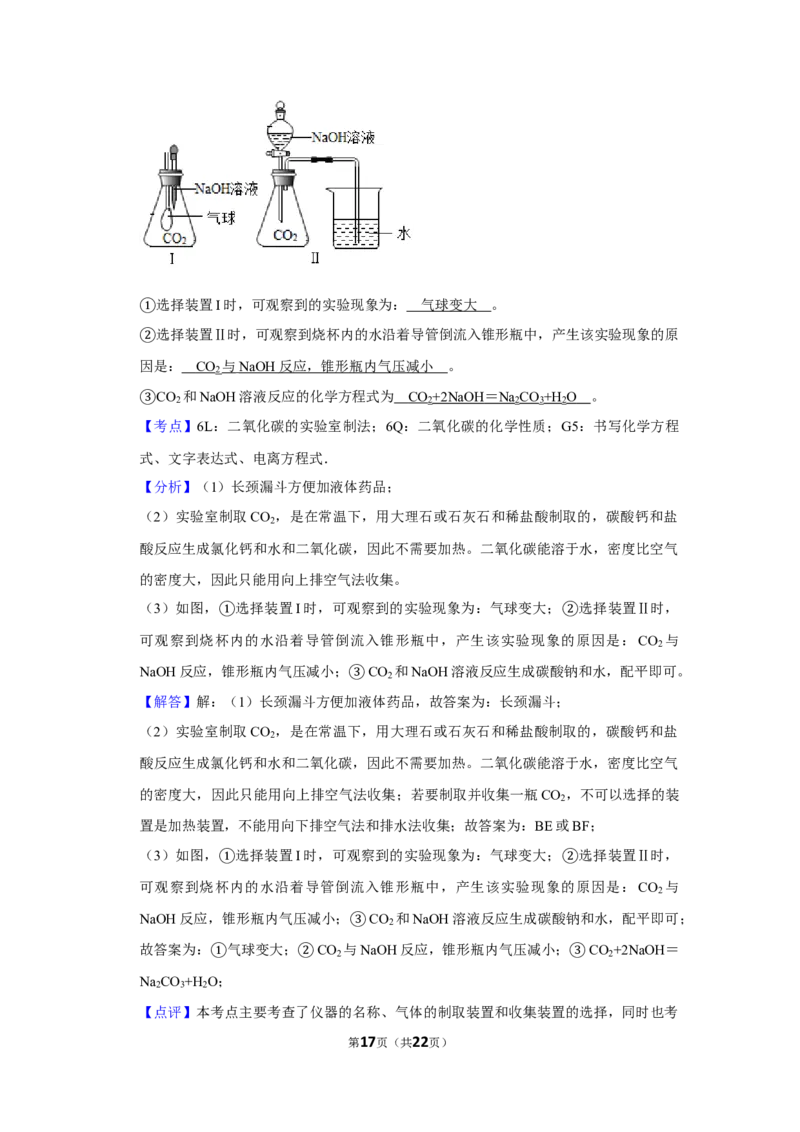
第16页(共22页)选择装置I时,可观察到的实验现象为: 气球变大 。
①选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原
②因是: CO 与 NaOH 反应,锥形瓶内气压减小 。
2
CO 和NaOH溶液反应的化学方程式为 CO +2NaOH = Na CO +H O 。
2 2 2 3 2
③【考点】6L:二氧化碳的实验室制法;6Q:二氧化碳的化学性质;G5:书写化学方程
式、文字表达式、电离方程式.
菁优网版权所有
【分析】(1)长颈漏斗方便加液体药品;
(2)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐
2
酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气
的密度大,因此只能用向上排空气法收集。
(3)如图, 选择装置I时,可观察到的实验现象为:气球变大; 选择装置Ⅱ时,
可观察到烧杯①内的水沿着导管倒流入锥形瓶中,产生该实验现象的②原因是:CO 与
2
NaOH反应,锥形瓶内气压减小; CO 和NaOH溶液反应生成碳酸钠和水,配平即可。
2
【解答】解:(1)长颈漏斗方便加③液体药品,故答案为:长颈漏斗;
(2)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐
2
酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶于水,密度比空气
的密度大,因此只能用向上排空气法收集;若要制取并收集一瓶CO ,不可以选择的装
2
置是加热装置,不能用向下排空气法和排水法收集;故答案为:BE或BF;
(3)如图, 选择装置I时,可观察到的实验现象为:气球变大; 选择装置Ⅱ时,
可观察到烧杯①内的水沿着导管倒流入锥形瓶中,产生该实验现象的②原因是:CO 与
2
NaOH反应,锥形瓶内气压减小; CO 和NaOH溶液反应生成碳酸钠和水,配平即可;
2
故答案为: 气球变大; CO 与③NaOH反应,锥形瓶内气压减小; CO +2NaOH=
2 2
Na CO +H O①; ② ③
2 3 2
【点评】本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考
第17页(共22页)查了化学方程式的书写、实验探究等,综合性比较强。气体的制取装置的选择与反应物
的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关。本考点
是中考的重要考点之一,主要出现在实验题中。
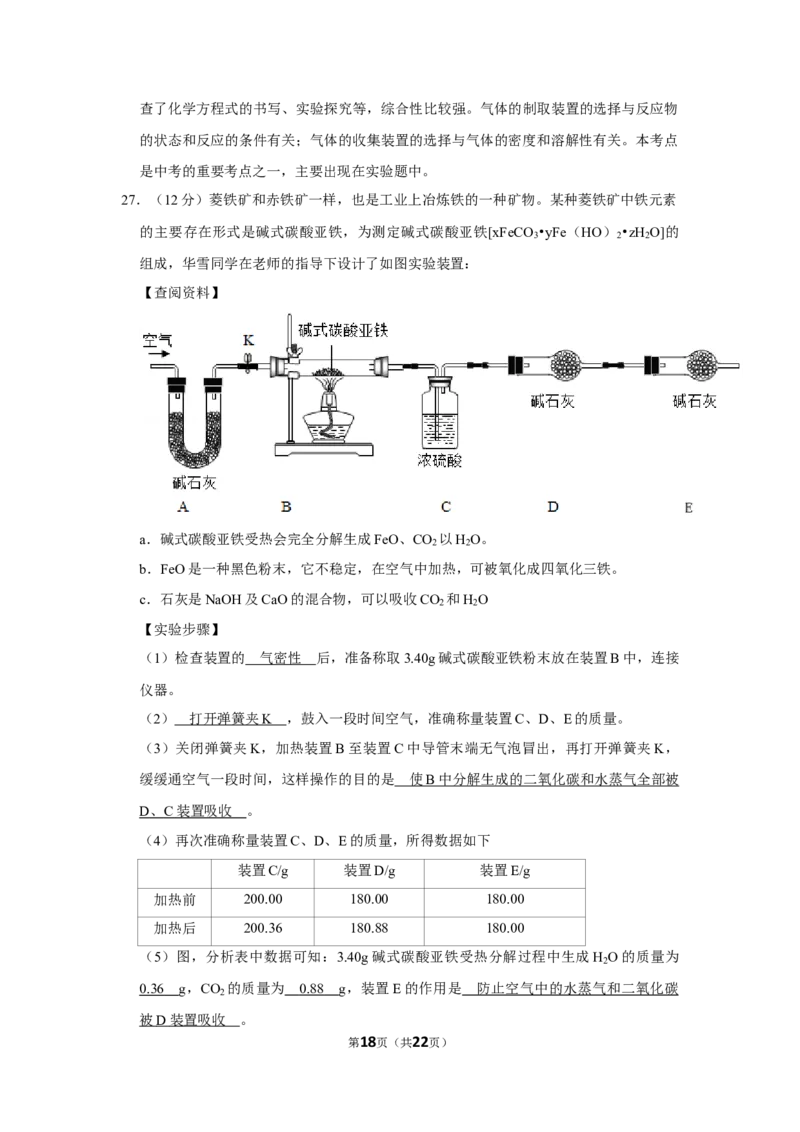
27.(12分)菱铁矿和赤铁矿一样,也是工业上冶炼铁的一种矿物。某种菱铁矿中铁元素
的主要存在形式是碱式碳酸亚铁,为测定碱式碳酸亚铁[xFeCO •yFe(HO) •zH O]的
3 2 2
组成,华雪同学在老师的指导下设计了如图实验装置:
【查阅资料】
a.碱式碳酸亚铁受热会完全分解生成FeO、CO 以H O。
2 2
b.FeO是一种黑色粉末,它不稳定,在空气中加热,可被氧化成四氧化三铁。
c.石灰是NaOH及CaO的混合物,可以吸收CO 和H O
2 2
【实验步骤】
(1)检查装置的 气密性 后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接
仪器。
(2) 打开弹簧夹 K ,鼓入一段时间空气,准确称量装置C、D、E的质量。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,
缓缓通空气一段时间,这样操作的目的是 使 B 中分解生成的二氧化碳和水蒸气全部被
D 、 C 装置吸收 。
(4)再次准确称量装置C、D、E的质量,所得数据如下
装置C/g 装置D/g 装置E/g
加热前 200.00 180.00 180.00
加热后 200.36 180.88 180.00
(5)图,分析表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成H O的质量为
2
0.36 g,CO 的质量为 0.88 g,装置E的作用是 防止空气中的水蒸气和二氧化碳
2
被 D 装置吸收 。
第18页(共22页)【实验结论】
在xFeCO •yFe(HO) •zH O中,氢原子与氧原子的个数之比为 4 : 9 。
3 2 2
【实验反思】
(1)装置A的作用是 除去空气中的水和二氧化碳 。
(2)实验结束后,装置B中的残留固体可能全部是FeO.也可能全部是Fe O .还可能
3 4
是 FeO 、 F e O 。
3 4
(3)为了得到装置B中残留固体的组成,华雪同学称得装置B中残留固体质量为2.24g
后,通过计算可知:残留固体的组成及各成分的质量为 FeO 和 F e O 质量分别为 1.08 g
3 4
和 1.16 g 。
【考点】2G:实验探究物质的组成成分以及含量;4Q:常见气体的检验与除杂方法.
菁优网版权所有
【分析】碱石灰能够吸收水蒸气和二氧化碳,浓硫酸能够吸收水蒸气;
CD装置增大的质量分别是反应生成水的质量和二氧化碳的质量;
氧化亚铁和氧气反应生成四氧化三铁;
反应前后元素种类、原子总个数和质量都不变。
【解答】解:【实验步骤】
(1)检查装置的气密性后,准备称取3.40g碱式碳酸亚铁粉末放在装置B中,连接仪器。
故填:气密性。
(2)打开弹簧夹K,鼓入一段时间空气,准确称量装置C、D、E的质量。
故填:打开弹簧夹K。
(3)关闭弹簧夹K,加热装置B至装置C中导管末端无气泡冒出,再打开弹簧夹K,
缓缓通空气一段时间,这样操作的目的是使 B中分解生成的二氧化碳和水蒸气全部被
D、C装置吸收。
故填:使B中分解生成的二氧化碳和水蒸气全部被D、C装置吸收。
(4)再次准确称量装置C、D、E的质量,所得数据如下
(5)分析表中数据可知:3.40g碱式碳酸亚铁受热分解过程中生成 H O的质量为:
2
200.36g﹣200.00g=0.36g,CO 的质量为:180.88g﹣180.00g=0.88g,装置E的作用是
2
防止空气中的水蒸气和二氧化碳被D装置吸收。
故填:0.36;0.88;防止空气中的水蒸气和二氧化碳被D装置吸收。
【实验结论】
在 xFeCO •yFe(HO) •zH O 中,氢元素质量:0.36g× =0.04g,氧元素质量:
3 2 2
第19页(共22页)(0.36g﹣0.04g)+0.88g× +(3.40g﹣0.36g﹣0.88g)× =1.44g,氢原子与氧原子的
个数之比为: : =4:9。
故填:4:9。
【实验反思】
(1)装置A的作用是除去空气中的水和二氧化碳。
故填:除去空气中的水和二氧化碳。
(2)实验结束后,装置B中的残留固体可能全部是FeO,也可能全部是Fe O .还可能
3 4
是FeO、Fe O 。
3 4
故填:FeO、Fe O 。
3 4
(3)如果残留固体是氧化亚铁,则氧化亚铁质量:3.40g﹣0.36g﹣0.88g=2.16g,
如果残留固体是四氧化三铁,则四氧化三铁质量:2.16g× ÷ =2.32g,
称得装置B中残留固体质量为2.24g,大于2.16g,小于2.32g,通过计算可知:残留固
体是氧化亚铁和四氧化三铁的混合物;
设氧化亚铁质量为x,则四氧化三铁质量为2.24g﹣x,
根据题意有:x× +(2.24g﹣x)× =2.16g× ,
x=1.08g,则四氧化三铁质量:2.24g﹣1.08g=1.16g,
故填:FeO和Fe O 质量分别为1.08g和1.16g。
3 4
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进
行分析、判断,从而得出正确的结论。
五、计算题(2小题,共10分)
28.(4分)超市购物小票上含有BPA(双酚A),网上流传消费者接触小票会致癌。我
国规定:超市购物小票上双酚A的含量应不超过0.6mg/Kg.按照这个标准,收银员即
使每天接触小票10个小时,双酚A通过接触进入人体的量也不会比安全剂量低几十倍。
因此,普通消费者一天接触几张购物小票,致癌概率是完全可以忽略不计的。
(1)双酚A的化学式为C H O ,其相对分子质量为 22 8 。
15 16 2
(2)若每张超市购物小票的质量为 5g,则其中含有双酚A的质量应不能超过 0.003
mg才能符合国家标准。
【考点】D8:相对分子质量的概念及其计算.
菁优网版权所有
第20页(共22页)【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析
解答。
(2)超市购物小票上双酚A的含量应不超过0.6mg/Kg,进行分析解答。
【解答】解:(1)双酚A的相对分子质量为12×15+1×16+16×2=228。
(2)超市购物小票上双酚A的含量应不超过0.6mg/Kg,若每张超市购物小票的质量为
5g,则其中含有双酚A的质量应不能超过 0.6mg=0.003mg。
故答案为:
(1)228;
(2)0.003。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析
问题、解决问题的能力。
29.(6分)在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁
钉用砂纸打磨干净后在天平上称得质量为 56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉
一起放在天平上称量,记录所称得质量m .将上述铁钉浸到硫酸铜溶液中,待反应一
1
段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质
量为m 。
2
(1)m = m (填“>”或“=”或“<”)。
1 2
(2)锥形瓶的质量为 m ﹣ 136 g (或 m ﹣ 136 g ) (用含m 或m 的代数式表示)。
1 2 1 2
(3)若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。
【考点】G6:根据化学反应方程式的计算.
菁优网版权所有
【分析】铁和硫酸铜反应生成硫酸亚铁和铜,根据反应的化学方程式及其提供的数据可
以进行相关方面的计算。
【解答】解:(1)m =m 。
1 2
故填:=。
(2)锥形瓶的质量为:m ﹣(56.0g+80.0g)=m ﹣136g,或m ﹣(56.0g+80.0g)=m
1 1 2 2
﹣136g,
故填:m ﹣136g(或m ﹣136g)。
1 2
(3)设反应的铁的质量为x,生成铜质量为y,
Fe+CuSO ═FeSO +Cu,
4 4
56 160 64
第21页(共22页)x 80.0g×10% y
= = ,
x=2.8g,y=3.2g,
若硫酸铜反应完全,此时所得溶液的质量:80.0g+2.8g﹣3.2g=79.6g,
答:若硫酸铜反应完全,此时所得溶液的质量是79.6g。
【点评】本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要
注意规范性和准确性。
声明:试题解析著作权属菁优网所有,未经书面同意,不得复制发布
日期:2019/12/22 10:57:25;用户:初中化学;邮箱:hx0123@xyh.com;学号:30177334
第22页(共22页)