文档内容
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
2023-2024 学年九年级化学上学期第一次月考卷(北京专用)
(本卷共39小题,满分70分,考试用时70分钟)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
第一部分(选择题,共25分)
本部分共25题,每题1分,共25分。在每题列出的四个选项中,选出最符合题目要求的一
项。
1.下列物质的性质,属于化学性质的是
A.颜色 B.密度 C.可燃性 D.导电性
2.下列物质的用途中,利用物理性质的是
A.氧气用于气焊 B.干冰用于人工降雨
C.氮气用作保护气 D.铁矿石用于炼铁
3.下列变化中,属于化学变化的是
A.矿石粉碎 B.纸张燃烧 C.酒精挥发 D.冰雪融化
4. 下列氧气的性质中,属于化学性质的是
A. 无色无味 B. 沸点低 C. 能支持燃烧 D. 密度比空气大
5. 空气中氮气的体积分数约为
A. 21% B. 0.94% C. 0.03% D. 78%
6.下列气体中,能供给动植物呼吸的是
A.H B.O C.N D.CO
2 2 2 2
7. 下列方法能区分氮气和二氧化碳两瓶气体的是
A. 闻气味 B. 观察颜色
C. 倒入适量澄清的石灰水 D. 将燃着的木条伸入集气瓶中
8.能使带火星的木条复燃的气体是
A.空气 B.氧气 C.氮气 D.二氧化碳
9.用如图装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后进行后续操作。下列说法正确的
是
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
A.所用红磷要过量,以保证集气瓶内空气里的氧气能充分反应
B.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡胶塞
C.该实验可以测得氧气占空气体积的21%
D.仍用本装置,把红磷换成硫,能更精确测定空气里氧气的含量
10. 下列气体中,都被计入空气污染指数项目的是
A. 二氧化硫、二氧化氮、一氧化碳 B. 二氧化硫、二氧化氮、氮气
C. 二氧化硫、一氧化碳、氧气 D. 二氧化碳、二氧化硫、臭氧
11. 有关空气的叙述中,正确的是( )
A. 空气中的氧气具有可燃性,可用作火箭燃料
B. 化工厂废气及汽车尾气,不会造成空气污染
C. 稀有气体有广泛的用途,可制成多种用途的电光源
D. 空气中的氮气与氧气体积比约为5:1
12.下列物质属于纯净物的是
A.雪碧 B.牛奶 C.干冰 D.食醋
13.下列物质属于氧化物的是
A.O B.HSO C.CaO D.ZnCl
2 2 4 2
14.下列物质在氧气中燃烧,火星四射、生成黑色固体的是
A.木炭 B.铁丝 C.蜡烛 D.红磷
15.下列物质在氧气中燃烧,产生大量白烟的是
A.木炭 B.铁丝 C.酒精 D.红磷
16. 用过氧化氢溶液制取氧气时,若忘记加二氧化锰,其结果是
A. 不放出氧气 B. 放出的氧气不纯
C. 放出氧气的总量会减少 D. 放出氧气的速率慢
17. 下列实验现象的描述中,正确的是
A. 碳在空气中燃烧,放热,发出白光
B. 红磷燃烧,放热,生成大量白雾
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
C. 硫在空气中燃烧时,发出淡蓝色火焰,放热,生成无色有刺激性气味的气体
D. 向胆矾(硫酸铜)溶液中加入氢氧化钠溶液,产生氢氧化铜沉淀
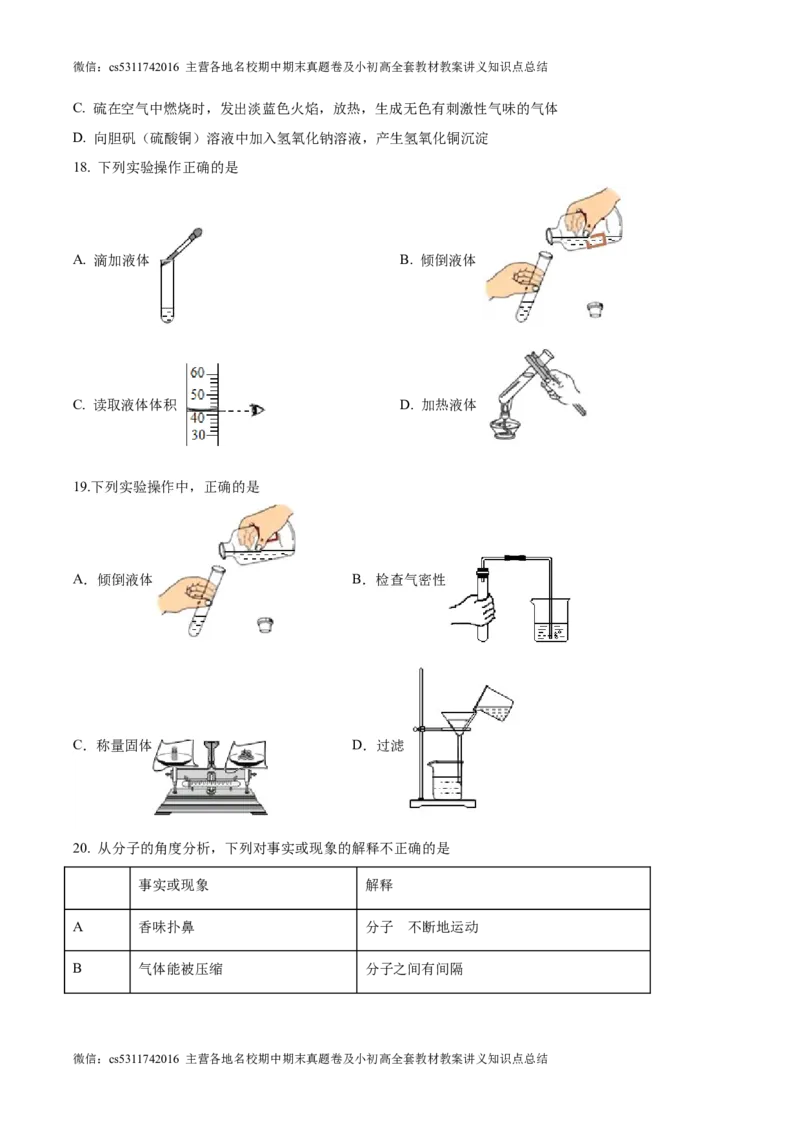
18. 下列实验操作正确的是
A. 滴加液体 B. 倾倒液体
C. 读取液体体积 D. 加热液体
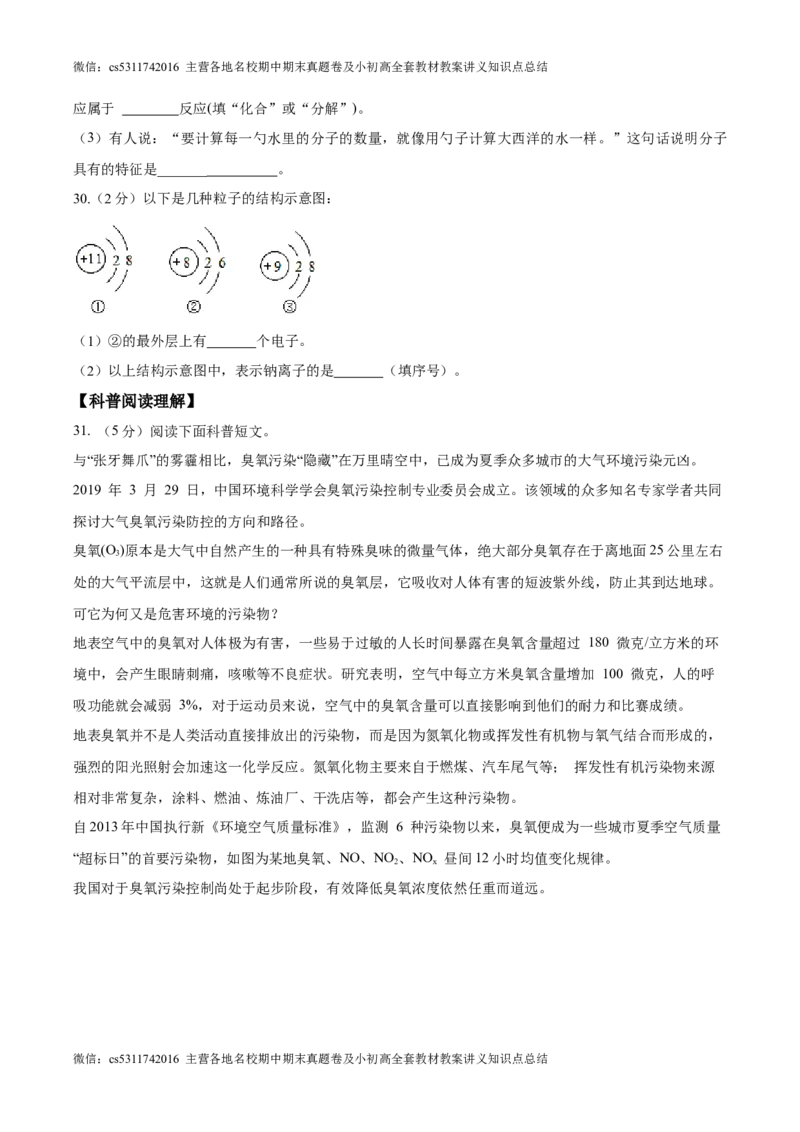
19.下列实验操作中,正确的是
A.倾倒液体 B.检查气密性
C.称量固体 D.过滤
20. 从分子的角度分析,下列对事实或现象的解释不正确的是
事实或现象 解释
A 香味扑鼻 分子 在不断地运动
B 气体能被压缩 分子之间有间隔
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
C 热胀冷缩 分子的大小随温度的改变而改变
D 过氧化氢分解生成水和氧气 分子可以分成原子原子再重新构成新分子
21.如图进行实验。当观察到热水大面积变成红色时,冷水中只有品红周围变成红色。该实验可以得到的结
论是
A.分子的质量很小 B.分子的大小与温度有关
C.分子由原子构成 D.分子运动速率与温度有关
22.已知一种氧原子,原子核内含有8个质子和10个中子,则该氧原子核外电子数为
A.18 B.10 C.2 D.8
23.嫦娥五号从月球带回的月壤样品向公众展出。月壤中存在着大量的3He,有望成为未来的清洁能源。3He
原子内质子数为2,中子数为1,核外电子数为
A.1 B.2 C.3 D.4
24.6000L氧气在加压的情况下可装入容积为40L的钢瓶中,是因为气体分子( )
A.质量变小 B.间隔变小 C.体积变小 D.个数变少
25.三月的田东,漫山芒果花开,阵阵清香沁人心脾,能闻到花香的原因是
A.分子很小 B.分子不断运动
C.分子间有间隔 D.分子由原子构成
第二部分
本部分共11题,共45分。
【生活现象解释】
26. (5分)空气是一种宝贵的资源,例如,
(1)夜幕降临的城市里,五彩缤纷的霓虹灯闪烁,往往在霓虹灯中充入某些气体,这些气体通电时能发
出不同颜色的光,这些气体是_______;
(2)在食品包装中充入氮气可以防腐,这利用了氮气_______的性质。
(3)下表为北京市某监测点监测到的空气质量。依据表格回答问题:
污染项目 PM PM SO CO NO
2.5 10 2 2
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
污染指数 69 95 9 0.8 42
①首要污染物是___________;其中会形成酸雨的是___________(填1种即可)。
②上图为一款新型环保车,可通过360°旋转的“大炮筒”向四周喷水,从而缓解极端恶劣天气给人带来的
不适。这款环保车喷水的作用是________。
27. (2分)进入地窖或深井前,需用燃着的蜡烛做烛火实验,如图所示。
(1)若蜡烛熄灭,说明地窖或深井中氧气含量 ________ (填“高于”或“低于”)空气。
(2)从氧气性质的角度,分析进入地窖或深井前需要做烛火实验的原因: __________ 。
28.(2分)化学是造福人类的科学,在生产生活中做出了重大贡献。一氧化二氮(NO)是人类最早应用
2
于医疗的麻醉剂之一。
①一氧化二氮属于____________(填“混合物”或“纯净物”)。
②下列信息中,描述了一氧化二氮化学性质的是_________(填字母序号)。
A. 无色有甜味的气体
B. 在高温下能分解生成氮气和氧气
C. 熔点-90.8℃,沸点-88.5℃
29.(5分)物质都是由微观粒子构成的。在构成下列四种物质的微粒示意图中,“ ”和 分别表示氢原
子和氧原子。
物质 甲 乙 丙 丁
构成该物质的粒子
(1)甲物质的一个分子中含有_______个原子。写出乙的化学式_______。
(2)乙物质在一定条件下反应可生成丙和丁,该反应的文字表达式为 ,该反
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
应属于 反应(填“化合”或“分解”)。
(3)有人说:“要计算每一勺水里的分子的数量,就像用勺子计算大西洋的水一样。”这句话说明分子
具有的特征是_______ 。
30.(2分)以下是几种粒子的结构示意图:
(1)②的最外层上有 个电子。
(2)以上结构示意图中,表示钠离子的是 (填序号)。
【科普阅读理解】
31. (5分)阅读下面科普短文。
与“张牙舞爪”的雾霾相比,臭氧污染“隐藏”在万里晴空中,已成为夏季众多城市的大气环境污染元凶。
2019 年 3 月 29 日,中国环境科学学会臭氧污染控制专业委员会成立。该领域的众多知名专家学者共同
探讨大气臭氧污染防控的方向和路径。
臭氧(O )原本是大气中自然产生的一种具有特殊臭味的微量气体,绝大部分臭氧存在于离地面25公里左右
3
处的大气平流层中,这就是人们通常所说的臭氧层,它吸收对人体有害的短波紫外线,防止其到达地球。
可它为何又是危害环境的污染物?
地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过 180 微克/立方米的环
境中,会产生眼睛刺痛,咳嗽等不良症状。研究表明,空气中每立方米臭氧含量增加 100 微克,人的呼
吸功能就会减弱 3%,对于运动员来说,空气中的臭氧含量可以直接影响到他们的耐力和比赛成绩。
地表臭氧并不是人类活动直接排放出的污染物,而是因为氮氧化物或挥发性有机物与氧气结合而形成的,
强烈的阳光照射会加速这一化学反应。氮氧化物主要来自于燃煤、汽车尾气等; 挥发性有机污染物来源
相对非常复杂,涂料、燃油、炼油厂、干洗店等,都会产生这种污染物。
自2013年中国执行新《环境空气质量标准》,监测 6 种污染物以来,臭氧便成为一些城市夏季空气质量
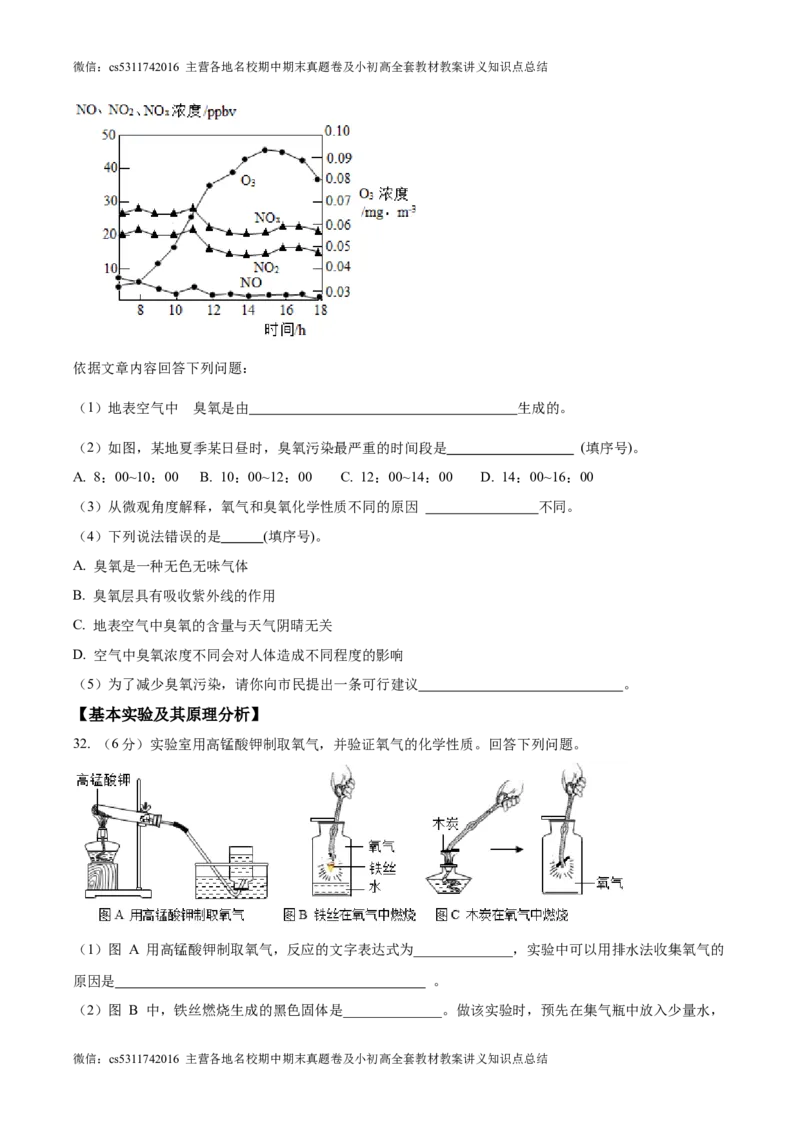
“超标日”的首要污染物,如图为某地臭氧、NO、NO 、NO 昼间12小时均值变化规律。
2 x
我国对于臭氧污染控制尚处于起步阶段,有效降低臭氧浓度依然任重而道远。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
依据文章内容回答下列问题:
的
(1)地表空气中 臭氧是由 生成的。
(2)如图,某地夏季某日昼时,臭氧污染最严重的时间段是 (填序号)。
A. 8:00~10:00 B. 10:00~12:00 C. 12:00~14:00 D. 14:00~16:00
(3)从微观角度解释,氧气和臭氧化学性质不同的原因 不同。
(4)下列说法错误的是 (填序号)。
A. 臭氧是一种无色无味气体
B. 臭氧层具有吸收紫外线的作用
C. 地表空气中臭氧的含量与天气阴晴无关
D. 空气中臭氧浓度不同会对人体造成不同程度的影响
(5)为了减少臭氧污染,请你向市民提出一条可行建议 。
【基本实验及其原理分析】
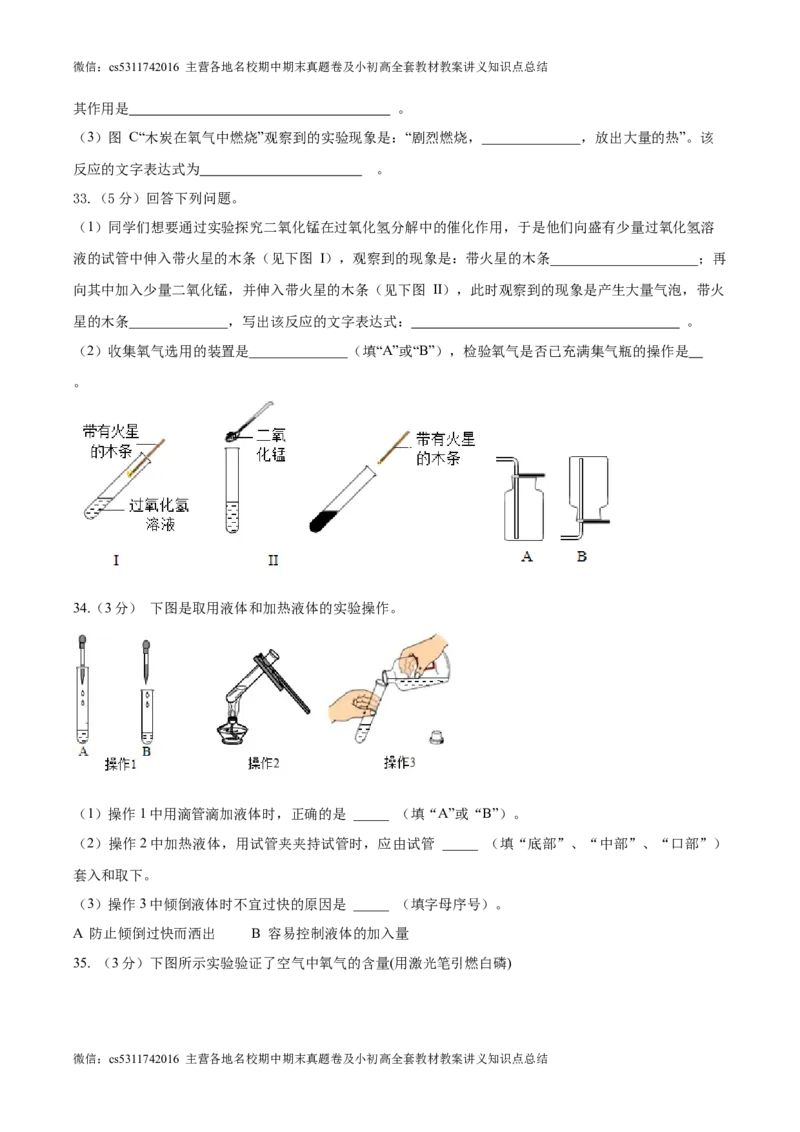
32. (6分)实验室用高锰酸钾制取氧气,并验证氧气的化学性质。回答下列问题。
(1)图 A 用高锰酸钾制取氧气,反应的文字表达式为______________,实验中可以用排水法收集氧气的
原因是 。
(2)图 B 中,铁丝燃烧生成的黑色固体是______________。做该实验时,预先在集气瓶中放入少量水,
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
其作用是 。
(3)图 C“木炭在氧气中燃烧”观察到的实验现象是:“剧烈燃烧,______________,放出大量的热”。该
反应的文字表达式为 。
33.(5分)回答下列问题。
(1)同学们想要通过实验探究二氧化锰在过氧化氢分解中的催化作用,于是他们向盛有少量过氧化氢溶
液的试管中伸入带火星的木条(见下图 I),观察到的现象是:带火星的木条_____________________;再
向其中加入少量二氧化锰,并伸入带火星的木条(见下图 II),此时观察到的现象是产生大量气泡,带火
星的木条______________,写出该反应的文字表达式: 。
(2)收集氧气选用的装置是______________(填“A”或“B”),检验氧气是否已充满集气瓶的操作是
。
34.(3分) 下图是取用液体和加热液体的实验操作。
(1)操作1中用滴管滴加液体时,正确的是 _____ (填“A”或“B”)。
(2)操作2中加热液体,用试管夹夹持试管时,应由试管 _____ (填“底部”、“中部”、“口部”)
套入和取下。
(3)操作3中倾倒液体时不宜过快的原因是 _____ (填字母序号)。
A 防止倾倒过快而洒出 B 容易控制液体的加入量
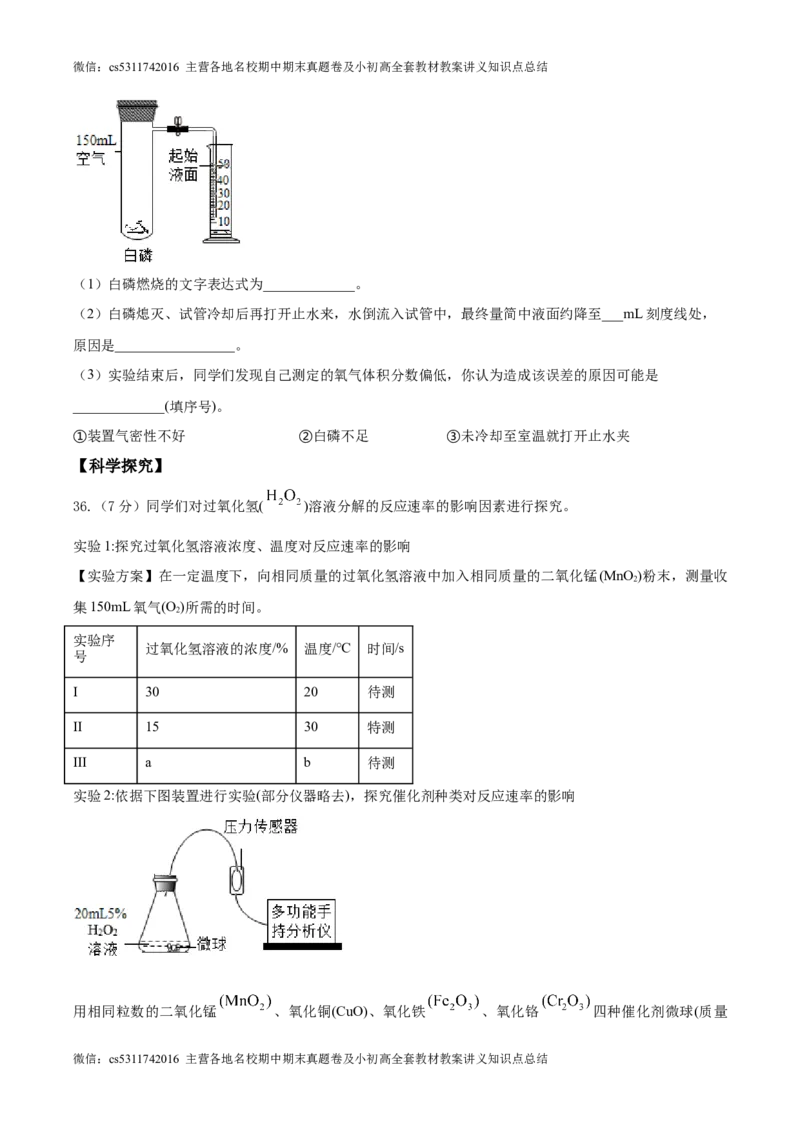
35. (3分)下图所示实验验证了空气中氧气的含量(用激光笔引燃白磷)
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
(1)白磷燃烧的文字表达式为_____________。
(2)白磷熄灭、试管冷却后再打开止水来,水倒流入试管中,最终量简中液面约降至___mL刻度线处,
原因是_________________。
(3)实验结束后,同学们发现自己测定的氧气体积分数偏低,你认为造成该误差的原因可能是
_____________(填序号)。
①装置气密性不好 ②白磷不足 ③未冷却至室温就打开止水夹
【科学探究】
36.(7分)同学们对过氧化氢( )溶液分解的反应速率的影响因素进行探究。
实验1:探究过氧化氢溶液浓度、温度对反应速率的影响
【实验方案】在一定温度下,向相同质量的过氧化氢溶液中加入相同质量的二氧化锰(MnO )粉末,测量收
2
集150mL氧气(O )所需的时间。
2
实验序
过氧化氢溶液的浓度/% 温度/℃ 时间/s
号
I 30 20 待测
Ⅱ 15 30 特测
Ⅲ a b 待测
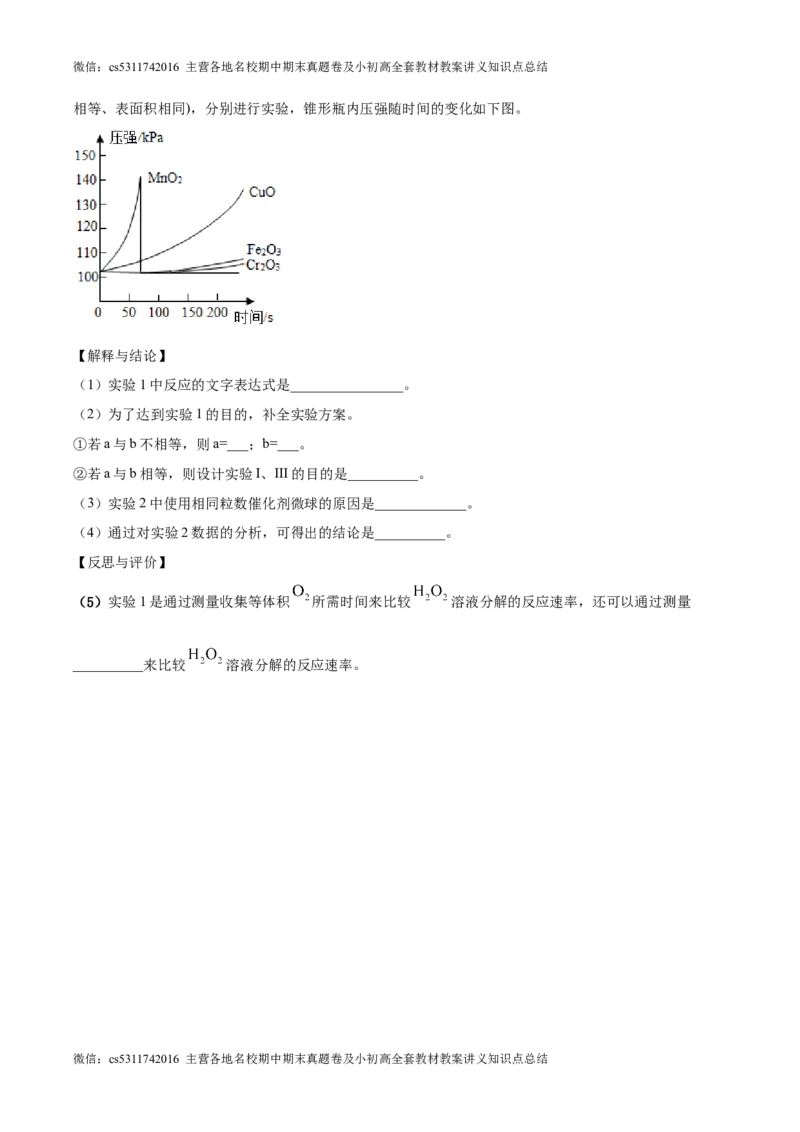
实验2:依据下图装置进行实验(部分仪器略去),探究催化剂种类对反应速率的影响
用相同粒数的二氧化锰 、氧化铜(CuO)、氧化铁 、氧化铬 四种催化剂微球(质量
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结
相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如下图。
【解释与结论】
(1)实验1中反应的文字表达式是________________。
(2)为了达到实验1的目的,补全实验方案。
①若a与b不相等,则a=___;b=___。
②若a与b相等,则设计实验I、III的目的是__________。
(3)实验2中使用相同粒数催化剂微球的原因是_____________。
(4)通过对实验2数据的分析,可得出的结论是__________。
【反思与评价】
(5)实验1是通过测量收集等体积 所需时间来比较 溶液分解的反应速率,还可以通过测量
__________来比较 溶液分解的反应速率。
微信:cs5311742016 主营各地名校期中期末真题卷及小初高全套教材教案讲义知识点总结