文档内容
考前特训
情境题专练
(一)关注碳中和,推进碳达峰
[分值:50分]
(选择题1~3题,每小题4分,4~7题,每小题6分,共36分)
1.为了2030年实现碳达峰和2060年实现碳中和,“十四五”期间生态环境与资源综合利用发展途径对
煤炭行业高质量发展具有重要意义。下列相关说法错误的是( )
A.开发煤炭废弃资源的高值、高效利用技术能降低二次污染
B.煤的综合利用有利于保护自然环境和社会的可持续发展
C.向煤中加入适量碳酸钙可减少燃烧产物中二氧化碳的量
D.利用太阳能等清洁能源代替煤炭,有利于节约资源、保护环境
答案 C
解析 煤中加入适量碳酸钙,可达到钙基固硫的作用,减少燃烧产物中二氧化硫的量,但不能减少二氧化
碳的排放量,故C错误。
2.我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对于改善环境、实现绿色发展至关
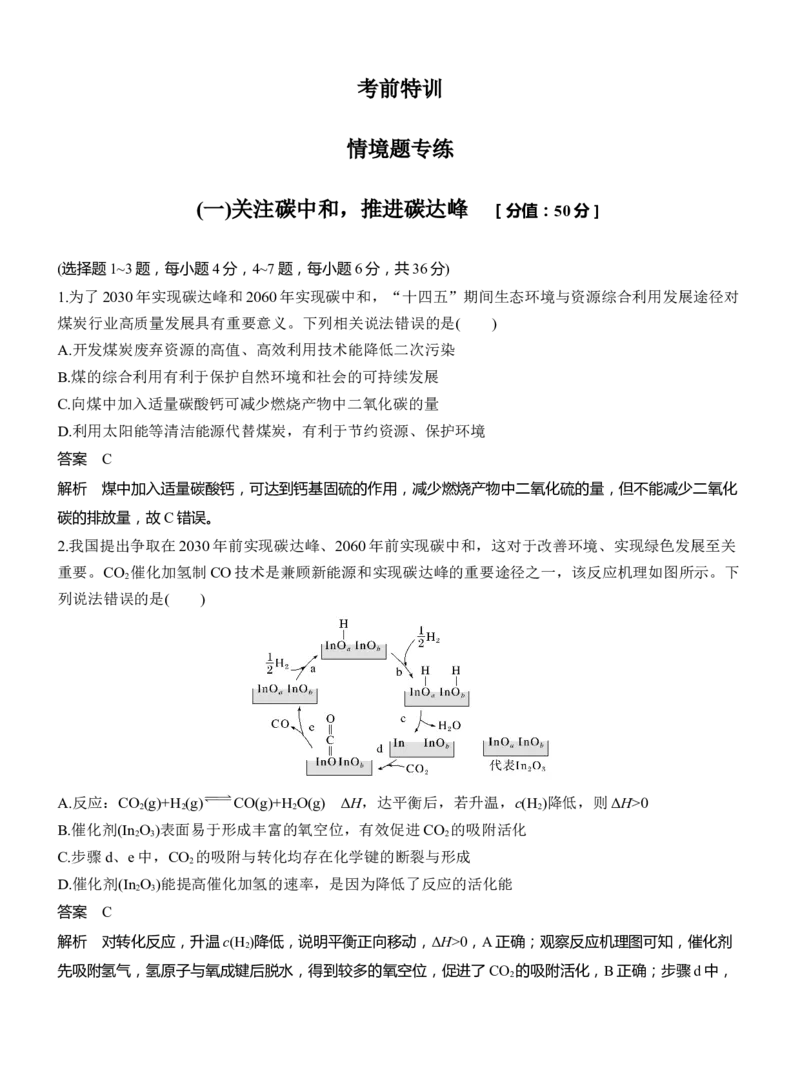
重要。CO 催化加氢制CO技术是兼顾新能源和实现碳达峰的重要途径之一,该反应机理如图所示。下
2
列说法错误的是( )
A.反应:CO (g)+H (g) CO(g)+H O(g) ΔH,达平衡后,若升温,c(H )降低,则ΔH>0
2 2 2 2
B.催化剂(In O )表面易于形成丰富的氧空位,有效促进CO 的吸附活化
2 3 2
C.步骤d、e中,CO 的吸附与转化均存在化学键的断裂与形成
2
D.催化剂(In O )能提高催化加氢的速率,是因为降低了反应的活化能
2 3
答案 C
解析 对转化反应,升温c(H )降低,说明平衡正向移动,ΔH>0,A正确;观察反应机理图可知,催化剂
2
先吸附氢气,氢原子与氧成键后脱水,得到较多的氧空位,促进了CO 的吸附活化,B正确;步骤d中,
2CO 只是进入氧空位被催化剂吸附,不存在化学键的断裂与形成,C错误;In O 作催化剂降低了反应的活
2 2 3
化能,从而提高化学反应速率,D正确。
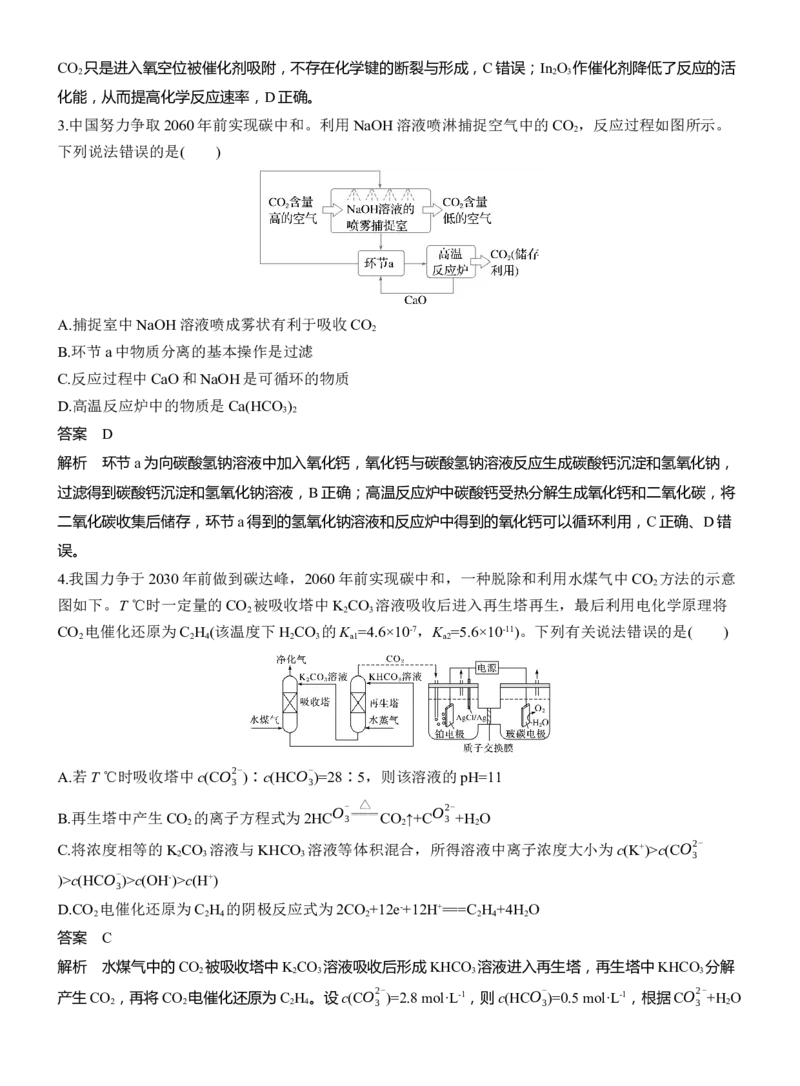
3.中国努力争取2060年前实现碳中和。利用NaOH溶液喷淋捕捉空气中的CO ,反应过程如图所示。
2
下列说法错误的是( )
A.捕捉室中NaOH溶液喷成雾状有利于吸收CO
2
B.环节a中物质分离的基本操作是过滤
C.反应过程中CaO和NaOH是可循环的物质
D.高温反应炉中的物质是Ca(HCO )
3 2
答案 D
解析 环节a为向碳酸氢钠溶液中加入氧化钙,氧化钙与碳酸氢钠溶液反应生成碳酸钙沉淀和氢氧化钠,
过滤得到碳酸钙沉淀和氢氧化钠溶液,B正确;高温反应炉中碳酸钙受热分解生成氧化钙和二氧化碳,将
二氧化碳收集后储存,环节a得到的氢氧化钠溶液和反应炉中得到的氧化钙可以循环利用,C正确、D错
误。
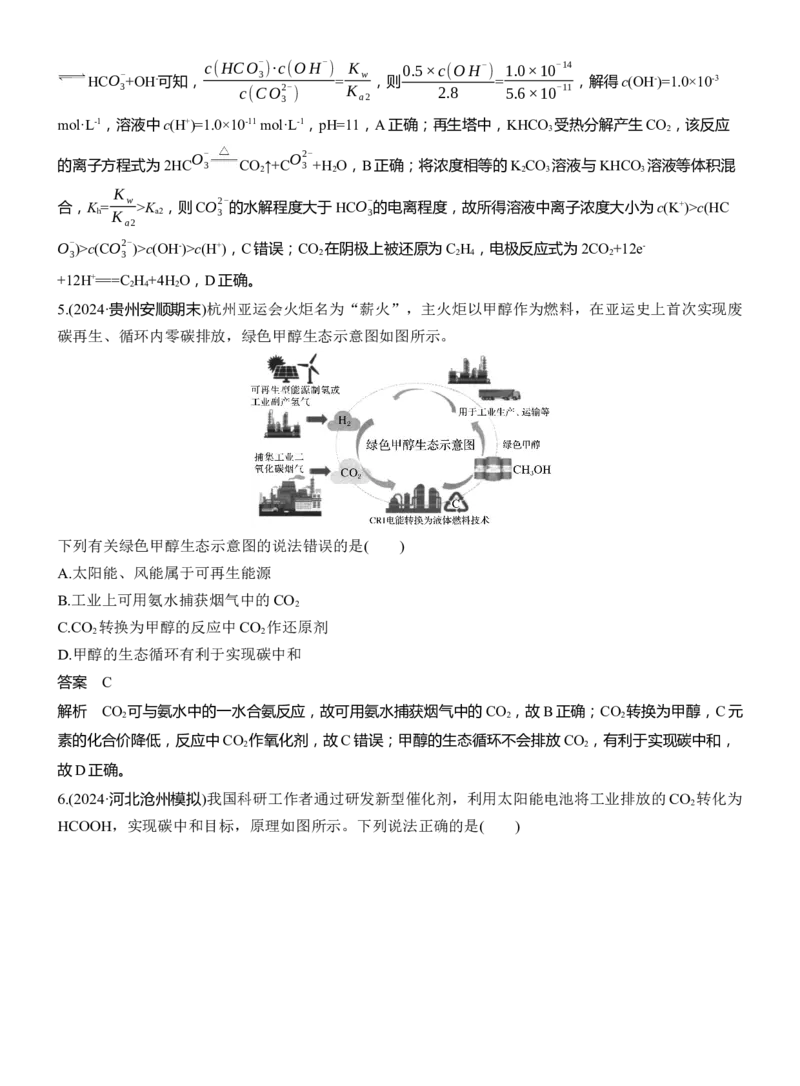
4.我国力争于2030年前做到碳达峰,2060年前实现碳中和,一种脱除和利用水煤气中CO 方法的示意
2
图如下。T ℃时一定量的CO 被吸收塔中K CO 溶液吸收后进入再生塔再生,最后利用电化学原理将
2 2 3
CO 电催化还原为C H (该温度下H CO 的K =4.6×10-7,K =5.6×10-11)。下列有关说法错误的是( )
2 2 4 2 3 a1 a2
A.若T ℃时吸收塔中c(CO2- )∶c(HCO- )=28∶5,则该溶液的pH=11
3 3
O- O2-
B.再生塔中产生CO 2 的离子方程式为2HC 3 CO 2 ↑+C 3 +H 2 O
C.将浓度相等的K CO 溶液与KHCO 溶液等体积混合,所得溶液中离子浓度大小为c(K+)>c(CO2-
2 3 3 3
)>c(HCO- )>c(OH-)>c(H+)
3
D.CO 电催化还原为C H 的阴极反应式为2CO +12e-+12H+===C H +4H O
2 2 4 2 2 4 2
答案 C
解析 水煤气中的CO 被吸收塔中K CO 溶液吸收后形成KHCO 溶液进入再生塔,再生塔中KHCO 分解
2 2 3 3 3
产生CO ,再将CO 电催化还原为C H
。设c(CO2-
)=2.8
mol·L-1,则c(HCO-
)=0.5
mol·L-1,根据CO2-
+H O
2 2 2 4 3 3 3 2c(HCO- )·c(OH- ) K 0.5×c(OH- ) 1.0×10-14
HCO-
+OH-可知,
3
=
w
,则 = ,解得c(OH-)=1.0×10-3
3 c(CO2- ) K 2.8 5.6×10-11
3 a2
mol·L-1,溶液中c(H+)=1.0×10-11 mol·L-1,pH=11,A正确;再生塔中,KHCO 受热分解产生CO ,该反应
3 2
O- O2-
的离子方程式为2HC 3 CO 2 ↑+C 3 +H 2 O,B正确;将浓度相等的K 2 CO 3 溶液与KHCO 3 溶液等体积混
K
合,K =
w
>K
,则CO2- 的水解程度大于HCO-
的电离程度,故所得溶液中离子浓度大小为c(K+)>c(HC
h K a2 3 3
a2
O- )>c(CO2- )>c(OH-)>c(H+),C错误;CO 在阴极上被还原为C H ,电极反应式为2CO +12e-
3 3 2 2 4 2
+12H+===C H +4H O,D正确。
2 4 2
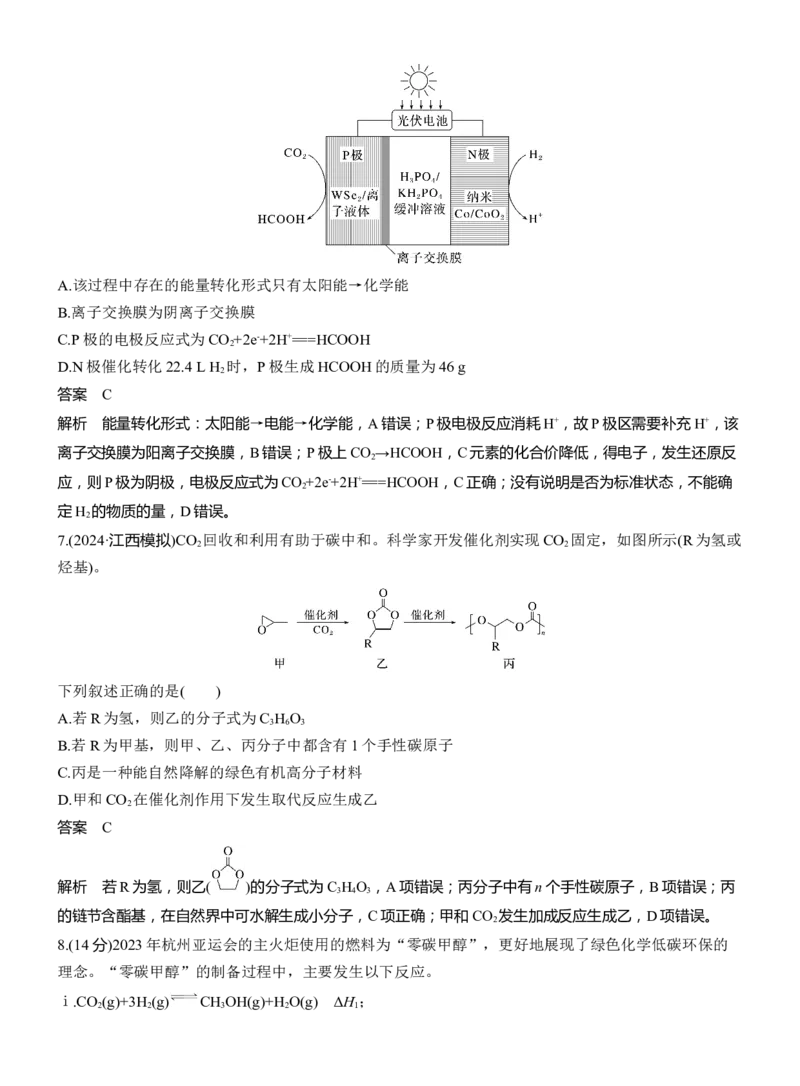
5.(2024·贵州安顺期末)杭州亚运会火炬名为“薪火”,主火炬以甲醇作为燃料,在亚运史上首次实现废
碳再生、循环内零碳排放,绿色甲醇生态示意图如图所示。
下列有关绿色甲醇生态示意图的说法错误的是( )
A.太阳能、风能属于可再生能源
B.工业上可用氨水捕获烟气中的CO
2
C.CO 转换为甲醇的反应中CO 作还原剂
2 2
D.甲醇的生态循环有利于实现碳中和
答案 C
解析 CO 可与氨水中的一水合氨反应,故可用氨水捕获烟气中的CO ,故B正确;CO 转换为甲醇,C元
2 2 2
素的化合价降低,反应中CO 作氧化剂,故C错误;甲醇的生态循环不会排放CO ,有利于实现碳中和,
2 2
故D正确。
6.(2024·河北沧州模拟)我国科研工作者通过研发新型催化剂,利用太阳能电池将工业排放的CO 转化为
2
HCOOH,实现碳中和目标,原理如图所示。下列说法正确的是( )A.该过程中存在的能量转化形式只有太阳能→化学能
B.离子交换膜为阴离子交换膜
C.P极的电极反应式为CO +2e-+2H+===HCOOH
2
D.N极催化转化22.4 L H 时,P极生成HCOOH的质量为46 g
2
答案 C
解析 能量转化形式:太阳能→电能→化学能,A错误;P极电极反应消耗H+,故P极区需要补充H+,该
离子交换膜为阳离子交换膜,B错误;P极上CO →HCOOH,C元素的化合价降低,得电子,发生还原反
2
应,则P极为阴极,电极反应式为CO +2e-+2H+===HCOOH,C正确;没有说明是否为标准状态,不能确
2
定H 的物质的量,D错误。
2
7.(2024·江西模拟)CO 回收和利用有助于碳中和。科学家开发催化剂实现CO 固定,如图所示(R为氢或
2 2
烃基)。
下列叙述正确的是( )
A.若R为氢,则乙的分子式为C H O
3 6 3
B.若R为甲基,则甲、乙、丙分子中都含有1个手性碳原子
C.丙是一种能自然降解的绿色有机高分子材料
D.甲和CO 在催化剂作用下发生取代反应生成乙
2
答案 C
解析 若R为氢,则乙( )的分子式为C H O ,A项错误;丙分子中有n个手性碳原子,B项错误;丙
3 4 3
的链节含酯基,在自然界中可水解生成小分子,C项正确;甲和CO 发生加成反应生成乙,D项错误。
2
8.(14分)2023年杭州亚运会的主火炬使用的燃料为“零碳甲醇”,更好地展现了绿色化学低碳环保的
理念。“零碳甲醇”的制备过程中,主要发生以下反应。
ⅰ.CO (g)+3H (g) CH OH(g)+H O(g) ΔH ;
2 2 3 2 1ⅱ.CO (g)+H (g) CO(g)+H O(g) ΔH =+41.2 kJ·mol-1;
2 2 2 2
ⅲ.CO(g)+3H (g) CH (g)+H O(g) ΔH =-206.2 kJ·mol-1
2 4 2 3
回答下列问题:
(1)反应ⅰ可能的反应历程如图1所示。
注:方框内包含微粒种类及数目,微粒的相对总能量[如最后一个方框表示1个CH OH(g)分子和1个
3
H O(g)分子的相对总能量为-0.51 eV,单位:eV],TS表示过渡态、*表示吸附在催化剂上的微粒,1
2
eV=1.6×10-22 kJ。
①ΔH = kJ·mol-1(计算结果保留1位小数)。
1
②该反应历程中,生成甲醇的决速步骤的反应方程式为 。
(2)在恒温恒压条件下,通入CO (g)与H (g)混合气体,发生反应ⅰ、ⅱ、ⅲ。下列可以说明反应达到平
2 2
衡状态的是 (填字母)。
A.反应混合物中各组分的物质的量浓度不再改变
B.反应后混合气体的压强不再改变
C.混合气体的密度不再改变
D.混合气体的平均相对分子质量不变
(3)一定温度下,将CO (g)和H (g)按n(CO )∶n(H )=1∶3充入恒容密闭容器中,发生反应ⅰ、ⅱ、ⅲ,
2 2 2 2
n(CH OH)
容器内总压强与反应时间的变化关系如图2所示。实验测得平衡时 3 =3,H O的分压为15
n(CH ) 2
4
kPa。
①0~10 min内,CO 的平均分压变化率为 kPa·min-1。
2②反应ⅲ的压强平衡常数K = kPa-2(以平衡分压代替平衡浓度计算,分压=总压×物质的量分数,
p
结果保留2位有效数字)。
(4)一定条件下,向恒温恒容密闭容器中充入CO (g)和H (g)只发生反应ⅰ,在两种不同催化剂下建立平
2 2
衡的过程中H 的转化率随反应时间的变化曲线如图3所示。
2
①两种催化剂催化效果较好的是 。
②催化剂Ⅰ条件下,t min时改变的反应条件可能是 (填字母)。
2
A.降低温度
B.容器容积不变,通入一定量He(g)
C.容器容积不变,通入一定量CH OH(g)
3
D.缩小容器容积
3 1
答案 (1)①-49.1 ②HCOOH*+2H (g)===H COOH*+ H (g)[或HCOOH*+ H (g)===H COOH*] (2)ACD
2 2 2 2 2 2 2
(3)①1.25 ②2.3×10-4 (4)①催化剂Ⅰ ②C
解析 (1)①根据ΔH=生成物的总能量-反应物的总能量可得,ΔH =(-0.51-0)eV×6.02×1023
1
mol-1=-0.51×1.6×10-22 kJ×6.02×1023 mol-1≈-49.1 kJ·mol-1。②反应的活化能=过渡态的能量-反应物的总能量,
则可比较经历过渡态TS1、TS2、TS3、TS4、TS5、TS6的反应的活化能可得,经历TS3过渡态时,反应
3 1
的活化能最大、反应速率最慢,反应方程式为HCOOH*+2H (g)===H COOH*+ H (g)或HCOOH*+
2 2 2 2 2
H (g)===H COOH*。(2)恒温恒压条件下,反应混合物中各组分的物质的量浓度不再改变,可说明反应达到
2 2
平衡状态,A符合题意,B不符合题意;由于反应ⅰ和反应ⅲ均为反应前后气体分子数发生变化的反应,
在恒温恒压条件下发生反应ⅰ、ⅱ、ⅲ,反应前后混合气体的体积发生变化,混合气体的质量不变,则反
应前后混合气体的密度、平均相对分子质量发生变化,当混合气体的密度、平均相对分子质量不变时,可
说明反应达到平衡状态,C、D符合题意。
(3)【第一步:根据信息假设反应物的量】设起始时n(CO )=1 mol,n(H )=3 mol。
2 2
【第二步:根据图像计算物质转化的量】设平衡时总物质的量为x mol,由题图2可知,起始时总压强为
100 kPa 4mol
100 kPa,平衡时总压强为80 kPa。恒温恒容条件下, = ,x=3.2,气体总物质的量减少0.8
80 kPa xmol
mol。由于反应ⅰ和反应ⅲ均为反应前后气体分子数减小的反应,反应ⅱ为反应前后气体分子数不变的反
应,设平衡时n(CH OH)=a mol,n(CH )=b mol,依据差量法计算:
3 4
CO (g)+3H (g) CH OH(g)+H O(g) Δn
2 2 3 2
1 2a mol 2a mol
CO(g)+3H (g)===CH (g)+H O(g) Δn
2 4 2
1 2
b mol 2b mol
a
=3,2a+2b=0.8,解得a=0.3,b=0.1。
b
【第三步:列三段式计算】假设反应ⅰ达到平衡后发生反应ⅱ,反应ⅱ达到平衡后发生反应ⅲ,设反应ⅱ
生成的CO的物质的量为y mol。
反应ⅰ CO (g)+3H (g) CH OH(g)+H O(g)
2 2 3 2
起始量/mol 1 3 0 0
转化量/mol 0.3 0.9 0.3 0.3
平衡量/mol 0.7 2.1 0.3 0.3
反应ⅱ CO (g) + H (g) CO(g) + H O(g)
2 2 2
起始量/mol 0.7 2.1 0 0.3
转化量/mol y y y y
平衡量/mol 0.7-y 2.1-y y 0.3+y
反应ⅲ CO(g) + 3H (g) CH (g)+H O(g)
2 4 2
起始量/mol y 2.1-y 0 0.3+y
转化量/mol 0.1 0.3 0.1 0.1
平衡量/mol y-0.1 1.8-y 0.1 0.4+y
p(H O) n(H O) 15 kPa n(H O)
根据 2 = 2 , = 2 可得,n(H O)=0.6 mol,即0.4+y=0.6,y=0.2。
p n 80 kPa 3.2mol 2
总 总
【第四步:根据具体问题计算】①反应过程中消耗的CO 的物质的量为0.5 mol,CO 的压强变化量为
2 2
0.5mol 12.5 kPa
×100 kPa=12.5 kPa,则0~10 min内,CO 的平均分压变化率为 =1.25 kPa·min-1。②平衡
4mol 2 10min
时n(H O)=0.6 mol,n(CH )=0.1 mol,n(CO)=0.1 mol,n(H )=1.6 mol,p(H O)=15 kPa,p(CH )=p(CO)=2.5
2 4 2 2 4
p(CH )·p(H O) 2.5 kPa×15 kPa
4 2
kPa,p(H )=40 kPa,则反应ⅲ的压强平衡常数K = = ≈2.3×10-4
2 p p(CO)·p3 (H ) 2.5 kPa×(40 kPa) 3
2
kPa-2。(4)②由题图3可知,从t min开始H 的转化率降低,平衡逆向移动。由于反应ⅰ的正反应为放热反
2 2
应,降低温度,平衡正向移动,H 的转化率增大,A不符合题意;容器容积不变,通入一定量He(g),各
2
组分的浓度不变,平衡不移动,H 的转化率不变,B不符合题意;容器容积不变,通入一定量
2
CH OH(g),平衡逆向移动,H 的转化率降低,C符合题意;缩小容器容积,相当于增大压强,由于反应ⅰ
3 2
为反应前后气体分子数减小的反应,平衡正向移动,H 的转化率增大,D不符合题意。
2