文档内容
(三)化学反应原理
1.环己烷和苯均是重要的化工原料,对环己烷—苯系统的研究既有生产实际价值,也具有
理论意义。回答下列问题。
(1)环己烷脱氢生苯的热效应研究
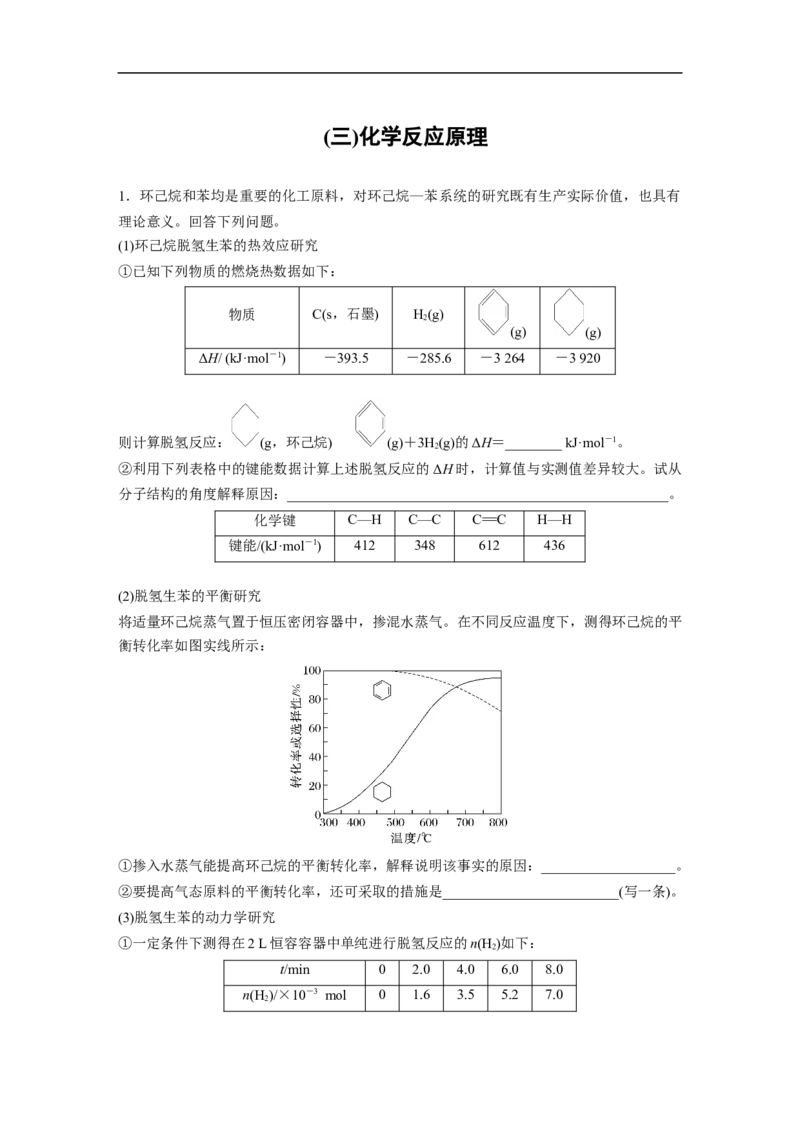
①已知下列物质的燃烧热数据如下:
物质 C(s,石墨) H(g)
2
(g) (g)
ΔH/ (kJ·mol-1) -393.5 -285.6 -3 264 -3 920
则计算脱氢反应: (g,环己烷) (g)+3H(g)的ΔH=________ kJ·mol-1。
2
②利用下列表格中的键能数据计算上述脱氢反应的ΔH时,计算值与实测值差异较大。试从
分子结构的角度解释原因:______________________________________________________。
化学键 C—H C—C C==C H—H
键能/(kJ·mol-1) 412 348 612 436
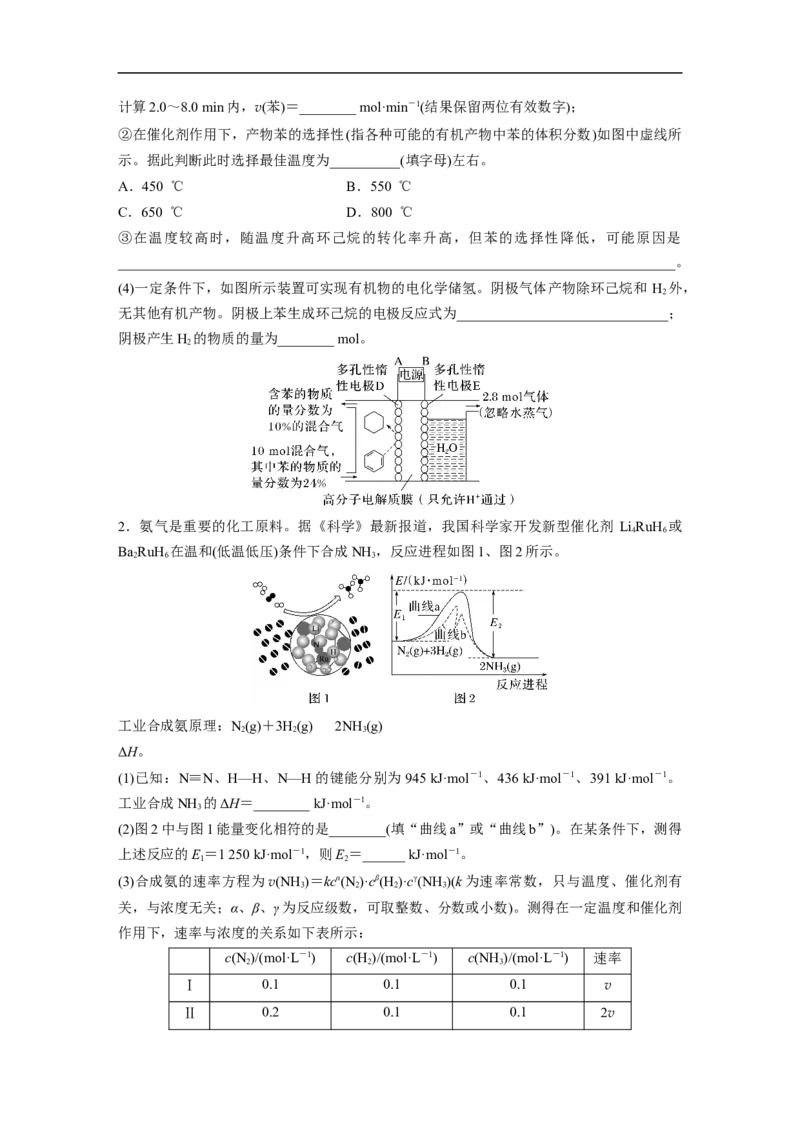
(2)脱氢生苯的平衡研究
将适量环己烷蒸气置于恒压密闭容器中,掺混水蒸气。在不同反应温度下,测得环己烷的平
衡转化率如图实线所示:
①掺入水蒸气能提高环己烷的平衡转化率,解释说明该事实的原因:___________________。
②要提高气态原料的平衡转化率,还可采取的措施是_________________________(写一条)。
(3)脱氢生苯的动力学研究
①一定条件下测得在2 L恒容容器中单纯进行脱氢反应的n(H )如下:
2
t/min 0 2.0 4.0 6.0 8.0
n(H )/×10-3 mol 0 1.6 3.5 5.2 7.0
2计算2.0~8.0 min内,v(苯)=________ mol·min-1(结果保留两位有效数字);
②在催化剂作用下,产物苯的选择性(指各种可能的有机产物中苯的体积分数)如图中虚线所
示。据此判断此时选择最佳温度为__________(填字母)左右。
A.450 ℃ B.550 ℃
C.650 ℃ D.800 ℃
③在温度较高时,随温度升高环己烷的转化率升高,但苯的选择性降低,可能原因是
_______________________________________________________________________________。
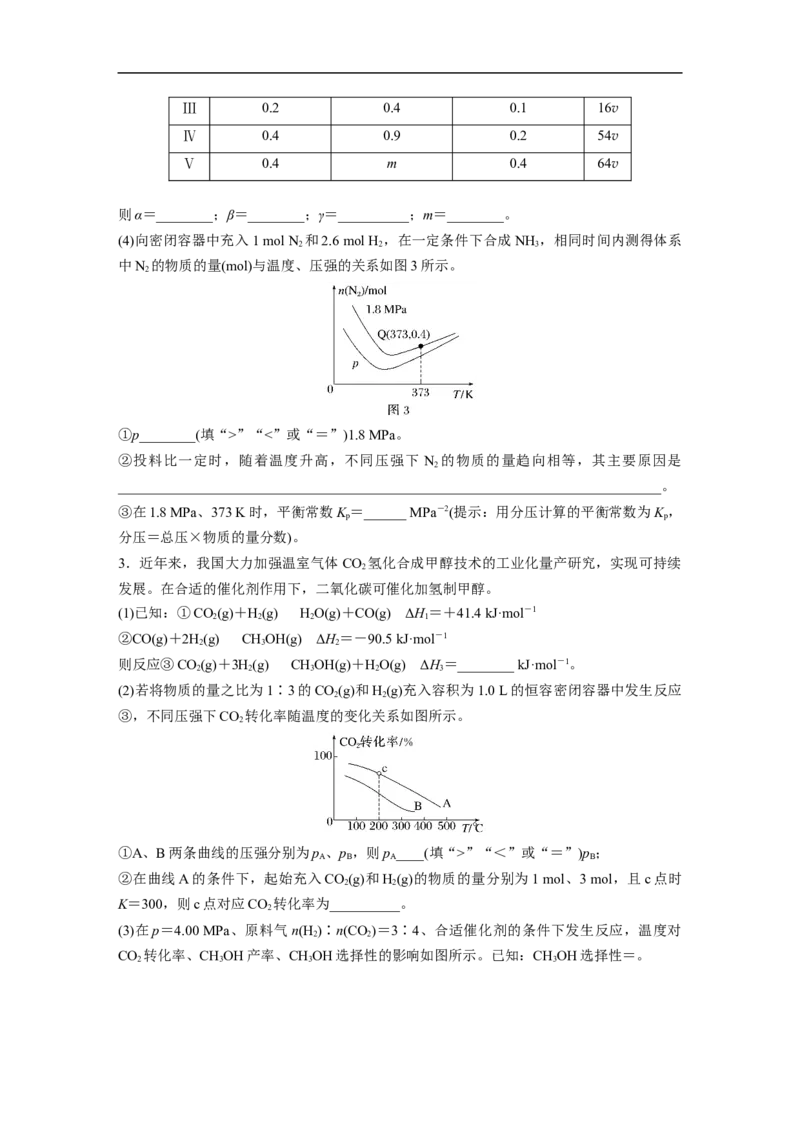
(4)一定条件下,如图所示装置可实现有机物的电化学储氢。阴极气体产物除环己烷和 H 外,
2
无其他有机产物。阴极上苯生成环己烷的电极反应式为______________________________;
阴极产生H 的物质的量为________ mol。
2
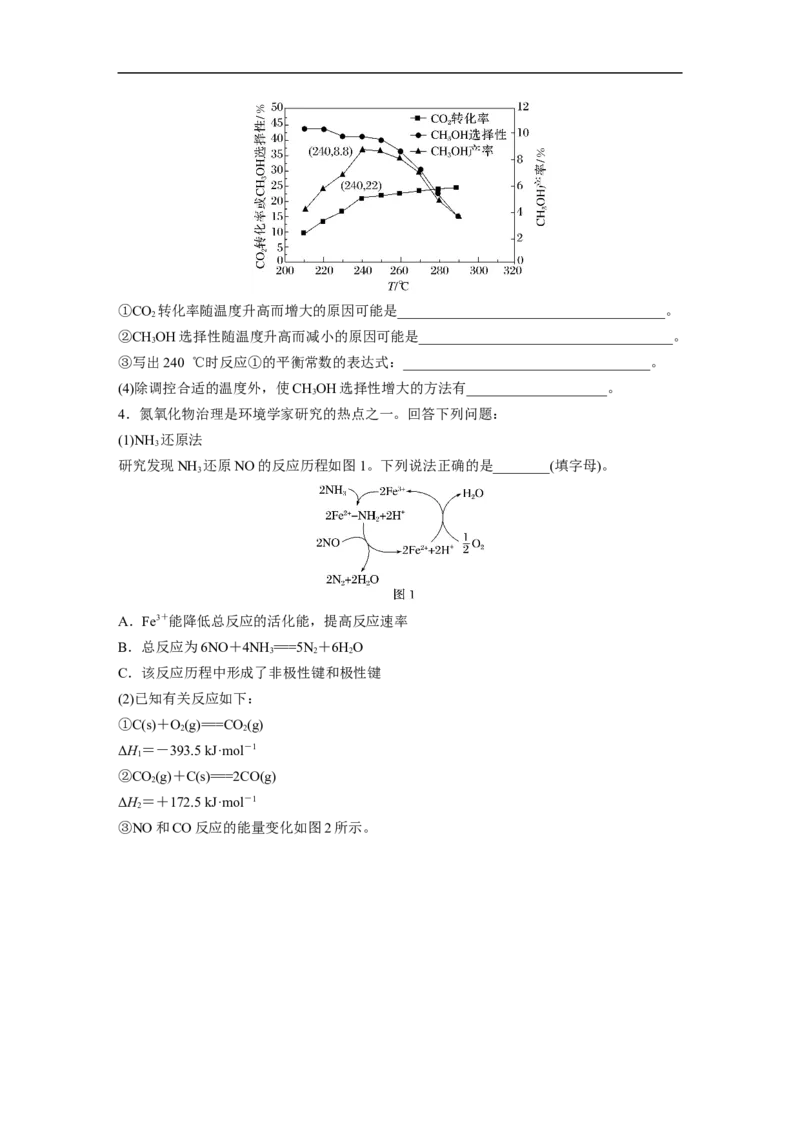
2.氨气是重要的化工原料。据《科学》最新报道,我国科学家开发新型催化剂 LiRuH 或
4 6
Ba RuH 在温和(低温低压)条件下合成NH ,反应进程如图1、图2所示。
2 6 3
工业合成氨原理:N(g)+3H(g)2NH (g)
2 2 3
ΔH。
(1)已知:N≡N、H—H、N—H的键能分别为945 kJ·mol-1、436 kJ·mol-1、391 kJ·mol-1。
工业合成NH 的ΔH=________ kJ·mol-1。
3
(2)图2中与图1能量变化相符的是________(填“曲线a”或“曲线b”)。在某条件下,测得
上述反应的E=1 250 kJ·mol-1,则E=______ kJ·mol-1。
1 2
(3)合成氨的速率方程为v(NH )=kcα(N )·cβ(H )·cγ(NH )(k为速率常数,只与温度、催化剂有
3 2 2 3
关,与浓度无关;α、β、γ为反应级数,可取整数、分数或小数)。测得在一定温度和催化剂
作用下,速率与浓度的关系如下表所示:
c(N )/(mol·L-1) c(H )/(mol·L-1) c(NH )/(mol·L-1) 速率
2 2 3
Ⅰ 0.1 0.1 0.1 v
Ⅱ 0.2 0.1 0.1 2vⅢ 0.2 0.4 0.1 16v
Ⅳ 0.4 0.9 0.2 54v
Ⅴ 0.4 m 0.4 64v
则α=________;β=________;γ=__________;m=________。
(4)向密闭容器中充入1 mol N 和2.6 mol H ,在一定条件下合成NH ,相同时间内测得体系
2 2 3
中N 的物质的量(mol)与温度、压强的关系如图3所示。
2
①p________(填“>”“<”或“=”)1.8 MPa。
②投料比一定时,随着温度升高,不同压强下 N 的物质的量趋向相等,其主要原因是
2
_____________________________________________________________________________。
③在1.8 MPa、373 K时,平衡常数K =______ MPa-2(提示:用分压计算的平衡常数为K ,
p p
分压=总压×物质的量分数)。
3.近年来,我国大力加强温室气体CO 氢化合成甲醇技术的工业化量产研究,实现可持续
2
发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
(1)已知:①CO(g)+H(g)HO(g)+CO(g) ΔH=+41.4 kJ·mol-1
2 2 2 1
②CO(g)+2H(g)CHOH(g) ΔH=-90.5 kJ·mol-1
2 3 2
则反应③CO(g)+3H(g)CHOH(g)+HO(g) ΔH=________ kJ·mol-1。
2 2 3 2 3
(2)若将物质的量之比为1∶3的CO(g)和H(g)充入容积为1.0 L的恒容密闭容器中发生反应
2 2
③,不同压强下CO 转化率随温度的变化关系如图所示。
2
①A、B两条曲线的压强分别为p 、p ,则p ____(填“>”“<”或“=”)p ;
A B A B
②在曲线A的条件下,起始充入CO(g)和H(g)的物质的量分别为1 mol、3 mol,且c点时
2 2
K=300,则c点对应CO 转化率为__________。
2
(3)在p=4.00 MPa、原料气n(H )∶n(CO)=3∶4、合适催化剂的条件下发生反应,温度对
2 2
CO 转化率、CHOH产率、CHOH选择性的影响如图所示。已知:CHOH选择性=。
2 3 3 3①CO 转化率随温度升高而增大的原因可能是______________________________________。
2
②CHOH选择性随温度升高而减小的原因可能是____________________________________。
3
③写出240 ℃时反应①的平衡常数的表达式:___________________________________。
(4)除调控合适的温度外,使CHOH选择性增大的方法有____________________。
3
4.氮氧化物治理是环境学家研究的热点之一。回答下列问题:
(1)NH 还原法
3
研究发现NH 还原NO的反应历程如图1。下列说法正确的是________(填字母)。
3
A.Fe3+能降低总反应的活化能,提高反应速率
B.总反应为6NO+4NH ===5N+6HO
3 2 2
C.该反应历程中形成了非极性键和极性键
(2)已知有关反应如下:
①C(s)+O(g)===CO(g)
2 2
ΔH=-393.5 kJ·mol-1
1
②CO(g)+C(s)===2CO(g)
2
ΔH=+172.5 kJ·mol-1
2
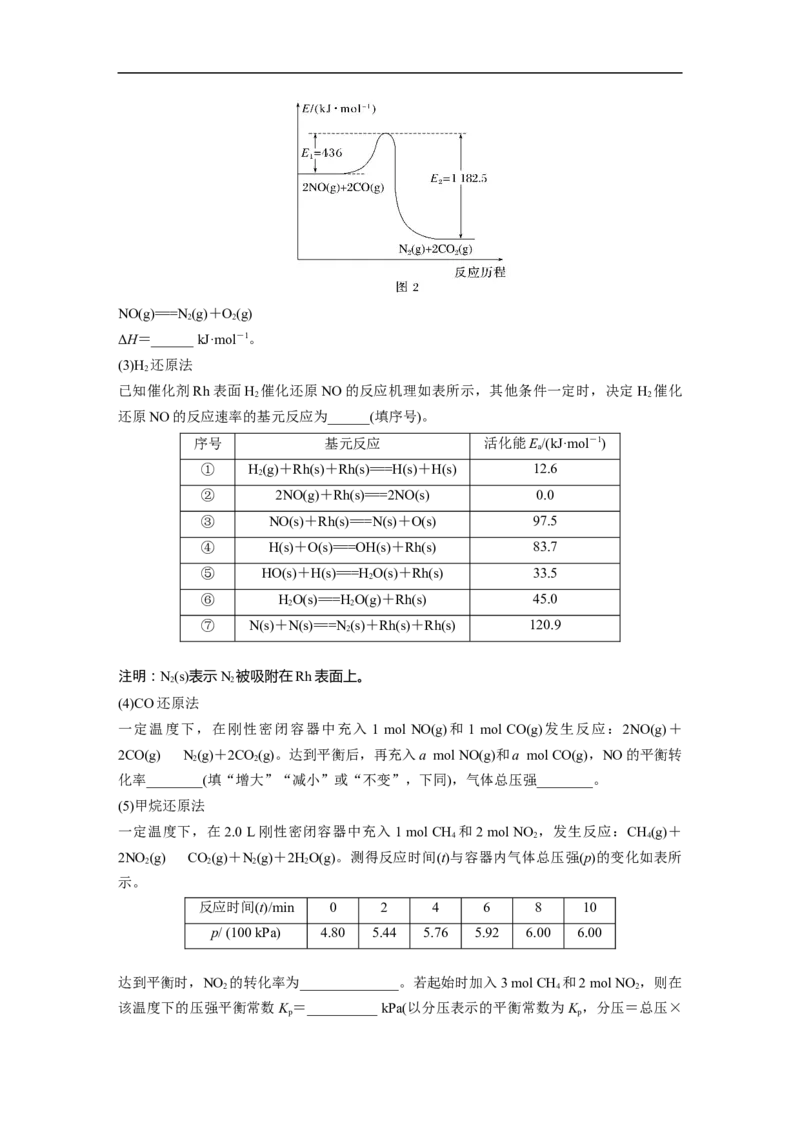
③NO和CO反应的能量变化如图2所示。NO(g)===N(g)+O(g)
2 2
ΔH=______ kJ·mol-1。
(3)H 还原法
2
已知催化剂Rh表面H 催化还原NO的反应机理如表所示,其他条件一定时,决定H 催化
2 2
还原NO的反应速率的基元反应为______(填序号)。
序号 基元反应 活化能E/(kJ·mol-1)
a
① H(g)+Rh(s)+Rh(s)===H(s)+H(s) 12.6
2
② 2NO(g)+Rh(s)===2NO(s) 0.0
③ NO(s)+Rh(s)===N(s)+O(s) 97.5
④ H(s)+O(s)===OH(s)+Rh(s) 83.7
⑤ HO(s)+H(s)===HO(s)+Rh(s) 33.5
2
⑥ HO(s)===HO(g)+Rh(s) 45.0
2 2
⑦ N(s)+N(s)===N(s)+Rh(s)+Rh(s) 120.9
2
注明:N(s)表示N 被吸附在Rh表面上。
2 2
(4)CO还原法
一定温度下,在刚性密闭容器中充入 1 mol NO(g)和 1 mol CO(g)发生反应:2NO(g)+
2CO(g)N(g)+2CO(g)。达到平衡后,再充入a mol NO(g)和a mol CO(g),NO的平衡转
2 2
化率________(填“增大”“减小”或“不变”,下同),气体总压强________。
(5)甲烷还原法
一定温度下,在2.0 L刚性密闭容器中充入1 mol CH 和2 mol NO ,发生反应:CH(g)+
4 2 4
2NO (g)CO(g)+N(g)+2HO(g)。测得反应时间(t)与容器内气体总压强(p)的变化如表所
2 2 2 2
示。
反应时间(t)/min 0 2 4 6 8 10
p/ (100 kPa) 4.80 5.44 5.76 5.92 6.00 6.00
达到平衡时,NO 的转化率为______________。若起始时加入3 mol CH 和2 mol NO ,则在
2 4 2
该温度下的压强平衡常数K =__________ kPa(以分压表示的平衡常数为K ,分压=总压×
p p物质的量分数)。
(6)电解氧化吸收法
电解0.1 mol·L-1 NaCl溶液时,溶液中相关成分的质量浓度与电流强度的变化关系如图3。
当电流强度为4 A时,吸收NO的主要反应的离子方程式为____________________(NO最终
转化为NO)。
5.随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.以CO 和NH 为原料合成尿素:2NH (g)+CO(g)CO(NH)(s)+HO(g)
2 3 3 2 2 2 2
ΔH=-87 kJ·mol-1。
(1)有利于提高CO 平衡转化率的措施是_______________________________(填字母)。
2
A.高温低压 B.低温高压
C.高温高压 D.低温低压
(2)研究发现,合成尿素反应分两步完成,其能量变化如图甲所示:
第一步: 2NH (g)+CO(g)NH COONH(s) ΔH
3 2 2 4 1
第二步:NH COONH(s)CO(NH)(s)+HO(g) ΔH
2 4 2 2 2 2
①图中ΔE=________ kJ·mol-1。
②反应速率较快的是________(填“第一步”或“第二步”)反应,理由是_______________。
Ⅱ.以CO 和CH 催化重整制备合成气:
2 4
CO(g)+CH(g)2CO(g)+2H(g)。
2 4 2
(3)在密闭容器中通入物质的量均为0.2 mol的CH 和CO ,在一定条件下发生反应:CH(g)
4 2 4
+CO(g)2CO(g)+2H(g),CH 的平衡转化率随温度、压强的变化关系如图乙所示。
2 2 4①若反应在恒温、恒容密闭容器中进行,下列叙述能说明反应到达平衡状态的是
____________(填字母)。
A.容器中混合气体的密度保持不变
B.容器内混合气体的压强保持不变
C.反应速率: 2v正 (CO
2
)=v正 (H
2
)
D.同时断裂2 mol C—H和1 mol H—H
②由图乙可知,压强p
1
________(填“>”“<”或“=”,下同)p
2;
Y点速率v正 ________v逆 。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡
常数K ,则X点对应温度下的K =__________(用含p 的代数式表示)。
p p 2
Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图丙所示:
(4)阴极电极反应式为__________________________,该装置中使用的是________(填“阴”
或“阳”)离子交换膜。