文档内容
氧化还原反应讲义(教师逐字稿)
课程简介:即 PPT(第 1 页):本节课我们主要学习:氧化还原反应。
氧化还原反应是高中化学的核心基本功,基本贯穿金属、非金属、电
化学等板块的学习,因为务必扎实掌握好。高考出题为电化学选择题
及综合大题里的某个问。高考题目难度不大,属于必得分题目。氧化
还原反应主要内容包括氧化还原反应的相关概念、氧化还原反应型方
程式的配平、氧化性还原性强弱的比较、结合转移电子数守恒进行计
算等。氧化还原反应知识点比较简单好理解,方法固定但注重细节,
需要比较细心。准备好了么?Let’s go!
PPT(第 2 页):先来了解一下氧化还原反应模块的知识特点。
1、“点少好懂,概念易混”;2、“方法固定、注重细节”
1、氧化还原反应的知识点相对比较少,并且好理解,学起来基
本没有太大难度,主要是在相关概念的记忆上容易记混,这也是大多
数同学的通病。
2、氧化还原反应的核心是方程式的配平,会有多种类型方程式
的配平,各类型会有对应的配平方法,因此方法是比较固定的,只是
在配平的过程中要细心观察,注意好细节,因为往往配平出错的地方
都是没有好细节。
PPT(第 3 页):现在我们进入氧还原反应的学习。
PPT(第 4 页):看,这就是氧化还原反应的知识网络图。我们按相关
概念,基本类型,配平方法,基本规律,氧化性、还原性强弱比较 5个分支来一一讲解。(若 PPT 中图看不清,可查看下载的原图)
PPT(第 5 页):我们先来看下相关概念。根据反应前后元素化合价有
无变化我们将反应分为两类,一类是有化合价变化的氧化还原反应,
一类是无化合价变化的非氧化还原反应。因此氧化还原反应最直观的
特征就是反应前后元素化合价发生了变化。那么化合价为什么会发生
变化呢?初中化学里学过原子最外层要达到 2 个或 8 个电子的稳定结
构,因此在反应的过程中最外层电子会发生电子的转移(得失或偏移)
使彼此都达到稳定的结构;在这个过程中,失去电子或电子偏离的原
子化合价升高,得到电子或电子靠近的原子化合价降低,因此元素化
合价变化的本质原因是发生电子转移。
PPT(第 6 页):接下来我们来看下氧化还原反应与四种基本反应类型
的关系,请看图,图中很清楚的说明了它们之间的关系,我们具体说
明下原因。由于置换反应中反应前后的单质元素都会在化合物里,因
此化合价发生了变化,所以置换反应均是氧化还原反应。由于复分解
反应的基本原理是反应物间交叉互换阴阳离子,化合价没有发生变
化,所以复分解反应均是非氧化还原反应。至于分解反应和化合反应,
高温 ,
我们举具体的方程式来说明下,分解反应:
CaCO3 CaO CO
3 CaO CO
2
2KMnO K MnO MnO O ,左边是非氧化还原反应,右边是氧化
4 2 4 2 2
还原反应;化合反应: O Ca(OH)
2
CaO H ,2FeCl Cl FeCl ,左边
2
2
2 2 3
是非氧化还原反应,右边是氧化还原反应。这里有个注意的点,即有单质参加或有单质生成的反应不一定都是氧化还原反应,例如
3O O 。
2
2
3PPT(第 7 页):接下来我们来看下专业术语,说白了就是名词记忆,
这就是最容易记混出错的地方,请认真听好了。我们结合具体的方程
式来详细说明下。(学霸照读 PPT)
PPT(第 8 页):接下来就是氧化还原反应的表示方法,主要用来标注
电子的转移情况,分别是双线桥法和单线桥法。请看 PPT 里标注的方
法,需要注意的是箭头的头尾均要指向化合价变化的元素。
PPT(第 9 页):现在我们学习氧化还原反应最核心的部分——方程式
的配平。根据氧化还原反应的类型我们分别讲解其对应的配平方法,
请务必认真听讲,重要的细节都在这里,稍不注意就很容易出错。氧
化还原反应主要分为三大类,分别是①氧化剂和还原剂是同一反应物
的自身氧化还原反应(包括分解反应和歧化反应),②氧化产物和还
原产物是同一生成物的特殊归中反应,③氧化剂、还原剂、氧化产物、
还原产物均是不同物质的各异型反应。方程式的配平遵循得失电子数
守恒、原子守恒、电荷守恒三大原则,这是配平的核心思想与方法指
导。
PPT(第 10 页):我们以各异型反应里最常见的方程式为例详细讲解下
配平步骤,其他类型的配平步骤与此一致,就不重复讲解了,侧重点
讲解注意的细节。配平步骤按“一标、二等、三定、四平、五查”依
次进行,环环相扣。请看具体例子:
①一标:标出化合价变化的元素的化合价
7 4 2 6
KMnO Na S O H Mn SO K Na S O
4 2 3SO 4 SO
H O
2 2 2
4 4 4
2
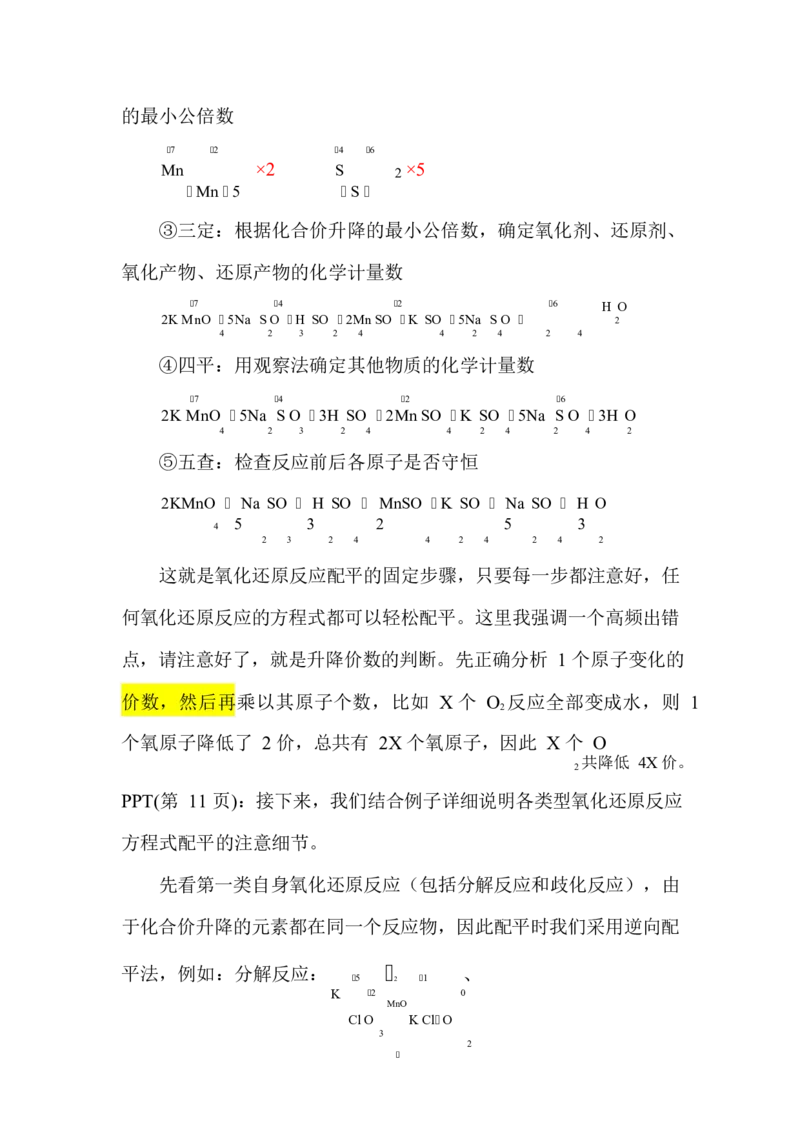
②二等:使变价元素的化合价升降总数相等,即求出化合价升降的最小公倍数
7 2 4 6
Mn ×2 S 2 ×5
Mn 5 S
③三定:根据化合价升降的最小公倍数,确定氧化剂、还原剂、
氧化产物、还原产物的化学计量数
7 4 2 6 H O
2K MnO 5Na S O H SO 2Mn SO K SO 5Na S O 2
4 2 3 2 4 4 2 4 2 4
④四平:用观察法确定其他物质的化学计量数
7 4 2 6
2K MnO 5Na S O 3H SO 2Mn SO K SO 5Na S O 3H O
4 2 3 2 4 4 2 4 2 4 2
⑤五查:检查反应前后各原子是否守恒
2KMnO Na SO H SO MnSO K SO Na SO H O
5 3 2 5 3
4
2 3 2 4 4 2 4 2 4 2
这就是氧化还原反应配平的固定步骤,只要每一步都注意好,任
何氧化还原反应的方程式都可以轻松配平。这里我强调一个高频出错
点,请注意好了,就是升降价数的判断。先正确分析 1 个原子变化的
价数,然后再乘以其原子个数,比如 X 个 O 反应全部变成水,则 1
2
个氧原子降低了 2 价,总共有 2X 个氧原子,因此 X 个 O
共降低 4X 价。
2
PPT(第 11 页):接下来,我们结合例子详细说明各类型氧化还原反应
方程式配平的注意细节。
先看第一类自身氧化还原反应(包括分解反应和歧化反应),由
于化合价升降的元素都在同一个反应物,因此配平时我们采用逆向配
平法,例如:分解反应: 、
5 2 1
K 2 0
MnO
Cl O K Cl O
3
2
4 5 2
歧化反应: N O H O H N O N O
2 2 3
标出反应前后变化的化合价后,根据化合价升降守恒先配平氧化产物
和还原产物的化学计量数,再配平氧化剂和还原剂的化学计量数。这里补充下歧化反应的定义,自身氧化还原反应里同种元素化合价既升
高又降低的反应。
接着是第二类特殊归中反应,归中反应的定义即不同反应物中同
种元素化合价升降生成中间价态产物的反应,归中反应有两类,一是
氧化产物和还原产物是同一生成物的第二类特殊归中反应,例如:
0 3 2
Fe Fe Cl Fe Cl
,二是氧化产物和还原产物不是同一生成物的归中
3 2
反 应 , 这 个 属 于 第 三 类 各 异 型 归 中 反 应 , 例 如 :
2 6 0 4
H O 浓 S S O H O 。归中反应有个价态变化规律,即两端
S ( )
2
H S
2 4 2 2
价态往中间价态靠拢,不交叉,所以在刚刚的例子里,第一个 0 价的
Fe 和+3 价的 Fe 都变成+2 价的 Fe,第二个-2 价的 S 只能变成 0 价的
S,+6 价的 S 只能变成+4 价的 S,这点切记,不然在分析转移电子数
以及结合转移电子数守恒计算时就 100%错。特殊归中反应,由于其
反应过程是歧化反应的逆过程,因此其配平方法采用正向配平法,即
先配平氧化剂和还原剂的化学计量数,再配平氧化产物和还原产物的
化学计量数。
最后是第三类各异型反应了,这里是注意细节最多的地方。先看
第一种,反应物中所标化合价升降的元素对应的原子全部升降,采用
正向配平法,例如:
3 0 2 2
,反应物中所有 N 原子和 O
N H O N O H O
2
3 2
原子的化合价均发生变化,因此采用正向配平法。第二种,反应物中
所标化合价升降的元素对应的原子部分升降,采用逆向配平法,例如:0 5 2 2
Cu H N O ) Cu(NO) N O H O
(稀 ,反应物中 N 原子只有部分发生变
3 3 2
化,因此采用逆向配平法。第三种,元素化合价不明确无法判断时,0 0 5 3 4 4
采用零价法,例如:Fe C H N O Fe NO N O C O H O
(浓) ( ) ,反 3
3 3 3 2 2 2
应物 Fe C 中 Fe 和 C 的化合价不明确,因此将不明确物质中所有元素
3
化合价默认为零价。第四种,反应物中有 3 种及以上的元素化合价变
化且同一物质中有 2 种元素化合价变化,采用整体法,例如
0 0 5 3 4 4
Fe C H N O ) Fe(NO ) N O C O H O
3 (浓 ,反应物 FeC 中 Fe 和
3
C
3 3 3 2 2 2
化合价均升高,因此把 Fe C 当做一个整体来分析化合价变化情况,
3
即一个 Fe C 共升高 13 价。
3
PPT(第 12 页):接着讲下氧化还原反应型离子方程式的书写,步骤与
上述基本一致,只是多了一个电荷守恒原则。我们还是举一个例子来
说明下,比如写出 SO 通入酸性 KMnO 溶液中的离子方程式。
2 4
①先判断需要保留下来的微粒。这个反应中只有 S 和 Mn 的化合
价发生变化,且价态变化后的产物微粒分别为 SO
4
含有 S 和 Mn 的微粒保留下来,即MnO 2 2 。
SO Mn SO
4
2 4
②根据化合价升降守恒配平氧化剂、还原剂、氧化产物、还原产
物,即2MnO SO Mn SO2 。
2
5 2 5
4
2 4
③判断两边电荷情况,结合电解质和电荷守恒先配带电介质,再
配中性介质。左边是 2 个负电荷,右边是 6 个负电荷,电解质可提供
满足电荷守恒,左边再配 2 个 H
+ +
H 和 H O,因此右边先配 4 个 H O 满足
2 2
H 和 O 原子守恒,即2MnO 5SO 2H O 2Mn 5SO2 4H 。
4 2
2 2 4
PPT(第 13 页):下面我们讲下氧化还原反应的一些基本规律,都是记
忆的内容。
①守恒规律,即氧化还原反应遵循原子守恒、得失电子数守恒、电荷守恒。
②强弱规律,即氧化还原反应里氧化剂的氧化性强于氧化产物,
还原剂的还原性强于还原产物,这个主要用于判断氧化还原反应能否
发生以及反应的方向。
③价态规律,即根据元素所处价态高低判断其氧化性还原性,最
低价态只有还原性,中间价态既有氧化性又有还原性,最高价态只有
氧化性。
④转化规律,主要用于判断同一元素两种价态之间的反应规律,
和
2+
Fe3+ 价态相邻能共存,价态相间能归中,比如 Fe
之间无中间价态,
3+
。归中价
2+
因此可共存;Fe 和 Fe 之间有中间价态+2,因此可反应归中为 Fe
态不交叉,低升高降只靠拢,讲的就是归中反应价态变化规律,即两
2 6 0 4
端价态往中间靠拢,不交叉,比如 H S H S O (浓) S S O H O ,这
2
2 4 2 2
个反应中-2 价的 S 只能变成 0 价的 S,+6 价的 S 只能变成+4 价的 S,
价态不交叉。
⑤先后规律,即强者先行原则,讲的是氧化还原反应中氧化性强
的物质和还原性强的物质优先反应,主要用于判断反应发生的先后顺
和 Br—,但由于还
2+
原 序,比如 Cl 通入 FeBr 溶液中,Cl 可氧化 Fe
2 2 2
>Br—,因此 Cl ,待 Fe2+反应完后,剩余的 Cl 性
2+ 2+
Fe 先氧化 Fe 氧化
2 2
Br
—。
PPT(第 14 页):最后就是氧化性、还原性强弱比较的判别方法,这里也是主要考查记忆。
①根据反应原理,即氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物。
②依据金属活动顺序表,越靠前的元素还原性越强,反之,越靠
后的元素氧化性越强。
③依据元素周期表,除了零族元素外,周期表中越往左下角排布
的元素还原性越强,越往右上角排布的元素氧化性越强。
④依据反应条件及反应的剧烈程度,反应条件要求越低,反应越
剧烈,对应物质的氧化性或还原性越强。比如 F 、Cl 、Br 、I 与 H
2 2 2 2 2
反应的条件越来越苛刻,因此氧化性 F >Cl >Br >I ;Na、Al、Fe 与盐
2 2 2 2
酸反应产生氢气的速率及剧烈程度递减,因此还原性 Na>Al>Fe。
⑤依据物质的浓度及溶液酸碱性,
物质浓度的影响:具有氧化性(或还原性)的物质的浓度越大,
其氧化性(或还原性)越强,反之越弱;比如氧化性:HNO (浓)>HNO
3 3
(稀),还原性:HCl(浓)>HCl(稀)
溶液酸碱性的影响,比如氧化性:KMnO (酸性)>KMnO (中性)
4 4
KMnO (碱性)。
4
PPT(第 15 页):⑥依据变价程度,同一物质被氧化后化合价变化越大,
则氧化剂氧化性越强,比如:
点燃
2Fe 3Cl 2FeCl
2
、Fe S FeS ,则氧化性 Cl >S。
2
3
同理,同一物质被还原后化合价变化越大,则还原剂还原性越强。比
如:
、 ,
5 稀 3Cu HNO 稀 C NO NO H O
Mg 12HNO M NO N O ( ) 3 u( ) 2 4
3
( ) 5 g( ) 6H
3
8
3 2 2 2 3 2 2则还原性:Mg>Cu。⑦依据化合价高低判断,一般来讲,同一元素的价态越高,其氧
>Fe2+。但
3+
化性越强,价态越低,其氧化性越弱。比如:氧化性:Fe
是有一些特例,比如氯的含氧酸,其价态越高,氧化性越弱:
HClO>HClO >HClO >HClO 。
2 3 4
⑧依据电化学原理,这部分放在电化学板块讲解。
PPT(第 16 页):OK,我的氧化还原反应知识网络图已构建完毕,你的
画得如何了?(若 PPT 中图看不清,可查看下载的原图)
PPT(第 17 页):让我们来一起看一下如何运用知识树来解题吧!(务
必看视频,学霸不必过多讲解)。
PPT(第 18—19 页):第 1 题和答案。
PPT(第 20—21 页):第 2 题和答案。
PPT(第 22—23 页):第 3 题和答案。
PPT(第 24 页):回顾落实。看完视频题目后,有没有学会如何运用知
识网络图来解题?我们再次总结一下知识网络图的要点吧。
PPT(第 25 页):要点总结(学霸照 PPT 读即可)。
PPT(第 26 页):注意事项提醒(4 个 tip,学霸照 PPT 读即可)。
PPT(第 27 页):课后作业布置,请完成我们为你准备的经典习题。
PPT(第 28 页):结束。