文档内容
2022 届高三化学二轮复习海洋化学资源的综合利用必刷卷
一、选择题(共17题)
1.下列说法不正确的是
A.二氧化硫可以使石蕊试液褪色
B.利用工业废气中的 制造全降解塑料,符合绿色环保要求
C.氧化镁熔点高,是一种优良的耐火材料
D.疫苗一般应冷藏存放,以避免蛋白质变性导致失效
2.下列有关金属的说法中不正确的是( )
A.钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来
B.镁燃烧发出耀眼的白光,常用于制造信号弹和烟火
C.铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作
D.铁能与硫酸发生反应,不能用铁制容器贮存浓硫酸
3.下列变化过程中,没有发生化学变化的是
A.铝的钝化 B.光合作用 C.碘的升华 D.海水提溴
4.下列海洋资源中,属于可再生资源的是
A.海洋潮汐能 B.海底多金属结核矿C.海滨砂矿 D.海水化学资源
5.从海带中提取碘单质,成熟的工艺流程如下。下列关于海带制碘的说法不正确的是
A.实验室也可以用酒精代替CCl 萃取碘水中的I
4 2
B.向滤液中加入稀硫酸和双氧水发生的反应是2H++H O+2I-=2H O+I
2 2 2 2
C.向碘水中加入几滴淀粉溶液,溶液变蓝色
D.实验室剪碎干海带用酒精湿润,放在坩埚中灼烧至完全变成灰烬
6.下列说法正确的有项:
(1)柠檬属于酸性食物(2)日照香炉生紫烟——碘的升华(3)若存在简单离子R2-,则R一定属于VIA
族(4)青石棉(化学式为NaFe Si O (OH)),是一种硅酸盐产品,它含有一定量的石英晶体(5)
2 5 8 22 2
“海沙危楼”是由于海沙带有腐蚀性,壶腐蚀混凝土中的钢筋等(6)用带橡皮塞的棕色试剂瓶存放浓HNO
3
A.2项
B.3项
C.4项
D.5项
7.从海水中提取下列物质,可以不涉及到化学变化的是( )
A.Mg B.NaCl C.Br D.K
2
8.NaCl是一种化工原料,可以制备一系列物质(如下图)。下列说法正确的是
A.25 ℃,NaHCO 在水中的溶解度比NaCO 的大
3 2 3
B.石灰乳与Cl 的反应中,Cl 既是氧化剂,又是还原剂
2 2
C.电解NaCl溶液的阳极产物为H 和NaOH
2
D.图中所示转化反应都是氧化还原反应
9.许多国家十分重视海水资源的综合利用,不需要化学变化就能够从海水中获得的物质是
A.氯、溴、碘 B.钠、镁、铝 C.烧碱、氢气 D.食盐、淡水
10.实验室用有机含碘 主要以I 和IO -的形式存在 废水制备单质碘的实验流程如下:
2 3
已知:Ⅰ.碘的熔点为113℃,但固态的碘可以不经过熔化直接升华;
Ⅱ.粗碘中含有少量的硫酸钠杂质。
下列说法正确的是( )
A.操作②中发生反应的离子方程式为IO -+3SO2-=I-+3SO2-
3 3 4
B.操作①和③中的有机相从分液漏斗上端倒出
C.操作④为过滤
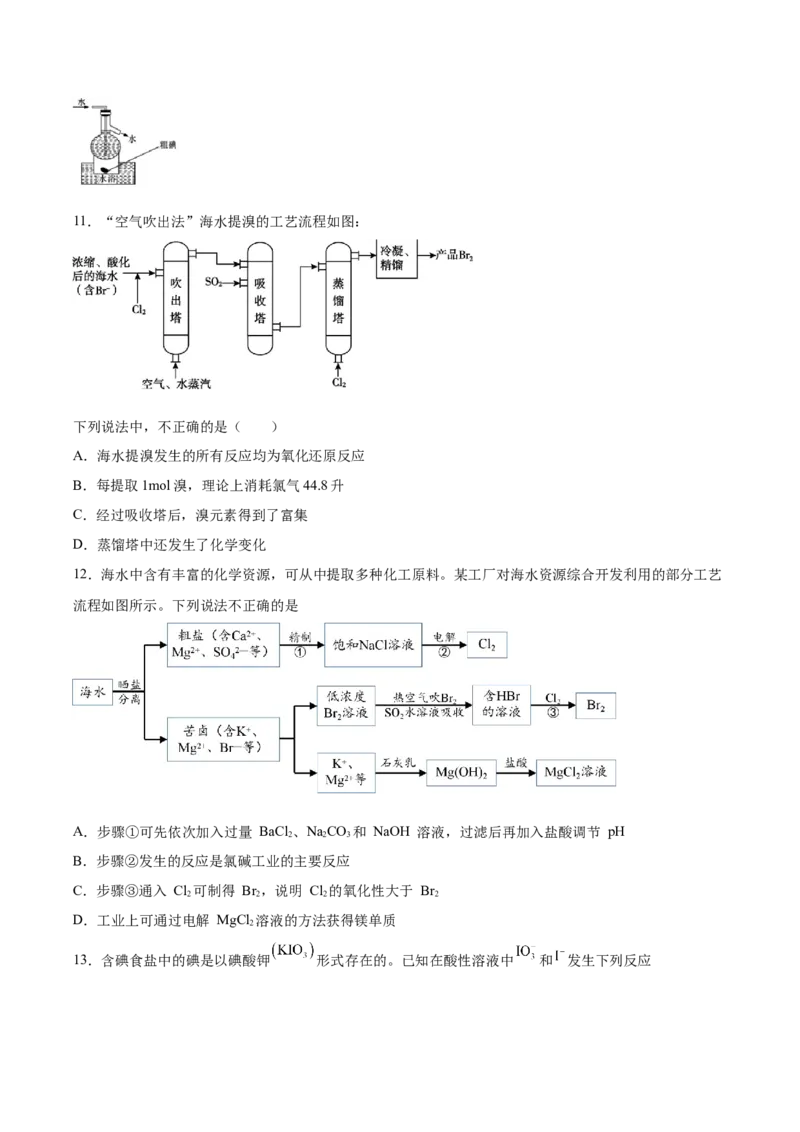
D.操作⑤可用如图所示的水浴装置进行11.“空气吹出法”海水提溴的工艺流程如图:
下列说法中,不正确的是( )
A.海水提溴发生的所有反应均为氧化还原反应
B.每提取1mol溴,理论上消耗氯气44.8升
C.经过吸收塔后,溴元素得到了富集
D.蒸馏塔中还发生了化学变化
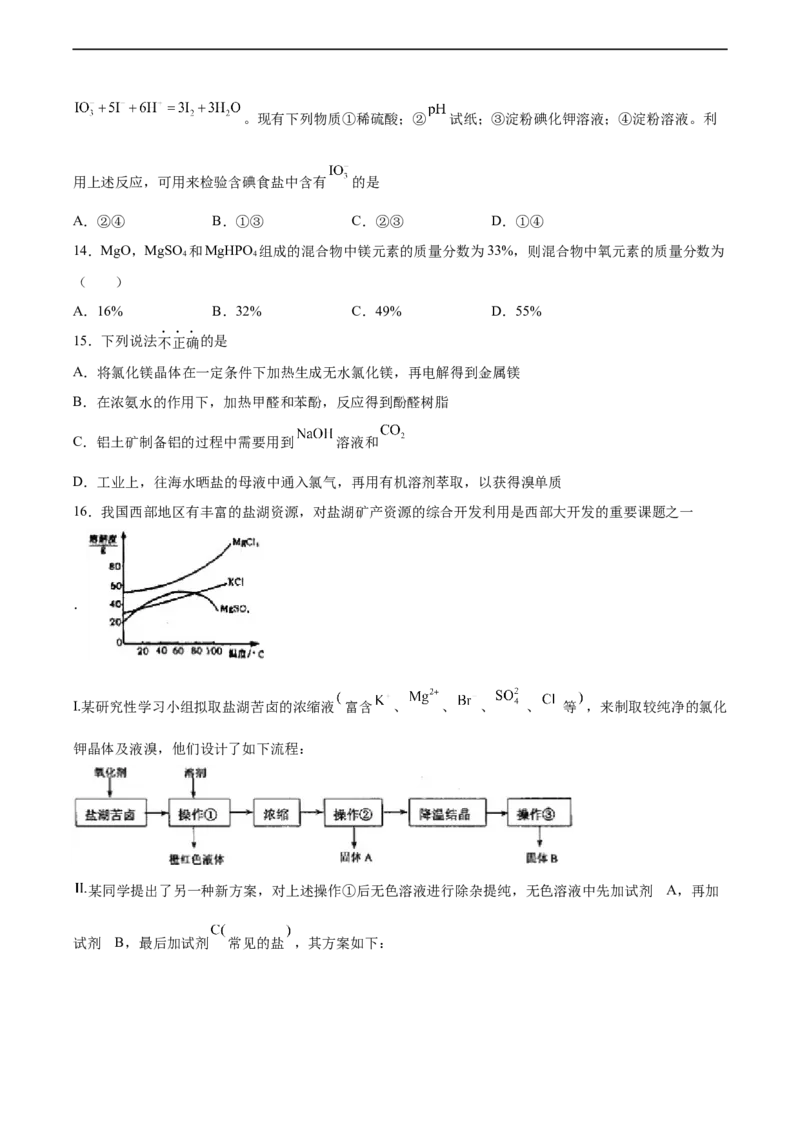
12.海水中含有丰富的化学资源,可从中提取多种化工原料。某工厂对海水资源综合开发利用的部分工艺
流程如图所示。下列说法不正确的是
A.步骤①可先依次加入过量 BaCl 、NaCO 和 NaOH 溶液,过滤后再加入盐酸调节 pH
2 2 3
B.步骤②发生的反应是氯碱工业的主要反应
C.步骤③通入 Cl 可制得 Br ,说明 Cl 的氧化性大于 Br
2 2 2 2
D.工业上可通过电解 MgCl 溶液的方法获得镁单质
2
13.含碘食盐中的碘是以碘酸钾 形式存在的。已知在酸性溶液中 和 发生下列反应。现有下列物质①稀硫酸;② 试纸;③淀粉碘化钾溶液;④淀粉溶液。利
用上述反应,可用来检验含碘食盐中含有 的是
A.②④ B.①③ C.②③ D.①④
14.MgO,MgSO 和MgHPO 组成的混合物中镁元素的质量分数为33%,则混合物中氧元素的质量分数为
4 4
( )
A.16% B.32% C.49% D.55%
15.下列说法不正确的是
A.将氯化镁晶体在一定条件下加热生成无水氯化镁,再电解得到金属镁
B.在浓氨水的作用下,加热甲醛和苯酚,反应得到酚醛树脂
C.铝土矿制备铝的过程中需要用到 溶液和
D.工业上,往海水晒盐的母液中通入氯气,再用有机溶剂萃取,以获得溴单质
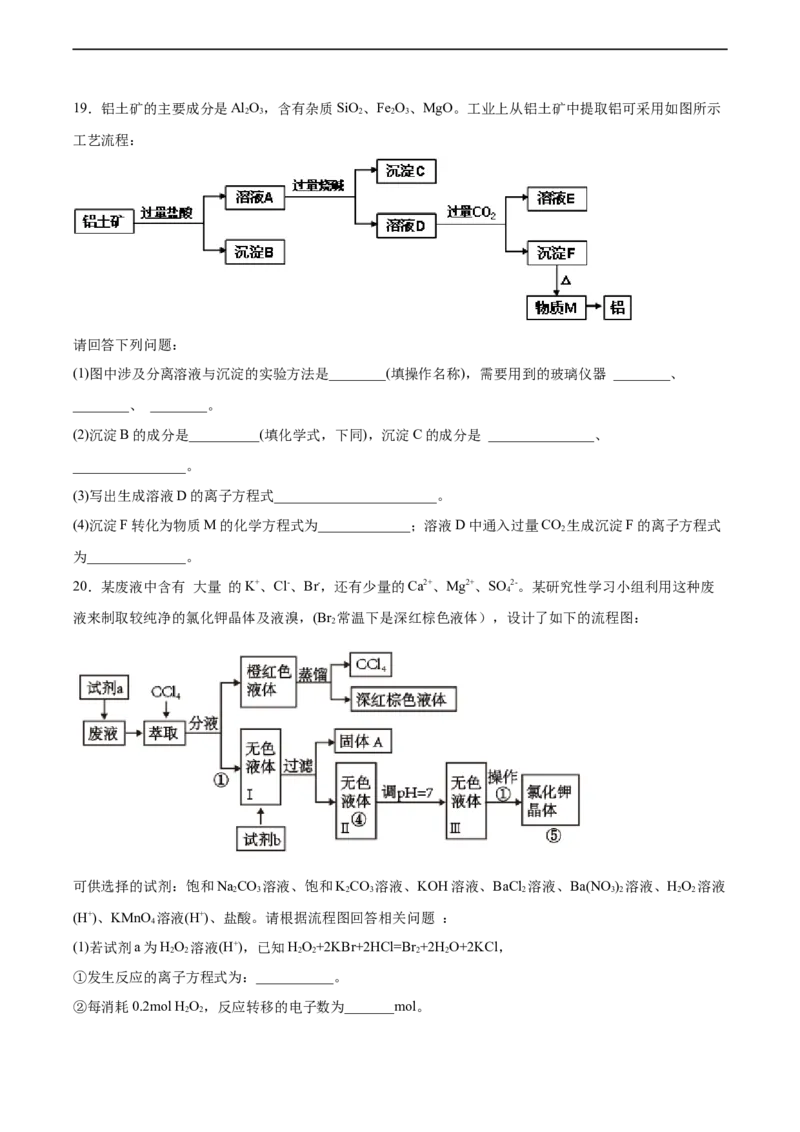
16.我国西部地区有丰富的盐湖资源,对盐湖矿产资源的综合开发利用是西部大开发的重要课题之一
.
I.某研究性学习小组拟取盐湖苦卤的浓缩液 富含 、 、 、 、 等 ,来制取较纯净的氯化
钾晶体及液溴,他们设计了如下流程:
某同学提出了另一种新方案,对上述操作①后无色溶液进行除杂提纯,无色溶液中先加试剂 A,再加
试剂 B,最后加试剂 常见的盐 ,其方案如下:下列说法不正确的是
A.要从橙红色液体中分离出单质溴,可采取的操作是蒸馏
B.操作 为过滤,主要目的是为了除去
C.试剂C为 ,固体D主要为 ,还有少量的
D.若在操作 结束后发现溶液略有浑浊,应采取的措施是更换滤纸,重新过滤
17.根据下列实验操作和现象所得到的结论正确的是( )
选
实验操作和现象 结论
项
向酸性含碘废水中加入淀粉溶液,然后滴入
A 该废水中可能含IO -
少量NaSO 溶液,废水立刻变蓝色 3
2 3
向蛋白质溶液中滴加饱和CuSO 溶液,有固 蛋白质的结构没有变化,但失
B 4
体析出,再加水固体不溶解 去生物活性
向1-溴丙烷中加入KOH溶液,加热并充分振
C 荡,然后取少量液体滴入AgNO 溶液,出现 1-溴丙烷中混有杂质
3
棕黑色沉淀
将乙醇与浓硫酸混合溶液加热,产生的气体
D 直接通入酸性KMnO 溶液,溶液紫色逐渐褪 产生的气体一定是乙烯
4
去
A.A B.B C.C D.D
二、综合题(共6题)
18.把10.2g镁铝合金的粉末放入过量的烧碱中,得到6.72L标准状况下的H,回答下列问题:
2
(1)写出铝与烧碱的反应的离子方程式_______
(2)列式计算:
①该合金中铝的质量_____。
②该合金溶于足量的盐酸溶液中,产生H 的体积____(标准状况下)。
219.铝土矿的主要成分是Al O,含有杂质SiO、Fe O、MgO。工业上从铝土矿中提取铝可采用如图所示
2 3 2 2 3
工艺流程:
请回答下列问题:
(1)图中涉及分离溶液与沉淀的实验方法是________(填操作名称),需要用到的玻璃仪器 ________、
________、 ________。
(2)沉淀B的成分是__________(填化学式,下同),沉淀C的成分是 _______________、
________________。
(3)写出生成溶液D的离子方程式_______________________。
(4)沉淀F转化为物质M的化学方程式为_____________;溶液D中通入过量CO 生成沉淀F的离子方程式
2
为______________。
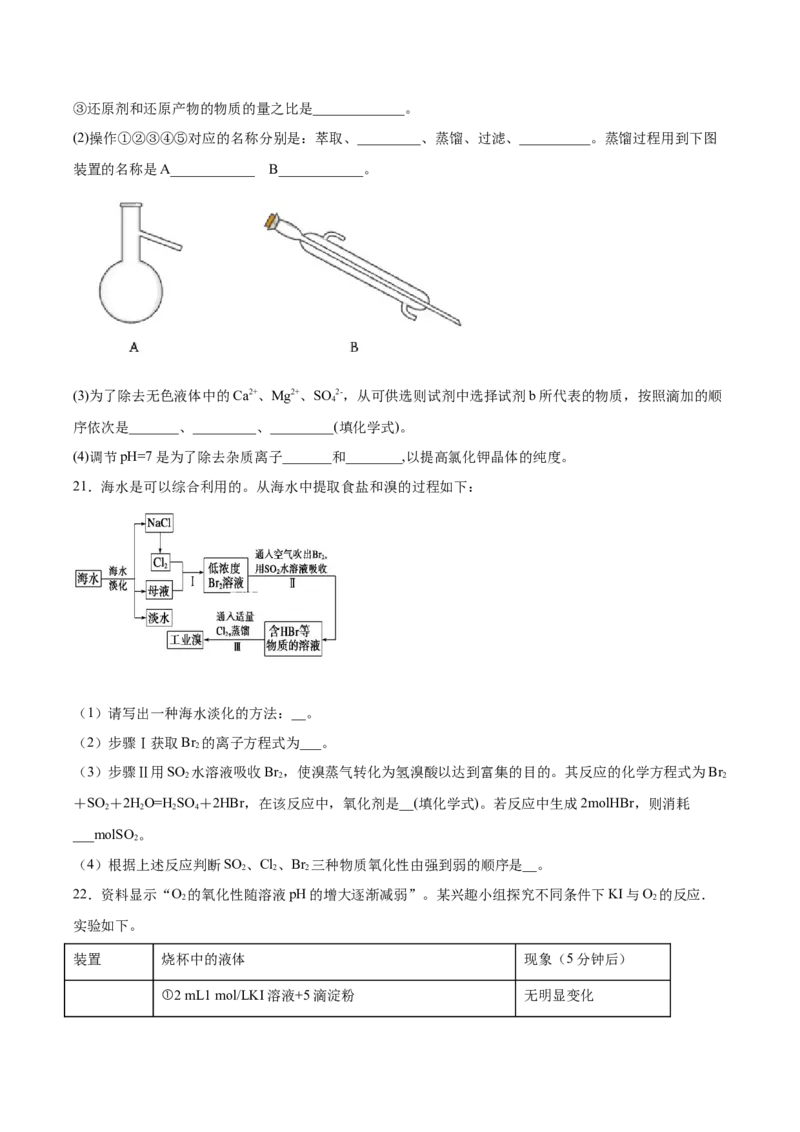
20.某废液中含有 大量 的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO 2-。某研究性学习小组利用这种废
4
液来制取较纯净的氯化钾晶体及液溴,(Br 常温下是深红棕色液体),设计了如下的流程图:
2
可供选择的试剂:饱和NaCO 溶液、饱和KCO 溶液、KOH溶液、BaCl 溶液、Ba(NO ) 溶液、HO 溶液
2 3 2 3 2 3 2 2 2
(H+)、KMnO 溶液(H+)、盐酸。请根据流程图回答相关问题 :
4
(1)若试剂a为HO 溶液(H+),已知HO+2KBr+2HCl=Br +2H O+2KCl,
2 2 2 2 2 2
①发生反应的离子方程式为:___________。
②每消耗0.2mol H O,反应转移的电子数为_______mol。
2 2③还原剂和还原产物的物质的量之比是_____________。
(2)操作①②③④⑤对应的名称分别是:萃取、_________、蒸馏、过滤、__________。蒸馏过程用到下图
装置的名称是A____________ B____________。
(3)为了除去无色液体中的Ca2+、Mg2+、SO 2-,从可供选则试剂中选择试剂b所代表的物质,按照滴加的顺
4
序依次是_______、_________、_________(填化学式)。
(4)调节pH=7是为了除去杂质离子_______和________,以提高氯化钾晶体的纯度。
21.海水是可以综合利用的。从海水中提取食盐和溴的过程如下:
(1)请写出一种海水淡化的方法:__。
(2)步骤Ⅰ获取Br 的离子方程式为___。
2
(3)步骤Ⅱ用SO 水溶液吸收Br ,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为Br
2 2 2
+SO +2HO=HSO +2HBr,在该反应中,氧化剂是__(填化学式)。若反应中生成2molHBr,则消耗
2 2 2 4
___molSO 。
2
(4)根据上述反应判断SO 、Cl、Br 三种物质氧化性由强到弱的顺序是__。
2 2 2
22.资料显示“O 的氧化性随溶液pH的增大逐渐减弱”。某兴趣小组探究不同条件下KI与O 的反应.
2 2
实验如下。
装置 烧杯中的液体 现象(5分钟后)
①2 mL1 mol/LKI溶液+5滴淀粉 无明显变化②2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L HCl 溶液变蓝
③2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L KCl 无明显变化
④2 mL1 mol/LKI溶液+5滴淀粉+2 mL0.2 mol/L 溶液变蓝,颜色较②
CHCOOH 浅
3
(1)实验②中生成I 的离子方程式是___________。
2
(2)实验③的目的是_________________________________________________________________。
(3)实验④比②溶液颜色浅的原因是________。
(4)为进一步探究KI与O 的反应,用上表中的装置继续进行实验:
2
现象(5小时
烧杯中的液体
后)
⑤2 mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀
溶液才略变蓝
粉
⑥2 mLpH=10混有KOH的1mol/L KI溶液+5滴淀
无明显变化
粉
I.对于实验⑥的现象.甲同学提出猜想“pH=10时O 不能氧化I-”,设计了下列装置进行实验,验证猜想。
2
i.烧杯a中的溶液为____。
ii.实验结果表明,此猜想不成立。支持该结论的实验现象是:通入O 后,_______。
2
Ⅱ.乙同学向pH=10的KOH溶液(含淀粉)中滴加碘水,溶液先变蓝后迅速褪色.经检测褪色后的溶液
中含有IO -,褪色的原因是(用离子方程式表示)____________。
3
(5)该小组同学对实验过程进行了整体反思.推测实验①的现象产生的原因可能是______;实验⑥的现
象产生的原因可能是_______。
23.嫦五升空登月取土,一共带回1731克月球样品,主要为月壤,包含微细的矿物颗粒、岩石碎屑和玻璃
质微粒等,主要由氧(O)、硅( )、铝( )、铁( )、镁( )、钙( )、钠( )、钾(K)、钛( )、镍( )
等元素构成,不含任何有机养分,而且非常干燥。请回答下列问题:
(1)基态镍( )原子的价电子排布式为_______。(2)从原子结构角度分析,第一电离能 ( )与 ( )的关系是 ( )____ ( )(填“>”“<”或“=”),原因
是_______。
(3)已知 的熔点 ℃,沸点43℃, 晶体类型是_______,在 中与 形成配位键
的原子是_______。
(4)最常见的硅酸盐为 , 中心原子采用_____杂化,空间构型为_____。
(5) 的晶胞如图(a)所示,金属离子与氧离子间的作用力为____, 的配位数是_____。另一种立方
钙钛矿结构的金属卤化物光电材料的组成为 、 和有机碱离子 ,其晶胞如图(b)所示。其中
与图(a)中___的空间位置相同;若晶胞参数为 ,则晶体(b)的密度为____ (保留两位
小数)。参考答案
1.A
【详解】
A.二氧化硫虽然有漂白性,但是不能漂白酸碱指示剂,A错误;
B.利用工业生产产生的二氧化碳制造全降解塑料,符合绿色环保要求,B正确;
C.氧化镁晶格能较大,熔点高,是一种优良的耐火材料,C正确;
D.温度过高可以使蛋白质变性,所以疫苗一般应冷藏存放,D正确;
故答案为A。
2.D
【详解】
A、钠是一种强还原剂,可以把钛、锆、铌等从其熔融盐中置换出来,故A正确;
B、镁常用于制造信号弹和焰火,是因为燃烧发出耀眼的白光,故B正确;
C、印刷电路板的制作的原理是Cu+2FeCl =CuCl +2FeCl ,故C正确;
3 2 2
D、铁在浓硫酸中发生钝化,而在稀硫酸中要发生氧化还原反应,故能用铁制容器贮存的
是浓硫酸,故D错误;
故答案选D。
3.C
【解析】
试题分析:A.铝钝化生成三氧化二铝;
B.光合作用过程中有新物质氧气等生成;
C.碘的升华没有新物质生成;
D.海水提溴有新物质溴生成.
解:A.铝钝化生成三氧化二铝,有新物质生成,属于化学变化,故A错误;
B.光合作用过程中有新物质氧气等生成,属于化学变化,故B错误;
C.碘的升华没有新物质生成,属于物理变化,故C正确;
D.海水提溴有新物质溴生成,属于化学变化,故D错误.
故选C.
4.A
【分析】
用完之后不能再产生,属于不可再生能源。用完之后能够再产生的物质,属于可再生能源,
据此分析。
【详解】
海底多金属结核矿、海滨砂矿、海水化学资源,都属于不可再生的能源,海水的潮涨潮落
是自然现象,因此潮汐能属于可再生的能源;故选A。
5.A
【详解】A.萃取剂要和原溶剂互不相溶,而酒精和水互相溶解,不能代替四氯化碳作为萃取剂,
故A错误;
B.向滤液中加入稀硫酸和双氧水,双氧水在酸性条件下把碘离子氧化为碘单质,发生的
反应是2H++H O+2I-=2H O+I ,故B正确;
2 2 2 2
C.碘单质遇淀粉会变蓝色是碘的特征性质,向碘水中加入几滴淀粉溶液,溶液变蓝色,
故C正确;
D. 灼烧应该在坩埚中进行,实验室剪碎干海带用酒精湿润,放在坩埚中灼烧至完全变成
灰烬,故D正确;
故答案为:A
6.A
【详解】
(1)柠檬属于碱性食物,错误;(2)香炉中燃烧的香中不含有碘,错误;(3)若存在简
单离子R2-,则R的最低价是-2价,因此R一定属于VIA族,正确;(4)青石棉(化学
式为NaFe Si O (OH)),是一种硅酸盐产品,它不含有石英,错误;(5)“海沙危
2 5 8 22 2
楼”是由于海沙带有腐蚀性,会腐蚀混凝土中的钢筋等,正确;(6)浓硝酸具有腐蚀性,
见光受热易分解,用带玻璃塞的棕色试剂瓶存放浓HNO,错误;
3
故答案选A。
7.B
【详解】
A.海水中含有MgCl ,先向海水中加入生石灰得到Mg(OH) 沉淀,经过滤、洗涤得到纯
2 2
净的Mg(OH) ,然后用盐酸溶解获得MgCl 溶液,再将溶液蒸发浓缩获得氯化镁晶体,通
2 2
过在HCl气氛中加热获得无水MgCl ,然后电解熔融的无水MgCl 获得金属Mg,发生了化
2 2
学变化,A不符合题意;
B.海水中含有NaCl,由于NaCl的溶解度受温度的影响变化不大,所以采用蒸发溶剂的方
法获得NaCl,属于物理变化,B符合题意;
C.海水中的溴元素以NaBr等化合物的形式存在,要通过氧化还原反应得到单质Br ,发
2
生了化学变化,C不符合题意;
D.海水中钾元素以KCl等化合物形式存在,先分离得到纯净的KCl,然后电解熔融的
KCl,得到单质钾,发生了化学变化,D不符合题意;
答案选B。
8.B
【解析】
试题分析:A、25 ℃,NaHCO 在水中的溶解度比NaCO 的小,A错误;B、2Ca(OH)
3 2 3
+2Cl=CaCl +Ca(ClO)+2H O,Cl元素的化合价既升高又降低,所以氯气既是氧化剂,
2 2 2 2 2
又是还原剂,B正确;C、电解NaCl溶液的阴极产物为H 和NaOH,C错误;D、氯化钠
2
和水、氨气、二氧化碳的反应以及碳酸氢钠的分解反应都不是氧化还原反应,D错误,答
案选B。考点:考查盐的溶解性、氧化还原反应、电极产物判断
9.D
【详解】
A.从海水中提炼溴和碘,是用氯气把其中的碘离子和溴离子氧化为碘单质和溴单质,故
A错误;
B.海水中得到钠、镁,需要首先从海水中获得氯化钠和氯化镁,然后再去电解熔融状态
的氯化钠和氯化镁即得钠和镁,故B错误;
C.可从海水中获得氯化钠,然后电解饱和食盐水,即得烧碱、氢气和氯气,故C错误;
D.把海水用蒸馏等方法可以得到淡水,把海水用太阳暴晒,蒸发水分后即得食盐,不需
要化学变化就能够从海水中获得,故D正确;
故选:D。
10.D
【详解】
A. 由操作③用四氯化碳萃取可知,操作②中生成碘单质,发生反应的离子方程式为2IO -
3
+5SO2-+2H+=I +5SO2-+H O,故A错误;
3 2 4 2
B. 四氯化碳的密度大于水,有机相在下层,操作①和③中的有机相从分液漏斗下端放出,
故B错误;
C. 操作④是从碘的四氯化碳溶液溶液中分离出碘单质,方法为蒸馏,故C错误;
D. 碘易升华,可以通过水浴加热的方式使碘升华后,在冷的烧瓶底部凝华,故D正确;
答案选D。
11.B
【分析】
“空气吹出法”海水提溴的过程为向浓缩、酸化后的海水中通入氯气,氯气可以将溴离子
氧化成溴单质,然后在吹出塔中用空气和水蒸气将溴吹出,再在吸收塔中用二氧化硫还原
空气中的溴气为溴离子,实现与溴与空气分离,再在蒸馏塔中先通入氯气将溴离子氧化为
溴单质,后蒸馏使溴与溶液分离,最后冷凝、精馏后得到产品溴。
【详解】
A.海水提溴发生的反应依次有氯气氧化溴离子、二氧化硫还原溴单质成溴离子,氯气再氧
化溴离子,均为氧化还原反应,故A正确;
B.每提取1mol溴,需要用到两次氯气,一共2mol氯气,但因为未知温度压强,所以不能
计算氯气的体积,故B错误;
C.由分析可知,经过吸收塔后,溴元素的浓度明显提升,所以这个过程中溴元素得到了富
集,故C正确;
D.在蒸馏塔中氯气氧化溴离子为溴单质,发生了化学变化,故D正确;
综上所述,答案为B。
12.D
【详解】A.氯化钡可以除去硫酸根,碳酸钠可以除去钙离子和过量的钡离子,NaOH除去镁离子,
为了除去过量钡离子,碳酸钠需要在氯化钡之后加入,然后过滤,向滤液中加入适量盐酸
调节pH即可得精制的NaCl溶液,故A正确;
B.氯碱工业的主要反应即电解饱和食盐水得到NaOH和氯气的过程,故B正确;
C.步骤③通入Cl 可制得Br ,Cl 为氧化剂,Br 为氧化产物,说明Cl 的氧化性大于
2 2 2 2 2
Br ,故C正确;
2
D.电解氯化镁溶液得到的是氢氧化镁沉淀,应电解熔融氯化镁制取镁单质,故D错误;
综上所述答案为D。
13.B
【详解】
由 及 遇淀粉变蓝可知,检验食盐中存在 ,该反应需要酸
性条件,需要碘离子,则选淀粉碘化钾试纸检验,生成的 由淀粉检验,故选B。
14.C
【分析】
MgHPO 中H和P的相对原子质量之和为1+31=32和硫的相对原子质量是相等的,因此
4
MgHPO 可以看成是MgSO ,MgSO 可以看成是MgO∙SO ,所以MgO,MgSO ,和
4 4 4 3 4
MgHPO 组成的混合物实际可以看成是由氧化镁和三氧化硫组成,据此原子质量守恒进行
4
计算分析。
【详解】
混合物中氧化镁的质量分数为x,含硫元素的质量分数为y;
根据镁原子质量守恒可得:
x=55%,则三氧化硫的质量分数为1-55%=45%;
根据硫原子守恒可得:
解得y=18%,则混合物中氧元素的质量分数=1-18%-33%=49%,答案选C。
15.D
【详解】
A.将氯化镁晶体在干燥HCl氛围中加热,得到无水氯化镁,然后电解熔融的氨化镁得到
金属镁,正确;
B.在浓氨水的作用下,加热甲醛和苯酚,两者通过缩聚反应得到酚醛树脂,正确;
C.由铝土矿制备较高纯度Al,可用氧化铝与氢氧化钠反应生成偏铝酸钠溶液,过滤后通
入二氧化碳生成氢氧化铝,氢氧化铝分解生成氧化铝,电解氧化铝可生成铝,电解时为降低熔点,可加入冰晶石,正确;
D.将氯气通入提取粗食盐后的母液中,再鼓入热空气或水蒸气将溴吹出,错误;
故选D。
16.B
【分析】
Ⅰ.在盐湖苦卤的浓缩液中加入的氧化剂应为氯气,可使溴离子生成溴单质,通过萃取、分
液的方法分离、浓缩后得到硫酸镁和氯化钾的混合液,经重结晶可得硫酸镁,过滤得到氯
化钾溶液,经降温结晶,过滤可得到氯化钾;Ⅱ.上述操作①后无色溶液含有 、 、
、 等离子,在无色溶液中先加试剂 ,以除去 ,再加试剂
以除去 ,最后加试剂 ,可除去过量的钡离子,过滤可得到 、
沉淀以及少量 沉淀,然后加入盐酸可除去过量的氢氧化钾和碳酸钾,经蒸发、浓缩、
冷却结晶可得到氯化钾,据此分析解答。
【详解】
A.溴与有机溶剂互溶,利用溴与有机溶剂沸点的不同,可以采用蒸馏的方法分离,故A正
确;
B.硫酸镁在高温下溶解度较小,氯化钾在高温时溶解度大,采用趁热过滤,能除去不溶性
杂质硫酸镁,防止氯化钾冷却后析出,所以操作②为趁热过滤,故B错误;
C.操作①后无色溶液含有 、 、 、 以及实验的目的是制取较纯净的氯化钾
晶体,需先用氢氧化钾除去 ;再用氯化钡除去 ,最后再用碳酸钾除去过量的氯
化钡,得到的沉淀为氢氧化镁、硫酸钡和碳酸钡,故C正确;
D.溶液略有浑浊,说明滤纸破损,所以应更换滤纸,重新过滤,故D正确;
故选B。
17.A
【详解】
A.酸性条件下SO 2-和IO -能发生5SO 2-+2IO -+2H+═I +5SO2-+H O,生成的I 遇淀粉溶液,
3 3 3 3 2 4 2 2
使溶液变蓝色,则能说明废水中可能含IO -,故A正确;
3
B.蛋白质溶液中滴加饱和CuSO 溶液,蛋白质发生变性,则蛋白质的结构发生改变,也
4
失去了生理活性,故B错误;
C.1-溴丙烷中加入KOH溶液并加热,发生水解反应,未加入稀硝酸中和过量的NaOH,
直接滴加硝酸银溶液,会有灰黑色Ag O沉淀生成,则无法判断1-溴丙烷中是否混有杂质,
2
故C错误;
D.乙醇易挥发,挥发的乙醇及生成的乙烯均使高锰酸钾褪色,则高锰酸钾褪色不能说明
产生的气体一定是乙烯,故D错误;
故答案为A。
18.2Al+2OH-+2H O=2AlO +3H ↑ 5.4g 11.2L
2 2【详解】
(1)铝与烧碱反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H O=2AlO
2
+3H ↑;
2
(2)①10.2g合金生成气体的物质的量为:n(H )=6.72L÷22.4L/mol=0.3mol,则:
2
因此合金中铝的质量是0.2mol×27g/mol=5.4g;
②根据①可知,合金中镁的物质的量为:(10.2g-5.4g)÷24g/mol=0.2mol,根据反应方程式
Mg+2HCl=MgCl +H ↑可知,生成氢气的物质的量为:n(H )=n(Mg)=0.2mol,根据反应
2 2 2
2Al+6HCl=2AlCl +3H ↑可知,生成气体的物质的量为:
3 2
n(H )=1.5n(Al)=0.2mol×1.5=0.3mol,故生成标况下的氢气的体积为:(0.2mol+0.3mol)
2
×22.4L/mol=11.2L。
19.过滤 烧杯 玻璃棒 漏斗 SiO Mg(OH) Fe(OH) Al3++4OH-
2 2 3
=AlO -+2H O 2Al(OH) Al O+3H O AlO -+CO +2H O=Al(OH) ↓+HCO-
2 2 3 2 3 2 2 2 2 3 3
【分析】
铝土矿主要成分是Al O,其中含有杂质SiO、Fe O、MgO,向加入过量盐酸,Al O、
2 3 2 2 3 2 3
MgO、Fe O 与盐酸反应,产生溶液A中含有AlCl 、FeCl 、MgCl 及过量的盐酸,而SiO
2 3 3 3 2 2
与盐酸不反应,所以沉淀B为SiO,向溶液A加入过量烧碱,FeCl 、MgCl 反应产生
2 3 2
Fe(OH) 和Mg(OH) 沉淀,所以沉淀C为Fe(OH) 和Mg(OH) ,而AlCl 与过量NaOH溶液
3 2 3 2 3
反应产生NaAlO ,所以溶液D为NaAlO 、NaOH的混合物,向溶液D中通入过量CO 气
2 2 2
体,NaAlO 反应产生Al(OH) 沉淀,同时得到NaHCO ,则溶液E为NaHCO ,沉淀F为
2 3 3 3
Al(OH) 。加热Al(OH) ,分解得到M为Al O,经电解可得到Al,据此分析解答。
3 3 2 3
【详解】
经上述分析可知A为AlCl 、FeCl 、MgCl 、HCl的混合物;B为SiO,C为Fe(OH) 和
3 3 2 2 3
Mg(OH) ,D为NaAlO 、NaOH的混合物,E为NaHCO ,沉淀F为Al(OH) ,M为
2 2 3 3
Al O。
2 3
(1)图中分离溶液与沉淀的实验方法是过滤;需要用到的玻璃仪器有烧杯、玻璃棒、漏斗;
(2)根据上述分析可知:沉淀B的成分是SiO;沉淀C的成分是Mg(OH) 、Fe(OH) ;
2 2 3
(3)向含有Al3+的溶液中加入过量NaOH溶液,Al3+会反应转化为AlO-,则生成NaAlO 反应
2 2
的离子方程式为:Al3++4OH-=AlO -+2H O;
2 2
(4)沉淀F是Al(OH) ,该物质不稳定,加热分解产生Al O 和 HO,因此沉淀F转化为M
3 2 3 2
的化学方程式为:2Al(OH) Al O+3H O;
3 2 3 2
溶液D为NaAlO 和NaOH的混合物,向其中通入过量CO,NaAlO 与CO2及溶液中的水
2 2 2
反应生成Al(OH) 沉淀,该反应的离子方程式为AlO-+CO +2H O=Al(OH) ↓+HCO-。
3 2 2 2 3 3
20.HO+2Br-+2H+=Br ↑+2H O 0.4 2:1 分液 蒸发结晶 具支烧瓶 冷
2 2 2 2凝管 BaCl KOH K CO OH- CO 2-
2 2 3 3
【分析】
根据图示可知,制备流程为:废液中加入双氧水,将溴离子氧化成溴单质,然后加入四氯
化碳后通过萃取、分液分离出溴,通过操作③蒸馏得到四氯化碳和溴单质;无色液体Ⅰ中
含有K+、Cl-、Ca2+、Mg2+、SO 2-,分别加入BaCl 、KCO、KOH溶液过滤后得到无色溶
4 2 2 3
液Ⅱ和固体A,再调节溶液Ⅱ的pH萃取碳酸根离子、氢氧根离子,得到无色溶液Ⅲ,最后
通过蒸发结晶获得氯化钾固体;
(1)根据化学方程式HO+2KBr+2HCl=Br +2H O+2KCl写出离子方程式;找到过氧化氢
2 2 2 2
和转移的电子数之间的关系,找出还原剂和还原产物的物质的量之比;
(2)加入CCl 的目的是萃取;紧接着萃取后的操作是将有机层与水层分开,叫做分液;
4
从含有溴的CCl 溶液中分离得到CCl 和液溴的操作,是将两种相互混溶的液体进行分离的
4 4
操作,叫做蒸馏;操作④完成后得到固体A和无色液体I,分离固体和液体的操作是过滤;
操作⑤是从溶液中得到能溶解于水的氯化钾晶体,是蒸发结晶;
(3)除去Ca2+,选用饱和KCO 溶液;除去Mg2+,选用KOH溶液;除去SO 2-,选用
2 3 4
BaCl 溶液;
2
(4)无色液体Ⅱ中还含有杂质离子CO2-和OH-;用pH试纸测定至pH=7。
3
【详解】
制备流程为:废液中加入双氧水,将溴离子氧化成溴单质,然后加入四氯化碳后通过萃取、
分液分离出溴,通过操作③蒸馏得到四氯化碳和溴单质;无色液体Ⅰ中含有K+、Cl−、Ca2+、
Mg2+、SO 2−,分别加入BaCl 、KCO、KOH溶液过滤后得到无色溶液Ⅱ和固体A,再调
4 2 2 3
节溶液Ⅱ的pH萃取碳酸根离子、氢氧根离子,得到无色溶液Ⅲ,最后通过蒸发结晶获得
氯化钾固体;
(1)由加入的CCl 及得到的深红棕色液体知,试剂a能将Br−氧化为Br ,试剂a应具有氧化
4 2
性,所以应选用HO 溶液,离子方程式为HO +2Br-+2H+=Br ↑+2H O,HO 中氧的化合价
2 2 2 2 2 2 2 2
从-1到-2,氧原子个数为2,全部降低,故1mol HO 发生反应时转移的电子数2mol,每
2 2
消耗0.2mol H O 转移电子的物质的量为0.4mol;还原剂是溴化氢,还原产物为水,它们
2 2
的物质的量之比为2:1;
(2)由流程图知,无色液体Ⅰ中含有K+、Cl−、Ca2+、Mg2+、SO 2−,无色液体Ⅲ中只含有
4
K+、Cl−,则试剂b的作用是除去Ca2+、Mg2+、SO 2−;操作①是萃取,操作②是将互不相溶
4
的两种液体分开,为分液操作,操作③是将沸点不同、互溶的两液体分开,为蒸馏操作,
操作④是将溶液与沉淀分开,为过滤操作,操作⑤是将KCl从其水溶液中提取出来,为蒸
发结晶操作,操作①、②、③、④、⑤的名称是:萃取、分液、蒸馏、过滤、蒸发结晶,
蒸馏过程A为具支试管,B为冷凝管;
(3)由于除杂时除杂试剂需过量,且不能引入新杂质,所以除去Ca2+,选用饱和KCO 溶
2 3
液;除去Mg2+,选用KOH溶液;除去SO 2−,选用BaCl 溶液。要除去过量的BaCl ,要满
4 2 2
足BaCl 溶液在饱和KCO 溶液之前加入即可;
2 2 3
(4)由以上知,无色液体Ⅱ中还含有杂质离子CO2−和OH−,需用盐酸来除去过量的OH−及
3CO2−,调节pH=7的操作方法是滴加盐酸,无气体产生时,用pH试纸测定至pH=7。
3
21.蒸馏法 Cl+2Br-=Br +2Cl- Br 1 Cl >Br >SO
2 2 2 2 2 2
【分析】
(1)海水淡化的方法很多,可以让海水中的金属及酸根离子离开,如通过离子交换剂;可
以用电渗析法;也可用蒸馏法。
(2)步骤Ⅰ获取Br 的反应中氯气与溴离子发生反应。
2
(3)Br +SO +2HO=HSO +2HBr,在该反应中,Br 中的Br元素价态降低,SO 中的S
2 2 2 2 4 2 2
元素价态升高,从反应式看,生成2molHBr,消耗1molSO 。
2
(4)SO 、Cl、Br 三种物质氧化性关系,可利用反应中氧化剂的氧化性大于氧化产物的
2 2 2
氧化性进行判断.
【详解】
(1)海水淡化的方法:最常见的为蒸馏法。答案:蒸馏法;
(2)步骤Ⅰ获取Br 的离子方程式为Cl+2Br-=Br +2Cl-。答案为:Cl+2Br-=Br +2Cl
2 2 2 2 2
-;
(3)在该反应Br +SO +2HO=HSO +2HBr中,氧化剂是Br ;若反应中生成
2 2 2 2 4 2
2molHBr,则消耗1molSO 。答案为:Br ;1;
2 2
(4)在反应Cl+2Br-=Br +2Cl-中,氧化性Cl>Br ;在反应Br +SO +2HO=HSO +
2 2 2 2 2 2 2 2 4
2HBr中,氧化性Br >SO,所以SO 、Cl、Br 三种物质氧化性由强到弱的顺序是
2 2 2 2 2
Cl>Br >SO。答案为:Cl>Br >SO。
2 2 2 2 2 2
22.4I-+O +4H+=2I +2H O 验证Cl-是否影响KI与O 的反应 其他条件相同时,
2 2 2 2
CHCOOH是弱电解质,溶液中c(H+)较盐酸小,O 的氧化性减弱 pH=10的KOH溶液
3 2
电流表指针偏转,烧杯b的溶液颜色变深 3I+6OH-=IO -+5I-+3H O 中性条件下,O
2 3 2 2
的氧化性比较弱,该反应速率慢,短时间内难以生成“一定量” 碘单质使溶液颜色发生变
化 pH=10的KOH溶液中I-被氧化生成I,I 迅速发生歧化反应变为IO -和I-
2 2 3
【详解】
(1)实验②是在酸性条件下氧气将碘离子氧化生成碘单质,碘单质遇淀粉使溶液变蓝,其反
应的离子方程式是:4I-+O +4H+=2I +2H O;(2)实验②加入盐酸电离产生的H+和Cl-,通
2 2 2
过实验③可以排除是否为Cl-离子对于KI与O 的反应的影响;(3) 其他条件相同时,
2
CHCOOH是弱电解质,溶液中c(H+)较盐酸小,O 的氧化性随溶液pH的增大逐渐减弱,
3 2
故实验④比②溶液颜色浅;(4) i.甲同学提出猜想“pH=10时O 不能氧化I-”,故烧杯a中
2
的溶液可以为pH=10的KOH溶液;ii.通入O 后,若电流表指针偏转,烧杯b的溶液颜色
2
变深,则pH=10时O 也能氧化I-,此猜想不成立。Ⅱ.碱性条件下碘单质发生歧化反应生
2
成IO -和I-,则开始滴入时遇淀粉变蓝,后碘消耗而褪色,其离子反应方程式为:3I+6OH-
3 2
=IO -+5I-+3H O ;(5)实验①的现象产生的原因可能是中性条件下,O 的氧化性比较弱,该
3 2 2
反应速率慢,短时间内难以生成“一定量”的碘单质使溶液颜色发生变化;实验⑥的现象
产生的原因可能是pH=10的KOH溶液中I-被氧化生成I,I 迅速发生歧化反应变为IO -和
2 2 3
I-。23. > 最外层电子排布式为 ,而 最外层电子排布式为 ,当
3p处于全充满、半充满或全空时较稳定,因此Al失去p能级的1个电子相对比较容易
分子晶体 C 平面三角形 离子键 6 1.03 10-11
【详解】
(1)镍为28号元素,基态镍原子的价电子排布式为 ;
(2)根据第一电离能的变化规律 ,原因是 最外层电子排布式为 ,而
最外层电子排布式为 ,当3p处于全充满、半充满或全空时较稳定,因此 失去p能
级的1个电子相对比较容易;
(3)根据分子晶体熔、沸点特点确定 是分子晶体, 中C的电负性小,在
中与 形成配位键的原子是C;
(4)根据价层电子对互斥理论, 价层电子对数为3,中心原子 采用 杂化,空间构
型为平面三角形;
(5)金属离子与氧离子间的作用力为离子键,由图可知 的配位数是6;平移后得知其中
与图(a)中 的空间位置相同;若晶胞参数为 ,从图(b)可知,一个晶胞中
含有 的数目为1 1=1个, 的数目为8 =1个,I-的数目为6 =3个,故晶
胞的密度为 = =1.03 10-11 。