文档内容
第2讲 物质的量在化学实验中的应用
[考纲要求]
1.了解溶液的含义。
2.了解溶解度、饱和溶液的概念。
3.了解溶液浓度的表示方法。理解溶液中溶质的质量分数和物质的量浓度的概念,并能
进行有关计算。
4.掌握配制一定溶质质量分数溶液和物质的量浓度溶液的方法。
考点一 物质的量浓度
知识梳理
1.物质的量浓度
(1)概念:表示________________________物质的量。
(2)表达式:c=__________。
B
(3)单位:__________(或mol/L)。
2.物质的量浓度与溶质质量分数
内容 物质的量浓度 质量分数
以单位体积溶液里所含溶质的物质 用溶质质量与溶液质量之比来表示
定义
的量来表示溶液组成的物理量 溶液组成的物理量
溶质的单位 mol g
溶液的单位 L g
计算公式 ________ __________
[思考]
在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,溶质质量分
数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为________。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为________。
(3)用w、d表示溶液中溶质的物质的量浓度(c)为________。
(4)用c、d表示溶液中溶质的质量分数为________。
[判断] (正确的打“√”,错误的打“×”)
(1)1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl( )
(2)体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同( )(3)1 L 0.5 mol·L-1 CaCl 溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1(
2
)
(4)用100 mL水吸收0.1 mol HCl气体所得溶液的物质的量浓度恰好是1 mol·L-1(
)
(5)1 L水中溶解5.85 g NaCl所形成的溶液的物质的量浓度是0.1 mol·L-1( )
(6)将25 g CuSO·5HO晶体溶于75 g水中所得溶质的质量分数为25%( )
4 2
(7)将40 g SO 溶于60 g水中所得溶质的质量分数为49%( )
3
(8)将62 g Na O溶于水中,配成1 L溶液,所得溶质的物质的量浓度为1 mol·L-1(
2
)
[提醒]
1.准确计算溶液的体积
不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行
计算:
V=×10-3 L。
2.注意溶质的浓度与溶液中某离子浓度的关系
溶质的浓度和离子浓度可能不同,要注意根据化学式具体分析。如 1 mol·L-1
Al(SO) 溶液中c(SO2− )=3 mol·L-1,c(Al3+)=2 mol·L-1(考虑Al3+水解时,则其浓度
2 4 3 4
小于2 mol·L-1)。
对点速练
练点一 物质的量浓度的基本计算
1.如图是实验室配制好的两瓶NaOH溶液的标签(14%的NaOH溶液的密度为1.14 g·cm
-3)。
14%的NaOH溶液的物质的量浓度及从瓶中取出20 mL该溶液中含有溶质的质量分别是(
)
A.4.0 mol·L-1 3.2 g B.2.0 mol·L-1 3.2 g
C.4.0 mol·L-1 6.4 g D.2.0 mol·L-1 6.4 g2.在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此
氨水的物质的量浓度为__________mol·L-1。
3.将32.2 g NaSO·10HO溶于水配成1 L溶液。
2 4 2
(1)该溶液中 NaSO 的物质的量浓度为________,溶液中 Na+的物质的量浓度为
2 4
________。
(2)向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol·L-
1(假设溶液体积不变)需加入NaCl的质量为________,Cl-的物质的量浓度为________。
方法总结
1.标准状况下,气体溶解所得溶液的物质的量浓度的计算
c=
2.溶液中溶质的质量分数与物质的量浓度的换算
计算公式:c=(c为溶质的物质的量浓度,单位mol·L-1,ρ为溶液密度,单位g·cm
-3,w为溶质的质量分数,M为溶质的摩尔质量,单位g·mol-1)。
练点二 溶液的稀释与混合计算
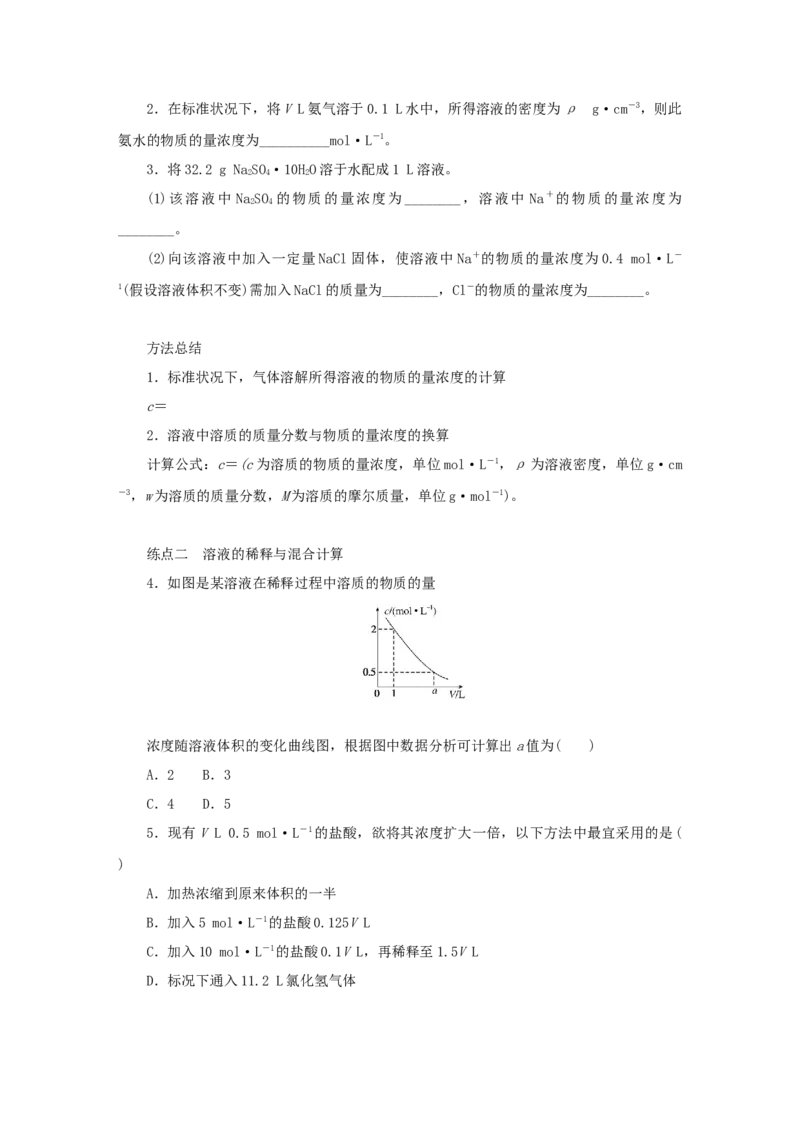
4.如图是某溶液在稀释过程中溶质的物质的量
浓度随溶液体积的变化曲线图,根据图中数据分析可计算出a值为( )
A.2 B.3
C.4 D.5
5.现有V L 0.5 mol·L-1的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是(
)
A.加热浓缩到原来体积的一半
B.加入5 mol·L-1的盐酸0.125V L
C.加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L
D.标况下通入11.2 L氯化氢气体6.V L Fe (SO) 溶液中含有a
gSO2−
,取此溶液0.5V L,用水稀释至2V L,则稀释后
2 4 3 4
溶液中Fe3+的物质的量浓度为( )
a 125a
A. mol·L-1 B. mol·L-1
576V 36V
250a 125a
C. mol·L-1 D. mol·L-1
36V 48V
方法总结
溶液稀释和混合的计算原理
(1)溶液稀释。
①溶质的质量在稀释前后保持不变,即mw=mw。
1 1 2 2
②溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
③溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
(2)溶液混合。
m混
混合前后:cV+cV=c V ,其中V = ,据此可进行相关计算。
1 1 2 2 混 混 混 ρ混
考点二 一定物质的量浓度溶液的配制
知识梳理
1.主要仪器
天平、药匙、量筒、玻璃棒、__________、__________、__________。
2.容量瓶的构造及使用
(1)容量瓶上标有________、________和________。常用规格有100 mL、250 mL、500mL、1 000 mL等。
(2)容量瓶在使用前要______________,其操作顺序为装水盖塞→倒立→正立→玻璃塞
旋转180°→倒立。
3.配制过程
以配制100 mL 1.00 mol·L-1 NaCl溶液为例。
(1)计算:需NaCl固体的质量为____ g。
(2)称量:用________称量NaCl固体。
(3)溶解:将称量好的NaCl固体放入烧杯中,用适量蒸馏水溶解,并用玻璃棒搅拌。
(4)移液:待烧杯中的溶液____________,用玻璃棒引流将溶液注入____ mL容量瓶。
(5)洗涤:用少量蒸馏水洗涤烧杯内壁和玻璃棒______次,洗涤液__________________。
轻轻摇动容量瓶,使溶液混合均匀。
(6)定容:将蒸馏水注入容量瓶,当液面距瓶颈刻度线______ cm时,改用________,
滴加蒸馏水至________________。
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀。
配制流程如下图所示:
4.质量百分比浓度、体积比浓度溶液的配制
(1)配制100 g 10%的NaCl溶液
用托盘天平称取________g NaCl固体,放入烧杯中,再用100 mL量筒量取________mL
的水注入烧杯中,然后用玻璃棒搅拌使之溶解。
(2)用浓硫酸配制1∶4的稀硫酸50 mL
用50 mL的量筒量取________mL的水注入100 mL的烧杯中,再用10 mL的量筒量取
________mL浓硫酸,然后沿烧杯内壁缓缓注入烧杯中,并用玻璃棒不停地搅拌。
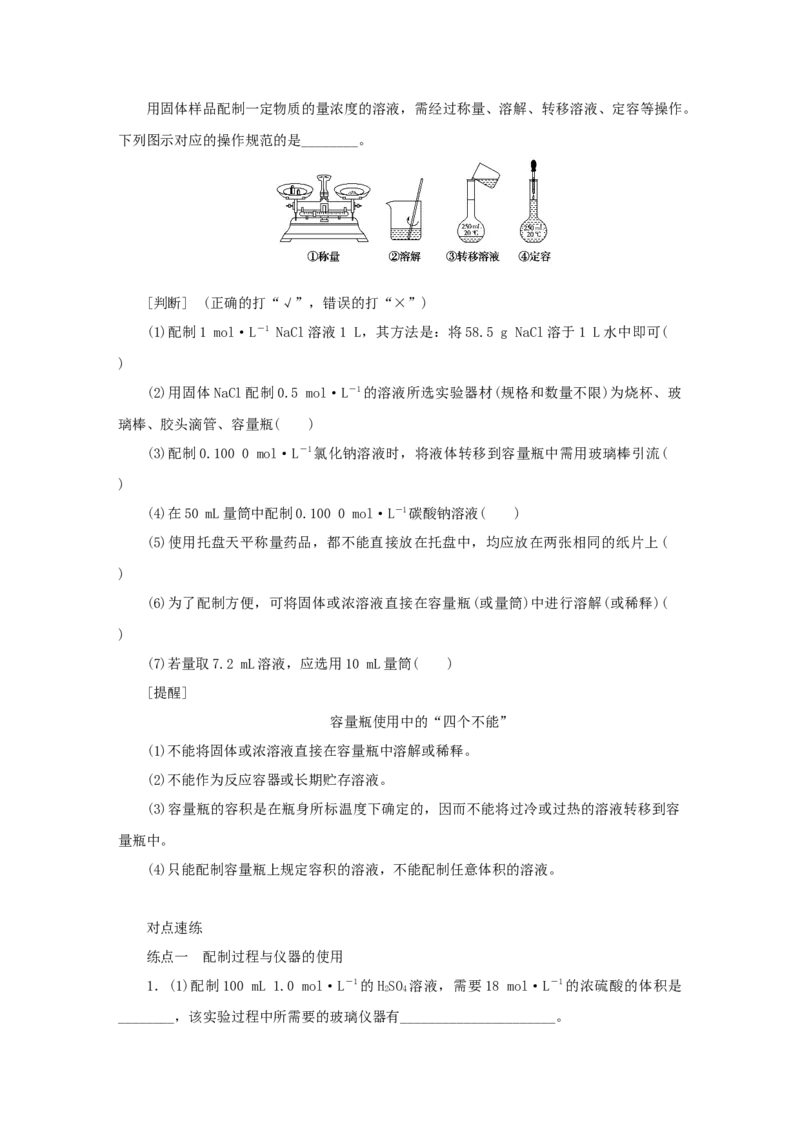
[思考]用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。
下列图示对应的操作规范的是________。
[判断] (正确的打“√”,错误的打“×”)
(1)配制1 mol·L-1 NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L水中即可(
)
(2)用固体NaCl配制0.5 mol·L-1的溶液所选实验器材(规格和数量不限)为烧杯、玻
璃棒、胶头滴管、容量瓶( )
(3)配制0.100 0 mol·L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流(
)
(4)在50 mL量筒中配制0.100 0 mol·L-1碳酸钠溶液( )
(5)使用托盘天平称量药品,都不能直接放在托盘中,均应放在两张相同的纸片上(
)
(6)为了配制方便,可将固体或浓溶液直接在容量瓶(或量筒)中进行溶解(或稀释)(
)
(7)若量取7.2 mL溶液,应选用10 mL量筒( )
[提醒]
容量瓶使用中的“四个不能”
(1)不能将固体或浓溶液直接在容量瓶中溶解或稀释。
(2)不能作为反应容器或长期贮存溶液。
(3)容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容
量瓶中。
(4)只能配制容量瓶上规定容积的溶液,不能配制任意体积的溶液。
对点速练
练点一 配制过程与仪器的使用
1.(1)配制100 mL 1.0 mol·L-1的HSO 溶液,需要18 mol·L-1的浓硫酸的体积是
2 4
________,该实验过程中所需要的玻璃仪器有______________________。(2)配制 0.2 mol·L-1的 NaCO 溶液 50 mL,计算出需要称取固体 NaCO 的质量是
2 3 2 3
________,用托盘天平称取固体NaCO 的质量是________。
2 3
2.实验室需要配制0.50 mol·L-1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,
以使整个操作完整。
(1)选择仪器
完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为 5 g)、药匙、烧杯、
__________、____________、________以及等质量的两片同种纸片。
(2)计算
配制该溶液需取NaCl晶体________g。
(3)称量
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边
缘所处的位置:
②称量过程中NaCl晶体应放于天平的______(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却
该步实验中需要使用玻璃棒,目的是
________________________________________________________________________
________________________________________________________________________。
(5)转移、洗涤
在 转 移 时 应 使 用 玻 璃 棒 引 流 , 需 要 洗 涤 烧 杯 2 ~ 3 次 是 为 了
________________________________________。
(6)定容
向容量瓶中加水至液面接近刻度线________处,改用________加水,使溶液凹液面与刻
度线相切。
(7)摇匀、装瓶
练点二 不当操作与实验误差
3.用NaOH固体配制1.0 mol·L-1的NaOH溶液220 mL,下列说法正确的是( )
A.首先称取NaOH固体8.8 gB.定容时仰视刻度线会使所配制的溶液浓度偏高
C.定容后将溶液振荡均匀,静置时发现液面低于刻度线,于是又加少量水至刻度线
D.容量瓶中原有少量蒸馏水没有影响
4.下列操作是否正确,对实验结果的影响请用“偏大”“偏小”或“无影响”表示。
(1)配制 450 mL 0.1 mol·L-1的 NaOH 溶液,用托盘天平称取 NaOH 固体 1.8 g:
__________。
(2)配制 500 mL 0.1 mol·L-1 的硫酸铜溶液,用托盘天平称取胆矾 8.0 g:
__________。
(3)配制NaOH溶液时,天平的两个托盘上放两张质量相等的纸片,其他操作均正确:
__________。
(4)配制一定物质的量浓度的 NaOH溶液,需称量溶质4.4 g,称量时物码放置颠倒:
__________。
(5)用量筒量取浓硫酸时,仰视读数:__________。
(6)定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:__________。
(7)未洗涤烧杯及玻璃棒:__________。
(8)配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到
容量瓶中并定容:__________。
(9)定容摇匀后,发现液面下降,继续加水至刻度线:__________。
(10)定容时仰视刻度线:__________。
(11)定容摇匀后少量溶液外流:__________。
(12)容量瓶中原有少量蒸馏水:__________。
方法总结
1.溶液配制过程中误差分析的依据
2.仰视、俯视的读数分析法结果:仰视时,容器内液面高于刻度线;俯视时,容器内液面低于刻度线。
本讲真题研练
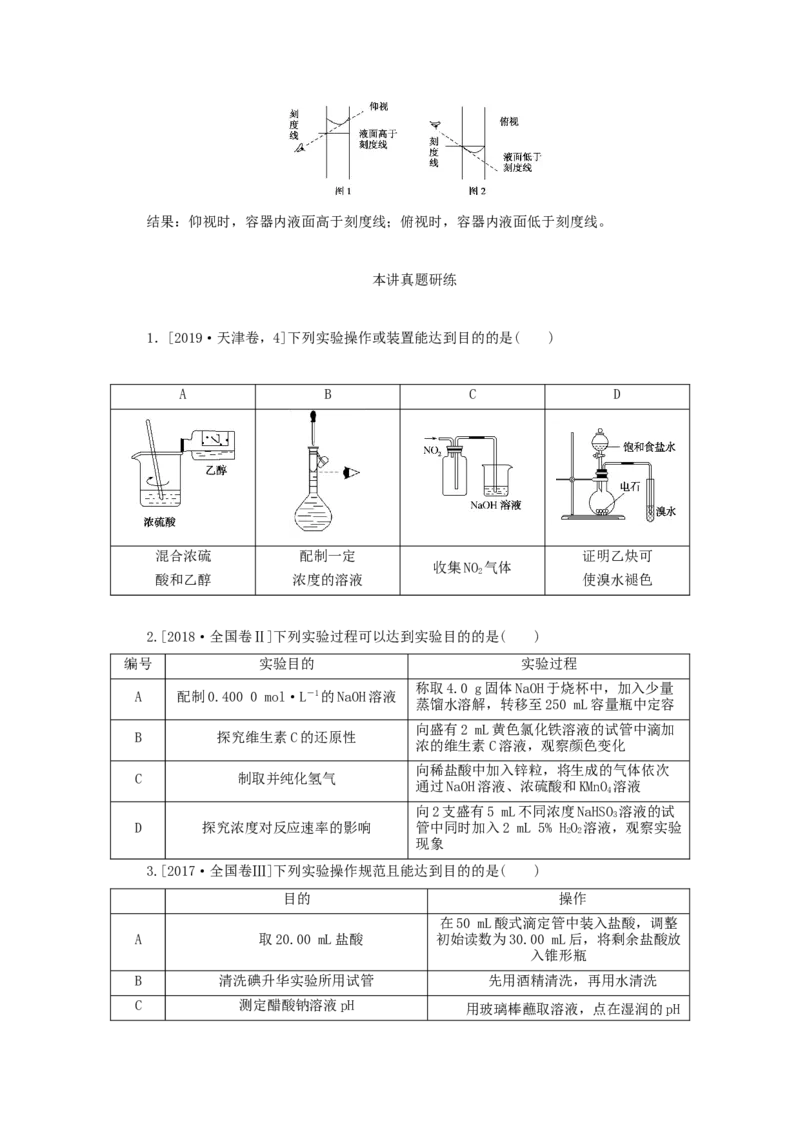
1.[2019·天津卷,4]下列实验操作或装置能达到目的的是( )
A B C D
混合浓硫 配制一定 证明乙炔可
收集NO 气体
2
酸和乙醇 浓度的溶液 使溴水褪色
2.[2018·全国卷Ⅱ]下列实验过程可以达到实验目的的是( )
编号 实验目的 实验过程
称取4.0 g固体NaOH于烧杯中,加入少量
A 配制0.400 0 mol·L-1的NaOH溶液
蒸馏水溶解,转移至250 mL容量瓶中定容
向盛有2 mL黄色氯化铁溶液的试管中滴加
B 探究维生素C的还原性
浓的维生素C溶液,观察颜色变化
向稀盐酸中加入锌粒,将生成的气体依次
C 制取并纯化氢气
通过NaOH溶液、浓硫酸和KMnO 溶液
4
向2支盛有5 mL不同浓度NaHSO 溶液的试
3
D 探究浓度对反应速率的影响 管中同时加入2 mL 5% HO 溶液,观察实验
2 2
现象
3.[2017·全国卷Ⅲ]下列实验操作规范且能达到目的的是( )
目的 操作
在50 mL酸式滴定管中装入盐酸,调整
A 取20.00 mL盐酸 初始读数为30.00 mL后,将剩余盐酸放
入锥形瓶
B 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010 mol·L-1的KMnO 溶 称取KMnO 固体0.158 g,放入100 mL
D 4 4
液 容量瓶中,加水溶解并稀释至刻度
4.(1)[2016·全国卷Ⅱ]一种双氧水的质量分数为27.5%,(密度为1.10 g·cm-3),其
浓 度 为 ________________________________________________________________________
mol·L-1。
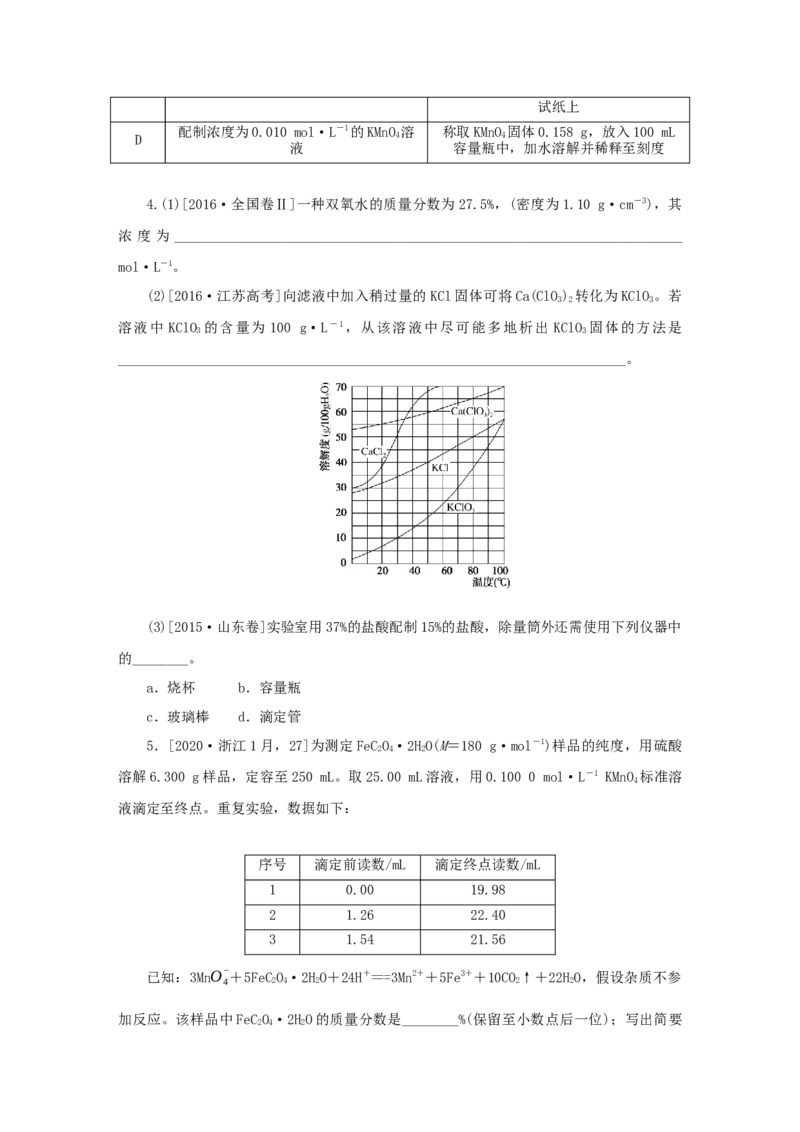
(2)[2016·江苏高考]向滤液中加入稍过量的KCl固体可将Ca(ClO) 转化为KClO 。若
3 2 3
溶液中 KClO 的含量为 100 g·L-1,从该溶液中尽可能多地析出 KClO 固体的方法是
3 3
________________________________________________________________________。
(3)[2015·山东卷]实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中
的________。
a.烧杯 b.容量瓶
c.玻璃棒 d.滴定管
5.[2020·浙江1月,27]为测定FeCO·2HO(M=180 g·mol-1)样品的纯度,用硫酸
2 4 2
溶解6.300 g样品,定容至250 mL。取25.00 mL溶液,用0.100 0 mol·L-1 KMnO 标准溶
4
液滴定至终点。重复实验,数据如下:
序号 滴定前读数/mL 滴定终点读数/mL
1 0.00 19.98
2 1.26 22.40
3 1.54 21.56
已知:3MnO− +5FeCO·2HO+24H+===3Mn2++5Fe3++10CO↑+22HO,假设杂质不参
4 2 4 2 2 2
加反应。该样品中FeCO·2HO的质量分数是________%(保留至小数点后一位);写出简要
2 4 2计算过程:__________________________________________________________________。
化学计算中的快捷解题方法
常见的守恒关系
1.质量守恒:m(反应物)=m(生成物)
2.元素守恒:反应过程中,同一元素原子的物质的量不变
3.电荷守恒:在电解质溶液中,N(正电荷)=N(负电荷),例如在KCl和NaSO 的混合
2 4
溶液中,存在关系:
c(K+)+c(Na+)=c(Cl-)+2c(SO2−
)
4
4.电子守恒:在氧化还原反应中,n(失电子)=n(得电子)
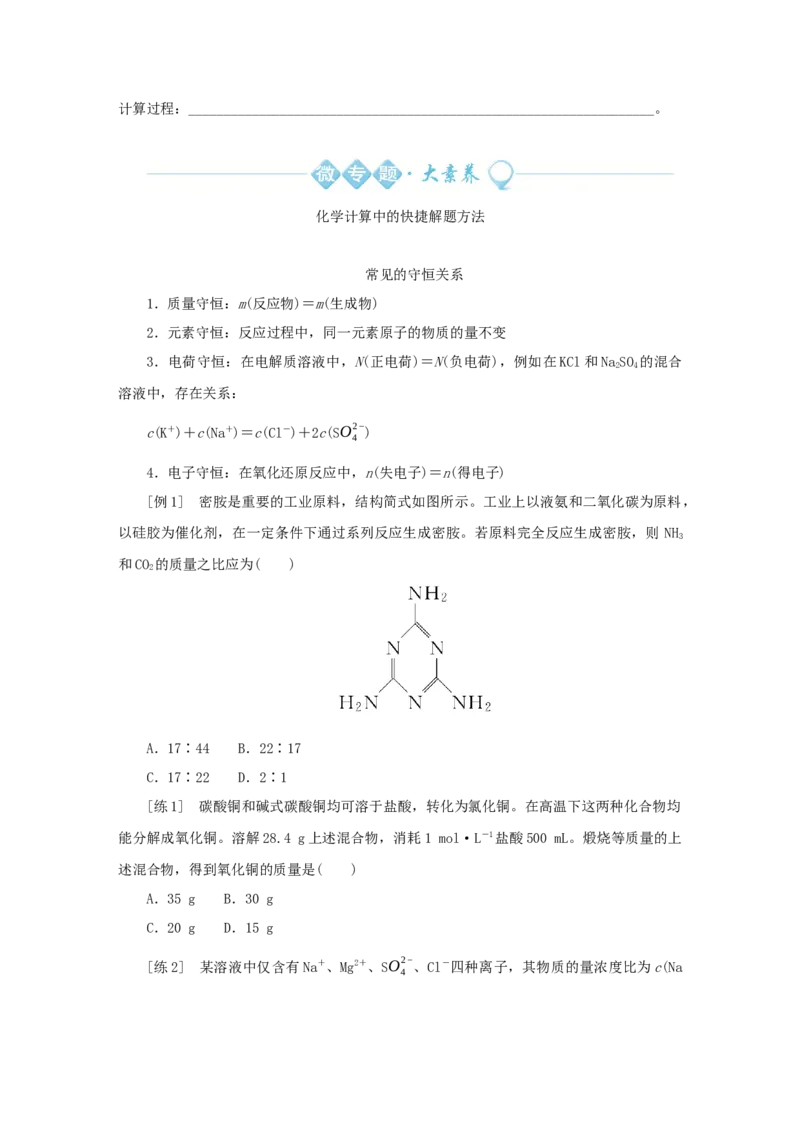
[例1] 密胺是重要的工业原料,结构简式如图所示。工业上以液氨和二氧化碳为原料,
以硅胶为催化剂,在一定条件下通过系列反应生成密胺。若原料完全反应生成密胺,则 NH
3
和CO 的质量之比应为( )
2
A.17∶44 B.22∶17
C.17∶22 D.2∶1
[练1] 碳酸铜和碱式碳酸铜均可溶于盐酸,转化为氯化铜。在高温下这两种化合物均
能分解成氧化铜。溶解28.4 g上述混合物,消耗1 mol·L-1盐酸500 mL。煅烧等质量的上
述混合物,得到氧化铜的质量是( )
A.35 g B.30 g
C.20 g D.15 g
[练2] 某溶液中仅含有Na+、Mg2+、SO2− 、Cl-四种离子,其物质的量浓度比为c(Na
4+)∶c(Mg2+)∶c(Cl-)=3∶5∶5,若Na+浓度为3 mol·L-1,则SO2− 的浓度为( )
4
A.2 mol·L-1 B.3 mol·L-1
C.4 mol·L-1 D.8 mol·L-1
[练3] 有14 g Na O 、NaO、NaOH的混合物与100 g质量分数为15%的盐酸恰好反应,
2 2 2
蒸干溶液,最终得固体质量为( )
A.20.40 g B.28.60 g
C.24.04 g D.无法计算
“守恒法”计算思维模型
使用差量法的三点注意
1.所选用差值要与有关物质的数值成正比例或反比例关系。
2.有关物质的物理量及其单位都要正确地使用,即“上下一致,左右相当”。
3.对于固体、液体,差量可以是质量差、微粒个数之差;对于气体,差量还可以是同
温、同压下的体积差。
[例2] 3 g镁铝合金与100 mL稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到
无水硫酸盐17.4 g,则原硫酸的物质的量浓度为( )
A.1 mol·L-1 B.1.5 mol·L-1
C.2 mol·L-1 D.2.5 mol·L-1
[练4] 为了检验某含有NaHCO 杂质的NaCO 样品的纯度,现将w g样品加热,其质量
3 2 3 1
变为w g,则该样品的纯度(质量分数)是( )
2
A. B.C. D.
[练5] 将11.5 g Na投入到过量的m g水中得到a溶液,将12 g Mg投入到过量的m
1 2
g盐酸中得到b溶液。若m=m,则a、b溶液的质量关系是( )
1 2
A.a>b B.a