文档内容
厦门外国语学校 2023 届高三上期末学科限时训练
化学试题
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Ca—40
第Ⅰ卷(选择题)
一、单选题(每个选择题只有一个正确答案,每个4分,共40分)
1.《博物新编》)有关于磺强水制法的记载:“以铅作一密炉,炉底贮以清水,焚硝碳于炉中,使硝磺之气重坠
入水,然后将水再行蒸炼,一如蒸酒甑油之法,务使水汽尽行升散,则所存者是磺强水矣。”(提示:“硝”指
KNO,“磺”指硫黄)下列有关磺强水的说法正确的是
3
A. “焚硝磺”时发生的是氧化还原反应
B. 磺强水是一种易挥发的强电解质
C. 0.01mol/L的磺强水溶液的pH=2
D. 磺强水溶液中不存在分子
2. N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 标准状况下,22.4LNO 气体中所含分子数为N
2 A
B. 用惰性电极电解1L0.2mol/LAgNO 溶液,当两极产生气体的物质的量相等时,电路中通过电子数为0.4N
3 A
C.64gCaC 中含有的共用电子对数为4N
2 A
D. 向含1molCH COONa的水溶液中滴加醋酸使溶液呈中性,CHCOO-数目大于N
3 3 A
3.2022年诺贝尔化学奖授予美国化学家卡罗琳·贝尔托西、丹麦化学家摩顿·梅尔达尔和美国化学家卡尔·巴里·
夏普莱斯,以表彰他们在点击化学和生物正交化学研究方面的贡献。如图是某点击反应的示意图,下列说法
正确的是
A.HN 和NH 的水溶液都显碱性
3 3
B.Cu+是该反应的催化剂,Cu+的价层电子排布式为3d94s1
C. 2—丁炔的键线式为
D. 该点击反应的产物为 ,反应类型为取代反应
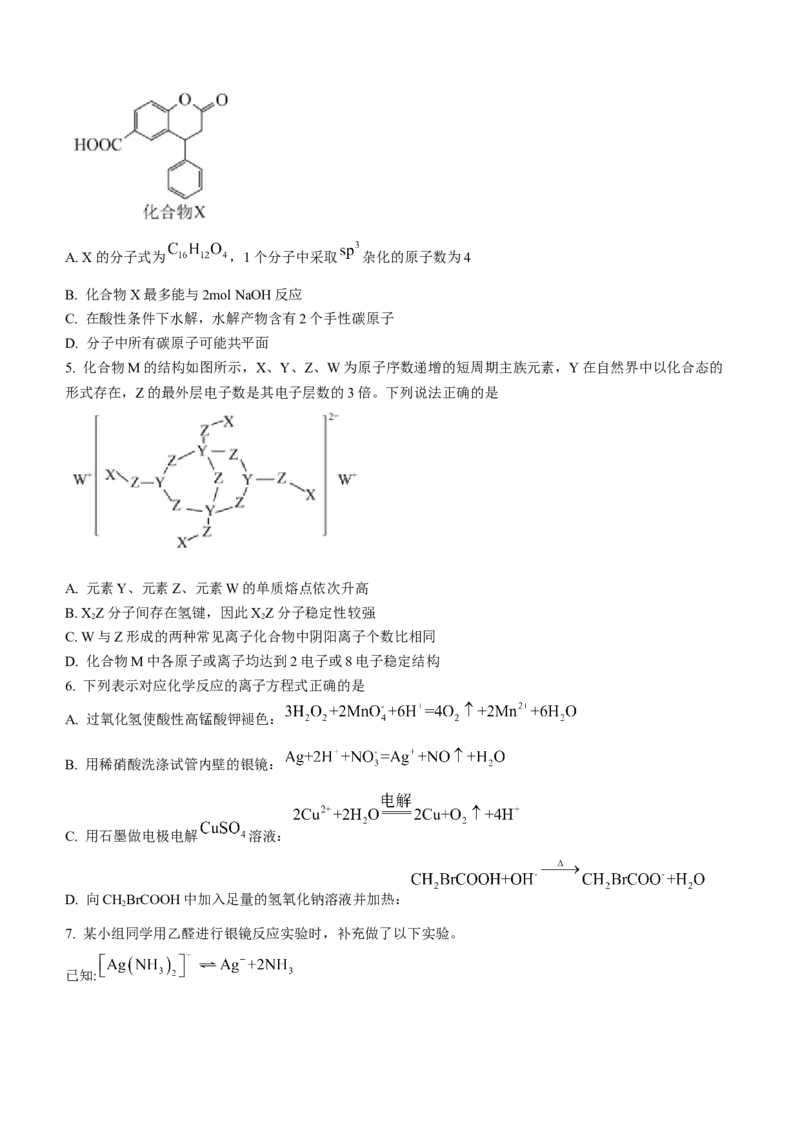
4. 有机化合物X的结构简式如图所示,下列说法正确的是A. X的分子式为 ,1个分子中采取 杂化的原子数为4
B. 化合物X最多能与2mol NaOH反应
C. 在酸性条件下水解,水解产物含有2个手性碳原子
D. 分子中所有碳原子可能共平面
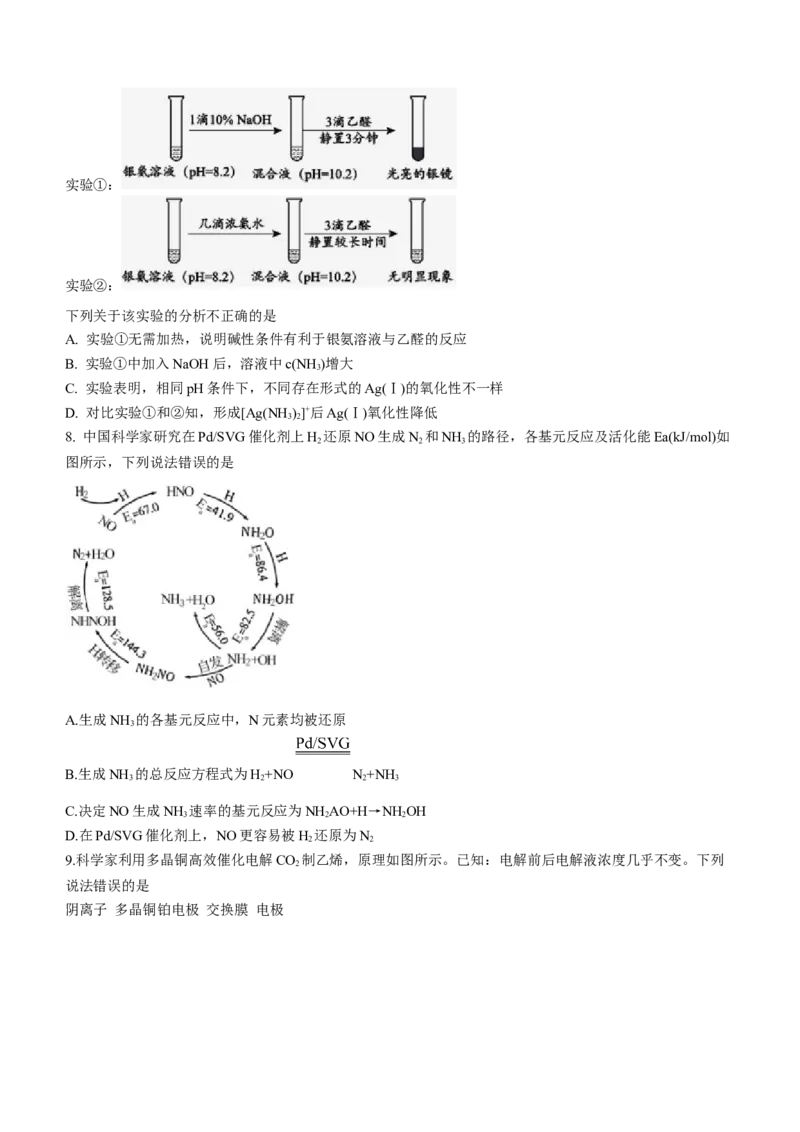
5. 化合物M的结构如图所示,X、Y、Z、W为原子序数递增的短周期主族元素,Y在自然界中以化合态的
形式存在,Z的最外层电子数是其电子层数的3倍。下列说法正确的是
A. 元素Y、元素Z、元素W的单质熔点依次升高
B. XZ分子间存在氢键,因此XZ分子稳定性较强
2 2
C. W与Z形成的两种常见离子化合物中阴阳离子个数比相同
D. 化合物M中各原子或离子均达到2电子或8电子稳定结构
6. 下列表示对应化学反应的离子方程式正确的是
A. 过氧化氢使酸性高锰酸钾褪色:
B. 用稀硝酸洗涤试管内壁的银镜:
C. 用石墨做电极电解 溶液:
D. 向CHBrCOOH中加入足量的氢氧化钠溶液并加热:
2
7. 某小组同学用乙醛进行银镜反应实验时,补充做了以下实验。
已知:实验①:
实验②:
下列关于该实验的分析不正确的是
A. 实验①无需加热,说明碱性条件有利于银氨溶液与乙醛的反应
B. 实验①中加入NaOH后,溶液中c(NH )增大
3
C. 实验表明,相同pH条件下,不同存在形式的Ag(Ⅰ)的氧化性不一样
D. 对比实验①和②知,形成[Ag(NH)]+后Ag(Ⅰ)氧化性降低
3 2
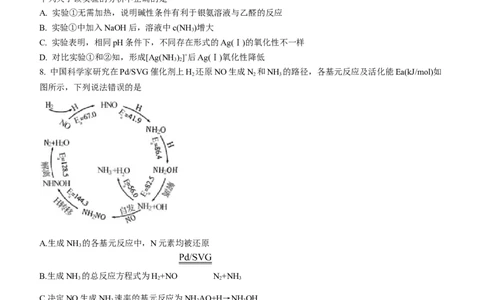
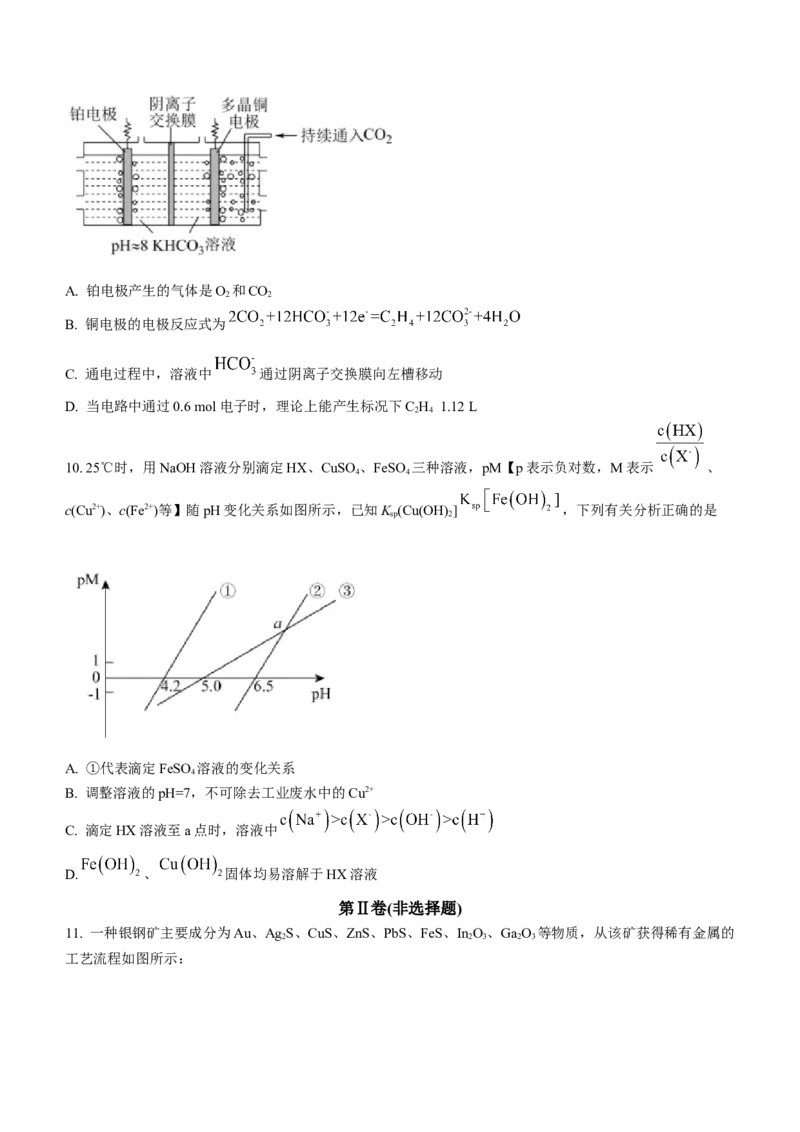
8. 中国科学家研究在Pd/SVG催化剂上H 还原NO生成N 和NH 的路径,各基元反应及活化能Ea(kJ/mol)如
2 2 3
图所示,下列说法错误的是
A.生成NH 的各基元反应中,N元素均被还原
3
B.生成NH 的总反应方程式为H+NO N+NH
3 2 2 3
C.决定NO生成NH 速率的基元反应为NH AO+H→NH OH
3 2 2
D.在Pd/SVG催化剂上,NO更容易被H 还原为N
2 2
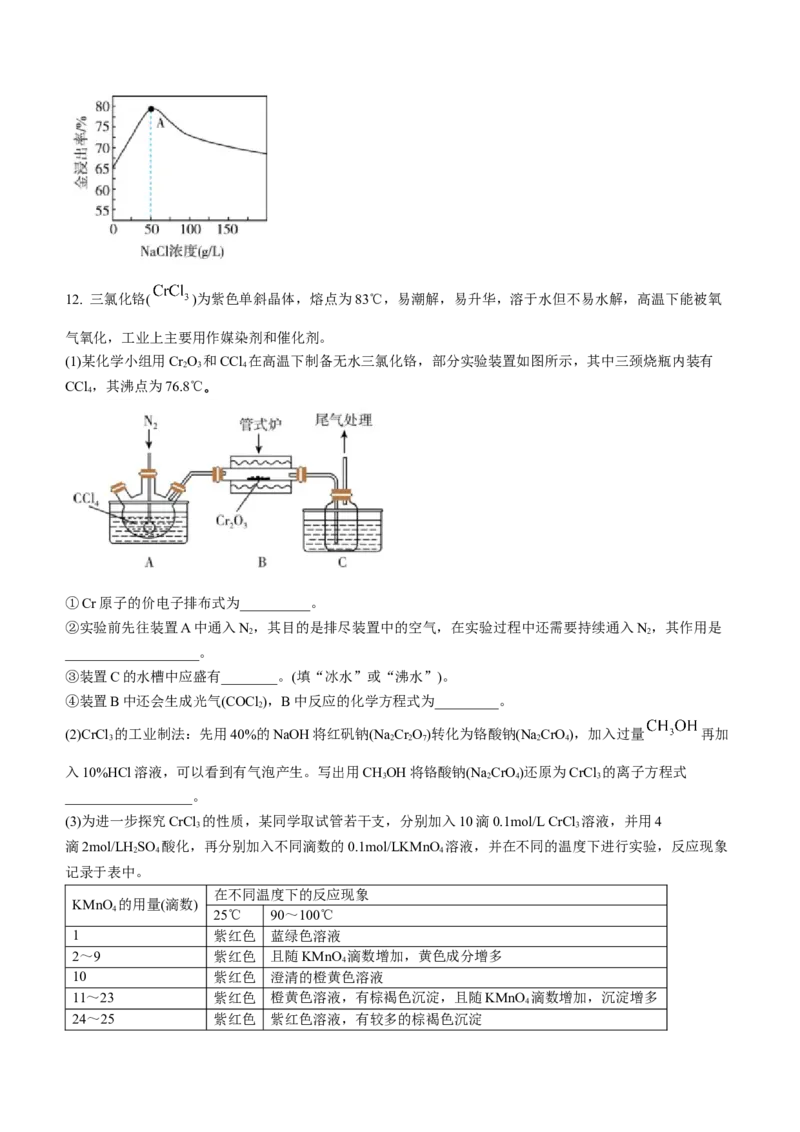
9.科学家利用多晶铜高效催化电解CO 制乙烯,原理如图所示。已知:电解前后电解液浓度几乎不变。下列
2
说法错误的是
阴离子 多晶铜铂电极 交换膜 电极A. 铂电极产生的气体是O 和CO
2 2
B. 铜电极的电极反应式为
C. 通电过程中,溶液中 通过阴离子交换膜向左槽移动
D. 当电路中通过0.6 mol电子时,理论上能产生标况下C H 1.12 L
2 4
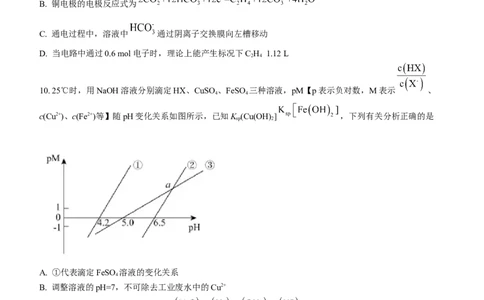
10. 25℃时,用NaOH溶液分别滴定HX、CuSO 、FeSO 三种溶液,pM【p表示负对数,M表示 、
4 4
c(Cu2+)、c(Fe2+)等】随pH变化关系如图所示,已知K (Cu(OH) ] ,下列有关分析正确的是
sp 2
A. ①代表滴定FeSO 溶液的变化关系
4
B. 调整溶液的pH=7,不可除去工业废水中的Cu2+
C. 滴定HX溶液至a点时,溶液中
D. 、 固体均易溶解于HX溶液
第Ⅱ卷(非选择题)
11. 一种银钢矿主要成分为Au、Ag S、CuS、ZnS、PbS、FeS、InO、GaO 等物质,从该矿获得稀有金属的
2 2 3 2 3
工艺流程如图所示:该工艺条件下,金属离子开始沉淀和完全沉淀的pH如表:
金属离子 Fe3+ In3+ Ga3+ Cu2+ Zn2+ Pb2+
开始沉淀的pH 2.2 2. 2.6 4.6 6.24 7.1
完全沉淀(c=1.0×10-5mol/L)的pH 3.2 3.4 4.3 6.6 8.24 9.1
(1) “浸出”过程中金、银分别转化为 、 进入溶液,同时生成硫,写出Ag S发生反应的离子方
2
程式___________。
(2)高温水蒸气除铁利用了FeCl 易水解的性质,写出该反应的化学方程式____________。
3
(3)“二次还原”得到的滤液中主要的阳离子有H+、Na+、Ca2+、Zn2+、Pb3+、In3+、___。
(4)“二次中和”得到的滤渣除少量Fe(OH) 外,主要成分还有________(写化学式)。
3
(5)"分铅锌”步骤中,维持HS饱和水溶液的浓度为0.1 mol/L,为使Zn2+沉淀完全,需控制溶液的pH不小于
2
_____________。
已知: 13]
(6)已知:氧化还原反应可看成由两个半反应组成,每个半反应具有一定的电极电势(用“ψ”表示),ψ越大则
该物质的氧化性越强,ψ越低则该物质的还原性越强。浸出步骤中金反应的两个半反应如下:
HClO+H++2e-=Cl-+H O,ψ=0.994+
2
+3e-=4Cl-+Au,
(ψ与半反应式的系数无关,仅与浓度有关,cθ=1mol/L)
如图是Au的浸出率与NaCl溶液浓度的关系,请解释A点以后,金浸出率减小的原因是________。12. 三氯化铬( )为紫色单斜晶体,熔点为83℃,易潮解,易升华,溶于水但不易水解,高温下能被氧
气氧化,工业上主要用作媒染剂和催化剂。
(1)某化学小组用Cr O 和CCl 在高温下制备无水三氯化铬,部分实验装置如图所示,其中三颈烧瓶内装有
2 3 4
CCl ,其沸点为76.8℃。
4
①Cr原子的价电子排布式为__________。
②实验前先往装置A中通入N,其目的是排尽装置中的空气,在实验过程中还需要持续通入N,其作用是
2 2
___________________。
③装置C的水槽中应盛有________。(填“冰水”或“沸水”)。
④装置B中还会生成光气(COCl ),B中反应的化学方程式为_________。
2
(2)CrCl 的工业制法:先用40%的NaOH将红矾钠(Na Cr O)转化为铬酸钠(NaCrO),加入过量 再加
3 2 2 7 2 4
入10%HCl溶液,可以看到有气泡产生。写出用CHOH将铬酸钠(Na CrO)还原为CrCl 的离子方程式
3 2 4 3
__________________。
(3)为进一步探究CrCl 的性质,某同学取试管若干支,分别加入10滴0.1mol/L CrCl 溶液,并用4
3 3
滴2mol/LHSO 酸化,再分别加入不同滴数的0.1mol/LKMnO 溶液,并在不同的温度下进行实验,反应现象
2 4 4
记录于表中。
在不同温度下的反应现象
KMnO 的用量(滴数)
4 25℃ 90~100℃
1 紫红色 蓝绿色溶液
2~9 紫红色 且随KMnO 滴数增加,黄色成分增多
4
10 紫红色 澄清的橙黄色溶液
11~23 紫红色 橙黄色溶液,有棕褐色沉淀,且随KMnO 滴数增加,沉淀增多
4
24~25 紫红色 紫红色溶液,有较多的棕褐色沉淀① 浓度对反应的影响
CrCl 与KMnO 在常温下反应,观察不到 离子的橙色,甲同学认为其中一个原因是 离子的橙色
3 4
被 离子的紫红色掩盖,另一种可能的原因是__________,(答案写反应速率较慢可以吗?)所以必须将
反应液加热至沸腾4~5min后,才能观察到反应液由紫红色逐渐变为橙黄色的实验现象。
②CrCl 与KMnO 的用量对反应的影响
3 4
对表中数据进行分析,在上述反应条件下,欲将Cr3+氧化为 ,CrCl 与KMnO 最佳用量比为_____。
3 4
这与由反应 所推断得到的用量比不符,你推测的原因是
__________________。
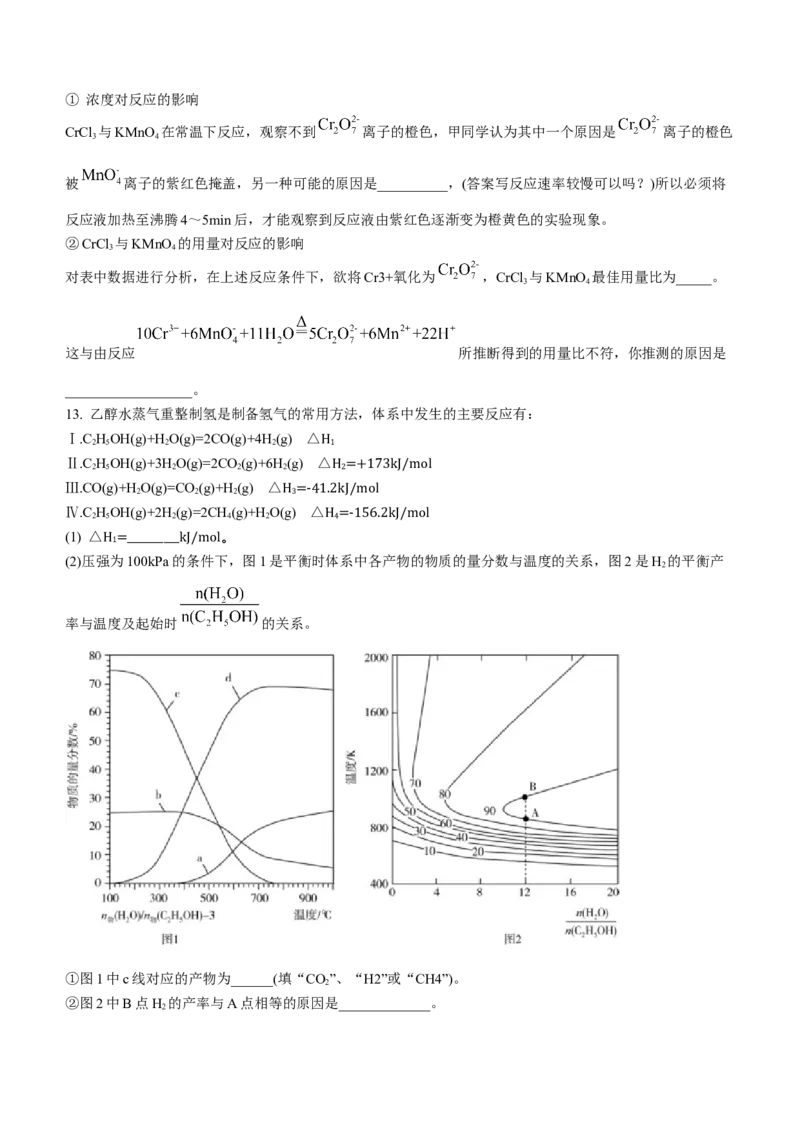
13. 乙醇水蒸气重整制氢是制备氢气的常用方法,体系中发生的主要反应有:
Ⅰ.C HOH(g)+H O(g)=2CO(g)+4H (g) △
2 5 2 2
Ⅱ.C HOH(g)+3H O(g)=2CO(g)+6H(g) △1
2 5 2 2 2 H
Ⅲ.CO(g)+HO(g)=CO(g)+H(g) △ 2
2 2 2 H =+173kJ/mol
Ⅳ.C HOH(g)+2H (g)=2CH (g)+HO(g)3 △
2 5 2 4 2 H =-41.2kJ/mol
(1) △ 。 4
H =-156.2kJ/mol
(2)压强为1 100kPa的条件下,图1是平衡时体系中各产物的物质的量分数与温度的关系,图2是H 的平衡产
H =__________kJ/mol 2
率与温度及起始时 的关系。
①图1中c线对应的产物为______(填“CO”、“H2”或“CH4”)。
2
②图2中B点H 的产率与A点相等的原因是_____________。
2(3)反应温度T℃、0.1MPa的恒压密闭容器中,充入1mol乙醇和xmolH O(g),若只发生反应CHCHOH(g)
2 3 2
+3H O(g) 2CO(g)+6H(g),平衡时,乙醇转化率为α,CO 的压强为_______MPa,反应平衡常数
2 2 2 2
Kp=_______(以分压表示,分压=总压×物质的量分数。列出计算式即可)
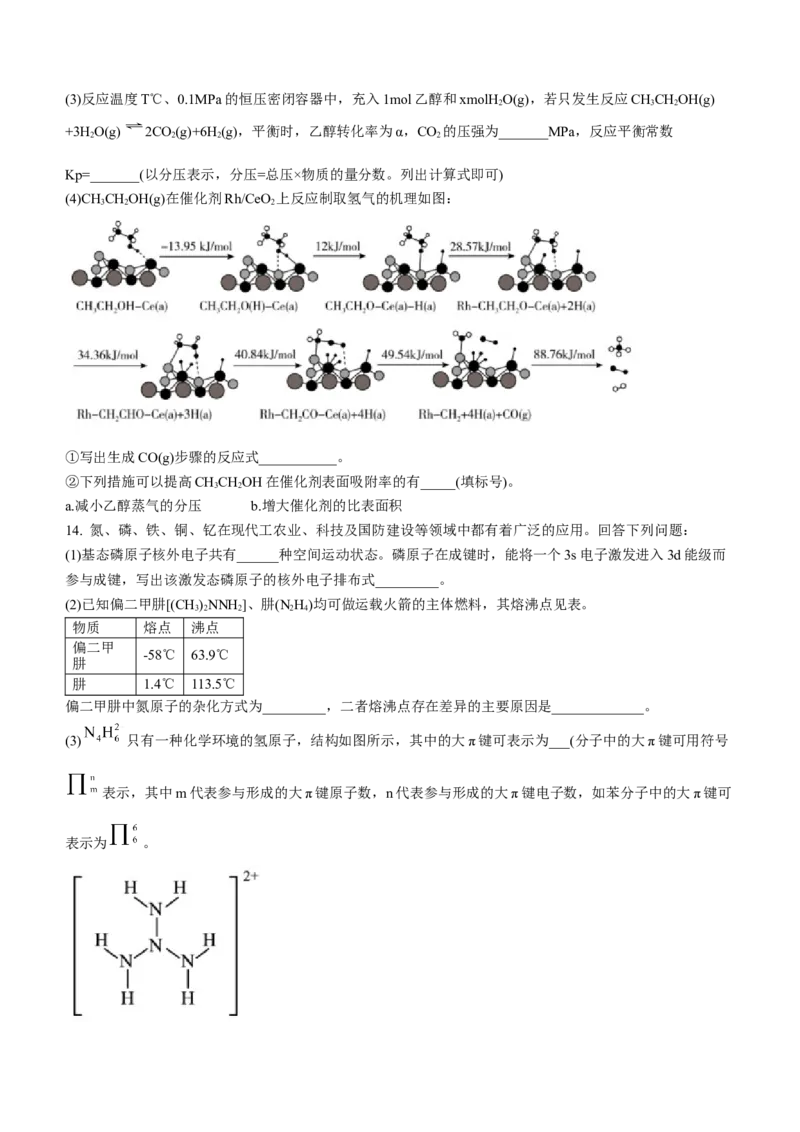
(4)CHCHOH(g)在催化剂Rh/CeO 上反应制取氢气的机理如图:
3 2 2
①写出生成CO(g)步骤的反应式___________。
②下列措施可以提高CHCHOH在催化剂表面吸附率的有_____(填标号)。
3 2
a.减小乙醇蒸气的分压 b.增大催化剂的比表面积
14. 氮、磷、铁、铜、钇在现代工农业、科技及国防建设等领域中都有着广泛的应用。回答下列问题:
(1)基态磷原子核外电子共有______种空间运动状态。磷原子在成键时,能将一个3s电子激发进入3d能级而
参与成键,写出该激发态磷原子的核外电子排布式_________。
(2)已知偏二甲肼[(CH )NNH]、肼(N H)均可做运载火箭的主体燃料,其熔沸点见表。
3 2 2 2 4
物质 熔点 沸点
偏二甲
-58℃ 63.9℃
肼
肼 1.4℃ 113.5℃
偏二甲肼中氮原子的杂化方式为_________,二者熔沸点存在差异的主要原因是_____________。
(3) 只有一种化学环境的氢原子,结构如图所示,其中的大π键可表示为___(分子中的大π键可用符号
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数,如苯分子中的大π键可
表示为 。(4)Cu2+可形成[Cu(X) ]2+,其中X代表CH—NH—CH —CH—NH 。1mol[Cu(X) ]2+中,VSEPR模型为正四面
2 3 2 2 2 2
体的非金属原子共有________mol。
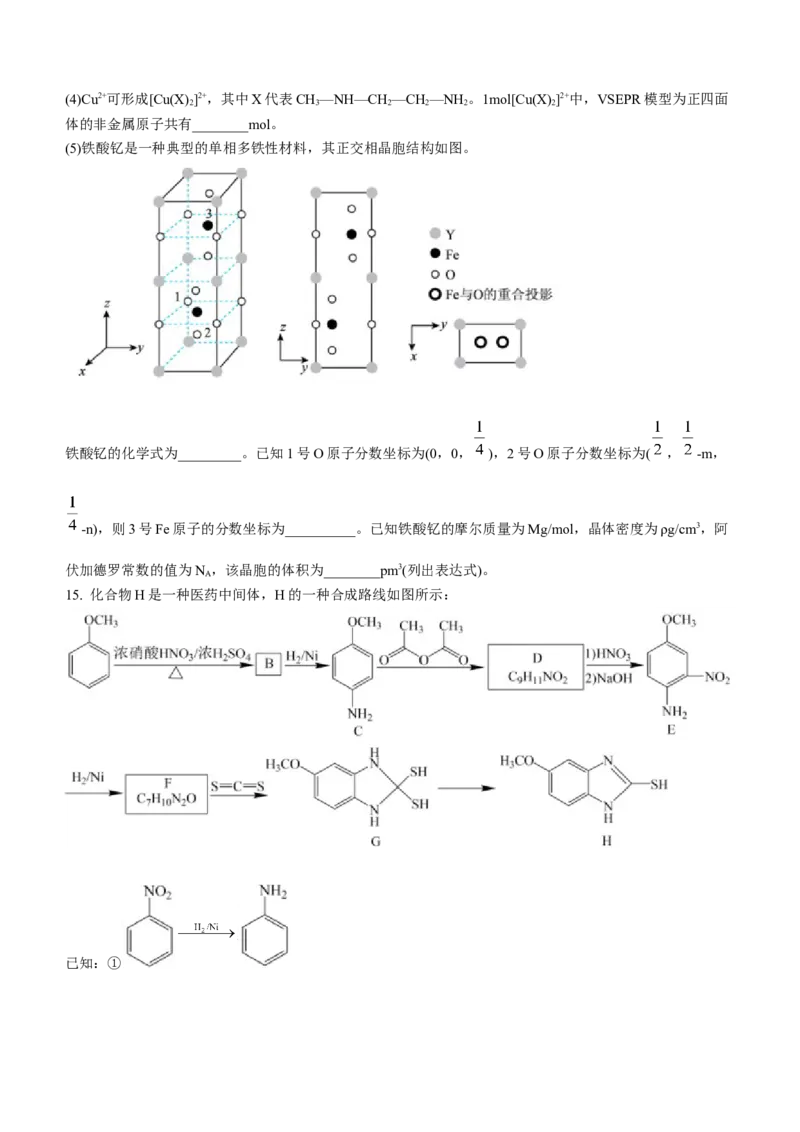
(5)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构如图。
铁酸钇的化学式为_________。已知1号O原子分数坐标为(0,0, ),2号O原子分数坐标为( , -m,
-n),则3号Fe原子的分数坐标为__________。已知铁酸钇的摩尔质量为Mg/mol,晶体密度为ρg/cm3,阿
伏加德罗常数的值为N ,该晶胞的体积为________pm3(列出表达式)。
A
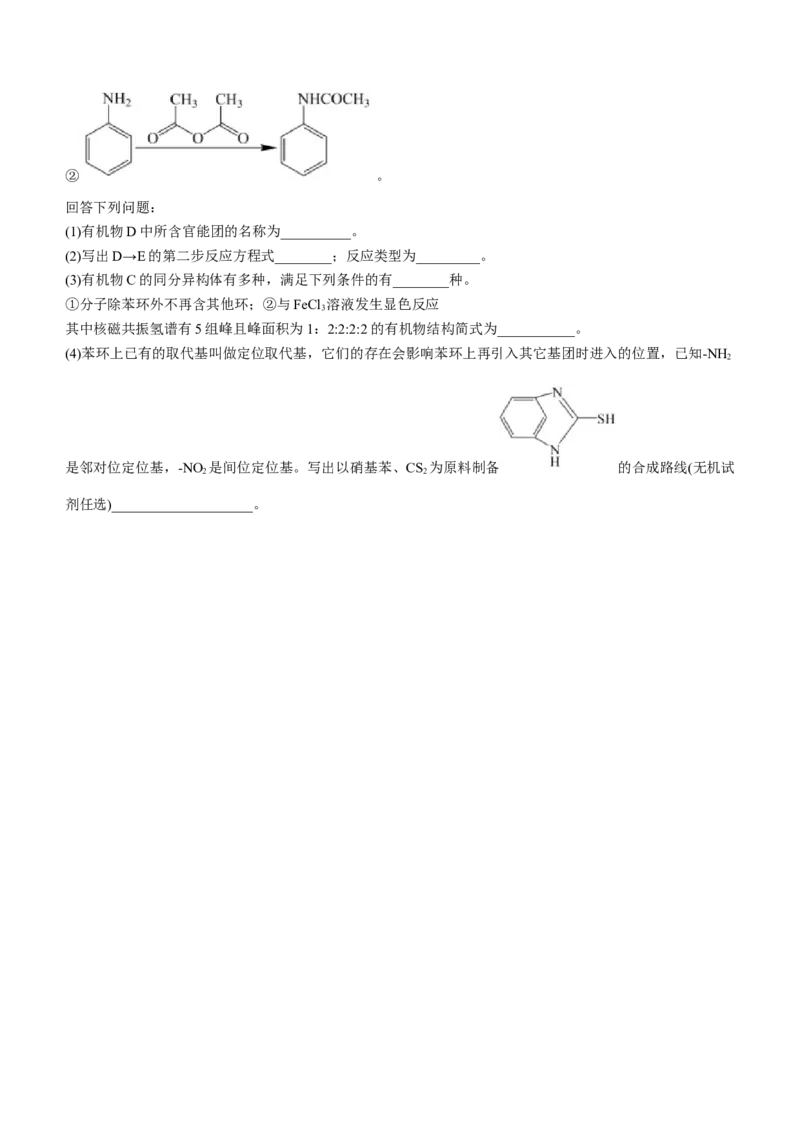
15. 化合物H是一种医药中间体,H的一种合成路线如图所示:
已知:①② 。
回答下列问题:
(1)有机物D中所含官能团的名称为__________。
(2)写出D→E的第二步反应方程式________;反应类型为_________。
(3)有机物C的同分异构体有多种,满足下列条件的有________种。
①分子除苯环外不再含其他环;②与FeCl 溶液发生显色反应
3
其中核磁共振氢谱有5组峰且峰面积为1:2:2:2:2的有机物结构简式为___________。
(4)苯环上已有的取代基叫做定位取代基,它们的存在会影响苯环上再引入其它基团时进入的位置,已知-NH
2
是邻对位定位基,-NO 是间位定位基。写出以硝基苯、CS 为原料制备 的合成路线(无机试
2 2
剂任选)____________________。s