文档内容
热点强化 17 电解原理创新应用
1.电解原理常见的考查点
电解原理及应用是高考高频考点,该类试题往往与生产、生活及新科技等相联系,以装置图
或流程图为载体呈现,题材广、信息新,题目具有一定难度。主要考查阴、阳极的判断、电
极反应式、电解反应方程式的书写、溶液离子浓度变化及有关计算等。
2.“5点”突破电解综合应用题
(1)分清阴、阳极,与电源正极相连的为阳极,与电源负极相连的为阴极,两极反应为“阳
氧阴还”。
(2)剖析离子移向,阳离子移向阴极,阴离子移向阳极。
(3)注意放电顺序,正确判断放电的微粒或物质。
(4)注意介质,正确判断反应产物,酸性介质不出现OH-,碱性介质不出现H+;不能想当然
地认为金属作阳极,电极产物为金属阳离子。
(5)注意得失电子守恒和电荷守恒,正确书写电极反应式。
题组一 电解原理在物质提纯中的应用
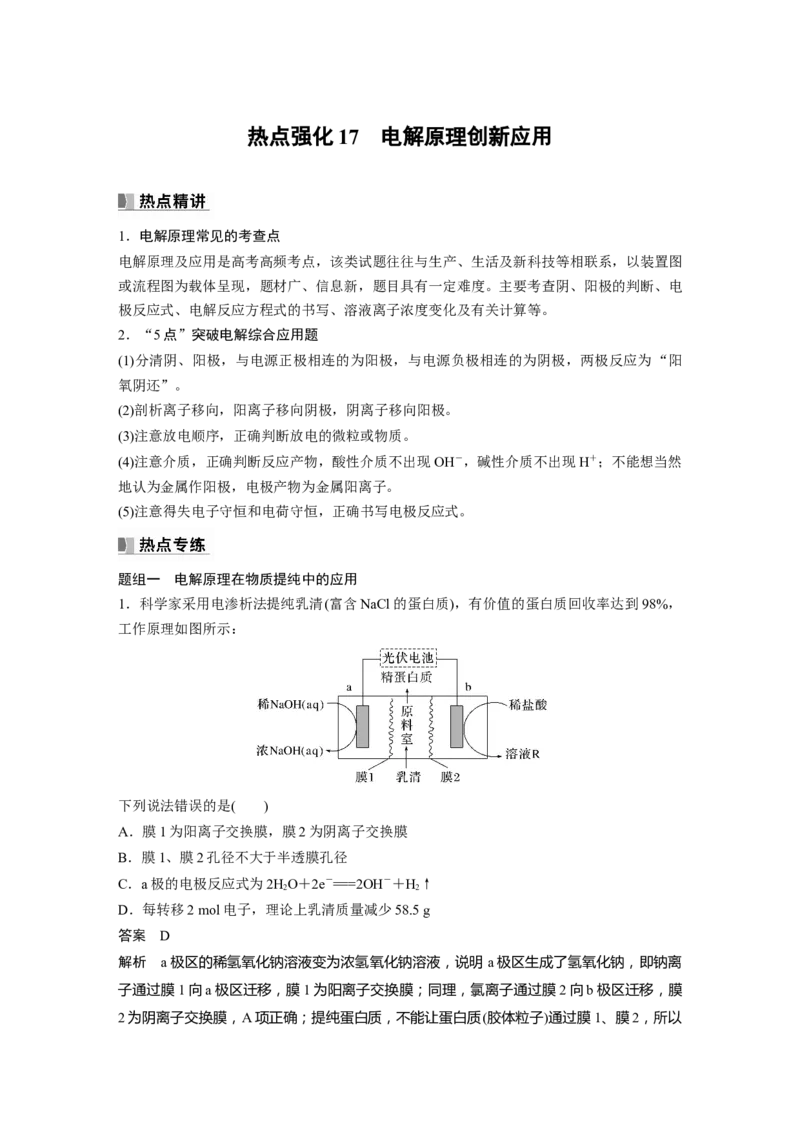
1.科学家采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质回收率达到98%,
工作原理如图所示:
下列说法错误的是( )
A.膜1为阳离子交换膜,膜2为阴离子交换膜
B.膜1、膜2孔径不大于半透膜孔径
C.a极的电极反应式为2HO+2e-===2OH-+H↑
2 2
D.每转移2 mol电子,理论上乳清质量减少58.5 g
答案 D
解析 a极区的稀氢氧化钠溶液变为浓氢氧化钠溶液,说明 a极区生成了氢氧化钠,即钠离
子通过膜1向a极区迁移,膜1为阳离子交换膜;同理,氯离子通过膜2向b极区迁移,膜
2为阴离子交换膜,A项正确;提纯蛋白质,不能让蛋白质(胶体粒子)通过膜1、膜2,所以膜1、膜2孔径应不大于半透膜孔径,B项正确;a极为阴极,发生还原反应:2HO+2e-
2
===2OH-+H↑,C项正确;每转移2 mol电子,结合电极反应和电荷守恒可知,理论上乳
2
清减少的质量为2 mol NaCl的质量,即质量减少117 g,D项错误。
2.(2022·广东梅州模拟)电解法常用于分离提纯物质,某混合物浆液含Al(OH) 、MnO 和少
3 2
量NaCrO 。考虑到胶体的吸附作用使NaCrO 不易完全被水浸出,某研究小组利用设计的
2 4 2 4
电解分离装置(如图),使浆液分离成固体混合物和含铬元素溶液进行回收利用(已知:2CrO
+2H+Cr O+HO),下列说法不正确的是( )
2 2
A.阴极室生成的物质为NaOH和H
2
B.阳极的电极反应式是2HO-4e-===4H++O↑
2 2
C.a离子交换膜为阳离子交换膜
D.当外电路中转移2 mol电子时,阳极室可生成1 mol Cr O
2
答案 D
解析 电解时,阳极上水中的OH-放电:2HO-4e-===O +4H+,浆液中的CrO通过阴离
2 2
子交换膜向阳极移动,从而从浆液中分离出来,因存在 2CrO+2H+Cr O+HO,则分离
2 2
后含铬元素的粒子是CrO、Cr O;阴极上水中的H+放电:2HO+2e-===H↑+2OH-,混
2 2 2
合物浆液中的钠离子通过阳离子交换膜进入阴极,故阴极反应生成氢气和NaOH;电解时,
每转移2 mol电子,阳极区生成2 mol H+,由于2CrO+2H+Cr O+HO为可逆反应,阳
2 2
极室生成的Cr O小于1 mol,D错误。
2
题组二 电解原理在无机物制备中的应用
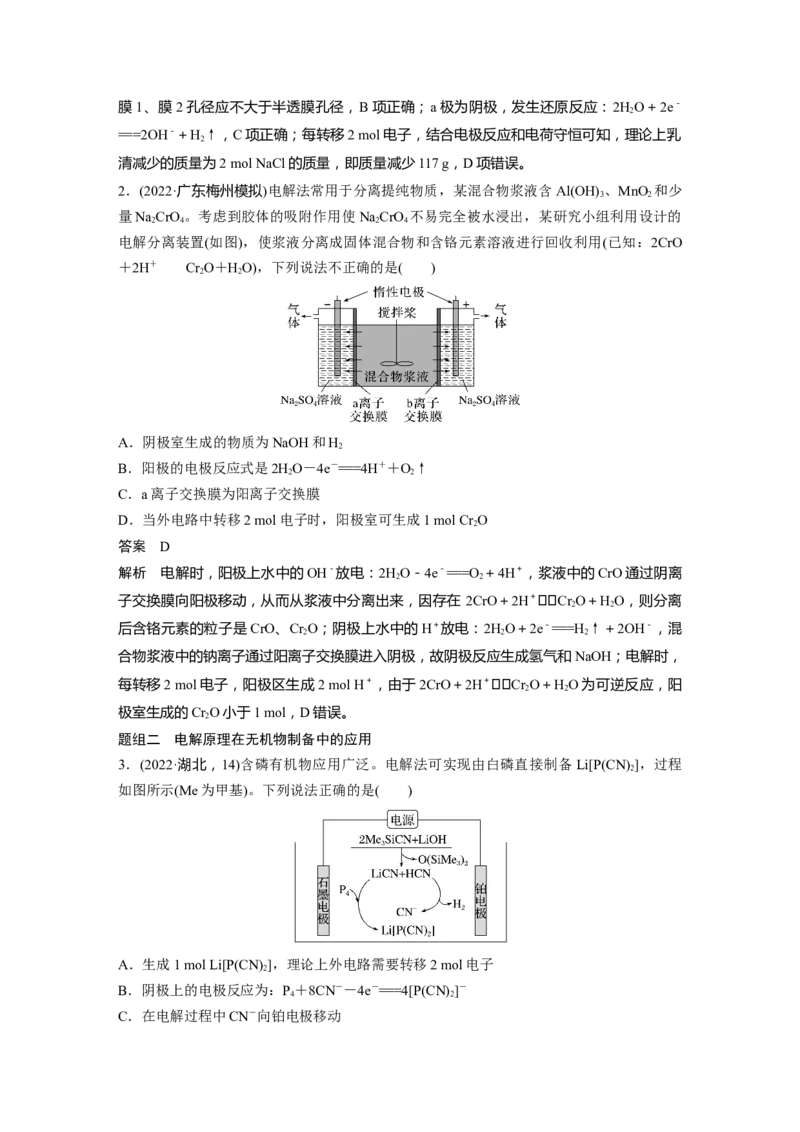
3.(2022·湖北,14)含磷有机物应用广泛。电解法可实现由白磷直接制备 Li[P(CN)],过程
2
如图所示(Me为甲基)。下列说法正确的是( )
A.生成1 mol Li[P(CN) ],理论上外电路需要转移2 mol电子
2
B.阴极上的电极反应为:P+8CN--4e-===4[P(CN) ]-
4 2
C.在电解过程中CN-向铂电极移动D.电解产生的H 中的氢元素来自于LiOH
2
答案 D
解析 石墨电极为阳极,对应的电极反应式为P +8CN--4e-===4[P(CN) ]-,则生成1 mol
4 2
Li[P(CN)],理论上外电路需要转移1 mol电子,A错误;阴极上发生还原反应,应该得电
2
子,电极反应式为2HCN+2e-===H↑+2CN-,B错误;石墨电极为阳极,铂电极为阴极,
2
CN-应该向阳极移动,即移向石墨电极,C错误;由所给图示可知HCN在阴极放电,产生
CN-和H ,而HCN中的H来自于LiOH,则电解产生的H 中的氢元素来自于LiOH,D正
2 2
确。
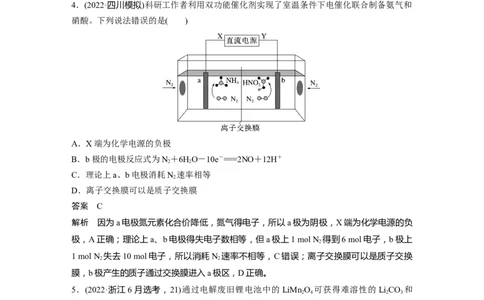
4.(2022·四川模拟)科研工作者利用双功能催化剂实现了室温条件下电催化联合制备氨气和
硝酸。下列说法错误的是( )
A.X端为化学电源的负极
B.b极的电极反应式为N+6HO-10e-===2NO+12H+
2 2
C.理论上a、b电极消耗N 速率相等
2
D.离子交换膜可以是质子交换膜
答案 C
解析 因为a电极氮元素化合价降低,氮气得电子,所以a极为阴极,X端为化学电源的负
极,A正确;理论上a、b电极得失电子数相等,但a极上1 mol N 得到6 mol电子,b极上
2
1 mol N 失去10 mol电子,所以消耗N 速率不相等,C错误;离子交换膜可以是质子交换
2 2
膜,b极产生的质子通过交换膜进入a极区,D正确。
5.(2022·浙江6月选考,21)通过电解废旧锂电池中的 LiMn O 可获得难溶性的LiCO 和
2 4 2 3
MnO ,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中
2
溶液的体积变化忽略不计)。下列说法不正确的是( )A.电极A为阴极,发生还原反应
B.电极B的电极反应:2HO+Mn2+-2e-===MnO +4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节pH除去Mn2+,再加入NaCO 溶液以获得LiCO
2 3 2 3
答案 C
解析 由电解示意图可知,电极B上Mn2+转化为MnO ,锰元素化合价升高,失电子,则
2
电极B为阳极,电极A为阴极,得电子,发生还原反应,A正确;由电解示意图可知,电
极B上Mn2+失电子转化为MnO ,电极反应式为2HO+Mn2+-2e-===MnO +4H+,B正确;
2 2 2
电极A为阴极,LiMn O 得电子,电极反应式为 LiMn O +3e-+8H+===Li++2Mn2++
2 4 2 4
4HO,依据得失电子守恒,电解池总反应为 2LiMn O +4H+===2Li++Mn2++3MnO +
2 2 4 2
2HO,反应生成了Mn2+,Mn2+浓度增大,C错误;电解池总反应为2LiMn O +4H+===2Li
2 2 4
++Mn2++3MnO +2HO,电解结束后,可通过调节溶液pH将锰离子转化为沉淀除去,然
2 2
后再加入碳酸钠溶液,从而获得碳酸锂,D正确。
题组三 电解原理在有机合成方面的应用
6.(2020·浙江7月选考,21)电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO-放
电可得到R—R(烷烃)。下列说法不正确的是( )
A.电解总反应方程式:2RCOONa+2HO=====R—R+2CO↑+H↑+2NaOH
2 2 2
B.RCOO-在阳极放电,发生氧化反应
C.阴极的电极反应:2HO+2e-===2OH-+H↑
2 2
D.电解CHCOONa、CHCHCOONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
答案 A
解析 由于电解液呈强碱性,电解反应不能释放出 CO 气体,A 错误;电解高浓度
2
RCOONa的NaOH溶液,阳极上RCOO-发生氧化反应,得到R—R(烷烃),B正确;阴极上
HO得电子放出H ,电极反应式为2HO+2e-===2OH-+H↑,C正确;根据题中电解原
2 2 2 2
理,电解 RCOONa 和NaOH 混合液可得到 R—R(烷烃),类比推理,电解 CHCOONa、
3
CHCHCOONa 和 NaOH 混合溶液,可得到 CHCH(乙烷)、CHCHCH(丙烷)和
3 2 3 3 3 2 3
CHCHCHCH(丁烷),D正确。
3 2 2 3
7.(2022·长春模拟)乙醛酸(HOOCCHO)是有机合成的重要中间体。工业上以乙二醛
(OHCCHO)和乙二酸(HOOCCOOH)为原料,用“双极室成对电解法”生产乙醛酸,原理如
图所示。该装置中阴、阳两极均为惰性电极,两极室均可产生乙醛酸,其中乙二醛与 M电
极生成的物质反应生成乙醛酸。下列说法错误的是( )A.M极与直流电源的正极相连
B.N极上的电极反应式为HOOCCOOH+2e-+2H+===HOOCCHO+HO
2
C.电解一段时间后,N极附近溶液的pH变小
D.若有2 mol H+通过质子交换膜,则该装置中生成2 mol乙醛酸
答案 C
解析 由图中质子的移动方向可知,M极为电解池的阳极,与电源正极相连,A正确;N极
为阴极,乙二酸在阴极的电极反应式为HOOCCOOH+2e-+2H+===HOOCCHO+HO,放
2
电时消耗氢离子,溶液pH增大,B正确、C错误;若有2 mol氢离子通过质子交换膜,阴
极和阳极各生成1 mol乙醛酸,则装置中生成2 mol乙醛酸,D正确。
题组四 应用电解原理回收空气中的CO
2
8.(2022·广西柳州模拟)实现“碳中和”的重要方式之一是将CO 重新转化成能源,在金属
2
氧化物电解池,高温下电解HO-CO 的混合气体制备H 和CO是一种新的能源利用方式,
2 2 2
基本原理如图所示。下列说法错误的是( )
A.Y是电源的正极
B.阳极的电极反应式是2O2--4e-===O↑
2
C.总反应可表示为HO+CO=====H+CO+O
2 2 2 2
D.阴、阳两极生成的气体的物质的量之比是1∶2
答案 D
解析 由图可知与X相连的电极产生氢气和CO,H、C元素化合价降低,发生还原反应,
为电解池的阴极,则X是电源的负极,Y为正极,A正确;金属氧化物为电解质,则阳极的
电极反应式为2O2--4e-===O↑,B正确;由图可知反应物为水和二氧化碳,生成物为氢
2
气、一氧化碳和氧气,则该电解池的总反应可表示为HO+CO=====H +CO+O ,C正确
2 2 2 2
结合总反应的化学方程式可知,阴极产生1 mol H 和1 mol CO时,阳极产生1 mol O ,则阴、
2 2
阳两极生成的气体的物质的量之比是2∶1,D错误。9.(2022·河北模拟)为实现碳回收,我国科学家设计的用电化学法还原CO 制备草酸的装置如
2
图所示。下列有关该装置的说法错误的是( )
A.a、b分别为电源的负极、正极
B.电解装置左池发生的电极反应为2CO+2e-===C O
2 2
C.为增强溶液导电性,左池中可加入少量NaC O 溶液
2 2 4
D.右池电解质溶液为稀硫酸,发生的电极反应为2HO-4e-===O↑+4H+
2 2
答案 B
解析 由图可知,左池发生的反应为CO 得电子被还原为HC O ,电极反应式为2CO +2e-
2 2 2 4 2
+2H+===HC O,M极作阴极,电解池阴极与电源负极相连,则a为电源的负极,b为电源
2 2 4
的正极,A正确、B错误;为增强溶液导电性,同时减少杂质,左池可加入少量 NaC O 溶
2 2 4
液,C正确;右池为电解池的阳极区,HO失电子发生氧化反应生成O 和H+,D正确。
2 2
题组五 电解原理在污水处理方面的应用
10.某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,
原理如图所示,下列说法不正确的是( )
A.a接电源正极
B.阳极区溶液中发生的氧化还原反应为Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
C.若不考虑气体的溶解,当收集到13.44 L(标准状况)H 时,有0.2 mol Cr O被还原
2 2
D.阴极区附近溶液pH增大
答案 C
解析 由图可知,右侧生成氢气,发生还原反应,右侧铁板为阴极,则左侧铁板为阳极,故
a接电源正极,A项正确;左侧铁板为阳极,铁放电生成亚铁离子,亚铁离子被溶液中的
Cr O氧化,反应的离子方程式为Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO,B项正确;
2 2 2
标准状况下,13.44 L氢气的物质的量为=0.6 mol,根据转移电子守恒得 n(Fe2+)==0.6mol,根据Cr O~6Fe2+可知,被还原的Cr O的物质的量为0.6 mol×=0.1 mol,C项错误;
2 2
阴极氢离子放电生成氢气,氢离子浓度降低,溶液的pH增大,D项正确。
11.工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图所示,写出电解时铁电极发
生的电极反应:________________________。随后,铁电极附近有无色气体产生,写出有关
反应的离子方程式:____________________________。
答案 Fe-2e-===Fe2+ 2NO+8H++6Fe2+===N↑+6Fe3++4HO
2 2
解析 根据电解原理,阳离子向阴极移动,由装置图可知,A为电源的正极,B为电源的负
极,铁作阳极,电极反应式为Fe-2e-===Fe2+;NO在酸性条件下具有强氧化性,能将Fe2+
氧化,本身被还原成 N ,其反应的离子方程式为 2NO+8H++6Fe2+===N↑+6Fe3++
2 2
4HO。
2