文档内容
热点强化 19 化学反应速率和化学平衡简答题
文字描述代表一种开放性思维与能力,一般从速率问题、平衡(转化率)问题、安全问题、节
能减排等角度作答(考查前两个角度居多),实际上就是效益最大化的问题。
1.条件选择类
(1)实验最佳条件的选择或控制就是为了又“快”又“好”地生产,即主要是从反应速率与
转化率(化学平衡)两个角度来分析。“快”就是提高反应速率,“好”就是提高转化率,原
料利用率高,而影响速率与转化率的主要因素就是浓度、温度、压强与催化剂,其中温度与
压强是试题中经常考查的因素。
(2)从速率、转化率、产率、纯度等角度分析,选择最佳条件。如针对反应速率时,思考方
向为如何提高浸出速率、如何提高反应速率等;针对平衡转化率、产率时,可运用平衡移动
原理解释(其他条件不变的情况下,改变××条件,可逆反应平衡向××方向移动,导致
××发生变化);针对综合生产效益时,可从原料成本,原料来源是否广泛、是否可再生,
能源成本,对设备的要求,环境保护,绿色化学等方面作答。
(3)选择当前条件的优势,其他条件的不足,往往不足的描述比较容易疏忽,如温度过高或
过低,压强过小或过大,也要进行分析。
2.原因分析类
(1)依据化学反应速率和平衡移动原理,分析造成图像曲线变化的原因。
(2)催化剂对反应的影响、不同反应的选择性问题是这类题目的难点,解题时要多加关注,
不同的条件会有不同的选择性。
(3)这类题目一般都是多因素影响,需要多角度分析原因。
题组一 曲线上特殊点的分析
1.用(NH )CO 捕碳的反应:(NH )CO(aq)+HO(l)+CO(g)2NH HCO (aq)。为研究温
4 2 3 4 2 3 2 2 4 3
度对(NH )CO 捕获CO 效率的影响,将一定量的(NH )CO 溶液置于密闭容器中,并充入一
4 2 3 2 4 2 3
定量的CO 气体,保持其他初始实验条件不变,分别在不同温度下,经过相同时间测得 CO
2 2
气体浓度,得到趋势图:
(1)c点的逆反应速率和d点的正反应速率的大小关系为 v逆 (c)________(填“>”“=”或
“<”)v正 (d)。(2)b、c、d三点的平衡常数K 、K、K 从大到小的顺序为________。
b c d
(3)T ~T 温度区间,容器内 CO 气体浓度呈现增大的变化趋势,其原因是
3 4 2
________________________________________________________________________
________________________________________________________________________。
答案 (1)< (2)K >K>K (3)T ~T 温度区间,化学反应已达到平衡,由于正反应是放
b c d 3 4
热反应,温度升高平衡向逆反应方向移动,不利于CO 的捕获
2
解析 (1)温度越高,反应速率越快,d点温度高,则c点的逆反应速率和d点的正反应速率
的大小关系为v (c)<v (d)。(2)根据图像,温度为 T 时反应达平衡,此后温度升高,
逆 正 3
c(CO)增大,平衡逆向移动,说明正反应是放热反应。升高温度,平衡逆向移动,平衡常数
2
减小,故K >K>K 。
b c d
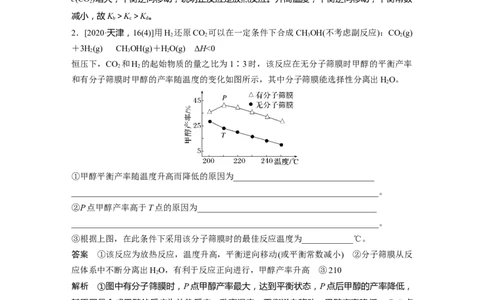
2.[2020·天津,16(4)]用H 还原CO 可以在一定条件下合成CHOH(不考虑副反应):CO(g)
2 2 3 2
+3H(g)CHOH(g)+HO(g) ΔH<0
2 3 2
恒压下,CO 和H 的起始物质的量之比为1∶3时,该反应在无分子筛膜时甲醇的平衡产率
2 2
和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出HO。
2
①甲醇平衡产率随温度升高而降低的原因为_________________________________
________________________________________________________________________。
②P点甲醇产率高于T点的原因为__________________________________________
________________________________________________________________________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为____________℃。
答案 ①该反应为放热反应,温度升高,平衡逆向移动(或平衡常数减小) ②分子筛膜从反
应体系中不断分离出HO,有利于反应正向进行,甲醇产率升高 ③210
2
解析 ①图中有分子筛膜时,P点甲醇产率最大,达到平衡状态,P点后甲醇的产率降低,
其原因是合成甲醇的反应为放热反应,升高温度,平衡逆向移动,甲醇产率降低。②P点
有分子筛膜,T点无分子筛膜,而分子筛膜能选择性分离出 HO,使平衡正向移动,提高甲
2
醇的产率。③由图可知,当有分子筛膜,温度为210 ℃时,甲醇产率最大,故该分子筛膜
的最佳反应温度为210 ℃。
3.[2020·山东,18(3)]探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产
3 3
率。以CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.CO (g)+3H(g)CHOH(g)+HO(g)
2 2 3 2
ΔH=-49.5 kJ·mol-1
1Ⅱ.CO(g)+2H(g)CHOH(g)
2 3
ΔH=-90.4 kJ·mol-1
2
Ⅲ.CO (g)+H(g)CO(g)+HO(g) ΔH
2 2 2 3
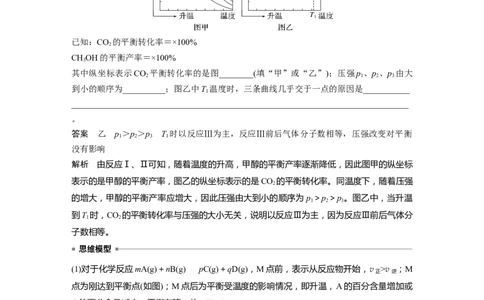
不同压强下,按照n(CO)∶n(H )=1∶3投料,实验测定CO 的平衡转化率和CHOH的平衡
2 2 2 3
产率随温度的变化关系如下图所示。
已知:CO 的平衡转化率=×100%
2
CHOH的平衡产率=×100%
3
其中纵坐标表示CO 平衡转化率的是图________(填“甲”或“乙”);压强p 、p 、p 由大
2 1 2 3
到小的顺序为__________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________
1
_______________________________________________________________________________
。
答案 乙 p >p >p T 时以反应Ⅲ为主,反应Ⅲ前后气体分子数相等,压强改变对平衡
1 2 3 1
没有影响
解析 由反应Ⅰ、Ⅱ可知,随着温度的升高,甲醇的平衡产率逐渐降低,因此图甲的纵坐标
表示的是甲醇的平衡产率,图乙的纵坐标表示的是CO 的平衡转化率。同温度下,随着压强
2
的增大,甲醇的平衡产率应增大,因此压强由大到小的顺序为p >p >p 。图乙中,当升温
1 2 3
到T 时,CO 的平衡转化率与压强的大小无关,说明以反应Ⅲ为主,因为反应Ⅲ前后气体分
1 2
子数相等。
(1)对于化学反应mA(g)+nB(g)pC(g)+qD(g),M点前,表示从反应物开始,v >v ;M
正 逆
点为刚达到平衡点(如图);M点后为平衡受温度的影响情况,即升温,A的百分含量增加或
C的百分含量减少,平衡左移,故ΔH<0。
(2)对于化学反应mA(g)+nB(g)pC(g)+qD(g),L线上所有的点都是平衡点(如图)。L线的左上方(如E点),A的百分含量大于此压强时平衡体系的A的百分含量,所以,E点:v >v
正
;则L线的右下方(如F点):v <v 。
逆 正 逆
题组二 曲线变化趋势的分析
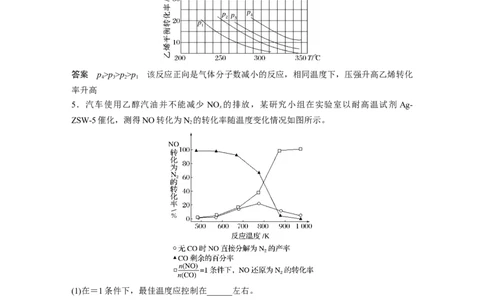
4.乙烯气相水合反应的热化学方程式为C H (g)+H O(g)C H OH(g) ΔH=-45.5 kJ·
2 4 2 2 5
mol-1,如图是乙烯气相水合法制乙醇中乙烯的平衡转化率与温度、压强的关系[其中
n(H O)∶n(C H)=1∶1]。图中压强(p 、p 、p 、p)的大小顺序为________,理由是
2 2 4 1 2 3 4
________________________________________________________________________
________________________________________________________________________。
答案 p>p>p>p 该反应正向是气体分子数减小的反应,相同温度下,压强升高乙烯转化
4 3 2 1
率升高
5.汽车使用乙醇汽油并不能减少 NO 的排放,某研究小组在实验室以耐高温试剂 Ag-
x
ZSW-5催化,测得NO转化为N 的转化率随温度变化情况如图所示。
2
(1)在=1条件下,最佳温度应控制在______左右。
(2)若不使用 CO,温度超过 775 K,发现 NO 的分解率降低,其可能的原因为
________________________________________________________________________。
(3) 用 平 衡 移 动 原 理 解 释 为 什 么 加 入 CO 后 NO 转 化 为 N 的 转 化 率 增 大 :
2
________________________________________________________________________
________________________________________________________________________。
答案 (1)870 K(860~880 K范围内都可以)
(2)该反应放热,升高温度,反应向逆反应方向进行
(3)加入的CO会与NO的分解产物O 发生反应,促进NO分解平衡向生成N 的方向移动,
2 2导致NO的转化率增大
6.下图是在一定时间内,使用不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知
工业使用的最佳催化剂为________,相应温度为________;使用Mn作催化剂时,脱氮率在
b~a段呈现如图变化的可能原因是__________________________________________
________________________________________________________________________。
答案 Mn 200 ℃ b~a段,开始温度较低,催化剂活性较低,脱氮反应速率较慢,反应
还没达到化学平衡,随着温度升高反应速率变大,一定时间参与反应的氮氧化物变多,导致
脱氮率逐渐增大
7.丙烯腈( )是一种重要的化工原料,广泛应用在合成纤维、合成橡胶及合成树脂等
工业生产中。以3-羟基丙酸乙酯[ (g)]为原料合成丙烯腈,主要反应过程如
下:
反应Ⅰ: (g) (g)+HO(g) ΔH
2 1
反应Ⅱ: (g)+NH (g) (g)+HO(g)+ (g) ΔH
3 2 2
在盛有催化剂TiO 、压强为200 kPa的恒压密闭容器中按体积比2∶15充入
2
(g)和NH (g)发生反应,通过实验测得平衡体系中含碳物质(乙醇除外)的物质的量分数随温度
3
的变化如图所示。随着温度的升高, (g)的平衡物质的量分数先增大后减小的原因为
________________________________________________________________________
________________________________________________________________________,
N点对应反应Ⅱ的平衡常数K=________(x代表物质的量分数)。
x
答案 温度较低时,反应Ⅰ进行的程度大, (g)的物质的量分数增大;温度较高
时反应Ⅱ进行的程度增大, (g)的物质的量分数减小
解析 根据图像可知,温度较低时, (g)的物质的量分数很小,随温度升高
(g)的物质的量分数增大, (g)是反应Ⅰ的生成物、反应Ⅱ的反应物,故随着温度
的升高, (g)的平衡物质的量分数先增大后减小的原因为温度较低时,反应Ⅰ进行
的程度大, (g)的物质的量分数增大;温度较高时反应Ⅱ进行的程度增大,
(g)的物质的量分数减小。N点时, (g)的物质的量分数为 0,
(g)完全消耗, (g)和 (g)的物质的量分数相等,即
(g)和 (g)物质的量相等,设起始 (g)、NH (g)物质的量依
3
次为2 mol、15 mol,平衡时 (g)物质的量为x mol,反应Ⅰ生成的 (g)和
HO(g)的物质的量均为2 mol,则反应Ⅱ消耗的 (g)和NH (g)、生成的HO(g)和
2 3 2
(g)物质的量都为x mol,则2-x=x,解得x=1,平衡时 (g)、NH (g)、
3(g)、HO(g)、 (g)物质的量依次为1 mol、14 mol、1 mol、3 mol、1 mol,气
2
体总物质的量为20 mol,物质的量分数依次为、、、、,N点对应反应Ⅱ的平衡常数K=
x
=。
8.汽车尾气是雾霾形成的原因之一,研究氮氧化物的处理方法可有效减少雾霾的形成,可
采用氧化还原法脱硝: 4NO(g)+4NH (g)+O(g) =====4N(g)+6HO(g) ΔH<0。根据下图
3 2 2 2
判断提高脱硝效率的最佳条件是____________________________________________________;
氨氮物质的量之比一定时,在400 ℃时,脱硝效率最大,其可能的原因是__________
________________________________________________________________________。
答案 氨氮物质的量之比为1,温度为400 ℃ 在400 ℃时,催化剂的活性最好,催化效
率最高,同时400 ℃温度较高,反应速率快
9.一种新型煤气化燃烧集成制氢发生的主要反应如下:
Ⅰ.C(s)+HO(g)CO(g)+H(g) ΔH
2 2 1
Ⅱ.CO(g)+HO(g)CO(g)+H(g) ΔH
2 2 2 2
Ⅲ.CaO(s)+CO(g)CaCO (s) ΔH
2 3 3
Ⅳ.C(s)+2HO(g)+CaO(s)CaCO (s)+2H(g) ΔH=-64.9 kJ·mol-1
2 3 2 4
副反应:
Ⅴ.C(s)+2H(g)CH(g)
2 4
ΔH=-74.8 kJ·mol-1
5
Ⅵ.CO(g)+3H(g)CH(g)+HO(g)
2 4 2
ΔH=-206.1 kJ·mol-1
6
回答下列问题:
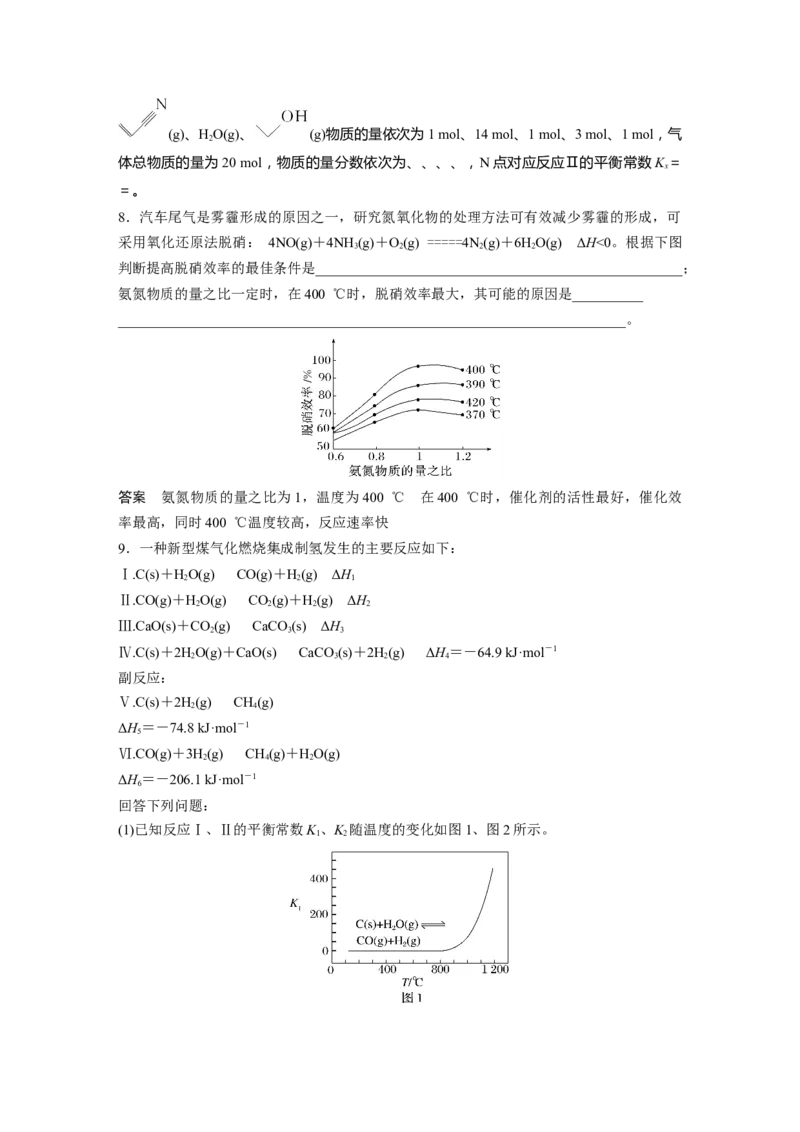
(1)已知反应Ⅰ、Ⅱ的平衡常数K 、K 随温度的变化如图1、图2所示。
1 2①由反应Ⅴ和反应Ⅵ可知,ΔH=________;反应Ⅰ的ΔS________(填“>”或“<”)0。
1
② 温 度 小 于 800 ℃ 时 , K = 0 , 原 因 是
1
________________________________________________。
③为提高反应Ⅱ中CO的转化率,可采取的措施是____________________________
_________________________________________________________________(写一条)。
④T ℃时,向密闭容器中充入1 mol CO(g)和3 mol H O(g),只发生反应Ⅱ ,此时该反应的
2
平衡常数K =1,CO的平衡转化率为________。
2
(2)从环境保护角度分析,该制氢工艺中设计反应Ⅲ的优点是___________________________。
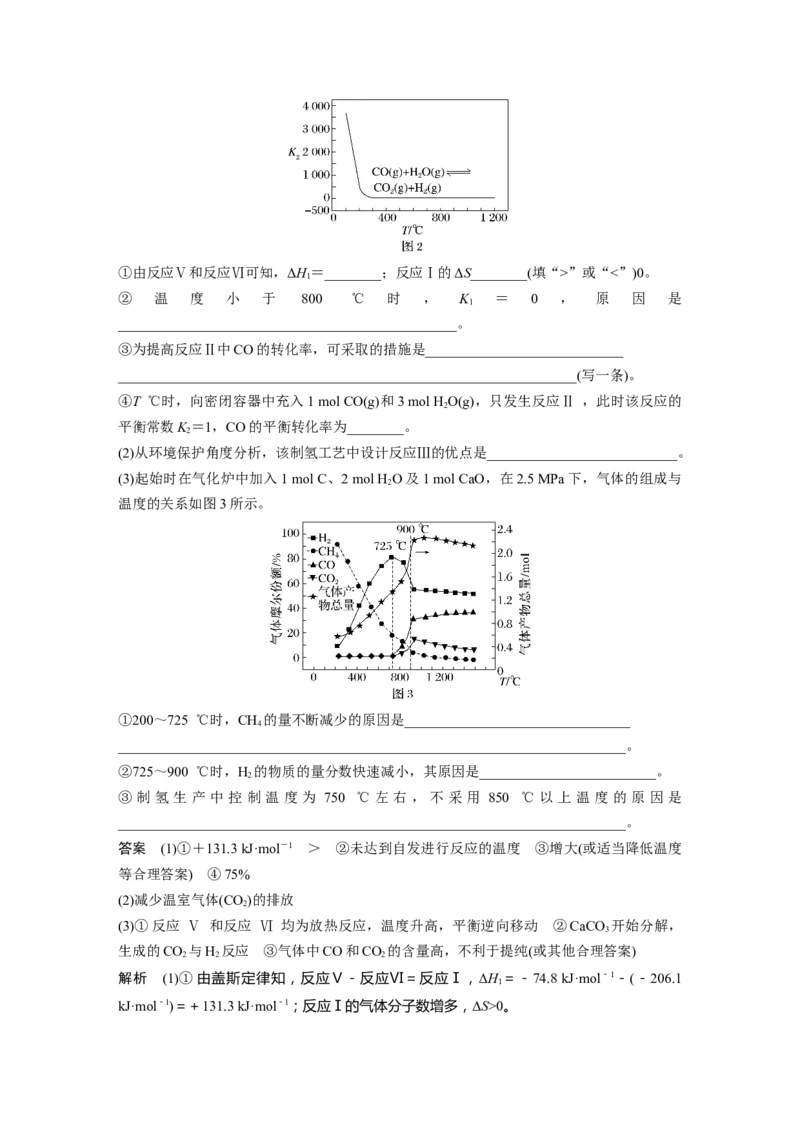
(3)起始时在气化炉中加入1 mol C、2 mol H O及1 mol CaO,在2.5 MPa下,气体的组成与
2
温度的关系如图3所示。
①200~725 ℃时,CH 的量不断减少的原因是________________________________
4
________________________________________________________________________。
②725~900 ℃时,H 的物质的量分数快速减小,其原因是_________________________。
2
③ 制 氢 生 产 中 控 制 温 度 为 750 ℃ 左 右 , 不 采 用 850 ℃ 以 上 温 度 的 原 因 是
________________________________________________________________________。
答案 (1)①+131.3 kJ·mol-1 > ②未达到自发进行反应的温度 ③增大(或适当降低温度
等合理答案) ④75%
(2)减少温室气体(CO)的排放
2
(3)①反应 Ⅴ 和反应 Ⅵ 均为放热反应,温度升高,平衡逆向移动 ②CaCO 开始分解,
3
生成的CO 与H 反应 ③气体中CO和CO 的含量高,不利于提纯(或其他合理答案)
2 2 2
解析 (1)①由盖斯定律知,反应Ⅴ-反应Ⅵ=反应Ⅰ,ΔH =-74.8 kJ·mol-1-(-206.1
1
kJ·mol-1)=+131.3 kJ·mol-1;反应Ⅰ的气体分子数增多,ΔS>0。③由图2可知,反应Ⅱ的K 随温度升高而减小,该反应为放热反应,故为提高反应Ⅱ中CO
2
的转化率可采取降低温度、增大等方法。
④设容器体积为V L,
CO(g)+HO(g)CO(g)+H(g)
2 2 2
起始/mol 1 3 0 0
转化/mol x x x x
平衡/mol 1-x 3-x x x
x2=(1-x)(3-x),解得x=0.75。故CO的平衡转化率为×100%=75%。
(2)该制氢工艺中设计反应Ⅲ的优点是吸收二氧化碳,减少温室气体的排放。