文档内容
第 45 讲 化学反应速率与反应历程
[复习目标] 1.了解基元反应、过渡态理论,了解速率方程和速率常数。2.掌握多因素对化
学反应速率影响的分析方法。
考点一 基元反应 过渡态理论
1.基元反应
大多数化学反应都是分几步完成的,其中的每一步反应都称为基元反应。
2.对于基元反应aA+bB===gG+hH,其速率方程可写为v=k·ca(A)·cb(B)(其中k称为速率
常数,恒温下,k不因反应物浓度的改变而变化),这种关系可以表述为基元反应的化学反应
速率与反应物浓度以其化学计量数为指数的幂的乘积成正比。有时称其为质量作用定律。
3.许多化学反应,尽管其反应方程式很简单,却不是基元反应,而是经由两个或多个步骤
完成的复杂反应。例如H(g)+I(g)===2HI(g),它的反应历程有如下两步基元反应:
2 2
①II+I(快)
2
②H+2I===2HI(慢)
2
其中慢反应为整个反应的决速步骤。
4.过渡态理论
如图所示是两步完成的化学反应,分析并回答下列问题。
(1)该反应的反应物为 A 、 B ,中间体为C,生成物为D。
(2)由A、B生成C的反应为吸(填“吸”或“放”,下同)热反应,由C生成D的反应为放热
反应,总反应为放热反应。
(3)第一步为慢(填“快”或“慢”,下同)反应,第二步为快反应,决定总反应快慢的是第一
步反应。一、反应机理——快反应与慢反应
1.甲烷与氯气在光照条件下存在如下反应历程(“·”表示电子):
①Cl――→2Cl·(慢反应)
2
②CH+Cl·―→·CH+HCl(快反应)
4 3
③·CH+Cl―→CHCl+Cl·(快反应)
3 2 3
④·CH+Cl·―→CHCl(快反应)
3 3
已知在一个分步反应中,较慢的一步反应控制总反应的速率。下列说法不正确的是( )
A.上述过程的总反应方程式为CH+Cl――→CHCl+HCl
4 2 3
B.光照的主要作用是促进反应①的进行从而使总反应速率加快
C.反应②~④都是由微粒通过碰撞而发生的反应
D.反应①是释放能量的反应
答案 D
解析 由反应历程可知,甲烷与氯气发生取代反应生成一氯甲烷和氯化氢,则总反应方程式
为CH +Cl――→CHCl+HCl,故A正确;光照的主要作用是破坏氯气分子中的共价键,形
4 2 3
成氯原子,促进反应①的进行从而使总反应速率加快,故B正确;由反应历程可知,反应
②~④都是由微粒通过有效碰撞而发生的反应,故C正确;反应①是破坏氯气分子中的共
价键形成氯原子的过程,应吸收能量,故D错误。
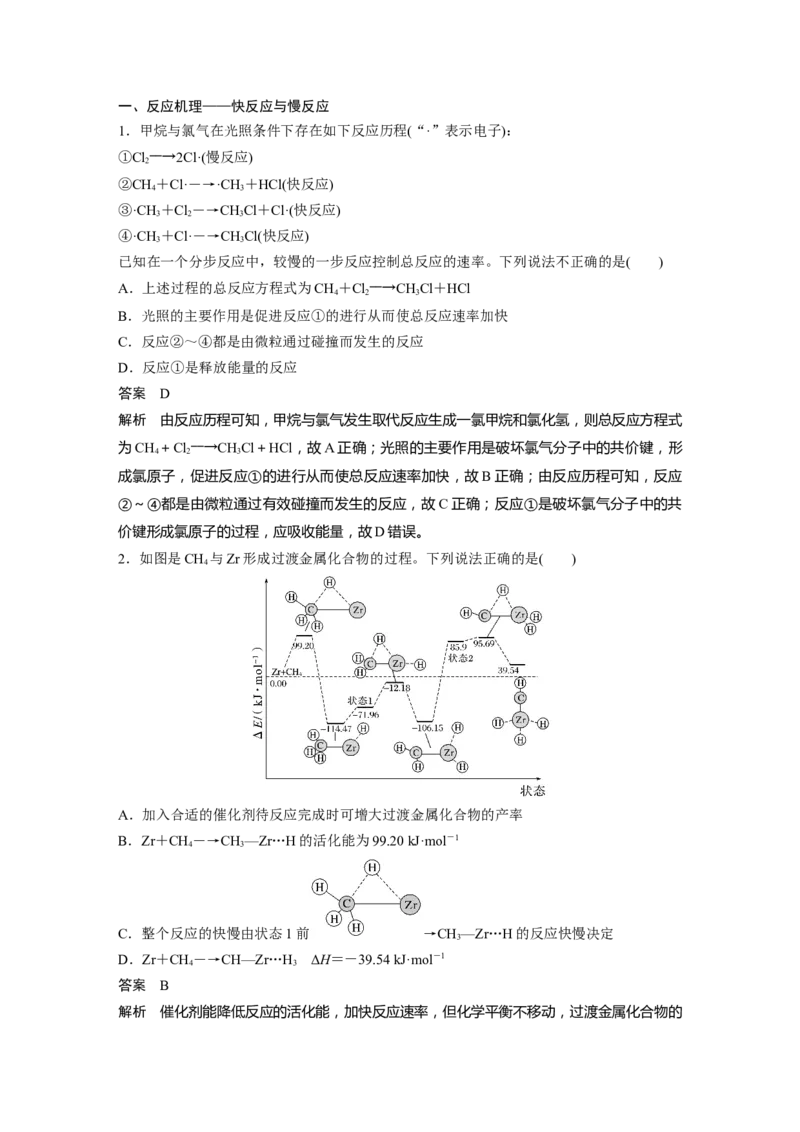
2.如图是CH 与Zr形成过渡金属化合物的过程。下列说法正确的是( )
4
A.加入合适的催化剂待反应完成时可增大过渡金属化合物的产率
B.Zr+CH―→CH—Zr…H的活化能为99.20 kJ·mol-1
4 3
C.整个反应的快慢由状态1前 →CH—Zr…H的反应快慢决定
3
D.Zr+CH―→CH—Zr…H ΔH=-39.54 kJ·mol-1
4 3
答案 B
解析 催化剂能降低反应的活化能,加快反应速率,但化学平衡不移动,过渡金属化合物的产率不变,故A错误;由图可知,反应Zr+CH―→CH—Zr…H的活化能为99.20 kJ·mol-
4 3
1,故B正确;由图可知, ―→状态2的活化能最大,反应速率最慢,决
定整个反应的快慢,故 C错误;由图可知,反应 Zr+CH―→CH—Zr…H ΔH=+39.54
4 3
kJ·mol-1,故D错误。
二、速率常数与速率方程
3.工业上利用 CH(混有 CO 和 H)与水蒸气在一定条件下制取 H ,原理为 CH(g)+
4 2 2 4
H
2
O(g)CO(g)+3H
2
(g),该反应的逆反应速率表达式为v逆 =k·c(CO)·c3(H
2
),k为速率常数,
在某温度下测得实验数据如表所示:
H 浓度/
2
CO浓度/ (mol·L-1) 逆反应速率/(mol·L-1·min-1)
(mol·L-1)
0.1 c 8.0
1
c c 16.0
2 1
c 0.15 6.75
2
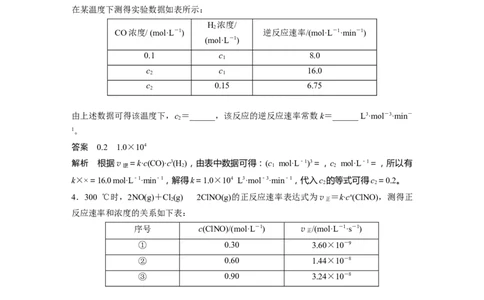
由上述数据可得该温度下,c =______,该反应的逆反应速率常数k=______ L3·mol-3·min-
2
1。
答案 0.2 1.0×104
解析 根据v =k·c(CO)·c3(H ),由表中数据可得:(c mol·L-1)3=,c mol·L-1=,所以有
逆 2 1 2
k××=16.0 mol·L-1·min-1,解得k=1.0×104 L3·mol-3·min-1,代入c 的等式可得c=0.2。
2 2
4.300 ℃时,2NO(g)+Cl
2
(g)2ClNO(g)的正反应速率表达式为v正 =k·cn(ClNO),测得正
反应速率和浓度的关系如下表:
序号 c(ClNO)/(mol·L-1) v正 /(mol·L-1·s-1)
① 0.30 3.60×10-9
② 0.60 1.44×10-8
③ 0.90 3.24×10-8
n=________;k=________。
答案 2 4.0×10-8 L·mol-1·s-1
解析 根据表格①②中的数据,代入正反应速率表达式然后做比值:=,解得 n=2,将n
和①或②或③中数据代入正反应速率表达式得k=4×10-8 L·mol-1·s-1。考点二 多因素影响下的速率图像分析
1.常考影响化学反应速率的因素:浓度、温度、压强、催化剂的活性、接触面积、原电池
原理、副反应等。
2.随着时间的推移,反应物浓度减小,反应速率减小。
3.绝大多数催化剂都有活性温度范围,温度太低时,催化剂的活性很小,反应速率很慢,
随温度升高,反应速率逐渐增大,物质转化率增大,温度过高又会破坏催化剂的活性。
4.速率图像分析的一般方法
(1)看清关键点:起点、终点和变化点。
(2)看清变化趋势。
(3)综合分析反应原理,如有的反应放热造成温度升高,反应速率加快;有的反应生成的金
属与原金属形成原电池,反应速率加快;有的反应物浓度减小,反应速率减慢;有的反应生
成物中有催化剂,反应速率加快;有的反应温度过高,造成催化剂失去活性,反应速率减慢
等。
一、温度与浓度的双重影响
1.把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1盐酸的烧杯中,该铝片与盐酸反
应生成氢气的速率v与反应时间t可用如图的坐标曲线来表示。
回答下列问题:
(1)O→a段不生成氢气的原因是_____________________________________________
________________________________________________________________________。
(2)b→c段生成氢气的速率增加较快的主要原因可能是__________________________
________________________________________________________________________。
(3)t>c时生成氢气的速率降低的主要原因是
________________________________________________________________________。
答案 (1)铝的表面有一层致密的Al O 薄膜,能与H+反应得到盐和水,无氢气放出
2 3
(2)反应放热,溶液温度升高,反应速率加快(或反应产生的铝离子是该反应的催化剂)
(3)随着反应的进行,溶液中氢离子的浓度逐渐降低二、温度与选择性的双重影响
2.汽车排气管装有三元催化剂装置,在催化剂表面通过发生吸附、解吸消除 CO、NO等污
染物。反应机理如下[Pt(s)表示催化剂,右上角带“*”表示吸附状态]:
Ⅰ.NO+Pt(s)===NO*
Ⅱ.CO+Pt(s)===CO*
Ⅲ.NO*===N*+O*
Ⅳ.CO*+O*===CO+Pt(s)
2
Ⅴ.N*+ N*===N+Pt(s)
2
Ⅵ.NO*+N*===NO+Pt(s)
2
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图1和图2所示。
(1)图1中温度从T升至T 的过程中,反应物浓度急剧减小的主要原因是__________
a b
________________________________________________________________________。
(2)图2中T ℃时反应Ⅴ的活化能________(填“<”“>”或“=”)反应Ⅵ的活化能;T ℃
2 3
时发生的主要反应为________(填“Ⅳ”“Ⅴ”或“Ⅵ”)。
答案 (1)温度升高,催化剂活性增强,反应速率加快 (2)> Ⅳ
解析 (1)由图1可知,温度升高,反应物的消耗量增大,说明催化剂的活性增强,反应速
率加快。
(2)由图2可知,T ℃时,N 的浓度小于NO的浓度,说明反应Ⅴ的反应速率小于反应Ⅵ的
2 2 2
反应速率,则反应Ⅴ的活化能大于反应Ⅵ的活化能;T ℃时,生成物二氧化碳的浓度最大,
3
说明发生的主要反应为反应Ⅳ。
1.(2021·山东,14)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为: +OH- +CHO-,能
3
量变化如图所示。已知 为快速平衡,下列说法正确的是(
)
.
A.反应Ⅱ 、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
答案 B
解析 一般来说,反应的活化能越高,反应速率越慢,由图可知,反应Ⅰ和反应Ⅳ的活化能
较高,因此反应的决速步为反应Ⅰ、Ⅳ,故A错误;反应Ⅰ为加成反应,而
为 快 速 平 衡 , 反 应 Ⅱ 的 成 键 和 断 键 方 式 为 或
,后者能生成18OH-,因此反应结束后,溶液中存在18OH-,故B正确;反
应Ⅲ的成键和断键方式为 或 ,因此反应结束后溶液中不会
存在CH18OH,故C错误;该总反应对应反应物的总能量高于生成物的总能量,总反应为放
3
热反应,因此 和CHO-的总能量与 和OH-的总能量
3之差等于图示总反应的焓变,故D错误。
2.(2022·北京,14)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反
2 2
应①完成之后,以N 为载气,以恒定组成的N 、CH 混合气,以恒定流速通入反应器,单
2 2 4
位时间流出气体各组分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到
CO,在催化剂上有积碳。
2
下列说法不正确的是( )
A.反应①为CaO+CO===CaCO ;反应②为CaCO +CH=====CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH=====C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
答案 C
解析 由题中图 1 所示信息可知,反应①为 CaO+CO===CaCO ,反应②为 CaCO +
2 3 3
CH=====CaO+2CO+2H ,A正确;由题中图2信息可知,t ~t ,n(H )比n(CO)多,且生
4 2 1 3 2
成H 的速率不变,且反应过程中始终未检测到 CO ,在催化剂上有积碳,故可能发生副反
2 2
应:CH=====C+2H ,B正确;由反应②的化学方程式可知,H 和CO的反应速率相等,
4 2 2
而t 时,H 的反应速率未变,仍然为2 mmol·min-1,而CO的反应速率为1~2 mmol·min-
2 2
1,故能够说明副反应生成H 的速率小于反应②生成H 速率,C错误;由图2可知,t 之后,
2 2 3
CO的速率为0,CH 的速率逐渐增大至1 mmol·min-1,说明反应②不再发生,而后副反应
4
逐渐停止,D正确。
3.[2018·江苏,20(4)②]NO(主要指NO和NO )是大气主要污染物之一。有效去除大气中的
x 2
NO 是环境保护的重要课题。在有氧条件下,新型催化剂 M能催化NH 与NO 反应生成
x 3 x
N。
2
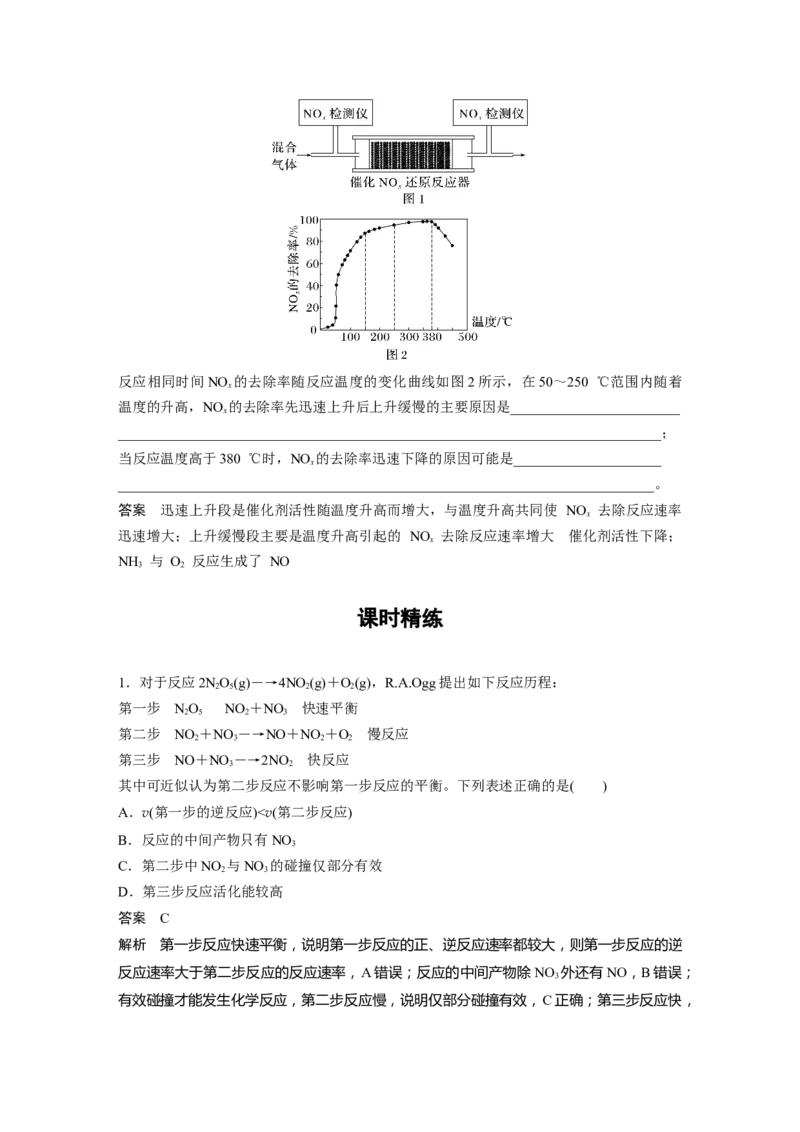
将一定比例的O 、NH 和NO 的混合气体,匀速通入装有催化剂M的反应器中反应(装置见
2 3 x
图1)。反应相同时间NO 的去除率随反应温度的变化曲线如图2所示,在50~250 ℃范围内随着
x
温度的升高,NO 的去除率先迅速上升后上升缓慢的主要原因是________________________
x
_____________________________________________________________________________;
当反应温度高于380 ℃时,NO 的去除率迅速下降的原因可能是_____________________
x
____________________________________________________________________________。
答案 迅速上升段是催化剂活性随温度升高而增大,与温度升高共同使 NO 去除反应速率
x
迅速增大;上升缓慢段主要是温度升高引起的 NO 去除反应速率增大 催化剂活性下降;
x
NH 与 O 反应生成了 NO
3 2
课时精练
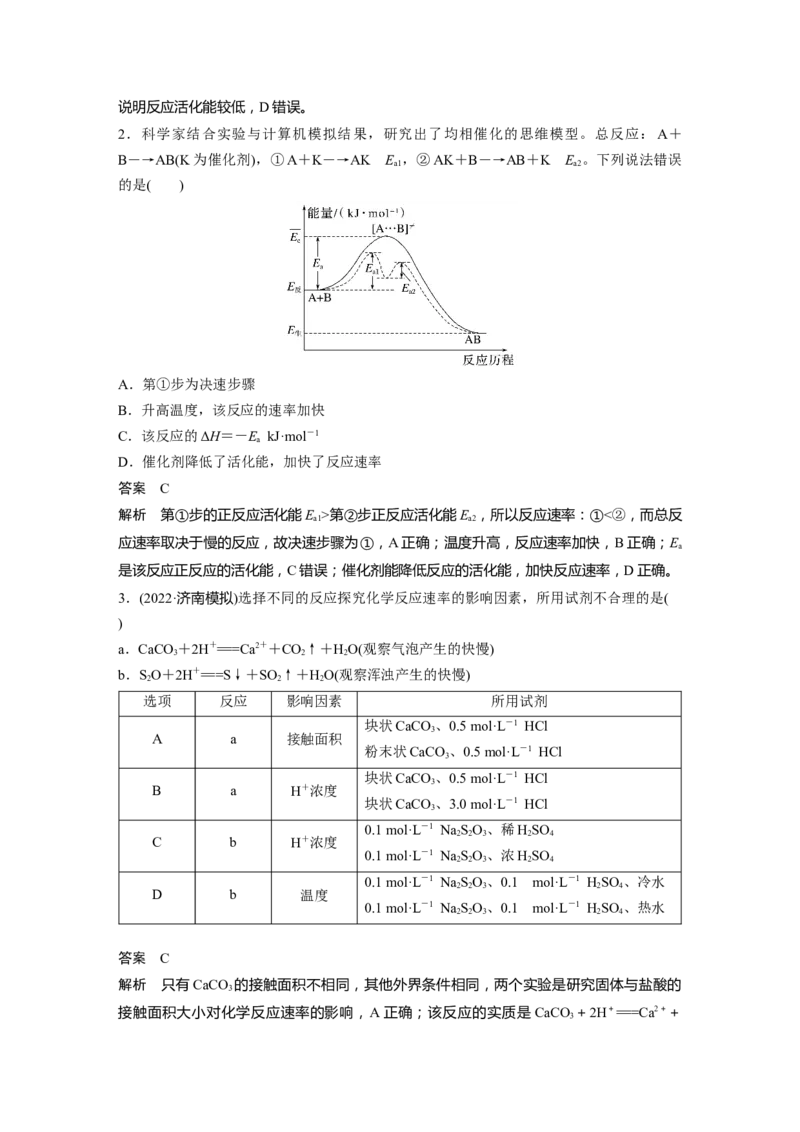
1.对于反应2NO(g)―→4NO (g)+O(g),R.A.Ogg提出如下反应历程:
2 5 2 2
第一步 NONO +NO 快速平衡
2 5 2 3
第二步 NO +NO ―→NO+NO +O 慢反应
2 3 2 2
第三步 NO+NO ―→2NO 快反应
3 2
其中可近似认为第二步反应不影响第一步反应的平衡。下列表述正确的是( )
A.v(第一步的逆反应)第②步正反应活化能E ,所以反应速率:①<②,而总反
a1 a2
应速率取决于慢的反应,故决速步骤为①,A正确;温度升高,反应速率加快,B正确;E
a
是该反应正反应的活化能,C错误;催化剂能降低反应的活化能,加快反应速率,D正确。
3.(2022·济南模拟)选择不同的反应探究化学反应速率的影响因素,所用试剂不合理的是(
)
a.CaCO +2H+===Ca2++CO↑+HO(观察气泡产生的快慢)
3 2 2
b.SO+2H+===S↓+SO ↑+HO(观察浑浊产生的快慢)
2 2 2
选项 反应 影响因素 所用试剂
块状CaCO 、0.5 mol·L-1 HCl
3
A a 接触面积
粉末状CaCO 、0.5 mol·L-1 HCl
3
块状CaCO 、0.5 mol·L-1 HCl
3
B a H+浓度
块状CaCO 、3.0 mol·L-1 HCl
3
0.1 mol·L-1 Na SO、稀HSO
2 2 3 2 4
C b H+浓度
0.1 mol·L-1 Na SO、浓HSO
2 2 3 2 4
0.1 mol·L-1 Na SO、0.1 mol·L-1 HSO 、冷水
2 2 3 2 4
D b 温度
0.1 mol·L-1 Na SO、0.1 mol·L-1 HSO 、热水
2 2 3 2 4
答案 C
解析 只有CaCO 的接触面积不相同,其他外界条件相同,两个实验是研究固体与盐酸的
3
接触面积大小对化学反应速率的影响,A正确;该反应的实质是CaCO +2H+===Ca2++
3CO↑+HO,只有HCl溶液中的c(H+)不相同,其他外界条件相同,是研究H+浓度大小对
2 2
化学反应速率的影响,B正确;浓硫酸中HSO 主要以电解质分子存在,稀硫酸中则完全电
2 4
离产生H+及SO,浓硫酸溶于水时会放出大量热量使溶液温度升高,因此两个实验对比,不
仅溶液中c(H+)不同,而且溶液温度也不相同,因此不是探究 H+浓度大小对化学反应速率
的影响,C不正确;两个实验对比,其他外界条件都相同,只有溶液温度不相同,是探究反
应温度对化学反应速率的影响,D正确。
4.(2022·济南历城第二中学模拟)二甲醚(CHOCH )被称为21世纪的“清洁能源”,科学家
3 3
研究在酸性条件下,用甲醇可合成二甲醚,反应历程中相对能量变化如图所示。
下列叙述错误的是( )
A.循环过程中,催化剂参与了中间反应
B.该历程中最小的能垒(基元反应活化能)为1.31 kJ·mol-1
C.制约总反应速率关键步骤的基元反应方程式为 ―→CHOCH +H+
3 3
D.总反应方程式为2CHOH=====CHOCH +HO
3 3 3 2
答案 B
解析 整个过程中H+是催化剂,先参与第一步反应,在最后一步反应生成,故A正确;由
图可知该历程中最小的能垒(基元反应活化能)为131 kJ·mol-1,故B错误;决定总反应速率
的是活化能或能垒最高的基元反应,由图可知,该基元反应为 ―→CHOCH +
3 3
H+,故C正确;整个过程消耗甲醇,生成二甲醚和水,故总反应为 2CHOH=====CHOCH
3 3 3
+HO,故D正确。
2
5.(2022·安徽淮北模拟)ICl 与 H 能发生的总反应为 H(g)+2ICl(g)===I(g)+2HCl(g)
2 2 2
ΔH<0。
已知:①该反应分两步完成,第一步为H(g)+ICl(g)===HI(g)+HCl(g)
2②两步反应的活化能分别为E 、E ,且E >E
a1 a2 a1 a2
下列判断正确的是( )
A.总反应中I 为氧化产物
2
B.第一步的化学反应速率大于第二步的化学反应速率
C.已知键能:H—H>I—I,可推知键能H—ClE ,活化能大的化学反应速率慢,
2 a1 a2
故第一步的化学反应速率小于第二步的化学反应速率,B错误;H—Cl的键长小于I—Cl的
键长,键长越短,键能越大,故键能:H—Cl>I—Cl,C错误;总反应方程式减去第一步反
应方程式可得第二步的化学方程式,D正确。
6.反应SO+3I-===2SO+I的反应机理为①SO+I-===SOI3-,②……,③I+I-===I(快
2 2 2 8 2
反应),改变反应物浓度时,反应的瞬时速率如表所示:
c(S O)/ (mol·L-1) c(I-)/ (mol·L-1) v/(mol·L-1·min-1)
2
0.038 0.060 1.4×10-5
0.076 0.060 2.8×10-5
0.076 0.030 1.4×10-5
下列说法正确的是( )
A.该反应的速率方程为v=k·c(S O)·c3(I-)
2
B.该反应的速率常数k的值为6.14×10-3
C.第②步的反应方程式为SOI3-+I===2SO+3I-
2 8 2
D.3步反应中反应③的活化能最大
答案 B
解析 由1、2两组数据,c(S O)增大1倍,速率增大1倍,由2、3两组数据,c(I-)增大1
2
倍,速率增大1倍,该反应的速率方程为v=k·c(S O)·c(I-),故A错误;将1组的数据代入
2
v=k·c(S O)·c(I-),1.4×10-5=k×0.038×0.060,k≈6.14×10-3,故B正确;总反应-①-
2
③可得第②步反应的化学方程式:SOI3-+I-===2SO+I ,故C错误;反应③为快反应,
2 8 2
活化能最小,故D错误。
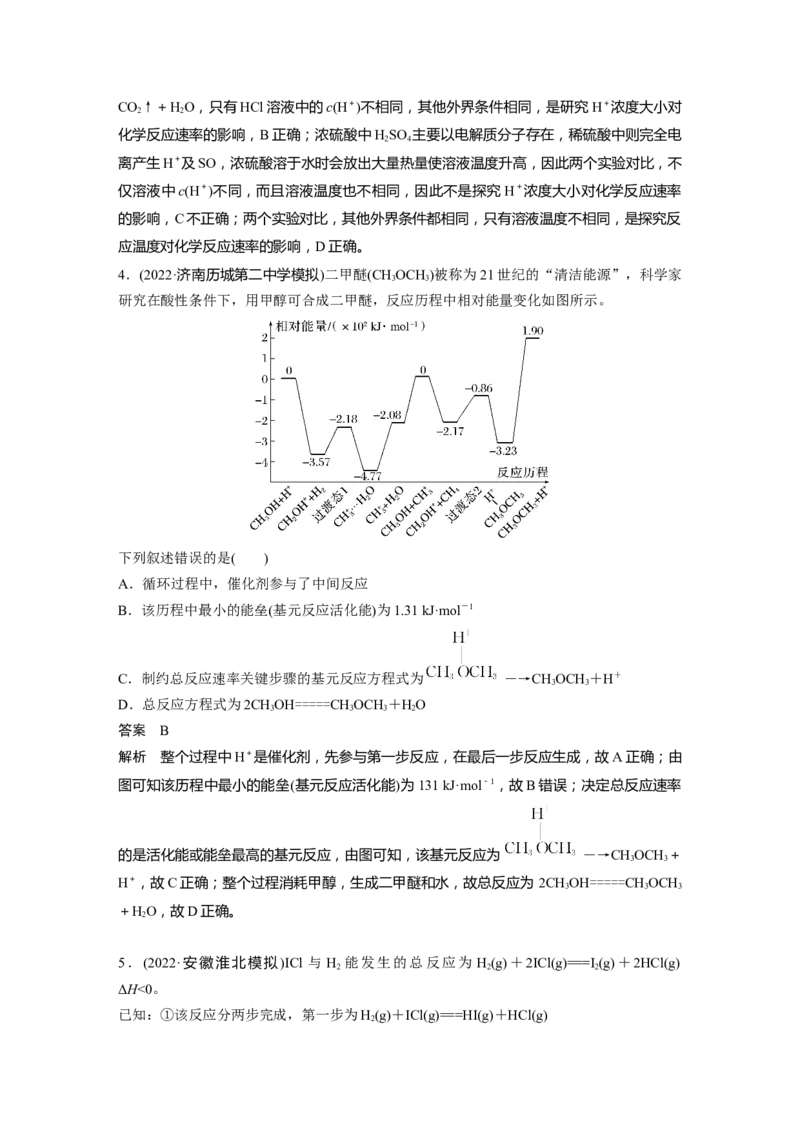
7.(2022·山东临沂模拟)一种以Pd-Cu为催化剂还原去除水体中NO的机理如图a所示;其
他条件相同,不同pH时,NO转化率和不同产物在总还原产物中所占的物质的量的百分比
如图b所示。已知:溶液pH会影响Pd对NO的吸附,不影响对H的吸附。
下列说法不正确的是( )
A.pH越小,Pd对NO的吸附能力越强
B.通过调节溶液的pH,可使NO更多的转化为N
2
C.反应ii中生成NH的离子方程式为NO+6H+2H+===NH+2HO
2
D.pH=12时,每处理6.2 g NO,理论上消耗标准状况下H 5.6 L
2
答案 D
解析 由图b可知,随着pH减小,n(N )增大,n(氨态氮)变化不大,n(NO)减小,说明pH
2
越小,Pd对NO的吸附能力越强,A正确;由图b信息可知,pH不同还原产物也不同,pH
为4时还原产物主要为N,pH为12时,还原产物几乎全是NO,故通过调节溶液的pH,可
2
使NO更多的转化为N ,B正确;由图a可知,反应ii即NO和H反应生成NH,根据氧化
2
还原反应配平可得,反应ii中生成NH的离子方程式为NO+6H+2H+===NH+2HO,C正
2
确;由图b可知,pH=12时,还原产物几乎全是NO,则每处理6.2 g NO转移电子×2=0.2
mol,根据得失电子守恒可知,理论上消耗标准状况下×22.4 L·mol-1=2.24 L H ,D错误。
2
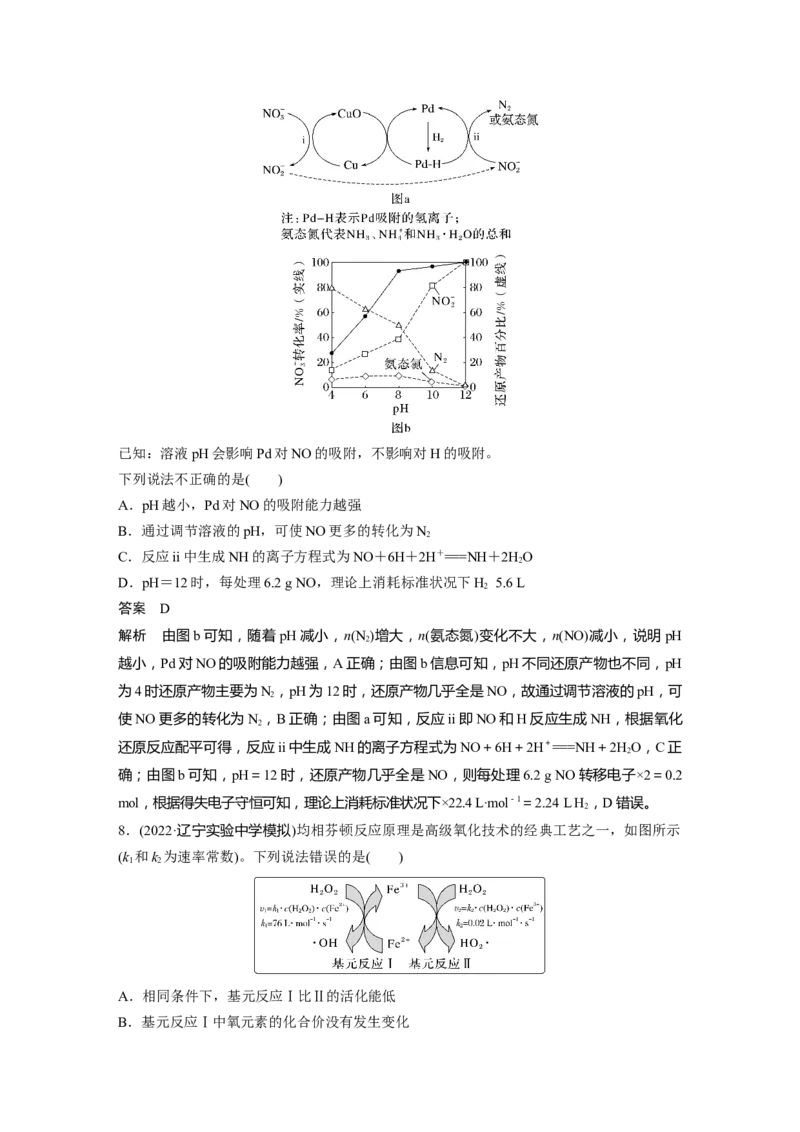
8.(2022·辽宁实验中学模拟)均相芬顿反应原理是高级氧化技术的经典工艺之一,如图所示
(k 和k 为速率常数)。下列说法错误的是( )
1 2
A.相同条件下,基元反应Ⅰ比Ⅱ的活化能低
B.基元反应Ⅰ中氧元素的化合价没有发生变化C.基元反应Ⅱ的化学方程式为HO+Fe3+===HO ·+Fe2++H+
2 2 2
D.芬顿反应进行的过程中,整个体系的pH会发生变化(忽略体积变化)
答案 B
解析 由题干信息可知,k >k ,说明相同条件下,基元反应Ⅰ比Ⅱ的反应速率更快,活化
1 2
能越低反应速率越快,即基元反应Ⅰ比Ⅱ的活化能低,A正确;由题图可知,基元反应Ⅰ为
H++HO +Fe2+===Fe3++·OH+HO,故基元反应Ⅰ中氧元素的化合价发生变化,B错误;
2 2 2
由题图可知,基元反应Ⅱ的化学方程式为HO+Fe3+===HO ·+Fe2++H+,C正确。
2 2 2
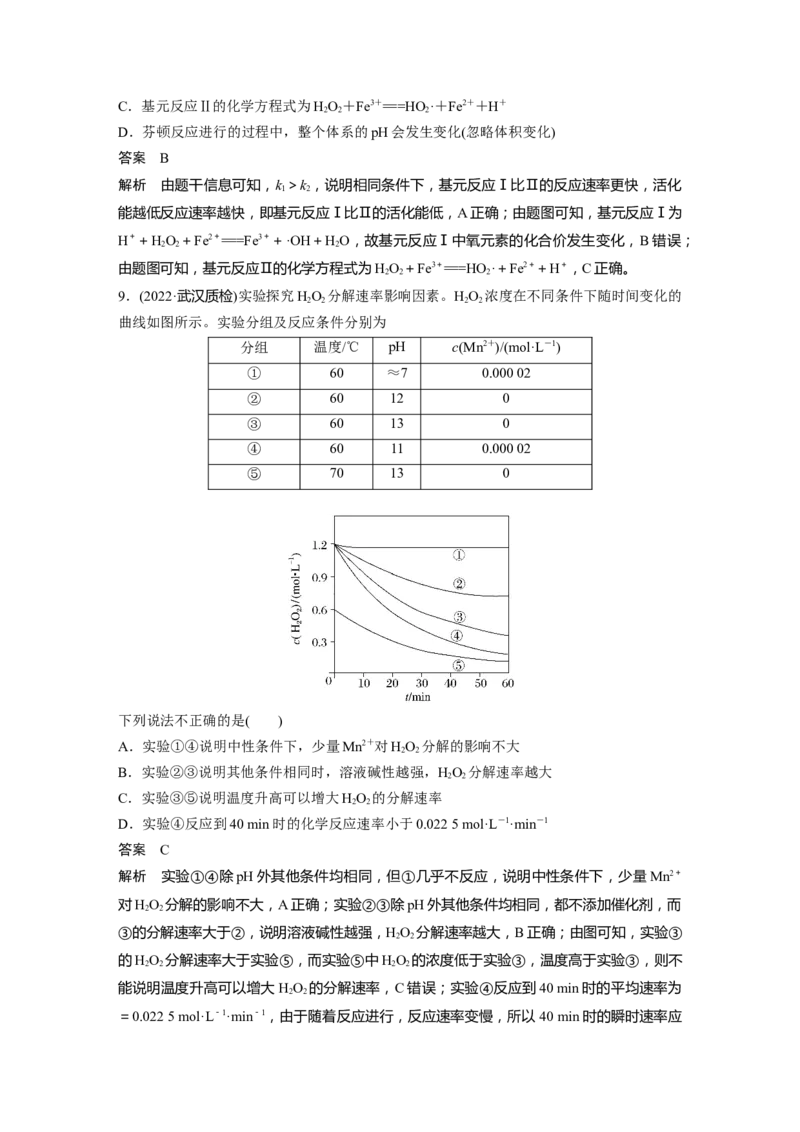
9.(2022·武汉质检)实验探究HO 分解速率影响因素。HO 浓度在不同条件下随时间变化的
2 2 2 2
曲线如图所示。实验分组及反应条件分别为
分组 温度/℃ pH c(Mn2+)/(mol·L-1)
① 60 ≈7 0.000 02
② 60 12 0
③ 60 13 0
④ 60 11 0.000 02
⑤ 70 13 0
下列说法不正确的是( )
A.实验①④说明中性条件下,少量Mn2+对HO 分解的影响不大
2 2
B.实验②③说明其他条件相同时,溶液碱性越强,HO 分解速率越大
2 2
C.实验③⑤说明温度升高可以增大HO 的分解速率
2 2
D.实验④反应到40 min时的化学反应速率小于0.022 5 mol·L-1·min-1
答案 C
解析 实验①④除pH外其他条件均相同,但①几乎不反应,说明中性条件下,少量Mn2+
对HO 分解的影响不大,A正确;实验②③除pH外其他条件均相同,都不添加催化剂,而
2 2
③的分解速率大于②,说明溶液碱性越强,HO 分解速率越大,B正确;由图可知,实验③
2 2
的HO 分解速率大于实验⑤,而实验⑤中HO 的浓度低于实验③,温度高于实验③,则不
2 2 2 2
能说明温度升高可以增大HO 的分解速率,C错误;实验④反应到40 min时的平均速率为
2 2
=0.022 5 mol·L-1·min-1,由于随着反应进行,反应速率变慢,所以40 min时的瞬时速率应小于0.022 5 mol·L-1·min-1,D正确。
10.对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L
-1)随时间(min)变化的有关实验数据见下表。
时间
0 5 10 15 20 25
水样
Ⅰ(pH=2) 0.40 0.28 0.19 0.13 0.10 0.09
Ⅱ(pH=4) 0.40 0.31 0.24 0.20 0.18 0.16
Ⅲ(pH=4) 0.20 0.15 0.12 0.09 0.07 0.05
Ⅳ(pH=4,含Cu2
0.20 0.09 0.05 0.03 0.01 0
+)
下列说法不正确的是( )
A.在0~20 min内,Ⅰ中M的平均分解速率为0.015 mol·L-1·min-1
B.其他条件相同时,水样酸性越强,M的分解速率越快
C.在0~25 min内,Ⅲ中M的分解百分率比Ⅱ中的大
D.由于Cu2+存在,Ⅳ中M的分解速率比Ⅰ中的快
答案 D
解析 v(M)==0.015 mol·L-1·min-1,故A正确;对比Ⅰ和Ⅱ,在相同的时间内,Ⅰ中消
耗M的量大于Ⅱ中消耗M的量,说明其他条件相同时,酸性越强,M的分解速率越快,故
B正确;在0~25 min内,Ⅲ中M的分解百分率为×100%=75%,Ⅱ中M的分解百分率为
×100%=60%,因此Ⅲ中M的分解百分率比Ⅱ中的大,故C正确;Ⅰ和Ⅳ中pH、起始浓度
均不同,因此不能说明由于Cu2+存在,Ⅳ中M的分解速率比Ⅰ中的快,故D错误。
11.某温度下,XY在金(Au)表面发生分解反应:2XY(g)===2X(g)+Y(g),该反应的速率
2 2 2 2
方程式为v=kca(X Y)(k为速率常数,k只与温度、催化剂、接触面积等有关,与浓度无关,
2
a为反应级数),实验测得剩余XY的物质的量浓度与时间的关系如表所示:
2
时间/min 0 20 40 60 80
c(X Y)/(mol·L-1) 0.100 0.080 0.060 0.040 0.020
2
下列说法正确的是( )
A.a=1
B.反应过程中c(X Y)与t的关系如图所示
2
C.速率常数k=1.0×10-2 mol·L-1·min-1
D.其他条件不变,仅增大c(X Y),反应速率增大
2答案 B
解析 由表中数据可知,在0~20 min、20~40 min、40~60 min,XY的浓度均减少了0.02
2
mol·L-1,即该反应速率与起始浓度无关,为匀速反应,故a=0,v=k,A、D错误,B正
确;0~20 min内,v=k===1.0×10-3 mol·L-1·min-1,C错误。
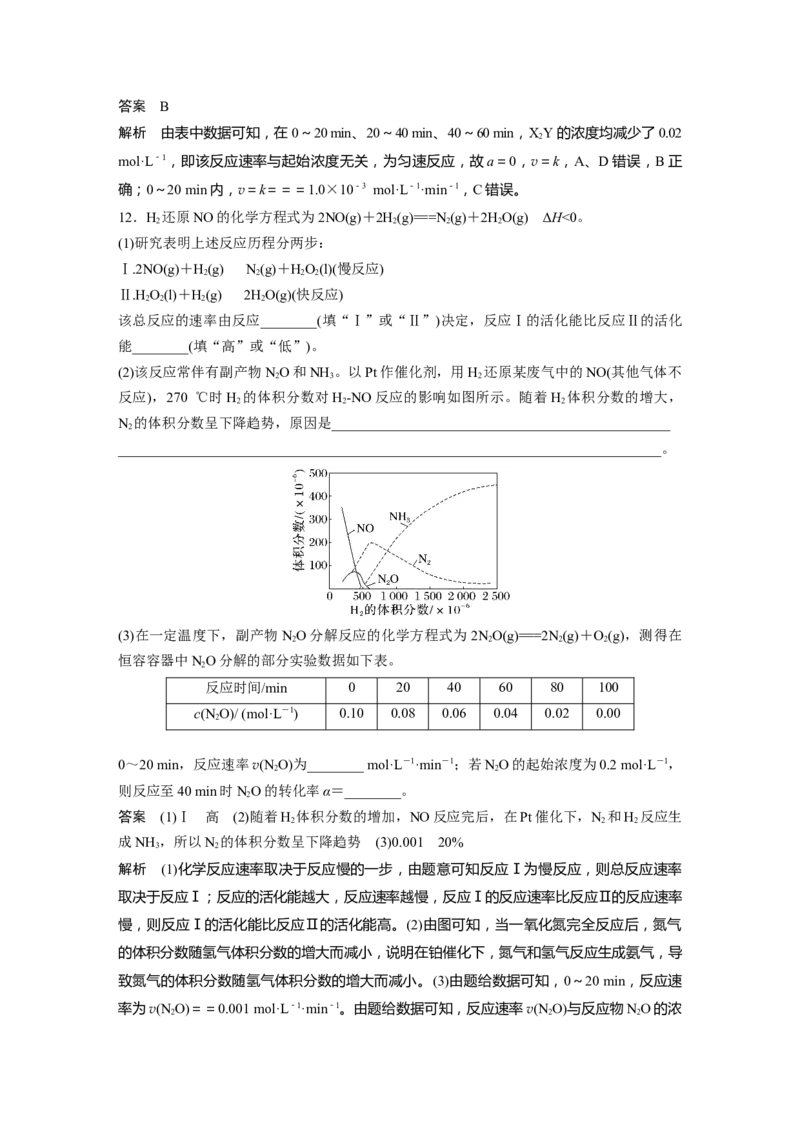
12.H 还原NO的化学方程式为2NO(g)+2H(g)===N(g)+2HO(g) ΔH<0。
2 2 2 2
(1)研究表明上述反应历程分两步:
Ⅰ.2NO(g)+H(g)N(g)+HO(l)(慢反应)
2 2 2 2
Ⅱ.H O(l)+H(g)2HO(g)(快反应)
2 2 2 2
该总反应的速率由反应________(填“Ⅰ”或“Ⅱ”)决定,反应Ⅰ的活化能比反应Ⅱ的活化
能________(填“高”或“低”)。
(2)该反应常伴有副产物NO和NH 。以Pt作催化剂,用H 还原某废气中的NO(其他气体不
2 3 2
反应),270 ℃时H 的体积分数对H-NO反应的影响如图所示。随着H 体积分数的增大,
2 2 2
N 的体积分数呈下降趋势,原因是________________________________________________
2
_____________________________________________________________________________。
(3)在一定温度下,副产物NO分解反应的化学方程式为2NO(g)===2N(g)+O(g),测得在
2 2 2 2
恒容容器中NO分解的部分实验数据如下表。
2
反应时间/min 0 20 40 60 80 100
c(N O)/ (mol·L-1) 0.10 0.08 0.06 0.04 0.02 0.00
2
0~20 min,反应速率v(N O)为________ mol·L-1·min-1;若NO的起始浓度为0.2 mol·L-1,
2 2
则反应至40 min时NO的转化率α=________。
2
答案 (1)Ⅰ 高 (2)随着H 体积分数的增加,NO反应完后,在Pt催化下,N 和H 反应生
2 2 2
成NH ,所以N 的体积分数呈下降趋势 (3)0.001 20%
3 2
解析 (1)化学反应速率取决于反应慢的一步,由题意可知反应Ⅰ为慢反应,则总反应速率
取决于反应Ⅰ;反应的活化能越大,反应速率越慢,反应Ⅰ的反应速率比反应Ⅱ的反应速率
慢,则反应Ⅰ的活化能比反应Ⅱ的活化能高。(2)由图可知,当一氧化氮完全反应后,氮气
的体积分数随氢气体积分数的增大而减小,说明在铂催化下,氮气和氢气反应生成氨气,导
致氮气的体积分数随氢气体积分数的增大而减小。(3)由题给数据可知,0~20 min,反应速
率为v(N O)==0.001 mol·L-1·min-1。由题给数据可知,反应速率v(N O)与反应物NO的浓
2 2 2度无关,反应速率恒定为0.001 mol·L-1·min-1,则反应至40 min时NO的转化率α=×100%
2
=20%。