文档内容
2025届高三化学一轮专题复习讲义(03)
专题一 基本概念
1-3 氧化还原反应(1课时)
【复习目标】
1.认识有化合价变化的反应是氧化还原反应,了解氧化还原反应的本质。
2.知道常见的氧化剂和还原剂,掌握氧化还原反应的基本规律。
3.运用氧化还原反应基本知识及规律解决实际问题。
【重点突破】
1.氧化还原反应规律。
2.氧化还原反应规律的实际应用。
【真题再现】
例1.(2022·北京·高考真题)下列物质混合后,因发生氧化还原反应使溶液pH减小的是
A.向NaHSO 溶液中加入少量BaCl 溶液,生成白色沉淀
4 2
B.向NaOH和Fe(OH) 的悬浊液中通入空气,生成红褐色沉淀
2
C.向NaHCO 溶液中加入少量CuSO 溶液,生成蓝绿色沉淀[Cu (OH) CO]
3 4 2 2 3
D.向HS溶液中通入氯气,生成黄色沉淀
2
解析:A项,向NaHSO 中加入少量BaCl 溶液,实际参与反应的只有硫酸根离子和钡离子,忽略体积
4 2
变化,H+的浓度不变,其pH不变,错误;B项,向 NaOH 和 Fe(OH) 的悬浊液中通入空气,虽然
2
有氢氧化亚铁被氧化成了红褐色的氢氧化铁,其方程式为4Fe(OH) +2HO+O=== 4Fe(OH) ,该
2 2 2 3
过和中会消耗水,则增大了氢氧根离子的浓度,pH会变大,错误;C项,向NaHCO 溶液中加入
3
少量 CuSO 溶液,生成蓝绿色沉淀 [Cu (OH) CO],其中没有元素的化合价发生变化,故没有氧
4 2 2 3
化还原反应,错误;D项,向HS中通入氯气生成HCl和单质硫沉淀,这个氧化还原反应增大了
2
H+的浓度,pH减小,正确。
答案:D。
例2.(江苏高考题整合):
(1)(2023·江苏高考) 在催化剂作用下MgSO 被O 氧化为MgSO 。已知MgSO 的溶解度为0.57g
3 2 4 3
(20℃),O 氧化溶液中SO的离子方程式为__________;
2
(2)(2022·江苏高考) 实验室以二氧化铈(GeO )废渣为原料制备Cl-含量少的Ge(CO),其部分实
2 2 3 3
验过程如下:
“酸浸”时GeO 与HO 反应生成Ge3+并放出O,该反应的离子方程式为 。
2 2 2 2
(3)(2022·江苏高考) “Fe—HCO—HO”“热循环制氢和甲酸”的原理为:在密闭容器中,铁粉
2
与吸收CO 制得的NaHCO 溶液反应,生成H、HCOONa和Fe O;Fe O 再经生物柴油副产
2 3 2 3 4 3 4
品转化为Fe。实验中发现,在300℃时,密闭容器中NaHCO 溶液与铁粉反应,反应初期有
3
FeCO 生成并放出H,该反应的离子方程式为 。
3 2
(4)(2021·江苏高考)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通过装有
2 2 2
ZnFe O 脱硫剂的硫化反应器。硫化过程中ZnFe O 与H、HS反应生成ZnS和FeS,其化学
2 4 2 4 2 2
方程式为 。
(5)(2020·江苏高考)CO 催化加氢。在密闭容器中,向含有催化剂的KHCO 溶液(CO 与KOH
2 3 2
溶液反应制得)中通入H 生成HCOO-,其离子方程式:____________________。
2
答案:(1)2+O =====2
2
(2)2CeO+H O+6H+=2Ce3++O ↑+4H O;
2 2 2 2 2
(3)
(4)ZnFe O+3H S+H=====ZnS+2FeS+4H O
2 4 2 2 2
(5)HCO+H
2
==HCOO-+H
2
O
例3. 化学反应计算及循环转化图(江苏高考题整合):
(1)(2023·江苏卷)金属硫化物(MS)催化反应CH(g)+2H S(g)===CS(g)+4H (g),既可以除去天
x y 4 2 2 2
然气中的HS,又可以获得H。下列说法正确的是
2 2
A.该反应的△S<0
B.该反应的平衡常数K=C.题图所示的反应机理中,步骤Ⅰ可理解为HS中带部分负电荷的S与催化剂中的M之间
2
发生作用
D.该反应中每消耗1mol HS,转移电子的数目约为2×6.02×1023
2
(2)(2022·江苏化学)“ 热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,
其过程如图所示。
电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价变化
的元素有_______(填元素符号)。
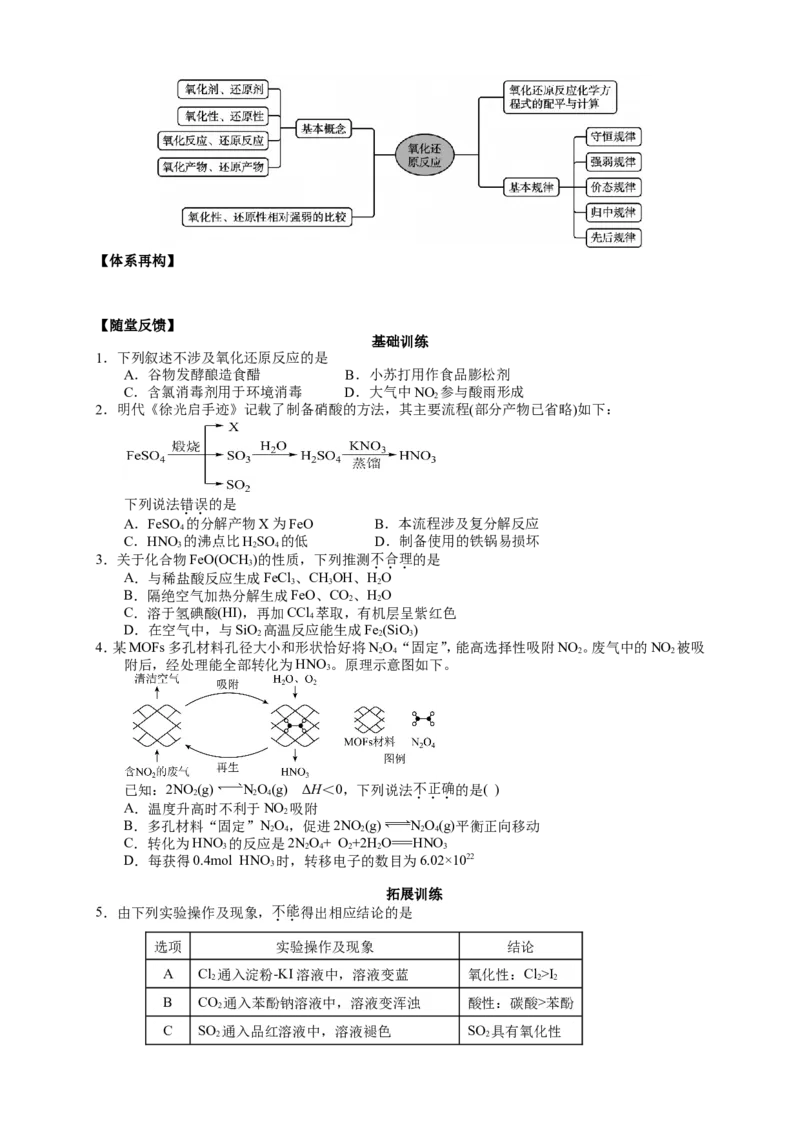
(3)(2021·江苏化学) 图2所示机理的步骤(i)中,元素Cu、Ce化
合价发生的变化为___。
(4)(2018·江苏化学,16)Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和SO ,理论上完全
2 3 2 3 4 2
反应消耗的n(FeS )∶n(Fe O)=________。
2 2 3
解析:(1)A项,左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5,△S>0,错误;B
项,由方程形式知,K= ,错误;C项,由题图知,经过步骤Ⅰ后,HS中带部分负电荷的S与催化
2
剂中的M之间形成了作用力,正确;D项,由方程式知,消耗1mol HS同时生成2 mol H,转移
2 2
4mole-,数目为4×6.02×1023,错误。(2)电解后,经热水解得到的HCl和热分解得到的CuCl等物
质可循环使用,从图中可知,热分解产物还有O,从详解①中得知,进入热水解的物质有 ,
2
故发生化合价变化的元素有Cu、O。(3)图2所示机理的步骤(i)中CO结合氧元素转化为二氧化
碳,根据Cu、Ce两种元素的核外电子排布式可判断元素Cu、Ce化合价发生的变化为铜的化合价
由+2变为+1价,铈的化合价由+4价变为+3价。(4)设参加反应的FeS 与Fe O 的物质的量分别
2 2 3
为x、y,由电子守恒有:(8/3 -2)x + 5×2x = (3- 8/3) ×2y,解得x∶y=1∶16。
答案:(1)B
(2)Cu、O
(3)铜的化合价由+2变为+1价,铈的化合价由+4价变为+3价
(4) 1∶16
小结:守恒法解题的思维流程
(1)找出氧化剂、还原剂及相应的还原产物和氧化产物。
(2)找准一个原子或离子得失电子数(注意化学式中粒子的个数)。
(3)根据题中物质的物质的量和得失电子守恒列出等式。
n(氧化剂)×变价原子个数×化合价变化值(高价-低价)=n(还原剂)×变价原子个数×化合价
变化值(高价-低价)
【知能整合】【体系再构】
【随堂反馈】
基础训练
1.下列叙述不涉及氧化还原反应的是
A.谷物发酵酿造食醋 B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒 D.大气中NO 参与酸雨形成
2
2.明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4
3.关于化合物FeO(OCH )的性质,下列推测不合理的是
3
A.与稀盐酸反应生成FeCl、CHOH、HO
3 3 2
B.隔绝空气加热分解生成FeO、CO、HO
2 2
C.溶于氢碘酸(HI),再加CCl 萃取,有机层呈紫红色
4
D.在空气中,与SiO 高温反应能生成Fe(SiO)
2 2 3
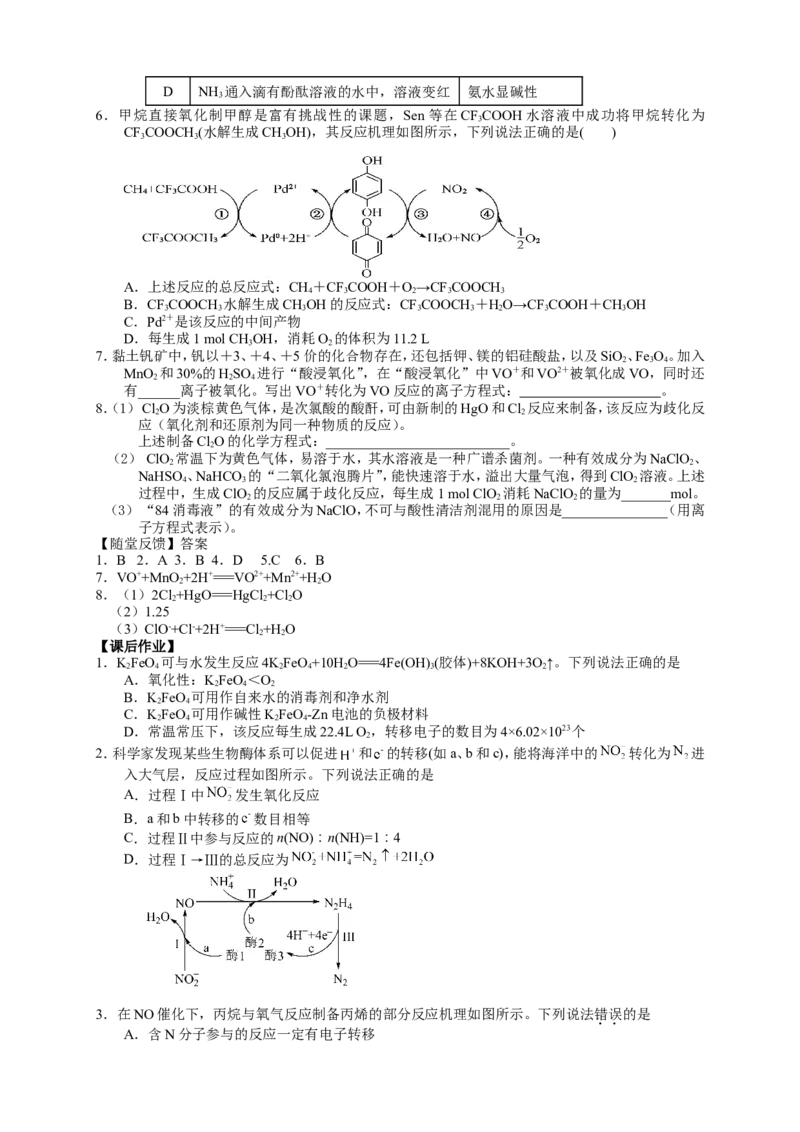
4.某MOFs多孔材料孔径大小和形状恰好将NO“固定”,能高选择性吸附NO 。废气中的NO 被吸
2 4 2 2
附后,经处理能全部转化为HNO。原理示意图如下。
3
已知:2NO(g) NO(g) ΔH<0,下列说法不正确的是( )
2 2 4
A.温度升高时不利于NO 吸附
2
B.多孔材料“固定”NO,促进2NO(g) NO(g)平衡正向移动
2 4 2 2 4
C.转化为HNO 的反应是2NO+ O+2HO===HNO
3 2 4 2 2 3
D.每获得0.4mol HNO 时,转移电子的数目为6.02×1022
3
拓展训练
5.由下列实验操作及现象,不能得出相应结论的是
选项 实验操作及现象 结论
A Cl 通入淀粉-KI溶液中,溶液变蓝 氧化性:Cl>I
2 2 2
B CO 通入苯酚钠溶液中,溶液变浑浊 酸性:碳酸>苯酚
2
C SO 通入品红溶液中,溶液褪色 SO 具有氧化性
2 2D NH 通入滴有酚酞溶液的水中,溶液变红 氨水显碱性
3
6.甲烷直接氧化制甲醇是富有挑战性的课题,Sen等在CFCOOH水溶液中成功将甲烷转化为
3
CFCOOCH (水解生成CHOH),其反应机理如图所示,下列说法正确的是( )
3 3 3
A.上述反应的总反应式:CH+CFCOOH+O→CFCOOCH
4 3 2 3 3
B.CFCOOCH 水解生成CHOH的反应式:CFCOOCH +HO→CF COOH+CHOH
3 3 3 3 3 2 3 3
C.Pd2+是该反应的中间产物
D.每生成1 mol CH OH,消耗O 的体积为11.2 L
3 2
7.黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO、Fe O。加入
2 3 4
MnO 和30%的HSO 进行“酸浸氧化”,在“酸浸氧化”中VO+和VO2+被氧化成VO,同时还
2 2 4
有______离子被氧化。写出VO+转化为VO反应的离子方程式: 。
8.(1) ClO为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反
2 2
应(氧化剂和还原剂为同一种物质的反应)。
上述制备ClO的化学方程式:__________________________。
2
(2) ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO、
2 2
NaHSO、NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述
4 3 2
过程中,生成ClO 的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量为_______mol。
2 2 2
(3) “84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是_______________(用离
子方程式表示)。
【随堂反馈】答案
1.B 2.A 3.B 4.D 5.C 6.B
7.VO++MnO+2H+===VO2++Mn2++H O
2 2
8.(1)2Cl+HgO===HgCl +ClO
2 2 2
(2)1.25
(3)ClO-+Cl-+2H+===Cl+H O
2 2
【课后作业】
1.KFeO 可与水发生反应4KFeO+10H O===4Fe(OH) (胶体)+8KOH+3O ↑。下列说法正确的是
2 4 2 4 2 3 2
A.氧化性:KFeO<O
2 4 2
B.KFeO 可用作自来水的消毒剂和净水剂
2 4
C.KFeO 可用作碱性KFeO-Zn电池的负极材料
2 4 2 4
D.常温常压下,该反应每生成22.4L O ,转移电子的数目为4×6.02×1023个
2
2.科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的 转化为 进
入大气层,反应过程如图所示。下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的n(NO)︰n(NH)=1︰4
D.过程Ⅰ→Ⅲ的总反应为
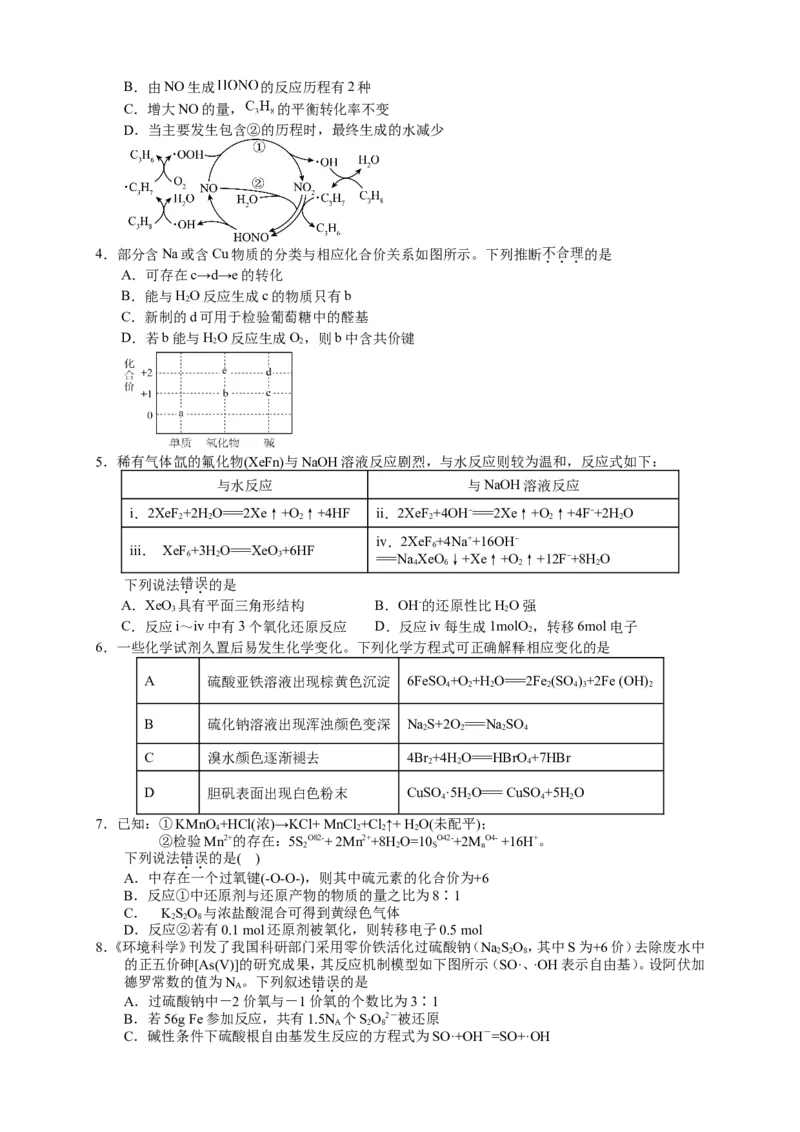
3.在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的是
A.含N分子参与的反应一定有电子转移B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
4.部分含Na或含Cu物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.可存在c→d→e的转化
B.能与HO反应生成c的物质只有b
2
C.新制的d可用于检验葡萄糖中的醛基
D.若b能与HO反应生成O,则b中含共价键
2 2
5.稀有气体氙的氟化物(XeFn)与NaOH溶液反应剧烈,与水反应则较为温和,反应式如下:
与水反应 与NaOH溶液反应
i.2XeF +2H O===2Xe↑+O↑+4HF ii.2XeF +4OH-===2Xe↑+O↑+4F-+2H O
2 2 2 2 2 2
iv.2XeF +4Na++16OH-
iii. XeF +3H O===XeO+6HF 6
6 2 3 ===NaXeO ↓+Xe↑+O↑+12F-+8H O
4 6 2 2
下列说法错误的是
A.XeO 具有平面三角形结构 B.OH-的还原性比HO强
3 2
C.反应i~iv中有3个氧化还原反应 D.反应iv每生成1molO ,转移6mol电子
2
6.一些化学试剂久置后易发生化学变化。下列化学方程式可正确解释相应变化的是
A 硫酸亚铁溶液出现棕黄色沉淀 6FeSO +O +H O===2Fe (SO )+2Fe (OH)
4 2 2 2 4 3 2
B 硫化钠溶液出现浑浊颜色变深 NaS+2O===NaSO
2 2 2 4
C 溴水颜色逐渐褪去 4Br +4H O===HBrO +7HBr
2 2 4
D 胆矾表面出现白色粉末 CuSO ·5H O=== CuSO +5H O
4 2 4 2
7.已知:①KMnO +HCl(浓)→KCl+ MnCl +Cl↑+ HO(未配平);
4 2 2 2
②检验Mn2+的存在:5SO82-+ 2Mn2++8H O=10 O42-+2MO4- +16H+。
2 2 S n
下列说法错误的是( )
A.中存在一个过氧键(-O-O-),则其中硫元素的化合价为+6
B.反应①中还原剂与还原产物的物质的量之比为8∶1
C. KSO 与浓盐酸混合可得到黄绿色气体
2 2 8
D.反应②若有0.1 mol还原剂被氧化,则转移电子0.5 mol
8.《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠(NaSO,其中S为+6价)去除废水中
2 2 8
的正五价砷[As(V)]的研究成果,其反应机制模型如下图所示(SO·、·OH表示自由基)。设阿伏加
德罗常数的值为N 。下列叙述错误的是
A
A.过硫酸钠中-2价氧与-1价氧的个数比为3∶1
B.若56g Fe参加反应,共有1.5N 个SO2-被还原
A 2 8
C.碱性条件下硫酸根自由基发生反应的方程式为SO·+OH-=SO+·OHD.pH越小,越不利于去除废水中的正五价砷
9.钴的化合物用途广泛,可用于指示剂和催化剂制备。
(1)以CoCl 溶液为原料,加入NH HCO 和氨水,控制温度为50~60℃制备CoCO,其反应的离
2 4 3 3
子方程式为 。
(2)钴有多种氧化物,其中Co O 可用作电极,若选用KOH电解质溶液,通电时可转化为
3 4
CoOOH,其电极反应式为 。
(3)加热CoCO 制备Co O 时有部分Co2+转化为Co3+。取1molCoCO 在空气中加热,反应温度对
3 3 4 3
反应产物的影响如下图所示。写出800℃时发生反应的化学方程式 。
1.1
CO
0.9 2
0.7
CoO
0.5
CoO 3 4
0.3
0.1
O2
CoCO
3
-0.1
0 200 400 600 800 1000
【课后作业】答案
1.B 2.D 3.D 4.B 5.A 6.D 7. B 8.B
9.(1)①Co2++NH·H O+ HCO=======CoCO↓+ NH + + H O
3 2 3 4 2
(2)Co O− e-+OH-+ HO=3CoOOH
3 4 2
(3)2Co O=====6CoO+O↑
3 4 2
物质的量
/
m o l
题17温图度 /℃ 温度/℃