文档内容
课时检测(四十九) 反应机理与能垒图像
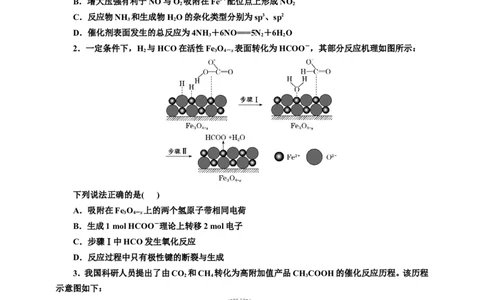
1.有氧条件下,在Fe基催化剂表面,NH 还原NO的反应机理如图所示。该反应能够有效脱除烟
3
气中的NO。下列说法正确的是( )
A.在酸性配位点上,NH 与H+通过离子键形成NH
3
B.增大压强有利于NO与O 吸附在Fe3+配位点上形成NO
2 2
C.反应物NH 和生成物HO的杂化类型分别为sp3、sp2
3 2
D.催化剂表面发生的总反应为4NH +6NO===5N +6HO
3 2 2
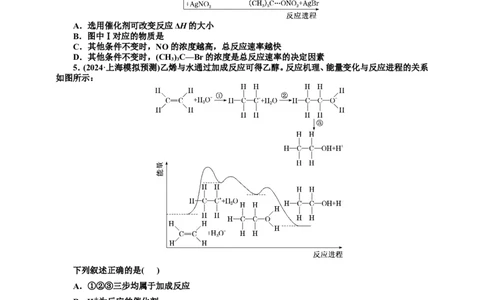
2.一定条件下,H 与HCO在活性FeO 表面转化为HCOO-,其部分反应机理如图所示:
2 3 4-x
下列说法正确的是( )
A.吸附在FeO 上的两个氢原子带相同电荷
3 4-x
B.生成1 mol HCOO-理论上转移2 mol电子
C.步骤Ⅰ中HCO发生氧化反应
D.反应过程中只有极性键的断裂与生成
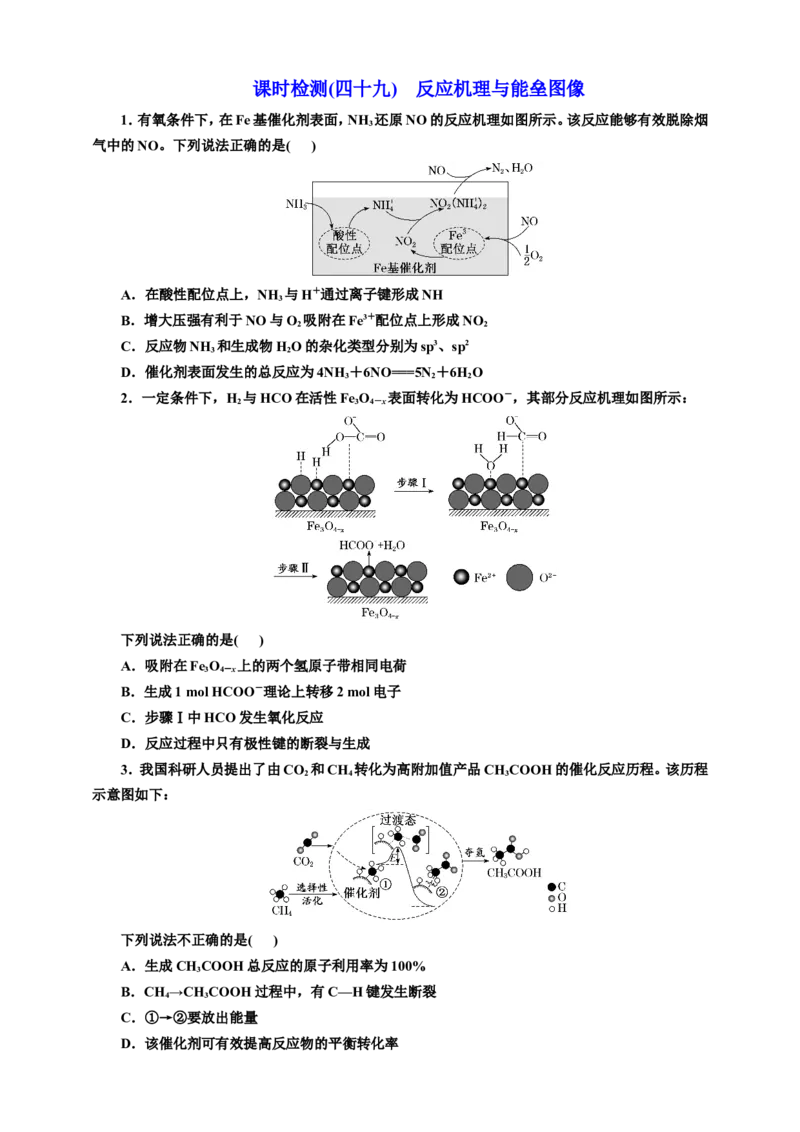
3.我国科研人员提出了由CO 和CH 转化为高附加值产品CH COOH的催化反应历程。该历程
2 4 3
示意图如下:
下列说法不正确的是( )
A.生成CH COOH总反应的原子利用率为100%
3
B.CH →CH COOH过程中,有C—H键发生断裂
4 3
C.①→②要放出能量
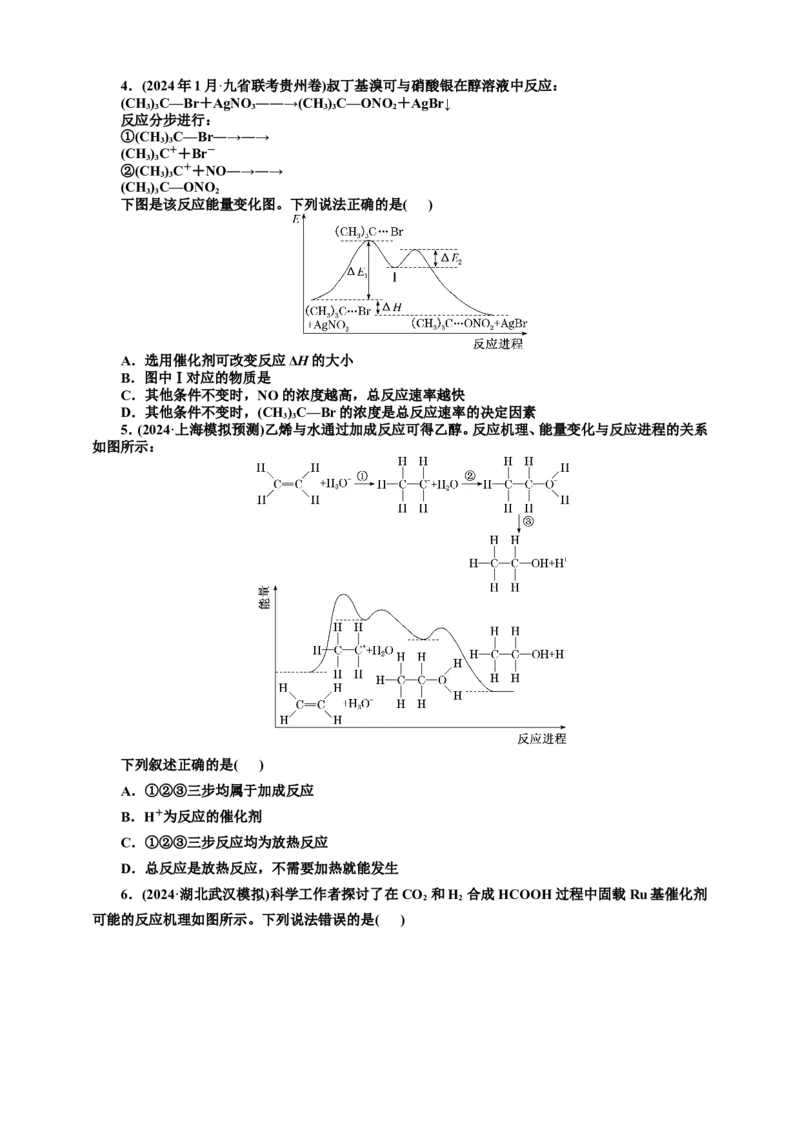
D.该催化剂可有效提高反应物的平衡转化率4.(2024年1月·九省联考贵州卷)叔丁基溴可与硝酸银在醇溶液中反应:
(CH)C—Br+AgNO ――→(CH)C—ONO +AgBr↓
3 3 3 3 3 2
反应分步进行:
①(CH)C—Br―→―→
3 3
(CH)C++Br-
3 3
②(CH)C++NO―→―→
3 3
(CH)C—ONO
3 3 2
下图是该反应能量变化图。下列说法正确的是( )
A.选用催化剂可改变反应ΔH的大小
B.图中Ⅰ对应的物质是
C.其他条件不变时,NO的浓度越高,总反应速率越快
D.其他条件不变时,(CH)C—Br的浓度是总反应速率的决定因素
3 3
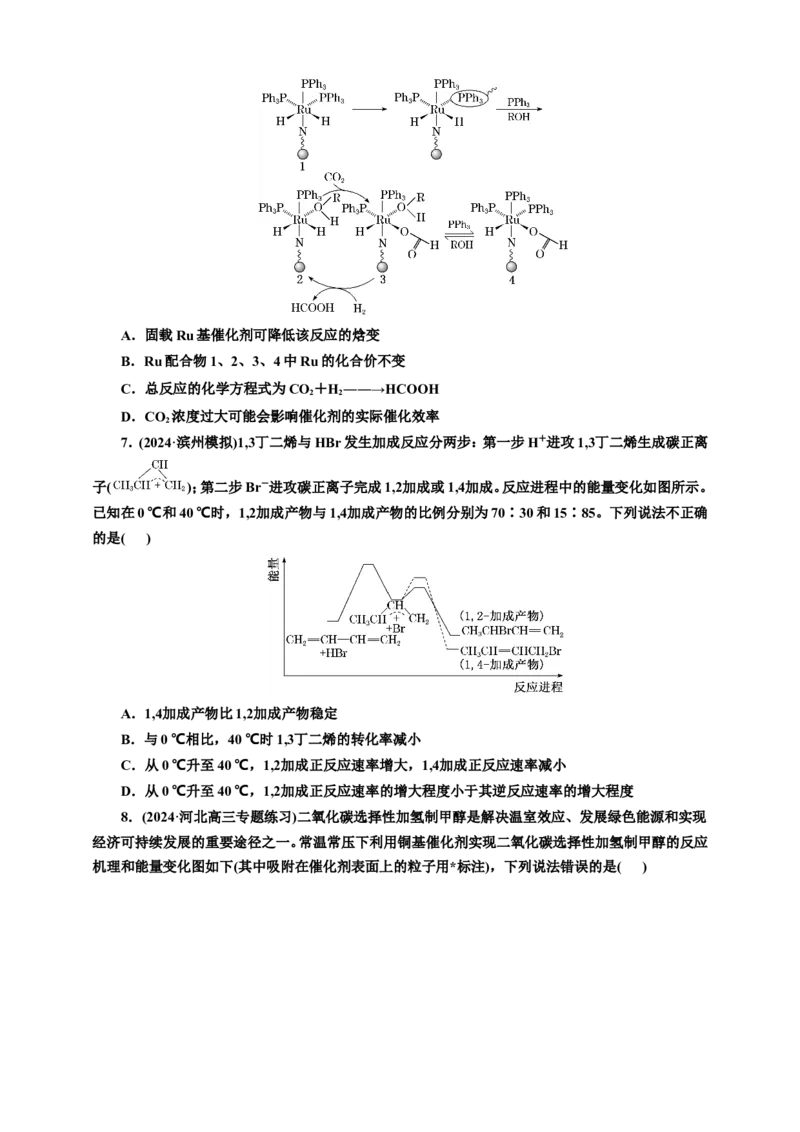
5.(2024·上海模拟预测)乙烯与水通过加成反应可得乙醇。反应机理、能量变化与反应进程的关系
如图所示:
下列叙述正确的是( )
A.①②③三步均属于加成反应
B.H+为反应的催化剂
C.①②③三步反应均为放热反应
D.总反应是放热反应,不需要加热就能发生
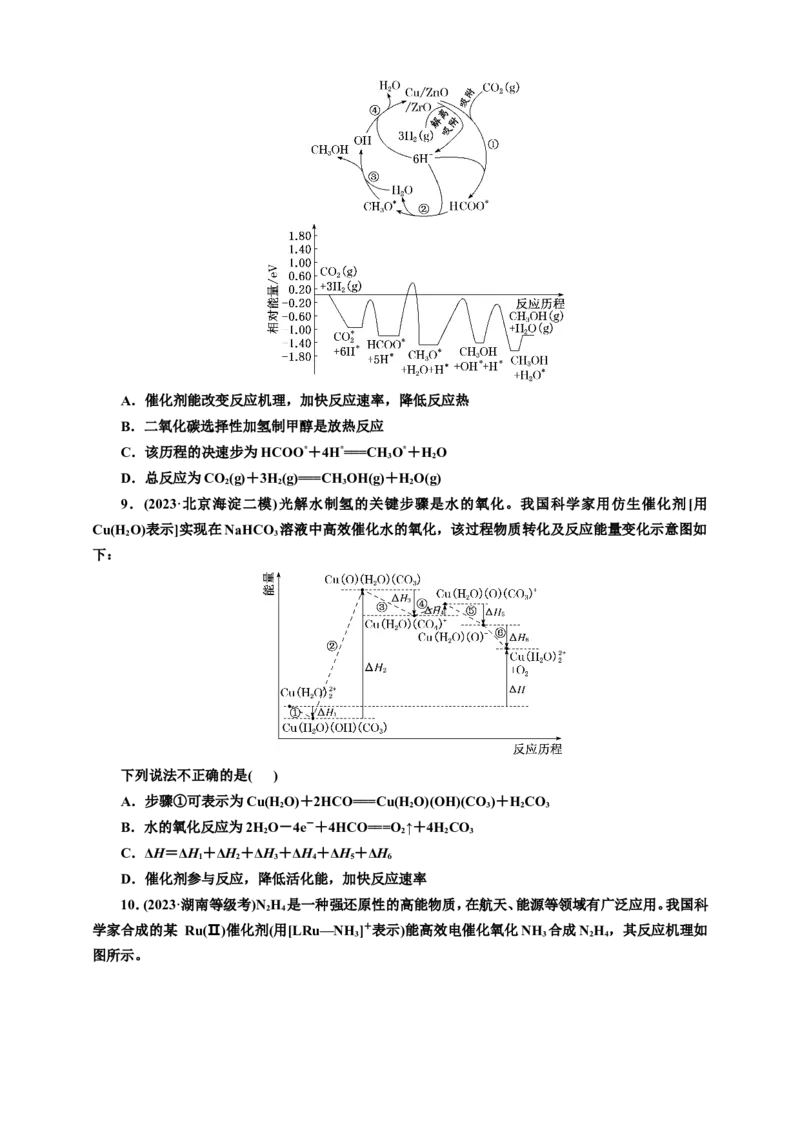
6.(2024·湖北武汉模拟)科学工作者探讨了在CO 和H 合成HCOOH过程中固载Ru基催化剂
2 2
可能的反应机理如图所示。下列说法错误的是( )A.固载Ru基催化剂可降低该反应的焓变
B.Ru配合物1、2、3、4中Ru的化合价不变
C.总反应的化学方程式为CO +H――→HCOOH
2 2
D.CO 浓度过大可能会影响催化剂的实际催化效率
2
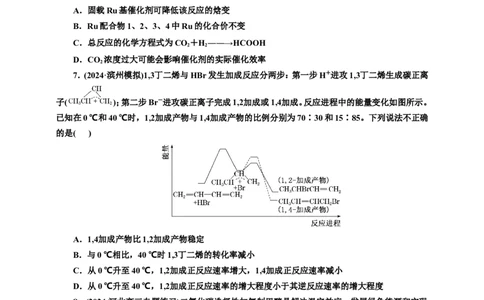
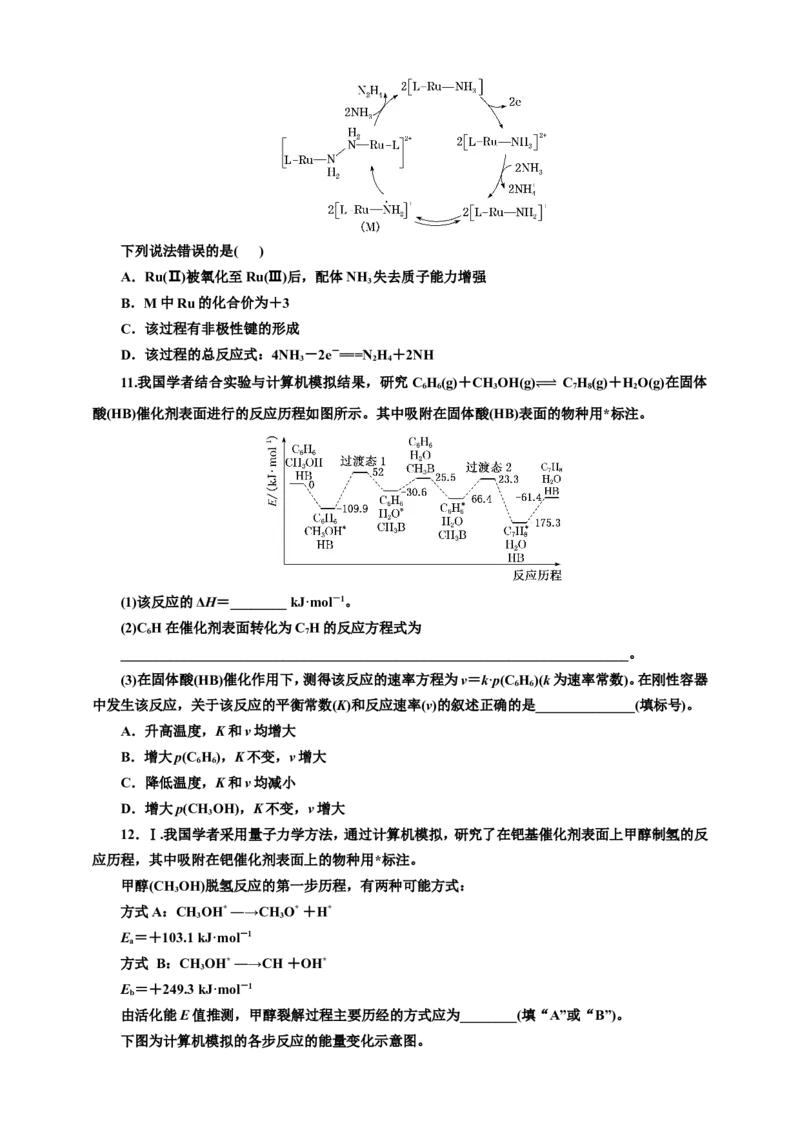
7.(2024·滨州模拟)1,3丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3丁二烯生成碳正离
子( );第二步Br-进攻碳正离子完成1,2加成或1,4加成。反应进程中的能量变化如图所示。
已知在0 ℃和40 ℃时,1,2加成产物与1,4加成产物的比例分别为70∶30和15∶85。下列说法不正确
的是( )
A.1,4加成产物比1,2加成产物稳定
B.与0 ℃相比,40 ℃时1,3丁二烯的转化率减小
C.从0 ℃升至40 ℃,1,2加成正反应速率增大,1,4加成正反应速率减小
D.从0 ℃升至40 ℃,1,2加成正反应速率的增大程度小于其逆反应速率的增大程度
8.(2024·河北高三专题练习)二氧化碳选择性加氢制甲醇是解决温室效应、发展绿色能源和实现
经济可持续发展的重要途径之一。常温常压下利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应
机理和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注),下列说法错误的是( )A.催化剂能改变反应机理,加快反应速率,降低反应热
B.二氧化碳选择性加氢制甲醇是放热反应
C.该历程的决速步为HCOO*+4H*===CHO*+HO
3 2
D.总反应为CO (g)+3H(g)===CHOH(g)+HO(g)
2 2 3 2
9.(2023·北京海淀二模)光解水制氢的关键步骤是水的氧化。我国科学家用仿生催化剂[用
Cu(H O)表示]实现在NaHCO 溶液中高效催化水的氧化,该过程物质转化及反应能量变化示意图如
2 3
下:
下列说法不正确的是( )
A.步骤①可表示为Cu(H O)+2HCO===Cu(H O)(OH)(CO )+HCO
2 2 3 2 3
B.水的氧化反应为2HO-4e-+4HCO===O ↑+4HCO
2 2 2 3
C.ΔH=ΔH+ΔH+ΔH+ΔH+ΔH+ΔH
1 2 3 4 5 6
D.催化剂参与反应,降低活化能,加快反应速率
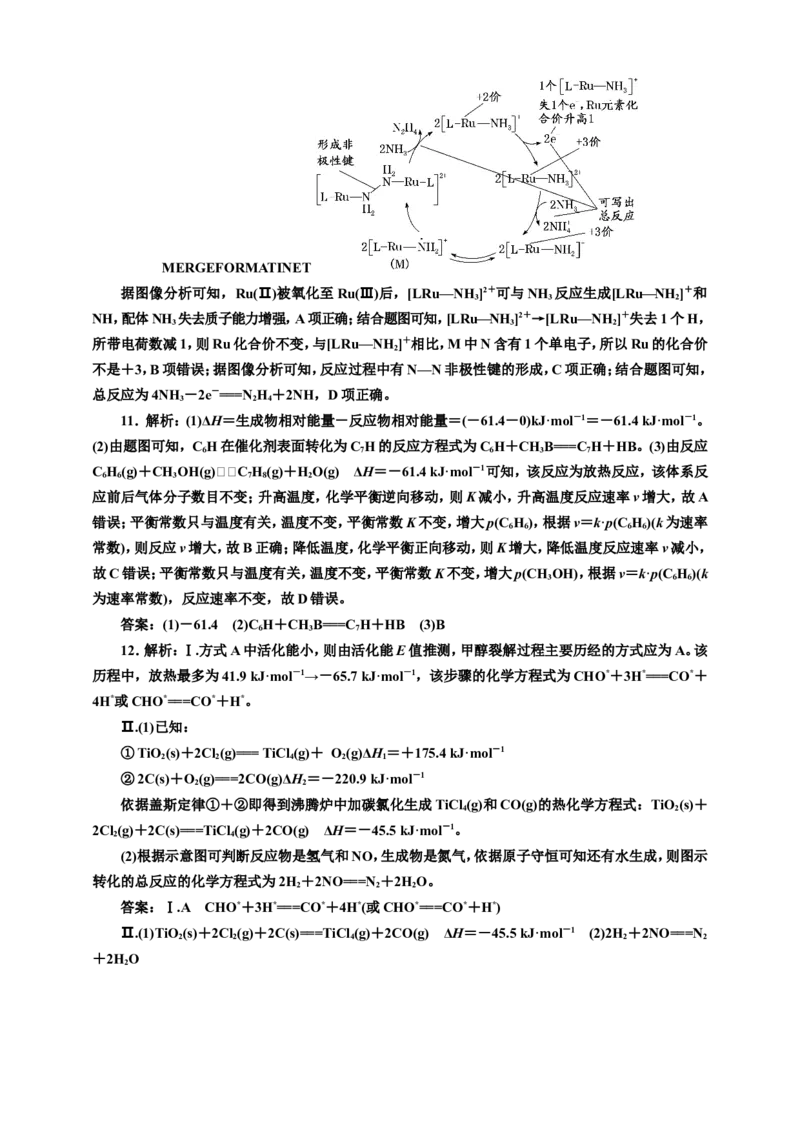
10.(2023·湖南等级考)N H 是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科
2 4
学家合成的某 Ru(Ⅱ)催化剂(用[LRu—NH ]+表示)能高效电催化氧化NH 合成NH ,其反应机理如
3 3 2 4
图所示。下列说法错误的是( )
A.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH 失去质子能力增强
3
B.M中Ru的化合价为+3
C.该过程有非极性键的形成
D.该过程的总反应式:4NH -2e-===N H+2NH
3 2 4
11.我国学者结合实验与计算机模拟结果,研究 CH(g)+CH OH(g) CH(g)+HO(g)在固体
6 6 3 7 8 2
酸(HB)催化剂表面进行的反应历程如图所示。其中吸附在固体酸(HB)表面⥫⥬的物种用*标注。
(1)该反应的ΔH=________ kJ·mol-1。
(2)C H在催化剂表面转化为CH的反应方程式为
6 7
________________________________________________________________________。
(3)在固体酸(HB)催化作用下,测得该反应的速率方程为v=k·p(C H)(k为速率常数)。在刚性容器
6 6
中发生该反应,关于该反应的平衡常数(K)和反应速率(v)的叙述正确的是______________(填标号)。
A.升高温度,K和v均增大
B.增大p(C H),K不变,v增大
6 6
C.降低温度,K和v均减小
D.增大p(CHOH),K不变,v增大
3
12.Ⅰ.我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反
应历程,其中吸附在钯催化剂表面上的物种用*标注。
甲醇(CHOH)脱氢反应的第一步历程,有两种可能方式:
3
方式A:CH OH* ―→CH O* +H*
3 3
E =+103.1 kJ·mol-1
a
方式 B:CH OH* ―→CH +OH*
3
E =+249.3 kJ·mol-1
b
由活化能E值推测,甲醇裂解过程主要历经的方式应为________(填“A”或“B”)。
下图为计算机模拟的各步反应的能量变化示意图。该历程中,放热最多的步骤的化学方程式为_________________________________
________________________________________________________________________。
Ⅱ.TiCl 是由钛精矿(主要成分为TiO)制备钛(Ti)的重要中间产物,制备纯TiCl 的流程示意图如
4 2 4
下:
氯化过程:TiO 与Cl 难以直接反应,加碳生成CO和CO 可使反应得以进行。
2 2 2
已知:TiO(s)+2Cl (g)=== TiCl(g)+ O(g)ΔH=+175.4 kJ·mol-1
2 2 4 2 1
2C(s)+O(g)===2CO(g)ΔH=-220.9 kJ·mol-1
2 2
(1) 沸 腾 炉 中 加 碳 氯 化 生 成 TiCl(g) 和 CO(g) 的 热 化 学 方 程 式 为
4
________________________________________________________________________
________________________________________________________________________。
(2)
工业上处理尾气中NO的方法为将NO与H 的混合气体通入Ce(SO ) 与Ce(SO ) 的混合溶液中,
2 4 2 2 4 3
其物质转化如图所示。写出图示转化的总反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
课时检测(四十九)
1.B 在酸性配位点上,NH 提供孤电子对,H+提供空轨道,二者通过配位键形成NH,A错误;增
3
大压强能增大微粒间的作用力,有利于NO与O 吸附在Fe3+配位点上,发生化合反应形成NO ,B正
2 2
确;反应物NH 和生成物HO的中心原子N、O的价层电子对数都为4,杂化类型都为sp3,C错误;从
3 2
图中可以看出,反应物为NH 、NO、O,生成物为N、HO,则在催化剂表面发生的总反应为4NH +
3 2 2 2 3
4NO+O===4N +6HO,D错误。
2 2 2
2.B 由题图可知,吸附在FeO 上的两个氢原子分别与Fe2+、O2-结合,故带不同电荷,A错误;
3 4-x
反应中HCO转化为HCOO-,根据碳元素化合价变化可知,生成1 mol HCOO-理论上转移电子2 mol,B
正确;步骤Ⅰ中HCO失去氧,发生还原反应,C错误;反应过程中H 和HCO转化为HCOO-和HO,
2 2
存在氢氢键、氢氧键、碳氧键的断裂和氢氧键、碳氢键的生成,D错误。3.D A项,生成CH COOH的总反应为CH +CO ――→CH COOH,原子利用率为100%;B
3 4 2 3
项,CH 选择性活化变为①过程中,有1个C—H键发生断裂;C项,根据图示,①的总能量高于②的总
4
能量,①→②放出能量;D项,催化剂只影响化学反应速率,不影响化学平衡,不能提高平衡转化率。
4.D 催化剂可以通过改变活化能来改变化学反应速率,对ΔH无影响,A错误;由题中反应分步
进行的式子可知,Ⅰ对应的物质是(CH)C+,B错误;总反应速率主要由活化能最大的步骤决定,即
3 3
(CH)C—Br―→,其他条件不变时,NO的浓度越高,反应②速率越快,但对总反应速率的影响不大,
3 3
C错误;由C可知,(CH)C—Br的浓度越大,该步骤反应速率越快,总反应速率越快,D正确。
3 3
5.B 不饱和碳原子与其他原子直接结合形成新的化合物为加成反应,反应①②为加成反应,故
A项错误;反应前加入H+,反应后又产生了H+,所以H+为催化剂,B项正确;反应①中反应物能量低
于生成物,该反应为吸热反应,②③反应的反应物能量均高于生成物的能量,这两步反应均为放热反
应,C项错误;对于总反应,反应物的总能量高于生成物的总能量,反应为放热反应,但反应是否加热
与反应热无关,D项错误。
6.A 催化剂降低反应活化能,不影响反应的焓变,故A错误;Ru配合物1、2、3、4中Ru所连的
键没有变化,所以Ru的化合价不变,故B正确;在有Ru基催化剂存在的条件下,CO 与H 合成
2 2
HCOOH,根据原子守恒,发生的反应为CO +H 催化剂,HCOOH,故C正确;CO 浓度过大将减小催
2 2 2
化剂与H 之间的接触,从而影响催化剂的实际催化效率,故D正确。
2
7.C 结合图像可知,1,4加成产物的能量比1,2加成产物的能量低,即1,4加成产物比1,2加成产物
稳定,A正确;从题图可以看出反应物比2种产物能量都高,属于放热反应,0 ℃→40 ℃升高温度,平
衡向逆反应方向移动,1,3丁二烯的转化率降低,B正确;温度升高,1,2加成反应和1,4加成反应的正反
应速率均加快,C错误;由0 ℃升温至40 ℃时,1,3丁二烯发生的反应由以1,2加成为主变为以1,4加成
为主,即1,2加成正反应速率的增大程度小于其逆反应速率的增大程度,D正确。
8.A 催化剂能改变反应机理,加快反应速率,不能改变反应热,A错误;由反应历程图可知反应
物的总能量大于生成物的总能量,该反应为放热反应,B正确;HCOO*+4H*===CHO*+HO的活化
3 2
能最大,是该历程的决速步,C正确;该反应的反应物是CO 和H,生成物是CH OH和HO,则总反
2 2 3 2
应为CO (g)+3H(g)===CHOH(g)+HO(g),D正确。
2 2 3 2
9.A 若步骤①表示为Cu(H O)+2HCO===Cu(H O)(OH)(CO )+HCO ,则H原子不守恒,A
2 2 3 2 3
错误;由题干图示信息可知,水的氧化反应(总反应)方程式为2HO-4e-+4HCO===O ↑+4HCO ,B
2 2 2 3
正确;根据盖斯定律结合题干图示信息可知,ΔH=ΔH+ΔH+ΔH+ΔH+ΔH+ΔH,C正确;根据
1 2 3 4 5 6
碰撞理论可知,催化剂参与反应,通过降低活化能,提高活化分子百分含量,从而加快反应速率,D正
确。
10.B 依题意分析:
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\4\\24HXGKTHB-50.TIF" \*MERGEFORMATINET
据图像分析可知,Ru(Ⅱ)被氧化至Ru(Ⅲ)后,[LRu—NH ]2+可与NH 反应生成[LRu—NH]+和
3 3 2
NH,配体NH 失去质子能力增强,A项正确;结合题图可知,[LRu—NH]2+→[LRu—NH ]+失去1个H,
3 3 2
所带电荷数减1,则Ru化合价不变,与[LRu—NH ]+相比,M中N含有1个单电子,所以Ru的化合价
2
不是+3,B项错误;据图像分析可知,反应过程中有N—N非极性键的形成,C项正确;结合题图可知,
总反应为4NH -2e-===N H+2NH,D项正确。
3 2 4
11.解析:(1)ΔH=生成物相对能量-反应物相对能量=(-61.4-0)kJ·mol-1=-61.4 kJ·mol-1。
(2)由题图可知,CH在催化剂表面转化为CH的反应方程式为CH+CH B===C H+HB。(3)由反应
6 7 6 3 7
CH(g)+CH OH(g)CH(g)+HO(g) ΔH=-61.4 kJ·mol-1可知,该反应为放热反应,该体系反
6 6 3 7 8 2
应前后气体分子数目不变;升高温度,化学平衡逆向移动,则K减小,升高温度反应速率v增大,故A
错误;平衡常数只与温度有关,温度不变,平衡常数K不变,增大p(C H),根据v=k·p(C H)(k为速率
6 6 6 6
常数),则反应v增大,故B正确;降低温度,化学平衡正向移动,则K增大,降低温度反应速率v减小,
故C错误;平衡常数只与温度有关,温度不变,平衡常数K不变,增大p(CHOH),根据v=k·p(C H)(k
3 6 6
为速率常数),反应速率不变,故D错误。
答案:(1)-61.4 (2)C H+CH B===C H+HB (3)B
6 3 7
12.解析:Ⅰ.方式A中活化能小,则由活化能E值推测,甲醇裂解过程主要历经的方式应为A。该
历程中,放热最多为41.9 kJ·mol-1→-65.7 kJ·mol-1,该步骤的化学方程式为CHO*+3H*===CO*+
4H*或CHO*===CO*+H*。
Ⅱ.(1)已知:
①TiO(s)+2Cl (g)=== TiCl(g)+ O(g)ΔH=+175.4 kJ·mol-1
2 2 4 2 1
②2C(s)+O(g)===2CO(g)ΔH=-220.9 kJ·mol-1
2 2
依据盖斯定律①+②即得到沸腾炉中加碳氯化生成TiCl(g)和CO(g)的热化学方程式:TiO(s)+
4 2
2Cl (g)+2C(s)===TiCl (g)+2CO(g) ΔH=-45.5 kJ·mol-1。
2 4
(2)根据示意图可判断反应物是氢气和NO,生成物是氮气,依据原子守恒可知还有水生成,则图示
转化的总反应的化学方程式为2H+2NO===N +2HO。
2 2 2
答案:Ⅰ.A CHO*+3H*===CO*+4H*(或CHO*===CO*+H*)
Ⅱ.(1)TiO (s)+2Cl (g)+2C(s)===TiCl (g)+2CO(g) ΔH=-45.5 kJ·mol-1 (2)2H +2NO===N
2 2 4 2 2
+2HO
2