文档内容
反应热&盖斯定律作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-5,7-8,10-15 题为三星,6,9,16 为四星。
1.下列关于化学变化的说法中,错误的是( ) ☆☆☆
A.化学键断裂时要吸收能量,形成新化学键时要放出能量
B.化学变化的实质是旧化学键断裂,新化学键形成
C.在化学变化过程中,一定要吸收或放出能量
D.吸收能量或放出能量的过程,一定是化学变化过程
【解答】
A、化学键是相邻原子间强烈的相互作用,破坏时要吸收能量,形成化学键要放
出能量,故 A 正确;
B、在化学变化中,分子分解成原子,原子再重新结合成新分子,分子变成原子
时化学键断裂,原子形成分子时化学键形成,所以化学反应中物质变化的实质是
旧化学键的断裂和新化学键的形成,故 B 正确;
C、化学变化一定存在能量的变化,在化学变化过程中,一定要吸收或放出能量,
故 C 正确;
D、物理变化也可能伴随能量变化,例如冰变成水要吸热,水蒸气冷凝成水会放
热,故 D 错误。
故选:D.
2.下列说法中错误的是( ) ☆☆☆
A.化学反应中的能量变化通常表现为热量的变化
第 1页(共 11页)B.需要加热才能发生的反应一定是吸热反应
C.化学键的断裂和形成是化学反应中能量变化的主要原因
D.反应物总能量和生成物总能量的相对大小决定了反应是放热还是吸热
【解答】
A、化学反应中的能量变化通常表现为热量的变化,有时以热能、光能、电能等
形式转化,故 A 正确;
B、需要加热才能发生的反应可能是放热反应,也可能为吸热反应,加热只是反
应的条件,故 B 错误;
C、化学键断裂需要吸收能量,化学键的形成需要释放能量,化学反应中一定存
在旧键断裂、新键形成,故 C 正确;
D、反应物总能量和生成物总能量的相对大小决定了反应是放热还是吸热,故 D
正确。
故选 B.
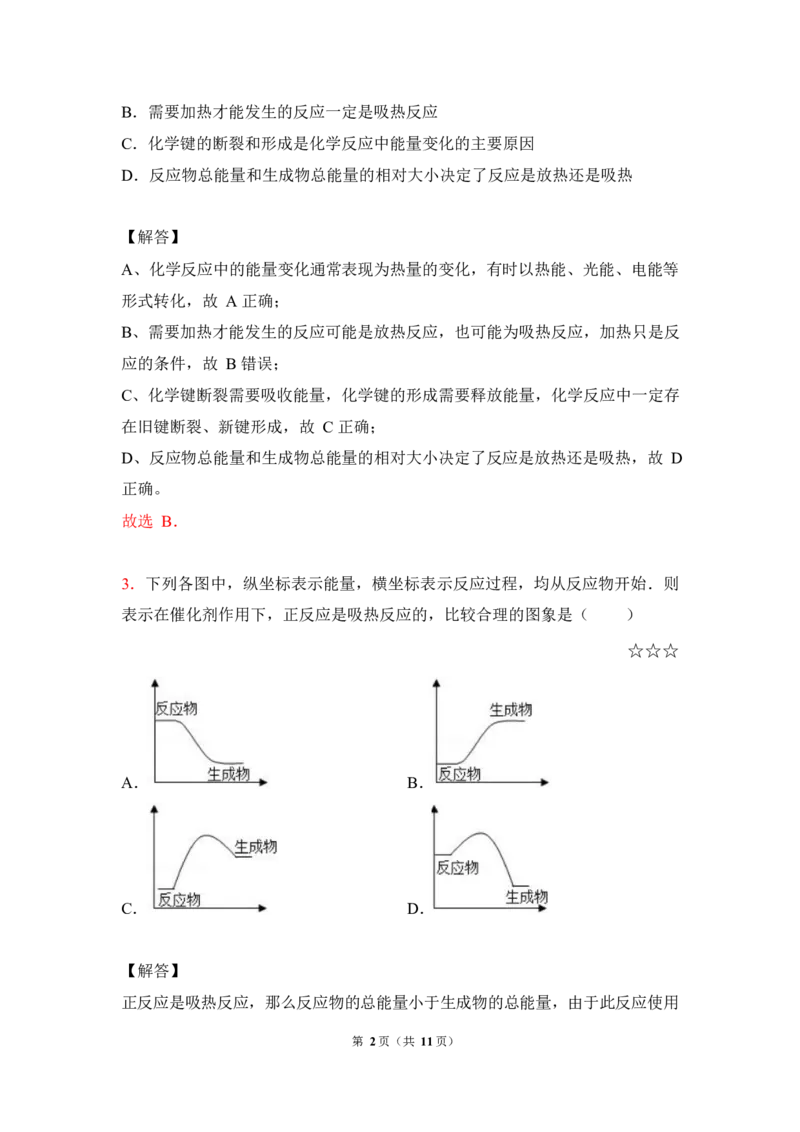
3.下列各图中,纵坐标表示能量,横坐标表示反应过程,均从反应物开始.则
表示在催化剂作用下,正反应是吸热反应的,比较合理的图象是( )
☆☆☆
A. B.
C. D.
【解答】
正反应是吸热反应,那么反应物的总能量小于生成物的总能量,由于此反应使用
第 2页(共 11页)了催化剂,故由反应物变成生成物,反应物先被活化,故 C 符合题意。
故选 C.
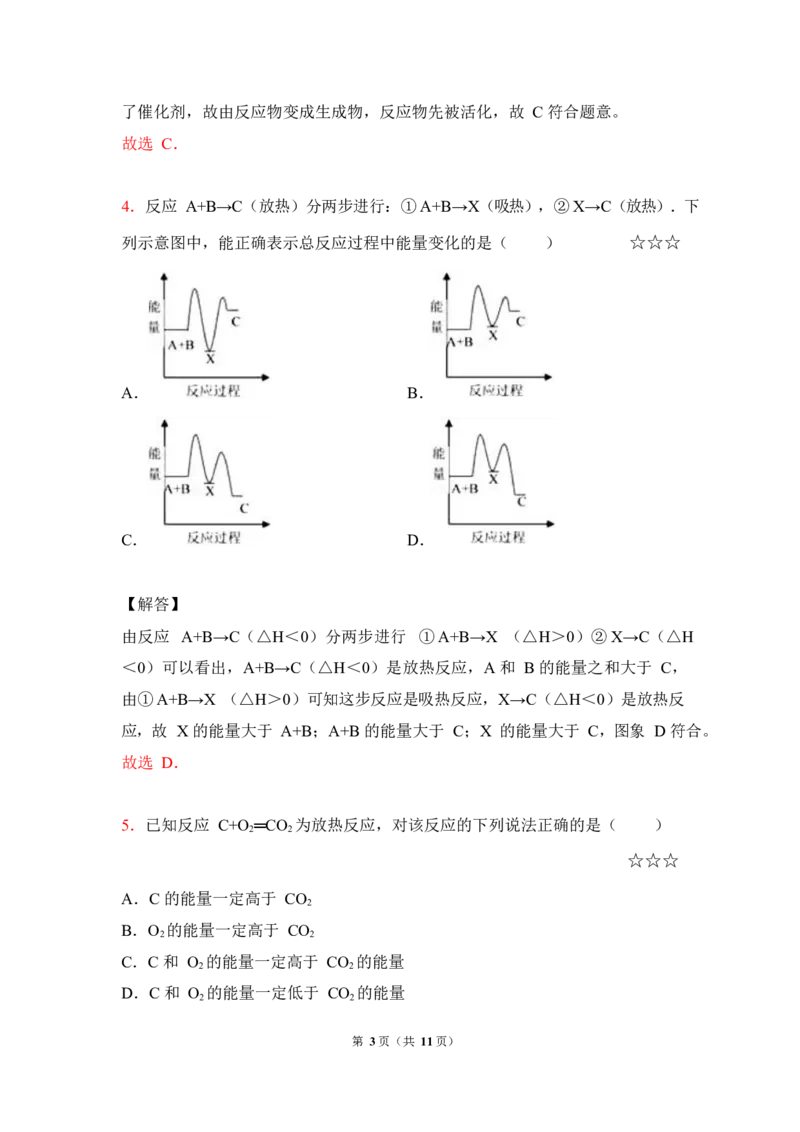
4.反应 A+B→C(放热)分两步进行:①A+B→X(吸热),②X→C(放热).下
列示意图中,能正确表示总反应过程中能量变化的是( ) ☆☆☆
A. B.
C. D.
【解答】
由反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H
<0)可以看出,A+B→C(△H<0)是放热反应,A 和 B 的能量之和大于 C,
由①A+B→X (△H>0)可知这步反应是吸热反应,X→C(△H<0)是放热反
应,故 X 的能量大于 A+B;A+B 的能量大于 C;X 的能量大于 C,图象 D 符合。
故选 D.
5.已知反应 C+O ═CO 为放热反应,对该反应的下列说法正确的是( )
2 2
☆☆☆
A.C 的能量一定高于 CO
2
B.O 的能量一定高于 CO
2 2
C.C 和 O 的能量一定高于 CO 的能量
2 2
D.C 和 O 的能量一定低于 CO 的能量
2 2
第 3页(共 11页)【解答】
因反应 C+O ═CO 为放热反应,所以 C 和 O 的能量和一定高于 CO 的能量,但
2 2 2 2
不能用某一个反应物和某一个生成物能量进行对比,故 C 选项正确。
故选 C.
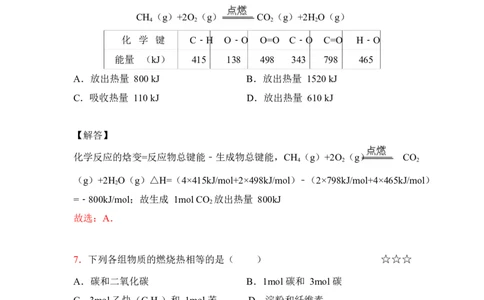
6.下表中的数据表示破坏 1mol 化学键需消耗的能量:根据下表数据计算以下反
应生成 1mol CO 时的热量变化( ) ☆☆☆☆
2
CH (g)+2O (g) CO (g)+2H O(g)
4 2 2 2
化 学 键 C﹣H O﹣O O=O C﹣O C=O H﹣O
能量 (kJ) 415 138 498 343 798 465
A.放出热量 800 kJ B.放出热量 1520 kJ
C.吸收热量 110 kJ D.放出热量 610 kJ
【解答】
化学反应的焓变=反应物总键能﹣生成物总键能,CH (g)+2O (g) CO
4 2 2
(g)+2H O(g)△H=(4×415kJ/mol+2×498kJ/mol)﹣(2×798kJ/mol+4×465kJ/mol)
2
=﹣800kJ/mol;故生成 1mol CO 放出热量 800kJ
2
故选:A.
7.下列各组物质的燃烧热相等的是( ) ☆☆☆
A.碳和二氧化碳 B.1mol 碳和 3mol 碳
C.3mol 乙炔(C H )和 1mol 苯 D.淀粉和纤维素
2 2
【解答】
燃烧热是指 1 mol 物质完全燃烧生成稳定氧化物时所放出的热量,只与物质种类
有关,与量的多少无关,故同一种物质燃烧热相同;
故选:B.
第 4页(共 11页)8.下列热化学方程式中△H 代表燃烧热的是( ) ☆☆☆
A.CH ( g )+ O ( g )═2H O ( l )+CO ( g )△H
4 2 2 1
B.S ( s )+ O ( g )═SO ( s )△H
2 3 2
C.C H O ( s )+6O ( g )═6CO (g)+6H O ( l )△H
6 12 6 2 2 2 3
D.2CO ( g )+O ( g )═2CO ( g )△H
2 2 4
【解答】
A.反应物中碳元素应生成 CO ,故 A 错误;
2
B.硫燃烧生成二氧化硫,不符合实际,故 B 错误;
C.可燃物 C H O (s)的物质的量是 1 mol,反应中 C→CO ,H→H O(液),
6 12 6 2 2
反应放出的热量是燃烧热,故 C 正确;
D.CO 的化学计量数应为 1,故 D 错误。
故选:C.
9.已知 H 的燃烧热是 akJ/mol,由 H 、CO 按 3:1 比例组成的混合物 2mol,
2 2
完全燃烧并恢复到常温吋,放出的热量为 bkJ,则 CO 的燃烧热为(kJ/mol)为
( ) ☆☆☆☆
A.2b﹣3a B.3a﹣2b C. (2b﹣3a) D. (a﹣2b)
【解答】
设 CO 的燃烧热为 x kJ•mol﹣1,又 H 的燃烧热是 a kJ/mol,所以由 H 、CO 按 3:
2 2
1 比例组成的混合物 2mol,完全燃烧并恢复到常温吋,放出的热量为 bkJ,可得
2× ×a+2× ×x=b,则解得 x=2b﹣3a
故选:A.
10.下列关于中和热的说法中正确的是( ) ☆☆☆
A.10 L 0.05 mol•L﹣1 Ba(OH) 溶液与 20 L 0.05 mol•L﹣1 HNO 反应时的反应热
2 3
是中和热
第 5页(共 11页)B.1 mol HCl 气体通入 1 L 0.01 mol•L﹣1 NaOH 溶液中反应时的反应热是中和热
C.1 mol HClO 与 2 mol NaOH 溶液反应时的反应热也可能是中和热
D.只要强酸与强碱在稀溶液中反应生成 1 mol 水时的反应热就是中和热
【解答】
A.10 L 0.05 mol•L﹣1Ba(OH) 溶液与 20 L 0.05 mol•L﹣1 HNO 反应生成 1mol
2 3
水,放出的热量就是中和热,故 A 正确;
B.1 mol HCl 气体通入 1 L 0.01 mol•L﹣1 NaOH 溶液中反应的热效应除了中和热
外还有 HCl 气体的溶解热和电离热效应,故 B 错误;
C.HClO 为弱酸,电离时需要吸收热量,所以 1 mol HClO 与 2 mol NaOH 溶液
反应时的反应热不是中和热,故 C 错误;
D.如果是硫酸与氢氧化钡反应,它们反应除生成水外还会生成硫酸钡沉淀,放
出更多热量,故 D 错误。
故选:A.
11.强酸和强碱的稀溶液中和热可表示为:H
+
(aq)+OH﹣(aq)═H
2
O(l)
H=﹣57.3kJ/mol 以下 4 个热化学方程式中,其中反应热为 57.3kJ/mol 的是
( )
△
☆☆☆
①H SO (aq)+2NaOH(aq)=Na SO (aq)+2H O(l)
2 4 2 4 2
②H SO (aq)+Ba(OH) (aq)=BaSO (s)+2H O(l)
2 4 2 4 2
③NH •H O(aq)+HCl(aq)=NH Cl(aq)+H O(l)
3 2 4 2
④NH •H O(aq)+CH COOH(aq)=CH COONH (aq)+H O(l)
3 2 3 3 4 2
A.①② B.③ C.④ D.均不符合
【解答】
①H SO (aq)+2NaOH(aq)=Na SO (aq)+2H O(l)反应是稀硫酸和氢氧化
2 4 2 4 2
钠溶液反应生成 2mol 水,放热 114.6KJ,故①不符合;
②H SO (aq)+Ba(OH) (aq)=BaSO (s)+2H O(l)反应是稀硫酸和氢氧
2 4 2 4 2
第 6页(共 11页)化钡反应生成硫酸钡沉淀放热,生成 2mol 水反应放热大于 114.6KJ,故②不符
合;
③NH •H O(aq)+HCl(aq)=NH Cl(aq)+H O(l)反应是弱碱和强酸反应生
3 2 4 2
成 1mol 水,弱电解质电离吸热,所以反应放热小于 57.3kJ,故③不符合;
④NH •H O(aq)+CH COOH(aq)=CH COONH (aq)+H O(l)反应是弱酸
3 2 3 3 4 2
和弱碱反应生成 1mol 水,弱电解质电离是吸热过程,反应放热小于 57.3kJ,故
④不符合。
故选 D.
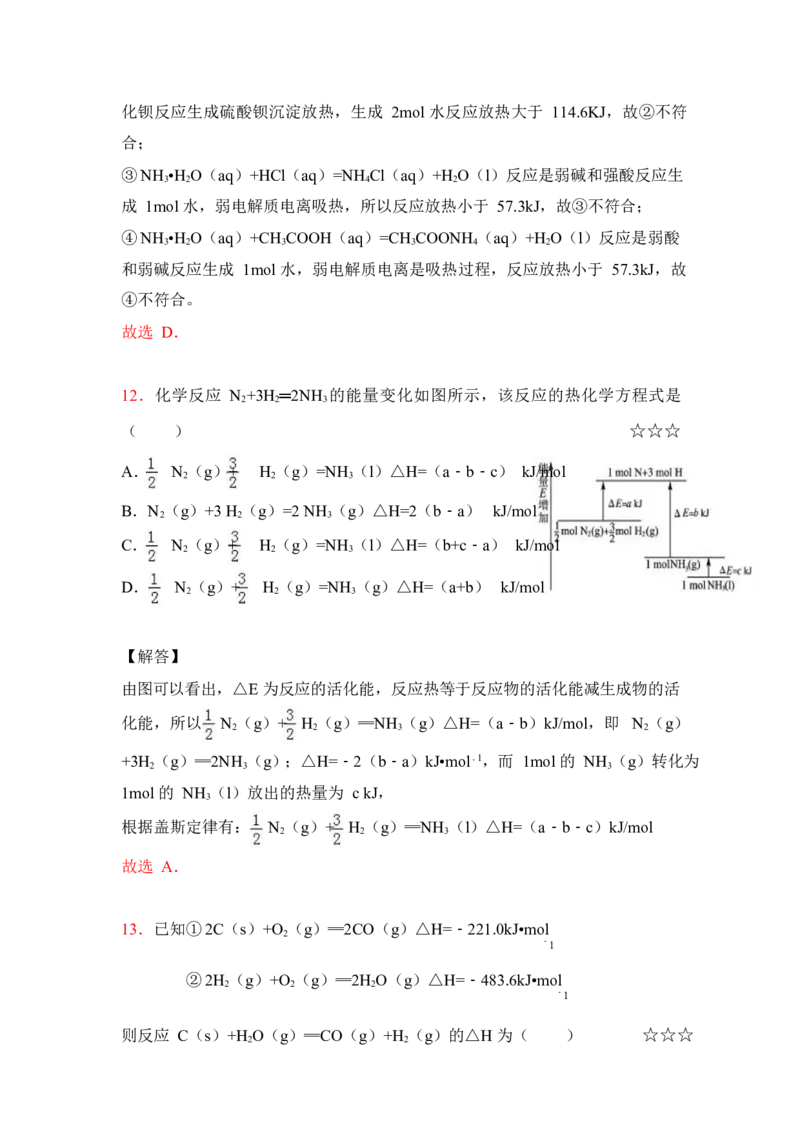
12.化学反应 N +3H ═2NH 的能量变化如图所示,该反应的热化学方程式是
2 2 3
( ) ☆☆☆
A. N (g)+ H (g)=NH (l)△H=(a﹣b﹣c) kJ/mol
2 2 3
B.N (g)+3 H (g)=2 NH (g)△H=2(b﹣a) kJ/mol
2 2 3
C. N (g)+ H (g)=NH (l)△H=(b+c﹣a) kJ/mol
2 2 3
D. N (g)+ H (g)=NH (g)△H=(a+b) kJ/mol
2 2 3
【解答】
由图可以看出,△E 为反应的活化能,反应热等于反应物的活化能减生成物的活
化能,所以 N (g)+ H (g)═NH (g)△H=(a﹣b)kJ/mol,即 N (g)
2 2 3 2
+3H (g)═2NH (g);△H=﹣2(b﹣a)kJ•mol﹣1,而 1mol 的 NH (g)转化为
2 3 3
1mol 的 NH (l)放出的热量为 c kJ,
3
根据盖斯定律有: N (g)+ H (g)═NH (l)△H=(a﹣b﹣c)kJ/mol
2 2 3
故选 A.
13.已知①2C(s)+O (g)═2CO(g)△H=﹣221.0kJ•mol
2
﹣1
②2H (g)+O (g)═2H O(g)△H=﹣483.6kJ•mol
2 2 2
﹣1
则反应 C(s)+H O(g)═CO(g)+H (g)的△H 为( ) ☆☆☆
2 2第 7页(共 11页)A.+131.3kJ•mol﹣1 B.﹣131.3kJ•mol﹣1
C.﹣352.3kJ•mol﹣1 D.+262.6kJ•mol﹣1
【解答】
①2C(s)+O (g)═2CO(g);△H=﹣221.0KJ/mol
2
②2H (g)+O (g)═2H O;△H=﹣483.6KJ/mol
2 2 2
依据盖斯定律 得到 C(s)+H O(g)═CO(g)+H (g)△H=+131.3KJ/mol
2 2
故选 A.
14.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO (s)+3C(s)═K S(s)+N (g)+3CO (g)△H=x kJ•mol
3 2 2 2
﹣1
碳的燃烧热△H =a kJ•mol
1
﹣1
S(s)+2K(s)═K
2
S(s)△H
2
=b kJ•mol﹣1
2K(s)+N
2
(g)+3O
2
(g)═2KNO
3
(s)△H
3
=c kJ•mol﹣1
则 x 为( ) ☆☆☆
A.3a+b﹣c B.c+3a﹣b C.a+b﹣c D.c+a﹣b
【解答】
碳的燃烧热△H =a kJ•mol﹣1,其热化学方程式为 C(s)+O (g)=CO (g)△
1 2 2
H
1
=a kJ•mol﹣1 ①
S(s)+2K(s)═K
2
S(s)△H
2
=b kJ•mol﹣1 ②
2K(s)+N
2
(g)+3O
2
(g)═2KNO
3
(s)△H
3
=c kJ•mol﹣1 ③
将方程式 3①+②﹣③得 S(s)+2KNO (s)+3C(s)═K S(s)+N (g)+3CO
3 2 2 2
(g),则△H=x kJ•mol﹣1=(3a+b﹣c)kJ•mol﹣1,所以 x=3a+b﹣c
故选 A.
15.已知:
①C(s)、H (g)的燃烧热分别是 393.5kJ•mol﹣1 、285.8kJ•mol
2
﹣1②CH COOH(l)+2O (g)═2CO (g)+2H O (g)△H =﹣782.3kJ•mol
3 2 2 2 1
﹣1
第 8页(共 11页)③H O(l)═H O (g)△H =+44.0kJ•mol﹣1 .
2 2 2
则反应:2C(s)+2H (g)+O (g)═CH COOH(l)的反应热△H 为( )
2 2 3
☆☆☆
A.﹣576.3kJ•mol﹣1 B.﹣532.3kJ•mol
﹣1
C.﹣488.3kJ•mol﹣1 D.﹣244.15kJ•mol
﹣1
【解答】
C(s)、H (g)的燃烧热分别是 393.5kJ•mol﹣1 、285.8kJ•mol﹣1 ,
2
则:①H (g)+ O (g)=H O(l)△H=﹣285.8kJ•mol﹣1,
2 2 2
④C(s)+O (g)=CO (g)△H=﹣393.5kJ•mol﹣1,
2 2
②CH COOH(l)+2O (g)═2CO (g)+2H O (g)△H =﹣782.3kJ•mol﹣1,
3 2 2 2 1
③H O(l)═H O(g)△H =+44.0kJ•mol﹣1,
2 2 2
根据盖斯定律,①×2+④×2﹣②+③×2 可得:2C(s)+2H (g)+O (g)═CH COOH
2 2 3
(l)△H=2×(﹣285.8kJ•mol﹣1)+2×(﹣393.5kJ•mol﹣1)﹣(﹣782.3kJ•mol﹣1)
+2×(44kJ•mol﹣1)=﹣488.3kJ•mol﹣1
故选 C.
16.实验室用 50mL 0.50mol•L﹣1 盐酸、50mL 0.55mol•L﹣1 NaOH 溶液和如图所示
装置,进行测定中和热的实验,得到表中的数据: ☆☆☆☆
起始温度 t /℃ 终止温度
1
t /℃ 实验次数
2
盐酸 NaOH 溶液
1 20.2 20.3 23.7
2 20.3 20.5 23.8
3 21.5 21.6 24.9
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 .
(2)在操作正确的前提下,提高中和热测定准确性的关键是: .
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H= [盐酸和第 9页(共 11页)NaOH 溶液的密度按 1g•cm﹣3 计算,反应后混合溶液的比热容(c)按
4.18J•(g•℃)﹣1 计算].如用 0.5mol/L 的盐酸与 NaOH 固体进行实验,则实验中
测得的“中和热”数值将 (填“偏大”、“偏小”、“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏
低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将 50mL0.55mol/L 氢氧化钠溶液取成了 50mL0.55mol/L 的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大
【解答】
(1)不能将环形玻璃搅拌棒改为铜丝搅拌棒,因为铜丝搅拌棒是热的良导体,
故答案为:Cu 传热快,热量损失大;
(2)中和热测定实验主要目的是测量反应放出的热量多少,所以实验成败的关
键是保温工作,所以提高中和热测定准确性的关键是提高装置的保温效果,
故答案为:提高装置的保温效果;
(3)第 1 次实验盐酸和 NaOH 溶液起始平均温度为 20.25℃,反应前后温度差为:
3.45℃;第 2 次实验盐酸和 NaOH 溶液起始平均温度为 20.40℃,反应前后温度
差为:3.40℃;第 3 次实验盐酸和 NaOH 溶液起始平均温度为 21.55℃,反应前
后温度差为:3.35℃;50mL 0.50mol•L﹣1 盐酸、50mL 0.55mol•L﹣1 NaOH 的质量
和为 m=100mL×1g/mL=100g,c=4.18J/(g•℃),代入公式 Q=cm T 得生成
0.025mol 的 水 放 出 热 量 Q=4.18J/ ( g• ℃ )
△
×100g× =1421.2J=1.4212KJ,即生成 0.025mol 的水放出热
量 1.4212KJ,所以生成 1mol 的水放出热量为 =56.8kJ,即该实
验测得的中和热△H=﹣56.8kJ/mol;氢氧化钠固体溶于水放热,所以实验中测得
的“中和热”数值将偏大
故答案为:﹣56.8 kJ/mol;偏大;
第 10页(共 11页)(4)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会
发生酸和碱的中和,温度计示数变化值减小,所以导致实验测得中和热的数值偏
小,故 A 正确;
B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,
实验测得中和热的数值偏小,故 B 正确;
C、做本实验的室温和反应热的数据之间无关,故 C 错误;
D、将 50mL0.55mol/L 氢氧化钠溶液取成了 50mL0.55mol/L 的氨水,由于氨水是
弱碱,碱的电离是吸热的过程,所以导致实验测得中和热的数值偏小,故 D 正
确;
E、在量取盐酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,
可以保证碱全反应,会使得中和和热的测定数据偏高,故 E 错误;
F、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,
故 F 正确。
故 ABDF 正确。
故答案为:ABDF.
第 11页(共 11页)