文档内容
专练 16 碳、硅与新型无机非金属材料
1.[2022·广东卷]广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。下列
文物主要由硅酸盐制成的是( )
文物
选项 A.南宋鎏金饰品 B.蒜头纹银盒
文物
选项 C.广彩瓷咖啡杯 D.铜镀金钟座
2.[2021·福建卷]建盏是久负盛名的陶瓷茶器,承载着福建历史悠久的茶文化。关于建
盏,下列说法错误的是( )
A.高温烧结过程包含复杂的化学变化
B.具有耐酸碱腐蚀,不易变形的优点
C.制作所用的黏土原料是人工合成的
D.属硅酸盐产品,含有多种金属元素
3.[2021·广东卷]化学创造美好生活。下列生产活动中,没有运用相应化学原理的是(
)
选项 生产活动 化学原理
A 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成CO 和HO
2 2
B 利用海水制取溴和镁单质 Br-可被氧化、Mg2+可被还原
C 利用氢氟酸刻蚀石英制作艺术品 氢氟酸可与SiO 反应
2
D 公园的钢铁护栏涂刷多彩防锈漆 钢铁与潮湿空气隔绝可防止腐蚀
4.[2021·全国乙卷]我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对
于改善环境、 实现绿色发展至关重要。“碳中和”是指CO 的排放总量和减少总量相当。
2
下列措施中能促进碳中和最直接有效的是( )
A.将重质油裂解为轻质油作为燃料
B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染
D.研发催化剂将CO 还原为甲醇
2
5.[2022·辽宁大连测试]《厉害了,我的国》展示了中国在航空、深海、交通、互联网
等方面取得的举世瞩目的成就,它们与化学有着密切联系。下列说法正确的是( )
A.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐B.港珠澳大桥使用高性能富锌底漆防腐,依据的是外加电流的阴极保护法
C.我国提出网络强国战略,光缆线路总长超过三千万公里,光缆的主要成分是晶体硅
D.化学材料在北京大兴机场的建设中发挥了巨大作用,其中高强度耐腐蚀钢筋属于无
机材料
6.[2022·云南昆明摸底]在海洋碳循环中,通过如图所示的途径固定碳。下列说法错误
的是( )
A.该循环过程中未涉及氧化还原反应
B.光合作用能将太阳能转化为化学能
C.钙化作用涉及的离子方程式之一为Ca2++2HCO===CaCO ↓+CO↑+HO
3 2 2
D.吸收作用中产生HCO的途径为CO
2
+H
2
O⇌H
2
CO
3
,H
2
CO 3⇌HCO+H+
7.[2022·天津五校期中]神舟十二号飞船的控制计算机、数据管理计算机完全使用国产
CPU芯片,制作芯片刻蚀液为硝酸与氢氟酸的混合溶液,其工艺涉及的反应为 Si+HNO
3
+6HF===H SiF+HNO+H↑+HO,下列说法正确的是( )
2 6 2 2 2
A.HSiF 中Si元素的化合价为+6价
2 6
B.该反应中,HNO 仅作氧化剂
3
C.该反应中,生成标准状况下2.24 L H 时,转移电子的物质的量为0.2 mol
2
D.芯片刻蚀液可用硫酸代替
8.[2022·辽宁沈阳期中]由下列实验事实得出碳元素与硅元素的非金属性强弱比较的结
论正确的是( )
A.SiO 能与HF反应,CO 不能与HF反应,可知碳的非金属性强于硅
2 2
B.由反应NaCO+SiO=====NaSiO+CO↑可知,硅的非金属性强于碳
2 3 2 2 3 2
C.CO 通入NaSiO 溶液产生白色沉淀,由酸性HCO>H SiO 可知,碳的非金属性强
2 2 3 2 3 2 3
于硅
D.由SiO+2C=====Si+2CO↑可知,碳的非金属性强于硅
2
9.[2022·河南信阳罗山调研]2020年11月“嫦娥五号”成功着陆月球,展示了以芳纶
为主要材料制成的五星红旗。用SiC增强铝基材料钻杆“挖土”,实现了中国首次月球无
人采样返回。研究表明月球表面的“土壤”主要含有氧、硅、铝、铁、镁、钙和钠等元素
下列有关说法错误的是( )
A.月球表面的“土壤”中所含金属元素镁和铝的单质均可以通过电解其熔融氯化物进
行冶炼
B.空间实验室的硅电池板可以将光能直接转化为电能
C.“嫦娥五号”望远镜的某些部件由SiC制成,硬度高,耐高温
D.“嫦娥五号”使用的碳纤维被誉为“新材料之王”,是一种新型无机非金属材料
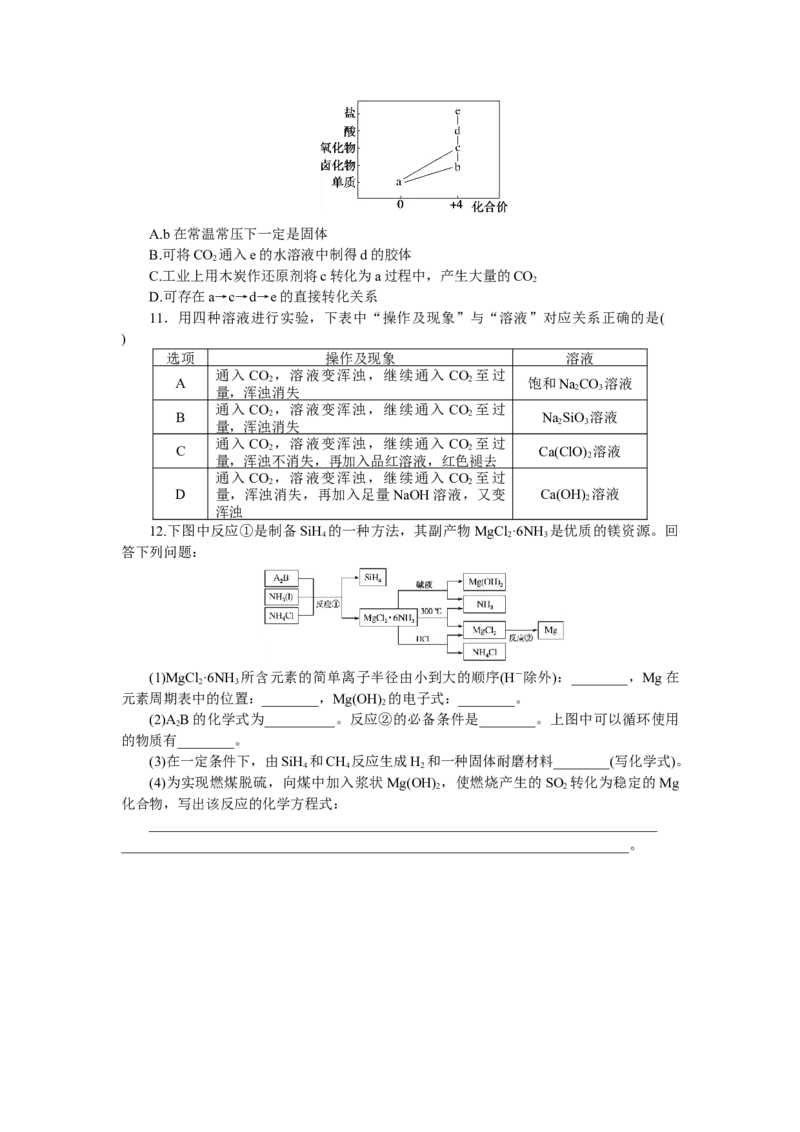
10.[2022·广东调研]部分含硅物质的分类与相应化合价关系如图所示。下列推断合理
的是( )A.b在常温常压下一定是固体
B.可将CO 通入e的水溶液中制得d的胶体
2
C.工业上用木炭作还原剂将c转化为a过程中,产生大量的CO
2
D.可存在a→c→d→e的直接转化关系
11.用四种溶液进行实验,下表中“操作及现象”与“溶液”对应关系正确的是(
)
选项 操作及现象 溶液
通入 CO ,溶液变浑浊,继续通入 CO 至过
A 2 2 饱和NaCO 溶液
量,浑浊消失 2 3
通入 CO ,溶液变浑浊,继续通入 CO 至过
B 2 2 NaSiO 溶液
量,浑浊消失 2 3
通入 CO ,溶液变浑浊,继续通入 CO 至过
C 2 2 Ca(ClO) 溶液
量,浑浊不消失,再加入品红溶液,红色褪去 2
通入 CO ,溶液变浑浊,继续通入 CO 至过
2 2
D 量,浑浊消失,再加入足量NaOH溶液,又变 Ca(OH) 溶液
2
浑浊
12.下图中反应①是制备SiH 的一种方法,其副产物MgCl ·6NH 是优质的镁资源。回
4 2 3
答下列问题:
(1)MgCl ·6NH 所含元素的简单离子半径由小到大的顺序(H-除外):________,Mg在
2 3
元素周期表中的位置:________,Mg(OH) 的电子式:________。
2
(2)A B的化学式为__________。反应②的必备条件是________。上图中可以循环使用
2
的物质有________。
(3)在一定条件下,由SiH 和CH 反应生成H 和一种固体耐磨材料________(写化学式)。
4 4 2
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH) ,使燃烧产生的SO 转化为稳定的Mg
2 2
化合物,写出该反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。