文档内容
专题 07 离子共存 离子的检验和推断
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 离子共存
考点二 离子的检验和推断
考点一 离子共存
1.(2023·福建泉州·福建省泉州第一中学校考模拟预测)下列离子在一定条件下能共存,且加入相应试剂
后发生反应的离子方程式正确的是
选项 离子组 加入试剂 加入试剂后发生反应的离子方程式
A 、 、
B 、 、
C 、 、 少量NaOH
D 、 、 少量
【答案】A
【解析】A. 、 、 能大量共存,加入 后, 、 、 发生氧化还原反应,生成
Fe3+、NO等,离子方程式为 ,A正确;B. 、 、 在
溶液中能大量共存,加入 后,除有BaSO 沉淀生成外,还发生反应 +H+=H O+SO ↑,B不正确;
4 2 2
C.在溶液中, 、 能发生氧化还原反应2 + =S↓+SO ↑+H O,C不正确;D. 、 、
2 2
Fe3+混合后,除发生S2-与Fe3+的氧化还原反应外,还会发生 、Fe3+的双水解反应,D不正确;故选A。
2.(2023·天津红桥·统考二模)室温时,下列各组离子在水溶液中可以大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】D
【解析】A.已知HClO是弱酸,故H+和ClO-不能大量共存,且 、 、 三者因发生氧化还原反应
而不能大量共存,A不合题意;B. 、 、 三者因发生氧化还原反应而不能大量共存,B不合题意;
C. 、 因发生双水解反应而不能大量共存,C不合题意;D. 、 、 、 各离子
间不反应,可以大量共存,D符合题意;故答案为:D。
1
原创精品资源学科网独家享有版权,侵权必究!3.(2023·湖北黄冈·黄冈中学校考二模)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.水电离的 mol·L 的溶液中: 、 、 、
B. 的溶液中: 、 、 、
C.0.1 mol/L氨水溶液中: 、 、 、
D.溶解少量 气体的溶液: 、 、 、
【答案】C
【解析】A.水电离的 的溶液,可能是酸性溶液或碱性溶液, 、 在酸性溶
液中不能大量存在,选项A不符合题意;B. 的溶液呈碱性,铵根离子不能大量存在,选
项B不符合题意;C.0.1mol/L氨水溶液中:Na+、K+、 、 各离子相互不反应,能大量共存,选
项C符合题意;D.SO 具有还原性,与ClO-不能大量共存,选项D不符合题意;答案选C。
2
4.(2023·重庆沙坪坝·重庆八中校考二模)含有下列各组离子的溶液中,通入(或加入)过量的某种物质后
仍能太量共存的是
A.通入 气体, 、 、 、
B.通入 气体, 、 、 、
C.通入 气体, 、 、 、
D.加入 溶液, 、 、 、
【答案】C
【解析】A.H++NO 组合具有强氧化性,能和 气体发生氧化还原反应,A不符合题意;B.NH 通入
3
溶液中生成 , 与 反应生成 沉淀,B不符合题意;C.溶液中有大量 ,
故 不与 反应,C符合题意;D. 与 发生双水解反应生成氢氧化铝沉淀和 ,D不符合题
意;故选C。
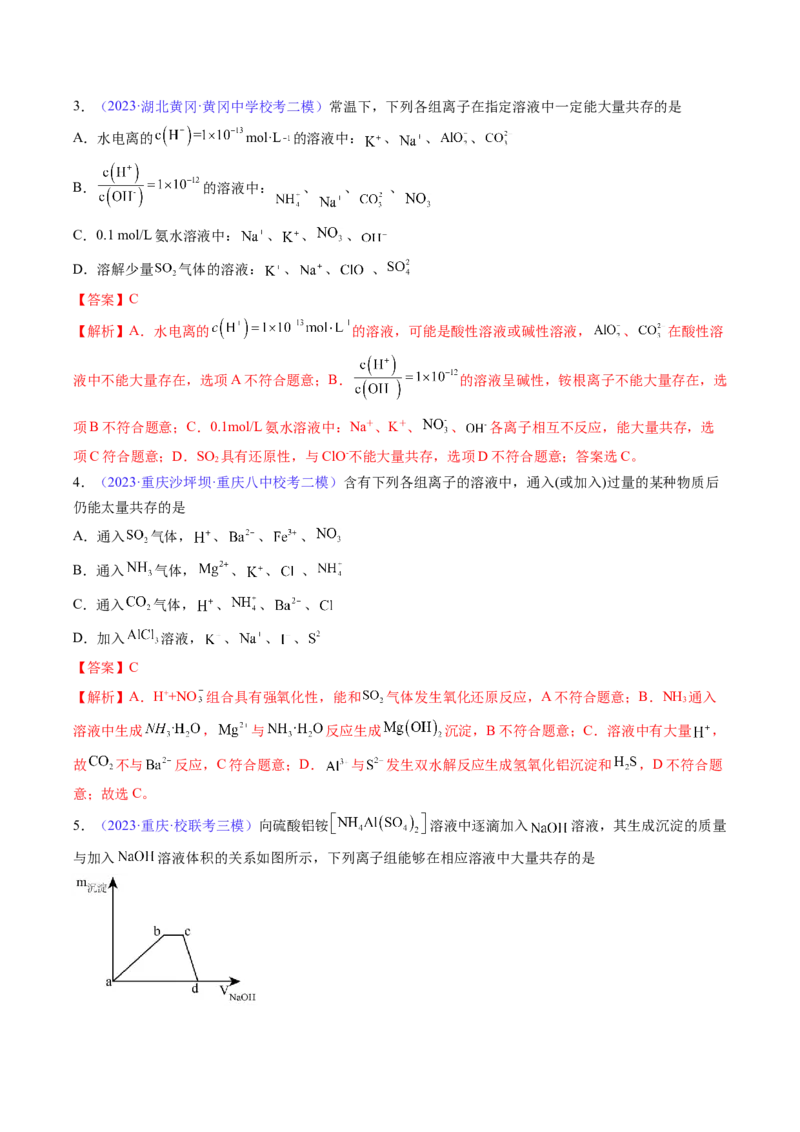
5.(2023·重庆·校联考三模)向硫酸铝铵 溶液中逐滴加入 溶液,其生成沉淀的质量
与加入 溶液体积的关系如图所示,下列离子组能够在相应溶液中大量共存的是A.a点: B.b点:
C.c点: D.d点:
【答案】D
【分析】硫酸铝铵溶液中滴加NaOH溶液,先发生Al3++3OH-=Al(OH) ↓,继续滴加NaOH溶液,发生NH
3
+OH-=NH·H O,继续滴加NaOH,发生Al(OH) +OH-=AlO +2H O,据此分析;【解析】A.a点溶液中所
3 2 3 2
含离子是NH 、Al3+、SO ,Ca2+与SO 生成微溶物CaSO,因此所给离子在指定溶液中不能大量共存,
4
故A不符合题意;B.根据上述分析,b点所含离子是NH 、SO 、Na+,NH 与SiO 发生双水解反应,
不能大量共存,故B不符合题意;C.题中所给OH-与Cu2+、NH 分别生成氢氧化铜沉淀、NH ·H O,因
3 2
此它们不能大量共存,故C不符合题意;D.d点所含微粒为Na+、NH ·H O、SO 、AlO ,所给离子在d
3 2
点能够大量共存,故D符合题意;答案为D。
6.(2023·湖北黄冈·黄冈中学校考三模)下列各组离子在所给定的条件下可以大量共存的是
选项 条件 离子
A 加入苯酚显紫色的溶液中 Na+、Mg2+、Cl—、SO
使KI—淀粉试纸变蓝的溶
B S2—、NH 、Mg2+
液
C 在含有大量HCO 的溶液中 K+、Na+、AlO 、Br—
D 能和Ca2+生成沉淀的溶液中 K+、Ba2+、CHCOO—、Cl—
3
【答案】A
【解析】A.加入苯酚显紫色的溶液中含有铁离子,铁离子、钠离子、镁离子、氯离子和硫酸根离子在溶
液中不发生任何反应,能大量共存,故A正确;B.使碘化钾淀粉试纸变蓝的溶液中含有氧化性比单质碘
氧化性强的微粒,能与溶液中的硫离子发生氧化还原反应,不能大量共存,故B错误;C.碳酸氢根离子
能与溶液中的偏铝酸根离子反应生成氢氧化铝沉淀和碳酸根离子,不能大量共存,故C错误;D.能和钙
离子生成沉淀的溶液中可能含有碳酸根离子或硫酸根离子,碳酸根离子或硫酸根离子能与溶液中的钡离子
反应生成沉淀,不能大量共存,故D错误;故选A。
7.(2023·福建厦门·厦门一中校考模拟预测)下列离子组能大量共存且加入(或通入)试剂发生反应的离子
方程式正确的是
选项 离子组 试剂 离子方程式
A 、 、 足量铁氰化钾溶液
B 、 、 少量C 、 、 少量
、
D 足量银氨溶液
、
【答案】B
【解析】A.该组离子互不反应可大量共存,其中 与铁氰化钾反应生成蓝色沉淀,离子方程式:
,故A错误;B.该组离子互不反应可大量共存,通少量氯气
后反应离子方程式为: ,故B正确;C.加入少量 离子
方程式为: ,故C错误;D.OH-与NH
不能大量共存,加入足量银氨溶液共热,离子方程式:
,故D错误;故选:B。
8.(2023·广东梅州·统考三模)室温下,下列各组离子一定能在指定溶液中共存的是
A. 的 溶液中: 、 、 、
B. 的 溶液中: 、 、 、
C. 的 溶液中: 、 、 、
D. 的 溶液中: 、 、 、
【答案】D
【解析】A. 与 会发生氧化还原反应, 溶液中不能含有大量 ,A项错误;B. 酸性条件下,
具有强氧化性,与 , 不能共存,B项错误;C. 与 会发生双水解,即
,不能大量共存,C项错误;D.溶液中 、 、 、 、
、 、 之间不能发生任何反应,可以大量共存,D项正确;答案选D。
9.(2023·辽宁·校联考一模)下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
选项 离子组 加(或通)入试剂 判断和分析
A 足量 能大量共存
不能大量共存,只发生下列反应
B 足量 溶液
C 足量 溶液 不能大量共存,因 和 之间会发生完全双水解生成 气体和 沉淀
不能大量共存,只发生下列氧化还原反应
D 少量
【答案】A
【解析】A.Na+、H+、Ba2+、Cl-、NO 之间不反应能够共存,通入足量CO 也不反应,能够大量共存,A
2
正确;B.生成的碳酸镁与氢氧化钠反应生成氢氧化镁,B错误;C.AlO 和HCO 之间反应生成氢氧化
铝沉淀和碳酸根离子,AlO 和HCO 发生的不是双水解反应,C错误;D.Na+、K+、ClO-、SO 之间不
反应能够共存,通入少量SO 后先发生的氧化还原反应为:ClO- +H O+SO =Cl-+ SO +2H+,后发生反应
2 2 2
H++ClO-=HClO, D错误;故选A。
10.(2023·湖南衡阳·校联考二模)下列离子组能否大量共存的判断及原因均正确的是
选项 离子组 判断及原因
不能大量共存,因发生 而使
A 、 、 、
溶液呈红色
B 、 、 、 能大量共存,离子间不反应
不能大量共存, 与 发生双水解反应:
C 、 、 、
不能大量共存,发生反应:
D 、 、 、
【答案】D
【解析】A.该组中四种离子能大量共存,判断及原因错误,A错误;B.该组中 、 均能氧化 ,
不能大量共存,判断错误,B错误;C.该组离子不能大量共存,判断正确,但 与 发生的不是双
水解反应,原因错误,C错误;D. 、 、 不能大量共存,会发生反应,
,判断及原因均正确,D正确;故答案为D。
考点二 离子的检验和推断
1.(2023·上海黄浦·一模)某溶液含有K+、Fe3+、SO 、CO 、I-中的几种。取样,滴加KSCN溶液后
显血红色。为确定该溶液的组成,还需检验的离子是( )A.K+ B.I- C.SO D.CO
【答案】A
【分析】能反应的不共存、电解质溶液呈电中性;
【解析】取样,滴加KSCN溶液后显血红色,则溶液含有Fe3+、Fe3+与CO 会发生双水解反应而不共存、
I-与Fe3+发生氧化还原反应而不共存,则阴离子只有SO ,电解质溶液呈电中性,故溶液中一定有SO
,为确定该溶液的组成,还需检验的离子只有K+;答案选A。
2.(2023·宁夏银川·统考一模)现有一澄清透明的溶液,可能含有大量的Fe3+、Fe2+、Al3+、H+、AlO 、
CO 、NO 七种离子中的几种,向该溶液中逐滴加入1mol•L-1NaOH溶液一定体积后才产生沉淀,则下列
判断正确的是
A.溶液中可能含有Fe2+ B.溶液中一定含有NO
C.溶液中可能含有CO D.溶液中一定不含Al3+
【答案】B
【分析】向该溶液中逐滴加入1mol•L-1氢氧化钠溶液一定体积后才产生沉淀说明溶液中一定含有氢离子,
溶液中氢离子与偏铝酸根离子和碳酸根离子反应,不能大量共存,则溶液中一定不含有偏铝酸根离子和碳
酸根离子;由电荷守恒可知,溶液中一定含有硝酸根离子,酸性条件下具有强氧化性的硝酸根离子会与亚
铁离子反应,则溶液中一定不含有亚铁离子,加入氢氧化钠溶液能生成沉淀,说明溶液中至少含有铁离子
和铝离子中的一种。
【解析】A.由分析可知,溶液中一定不含有亚铁离子,故A错误;B.由分析可知,溶液中一定含有硝
酸根离子,故B正确;C.由分析可知,溶液中一定不含有碳酸根离子,故C错误;D.由分析可知,溶
液中至少含有铁离子和铝离子中的一种,故D错误;故选B。
3.(2023·统考模拟预测)某溶液中只可能含有下列离子中的几种:K+、NO 、SO 、NH 、CO (不考
虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱浓溶液并加热,产生的气体在标准状况下为224mL。
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl 溶液,得固体2.33g。
2
下列说法正确的是
A.该溶液中无法确定是否含有K+
B.该溶液中肯定含有NO 、SO 、NH 、CO
C.该溶液中不含NO
D.该溶液中一定含有K+,且c(K+)≥0.1mol/L
【答案】D
【分析】100mL溶液中加入足量氢氧化钠加热,生成的气体为氨气,物质的量为0.01mol,第二份加入足
量的盐酸无现象,则无碳酸根离子,再加入足量的氯化钡溶液,生成硫酸钡沉淀为0.01mol,则200mL溶
液中含有铵根离子0.02mol,硫酸根离子0.02mol,根据电荷守恒则溶液中一定还含有钾离子。
【解析】A.根据分析可知,该溶液中一定含有钾离子,A错误;B.根据分析可知,该溶液中一定含有硫酸根离子、铵根离子,一定没有碳酸根离子,不能确定是否存在硝酸根离子,B错误;C.该溶液中是否
存在硝酸根离子无法确定,C错误;D.200mL溶液中存在硫酸根离子0.02mol,铵根离子0.02mol,则根
据电荷守恒可知,钾离子的物质的量至少为0.02mol,c(K+)≥0.1mol/L,D正确;故答案选D。
4.(2023·天津河西·统考三模)实验室进行粗盐提纯时,需除去 、 和 ,所用试剂除
、NaOH、盐酸和水外,还应该必备的试剂是
A. B. C.硝酸 D.小苏打
【答案】A
【解析】加入氯化钡时,能和 反应生成硫酸钡沉淀,从而除去 ,加入碳酸钠溶液时,能和
Ca2+、Ba2+反应生成碳酸钙沉淀、碳酸钡沉淀,从而除去钙离子和过量的钡离子;加入过量氢氧化钠溶液,
生成氢氧化镁沉淀,除去镁离子;过滤,向滤液中加入适量的稀盐酸时,可以把过量的氢氧化钠和碳酸钠
除去,故还应该必备的试剂是BaCl ,故选:A。
2
5.(2023·上海松江·统考二模)有一澄清透明的溶液,可能含有大量的 、 、 、 、 、
、 中的几种,向该溶液中滴入 溶液一定体积后才产生沉淀。下列判断正确的是
A.溶液中可能含有 B.溶液中一定不含
C.溶液中可能含有 D.溶液中一定不含
【答案】D
【分析】向该溶液中滴入 溶液一定体积后才产生沉淀,溶液中一定含有 ,因为 与
反应, ,所以溶液中一定不含 , 与 反应生成 , 一定不
存在,溶液中一定含有阴离子为 , 在酸性条件下有强氧化性, 一定不存在,加入 产生
沉淀, 和 可能都存在,或者存在其中之一。
【解析】A.根据以上分析,该溶液中 一定不存在,A错误;B.加入 产生沉淀, 和 可
能都存在,或者存在其中之一,B错误;C.根据以上分析,溶液中一定含有 ,C错误;D.溶液中含
有 ,一定不含 ,D正确;故选D。
6.(2023·安徽黄山·统考三模)某工业废水中可能含有K+、Ag+、Mg2+、Cu2+、Al3+、NH 、Cl-、CO 、
NO 、SO 、I-中的几种,且各离子物质的量浓度均为0.2mol/L(忽略水的电离及离子的水解),欲探究废
水的组成,进行了如下实验:
I.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV.向III中所得溶液中加入BaCl 溶液,有白色沉淀生成。
2
下列推断不正确的是A.溶液中一定不含的阳离子是K+、NH 、Cu2+、Ag+
B.III中加入盐酸生成无色气体的离子方程式为:8H++6I-+2NO =3I +2NO↑+4HO
2 2
C.原溶液除H+和OH-外只含有Mg2+、Al3+、NO 、SO 、I-
D.另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤、洗涤、灼烧沉淀至恒重,得到固体质
量0.8g
【答案】C
【分析】I.取该无色溶液5 mL,说明一定不含有Cu2+,滴加一滴氨水有沉淀生成,且离子种类增加,说
明增加的是NH ,所以原溶液中一定不含NH ,可能含有Mg2+、Al3+,不含NH 、CO ;II.用铂丝蘸
取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰,说明没有K+;III.另取溶液加入过量盐酸,
有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,说明有还原性离子I-与NO 和H+反
应生成NO,即溶液中有I-、NO ,一定不含有Ag+。
IV.向III中所得的溶液中加入BaCl 溶液,有白色沉淀生成,说明有SO ;综上所述,一定含有的阴离
2
子为NO 、SO 、I-,各离子物质的量浓度均为0.2mol/L,结合电荷守恒可知,溶液中一定有Mg2+和
Al3+,且还含有一种-1价的阴离子为Cl-。
【解析】A.由分析可知,溶液中一定不含的阳离子是K+、NH 、Cu2+、Ag+,故A正确;B.III中加入盐
酸,I-与NO 和H+反应生成NO,根据得失电子守恒和电荷守恒配平离子方程式为:8H++6I-+2NO
=3I +2NO↑+4HO,故B正确;C.由分析可知,原溶液除H+和OH-外只含有Mg2+、Al3+、NO 、SO 、
2 2
I-、Cl-,故C错误;D.另取100 mL原溶液,加入足量的NaOH溶液,Mg2+、Al3+反应生成Mg(OH) 、
2
NaAlO ,充分反应后过滤,洗涤,灼烧沉淀至恒重,根据元素守恒:n(MgO)=n(Mg2+)=cV=0.2 mol/L×0.1
2
L=0.02 mol,m(MgO)=0.02 mol×40 g/mol=0.8 g,故D正确;故选C。
7.(2023·陕西西安·西北工业大学附属中学校考模拟预测)某白色固体样品,可能含有 、 、
、 、 中的一种或几种。对该样品进行如下实验:
①取少量固体加入足量水中,固体部分溶解;②取①中滤液做焰色试验,透过蓝色钴玻璃未观察到紫色;
③取①中滤渣,向其中加入足量的盐酸,产生气泡,固体部分溶解.
下列说法不正确的是
A.固体粉末中一定不含
B.固体粉末中一定含有 和
C.取①中滤液,加入硝酸酸化的 溶液,若未产生白色沉淀,则样品中无
D.为进一步确定原样品组成,可以向③未溶解的固体中加入 溶液
【答案】C
【分析】①取少量固体加入足量水中,固体部分溶解,不溶性物质可能为 、 、 ;②取①中滤液做焰色试验,透过蓝色钴玻璃未观察到紫色,滤液中不存在钾离子,说明样品中一定没有 ;
③取①中滤渣,向其中加入足量的盐酸,产生气泡,固体部分溶解, 溶于盐酸,可知样品中存在
和 ,无法确定未溶解的物质是 ,还是 ,还是二者均有。
【解析】A.由分析可知,固体粉末中一定不含 ,A正确;B.由分析可知,固体粉末中一定含有
和 ,B正确;C.取①中滤液,加入硝酸酸化的 溶液,若未产生白色沉淀,有可
能是加水溶解时,硫酸根恰好沉淀完全,不能确定样品中有无 ,C错误;D. 可溶于 溶
液, 不溶于 溶液,故为进一步确定原样品组成,可以向③未溶解的固体中加入 溶液,D
正确;故选C。
8.(2023·江西抚州·江西省乐安县第二中学校考一模)在某强酸性溶液X中仅含有 、 、 、
、 、 、 、 、 、 中的一种或几种(忽略水的电离及离子的水解),取该溶液进
行连续实验,实验过程如图,下列有关推断正确的是
A.生成气体A的离子反应:
B.溶液X中一定含有 、 、 、
C.加热灼烧沉淀F,其产物一定是磁性氧化铁
D.沉淀H中一定含有 和 沉淀
【答案】A
【分析】在强酸性溶液中一定不会存在 、 离子;加入过量硝酸钡生成沉淀,则该沉淀C为
BaSO,说明溶液中含有SO ,不含Ba2+,生成气体A,则A只能是NO,说明溶液中含有还原性离子,
4
则一定为Fe2+,且溶液中不含 ;溶液B中加入过量NaOH溶液,沉淀F为Fe(OH) ,无气体产生,说
3
明溶液中没有NH 离子;溶液E中通入CO 气体,生成沉淀H,则H为Al(OH) ,E为NaOH和NaAlO ,
2 3 2
说明原溶液中含有Al3+离子;不能确定是否含有的离子Fe3+和Cl-。
【解析】A.由分析可知,气体A为NO,生成NO的离子反应为:
,故A正确;B.由分析可知,溶液中一定存在:H+、Al3+、
Fe2+、 ,不能确定Cl-是否存在,故B错误;C.由分析可知,F为Fe(OH) ,Fe(OH) 在加热条件下分
3 3
解产生Fe O,故C错误;D.由分析可知,溶液E中含有过量的Ba2+和OH-,若通入的CO 过量则没有
2 3 2BaCO 沉淀,故D错误;故选A。
3
9.(2023·甘肃兰州·统考一模)某固体样品可能含有NaNO 、NaHCO 、NaSO 和NaSO 。取少量样品进
3 3 2 3 2 4
行如下实验:步骤①:将样品溶于水,得到澄清溶液;步骤②:向①的溶液中滴加过量稀盐酸,有气泡产
生;步骤③:取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成。下列说法中正确的是
2
A.该固体样品中一定含有NaSO
2 4
B.该固体样品中一定含有NaHCO
3
C.该固体样品不可能只含有NaSO
2 3
D.步骤②的试管口产生的气体一定是无色的
【答案】C
【分析】步骤①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能大量共存;步骤②向
①的溶液中滴加过量稀盐酸,有气泡产生,说明可能含有NaHCO 或NaSO 或两者都有;若气泡是NO,
3 2 3
说明是NaNO 和NaSO 均有;步骤③取②的上层清液,向其中滴加BaCl 溶液,有沉淀生成,则沉淀为
3 2 3 2
BaSO,说明固体中存在NaSO 和NaSO 至少一种。
4 2 3 2 4
【解析】A.结合分析可知不一定含有NaSO ,白色沉淀可能是NaNO 和NaSO 在加盐酸后发生氧化还
2 4 3 2 3
原反应生成硫酸根离子,硫酸根离子和钡离子生成白色的硫酸钡沉淀,A错误;B.若气泡是NO,说明是
NaNO 和NaSO 均有,不一定有NaHCO ,B错误;C.该固体样品若只含有NaSO ,则步骤③不会产生
3 2 3 3 2 3
沉淀,故该固体样品不可能只含有NaSO ,C正确;D.由分析可知步骤②产生的气体可能是NaNO 和
2 3 3
NaSO 在加盐酸后发生氧化还原反应生成的NO,NO易与试管内氧气反应生成红棕色二氧化氮,试管口产
2 3
生的气体可能是红棕色的,D错误;答案选C。
10.(2023·辽宁·校联考二模)某溶液中可能存在K+、Na+、Fe2+、Al3+、SO 、SO 中的若干种(除水电
离出的H+、OH-之外),并且每种离子的浓度均为0.2mol/L。为确定溶液的组成进行了如下实验:
i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色。
ii.往i的溶液中加BaCl 溶液,产生难溶于水的白色沉淀。
2
下列有关判断正确的是
A.SO ,Fe2+可能同时存在于溶液中
B.若溶液中有SO ,则蘸取该溶液做焰色试验,可能观察到黄色火焰
C.溶液中可能有Al3+,一定没有SO
D.产生红棕色气体的离子方程式一定是3Fe2++4H++NO=3Fe3++NO↑
【答案】B
【分析】i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色,则含有还原性的离
子 或 ;ii.往i的溶液中加BaCl 溶液,产生难溶于水的白色沉淀,则为硫酸钡沉淀。由电荷守恒分
2
析出该溶液可能有两种组成,一种是 , 。一种是 , , 。
【解析】A. , 因双水解而不可能同时存在,只能二选一,A选项错误;B.若溶液中有 ,
则含有 , ,做焰色试验,可能观察到黄色火焰,B选项正确;C.据分析,溶液中不可能有 ,故C选项错误;D.产生红棕色气体的离子方程式可能是 ,也可能是
和 反应,故D选项错误;故选B。
11.(2023·浙江杭州·校联考模拟预测)化合物A由3种元素组成,某学习小组按如下流程进行实验:
已知:无色气体B高温下分解得到的混合气体X,在相同条件下体积增大到原来的1.5倍;无色气体G为
单质,混合气体Z呈红棕色。
(1)化合物A的组成元素是 ,A的化学式是 。
(2)写出无色晶体A受热分解生成无色气体B的化学方程式: 。
(3)写出F→Y过程中棕黑色固体溶解所发生反应的离子方程式: 。
(4)设计实验检验白色固体E中的阴离子: 。
【答案】(1)H、N、O
(2)
(3)
(4)将少量白色固体E溶于水分装成两份,将一份溶液用玻璃棒蘸取点在pH试纸上,若试纸呈蓝色,说明
含有 ;另取少量溶液于试管中,加入铜丝,无明显变化,再滴加少量稀硫酸,溶液逐渐变蓝,试管口
出现红棕色,说明含有 。
【分析】由题可知,化合物A由3种元素组成,无色气体B的质量为8g-3.6g=4.4g,已知化合物A的组成
元素为,H、N、O,则无色气体B为N的氧化物,则B可为NO,则A的化学式为NH NO ,C为无色液
2 4 3
体,且C的质量为3.6g,则C为HO,由无色晶体A产生的混合气体Z呈红棕色,则Z中包含NO ;
2 2
【解析】(1)由分析可知,化合物A的组成元素为O、N、H;根据质量守恒定律可知,生成的无色气体
B的质量为8g-3.6g=4.4g,已知化合物A的组成元素为,H、N、O,无色液体C为HO,则无色气体B为
2
N的氧化物,则B可为NO,则A的化学式为NH NO ;
2 4 3
(2)无色晶体A受热分解生成无色气体B的化学方程式为NH NO NO+2HO;
4 3 2 2
(3)棕黑色固体溶解所发生反应的离子方程式为 Ag O+4NH +H O==2[Ag(NH )]++2OH-;
2 3 2 3 2
(4)将少量白色固体E溶于水分装成两份,将一份溶液用玻璃棒蘸取点在pH试纸上,若试纸呈蓝色,说明含有OH—;另取少量溶液于试管中,加入铜丝,无明显变化,再滴加少量稀硫酸,溶液逐渐变蓝,试管
口出现红棕色,说明含有 。
12.(2023春·云南昆明·高三统考开学考试)对于数以千万计的化学物质和为数众多的化学反应,分类法
的作用几乎是无可代替的。
I.现有物质:①HO ②Cu ③BaCO ④Fe(OH) 胶体 ⑤酒精 ⑥CO ⑦稀硫酸
2 3 3 2
(1)以上物质中属于混合物的是 (填序号,下同),属于电解质的是 。
(2)向④中逐滴滴加⑦,可观察到的现象是 。
II.某白色粉末中可能含有 、 、 ,现进行以下实验:
i.将部分粉末加入水中,振荡,有白色沉淀生成;ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有
气泡产生;iii.取少量ii的溶液滴入 溶液,有白色沉淀生成。
(3)根据上述实验现象,判断原白色粉末中肯定含有 ,可能含有 ,并写出有关反应的离子方
程式 。(写两个即可)
【答案】(1)④⑦ ①③
(2)先出现红褐色沉淀,后沉淀溶解
(3)CaCl 、KCO Ba(NO ) Ca2++ =CaCO ↓、2H++CaCO =Ca2++CO ↑+H O、Ag++Cl-
2 2 3 3 2 3 3 2 2
=AgCl↓、Ba2++ =BaCO ↓ 、BaCO +2H+=Ba2++CO ↑+H O
3 3 2 2
【解析】(1)胶体和溶液属于混合物,即④⑦是混合物;①HO和③BaCO 属于电解质,故答案为:
2 3
④⑦;①③;
(2)Fe(OH) 胶体中滴加稀硫酸,首先发生胶体聚沉出现红褐色沉淀,继续滴加硫酸,氢氧化铁沉淀与硫
3
酸发生反应生成硫酸铁,沉淀溶解,故答案为:先出现红褐色沉淀,后沉淀溶解;
(3)i可说明一定存在 ,产生白色沉淀的离子方程式可能为:Ca2++ =CaCO ↓、Ba2++
3
=BaCO ↓,ii.向i的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;反应的离子方程式为:2H+
3
+CaCO =Ca2++CO ↑+H O或BaCO +2H+=Ba2++CO ↑+H O;iii中滴入 溶液,有白色沉淀生成,反应
3 2 2 3 2 2
的离子方程式为:滴入 溶液,有白色沉淀生成,现象可说明溶液中含有氯离子,则一定含有 ,
硝酸钡为可能存在的物质, 故答案为:CaCl 、KCO;Ba(NO );Ca2++ =CaCO ↓、2H++CaCO =Ca2+
2 2 3 3 2 3 3
+CO ↑+H O、Ag++Cl-=AgCl↓、Ba2++ =BaCO ↓ 、BaCO +2H+=Ba2++CO ↑+H O;
2 2 3 3 2 2