文档内容
专题 09 化学反应原理综合
(考试时间:75分钟 试卷满分:100分)
1.(10分)(2024·山东枣庄高三期中)氮是空气中含量最多的元素,在自然界中的存在十分广泛,实验小
组对不同含氮物质做了相关研究。
(1)乙二胺(H NCH CHNH )是二元弱碱,分步电离,在溶液中的电离类似于氨。 时,乙二胺溶
2 2 2 2
液中各含氮微粒的分布分数δ(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液
的变化曲线如图所示。
①HNCH CHNH 在水溶液中第一步电离的方程式为 。
2 2 2 2
②乙二胺一级电离平衡常数。 为 。
(2)工业上利用氨气脱硝反应,实现二者的无害化处理,已知下列反应:
①2H (g)+ O (g) 2HO(g) ΔH=-483.6kJ·mol-1
2 2 2 1
②2NO (g) N(g)+ O (g) ΔH=-180kJ·mol-1
2 2 1
③N (g)+ 3H (g) 2NH (g) ΔH=-92.2kJ·mol-1
2 2 3 3
则 6NO(g)+4NH(g) 6HO(g)+5N (g) 。
3 2 2
(3)氨气常被用于对汽车尾气中的氮氧化物进行无害化处理,以消除其对空气的污染。去除NO的反应
历程如图1所示,此反应中的氧化剂为 (填化学式),含铁元素的中间产物有 种。
若选用不同的铁的氧化物为催化剂可实现较低温度下的转化,根据图 2选择的适宜条件为。
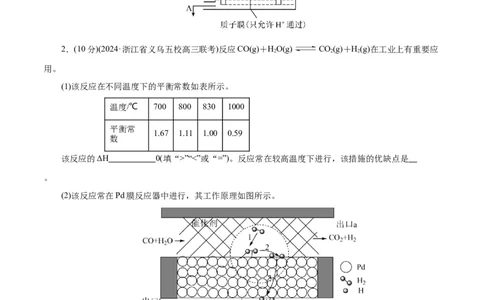
(4)利用电化学原理脱硝可同时获得电能,其工作原理如图所示。则负极发生的电极反应式为
,当外电路中有2mol电子通过时,理论上通过质子膜的微粒的物质的量为 。
2.(10分)(2024·浙江省义乌五校高三联考)反应CO(g)+HO(g) CO(g)+H(g)在工业上有重要应
2 2 2
用。
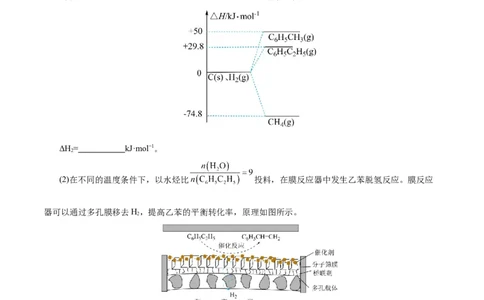
(1)该反应在不同温度下的平衡常数如表所示。
温度/℃ 700 800 830 1000
平衡常
1.67 1.11 1.00 0.59
数
该反应的ΔH 0(填“>”“<”或“=”)。反应常在较高温度下进行,该措施的优缺点是
。
(2)该反应常在Pd膜反应器中进行,其工作原理如图所示。
①利用平衡移动原理解释反应器存在Pd膜时具有更高转化率的原因是 。
②某温度下,H 在Pd膜表面上的解离过程存在如下平衡:H 2H (即图中过程2),其正反应的
2 2
活化能远小于逆反应的活化能。下列说法不正确的是
A.图中过程2的ΔH>0
B.Pd膜对气体分子的透过具有选择性C.加快Pd膜内H原子迁移有利于H 的解离
2
D.N 吹扫有助于H 分子脱离Pd膜
2 2
③同温同压下,将等物质的量的CO和HO通入无Pd膜反应器反应,测得CO的平衡转化率为50%;
2
若换成Pd膜反应器,CO的平衡转化率为80%,则相同时间内,出口a和出口b中H 的物质的量比为
2
。
3.(10分)(2024·浙江强基联盟高三联考)甲烷催化重整是工业制氢的重要途径。涉及的主要反应如下:
①甲烷部分氧化反应:CH (g)+1/2O (g) CO (g)+ 2H (g) ΔH=-35.7 kJ·mol-1
4 2 2
②甲烷水蒸气重整反应:CH (g)+HO(g) CO (g)+ 3H (g) ΔH=+206.2 kJ·mol-1
4 2 2
③水气转换反应:CO (g)+H O(g) CO(g)+ H (g) ΔH=-41.2 kJ·mol-1
2 2 2
请回答:
(1)甲烷水蒸气重整—水气变换耦合反应为CH (g)+2HO(g) CO (g)+ 4H (g),该反应的ΔH =
4 2 2 2
kJ·mol-1,该反应自发进行的条件是 。
(2)一定温度下,恒容反应器中注入初始浓度均为1mol·L-1的原料气CH (g)、O(g)、HO(g),充分反
4 2 2
应达到平衡状态,测得c [CH (g)]= c [CO(g)]=0.25mol·L-1、c [O (g)]=0.75mol·L-1。该条件下反应③的平衡
4 2 2
常数为 。
(3)下列说法正确的是_______。
A.通过控制氧气用量,有利于实现甲烷重整过程的热平衡
B.升高温度,水气变换反应速率降低, 产率降低
C.恒压条件比恒容条件利于提高 平衡转化率
D.一定温度下,恒容反应器中c [CO(g)]:c [CO(g)]=1,说明反应达到平衡状态
2
(4)在进气量为 下,CH (g)、O(g)、HO(g)以恒定比例通入催化反应器,研究温度对反应
4 2 2
的影响。结果如图1所示。
①
在图2中画出CH 转化率与温度关系示意图 。
4②近年来发展了钯膜催化甲烷重整制氢技术,反应器中 选择性透过膜的机理如图3所示。说明该制
备技术的优点: 。
4.(12分)(2024·浙江省温州市普通高中高三一模)苯乙烯是用来制备重要高分子聚苯乙烯的原料。以水
蒸气做稀释剂、催化剂存在条件下,乙苯催化脱氢可生成苯乙烯。可能发生如下两个反应:
主反应:C HC H(g) C HCH=CH(g)+H(g) ΔH =+117.5kJ·mol−1
6 5 2 5 6 5 2 2 1
副反应:C HC H(g)+H(g) C HCH(g)+CH(g) ΔH
6 5 2 5 2 6 5 3 4 2
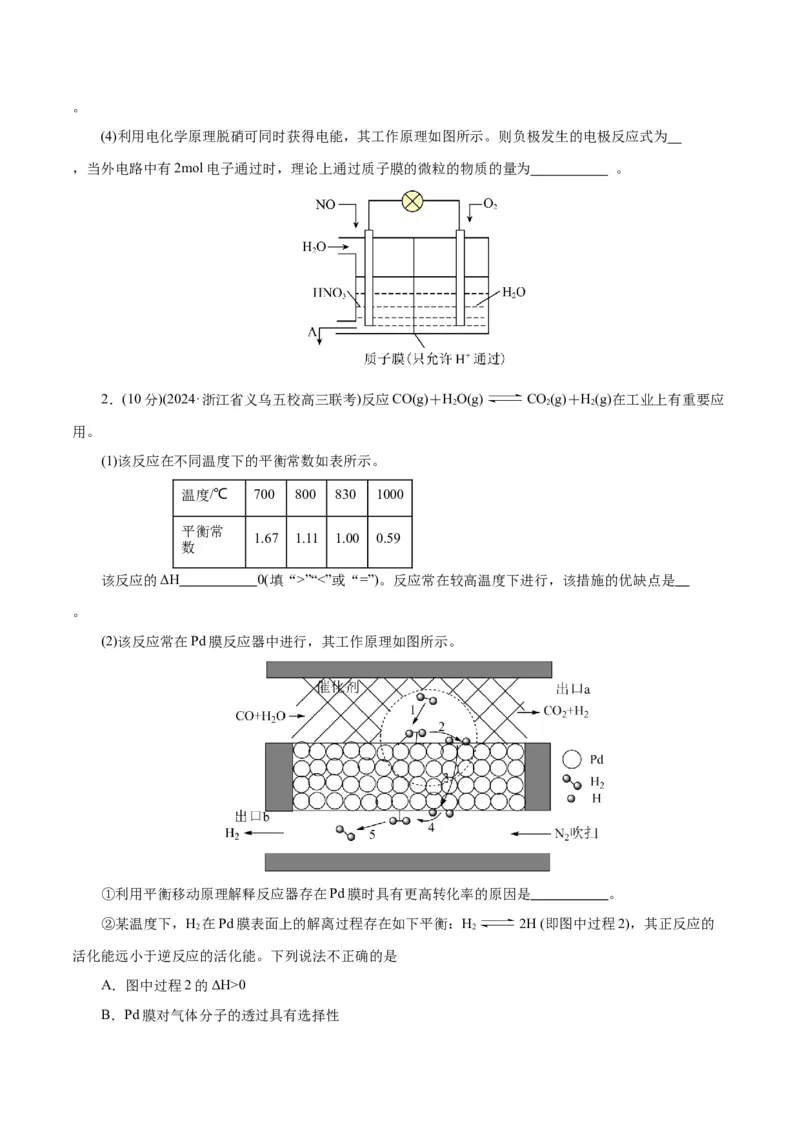
(1)已知,在298K、101kPa条件下,某些物质的相对能量( )变化关系如图所示:
ΔH= kJ·mol−1。
2
(2)在不同的温度条件下,以水烃比 投料,在膜反应器中发生乙苯脱氢反应。膜反应
器可以通过多孔膜移去H,提高乙苯的平衡转化率,原理如图所示。
2
已知 移出率
①忽略副反应。维持体系总压强p恒定,在温度T时,已知乙苯的平衡转化率为 , 的移出率为
b,则在该温度下主反应的平衡常数K = (用 等符号表示)。[对于气相反应,用某组分B的平
P衡压强 代替物质的量浓度 也可表示平衡常数,记作kJ·mol−1,如 ,p为平衡总压
强, 为平衡系统中B的物质的量分数];
②乙苯的平衡转化率增长百分数与 的移出率在不同温度条件下的关系如下表:
温度/℃
增长百分数/% 700 950 1000
移出率/%
60 8.43 4.38 2.77
80 16.8 6.1 3.8
90 27 7.1 4.39
高温下副反应程度极小。试说明当温度高于950℃时,乙苯的平衡转化率随 的移去率的变化改变程
度不大的原因: ;
③下列说法正确的是 。
A.生成H 的总物质的量与苯乙烯相等
2
B.因为H 被分离至隔离区,故反应器中不发生副反应
2
C.在恒容的膜反应器中,其他条件不变,增大水烃比,可提高乙苯的转化率
D.膜反应器可降低反应温度,减少副反应的影响
(3)不同催化剂效能与水烃比有关。保持体系总压为常压的条件下,水烃比为9(曲线Ⅰ)时乙苯的平衡
转化率与温度的关系的示意图如下:
①请在图中画出水烃比为1时乙苯的平衡转化率与温度的关系曲线(曲线Ⅱ) ;
②工业上,减小水烃比是降低苯乙烯脱氢装置能耗的一个重要方向。若其他条件不变,减少水烃比,
为使反应从起始到平衡均达到或接近原有的反应速率、限度,则可相应的改变的条件: 。
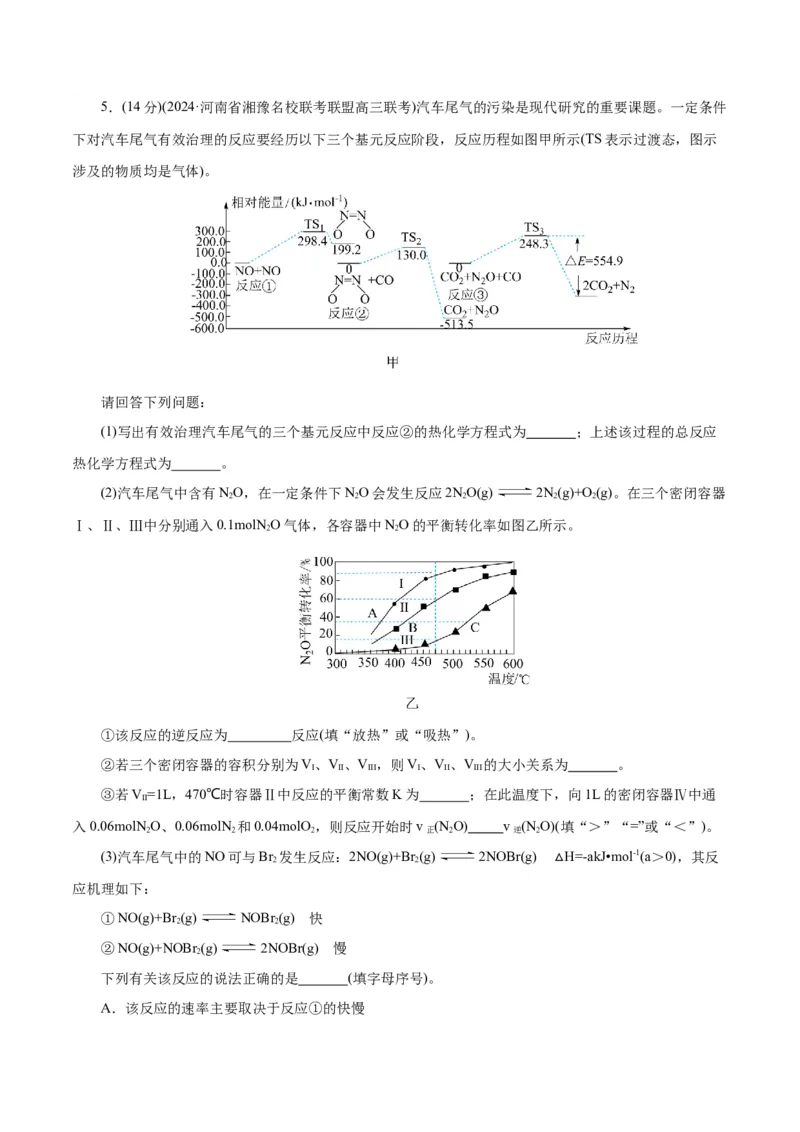
A.升温 B.降温 C.增压 D.减压 E.催化剂5.(14分)(2024·河南省湘豫名校联考联盟高三联考)汽车尾气的污染是现代研究的重要课题。一定条件
下对汽车尾气有效治理的反应要经历以下三个基元反应阶段,反应历程如图甲所示(TS表示过渡态,图示
涉及的物质均是气体)。
请回答下列问题:
(1)写出有效治理汽车尾气的三个基元反应中反应②的热化学方程式为 ;上述该过程的总反应
热化学方程式为 。
(2)汽车尾气中含有NO,在一定条件下NO会发生反应2NO(g) 2N(g)+O(g)。在三个密闭容器
2 2 2 2 2
Ⅰ、Ⅱ、Ⅲ中分别通入0.1molNO气体,各容器中NO的平衡转化率如图乙所示。
2 2
①该反应的逆反应为 反应(填“放热”或“吸热”)。
②若三个密闭容器的容积分别为V、V 、V ,则V、V 、V 的大小关系为 。
I II III I II III
③若V =1L,470℃时容器Ⅱ中反应的平衡常数K为 ;在此温度下,向1L的密闭容器Ⅳ中通
II
入0.06molNO、0.06molN 和0.04molO,则反应开始时v (N O) v (N O)(填“>”“=”或“<”)。
2 2 2 正 2 逆 2
(3)汽车尾气中的NO可与Br 发生反应:2NO(g)+Br (g) 2NOBr(g) H=-akJ•mol-1(a>0),其反
2 2
应机理如下: △
①NO(g)+Br (g) NOBr (g) 快
2 2
②NO(g)+NOBr (g) 2NOBr(g) 慢
2
下列有关该反应的说法正确的是 (填字母序号)。
A.该反应的速率主要取决于反应①的快慢B.NOBr 是该反应的催化剂
2
C.正反应的活化能比逆反应的活化能小akJ•mol-1
D.增大Br (g)的浓度能增大活化分子百分数,加快反应速率
2
6.(15分)(2024·云南部分名校高三联考理科综合)氨是一种重要的化工原料,可用于制造铵态化肥。已
知:N(g)+3H(g) 2NH (g) ΔH=-91kJ/mol。回答下列问题:
2 2 3
(1)已知上述反应的熵变(ΔS)为-198.9J·mol-1·K-1,该反应能自发进行的温度可能是___________(填标号)。
A.25 ℃ B.150 ℃ C.1273 ℃ D.1457.5 ℃
(2)在恒温恒容条件下,充入等物质的量的N 和H 合成氨气,下列情况表明该反应达到平衡状态的是
2 2
___________(填标号)。
A.混合气体密度不随时间变化 B.N 体积分数不随时间变化
2
C.混合气体总压强不随时间变化 D.H 与 NH 的消耗速率之比为3∶2
2 3
(3)在催化剂作用下,合成氨的反应速率为 (k为速率常数,只与温度、
催化剂有关,与浓度无关。a、β、γ为反应级数,可取正整数、负整数、0,也可取分数)。 为了测定反应
级数,在一定温度下进行实验,其结果如下:
序号 c(N)/(mol·L-1) c(H)/(mol·L-1) c(NH )/( mol·L-1) 反应速率
2 2 3
I 1 1 1 V
Ⅱ 2 1 1 2v
Ⅲ 1 4 1 16v
Ⅳ 1 4 2 16v
①α+β+γ=
②已知经验公式为 (其中,E、k分别为活化能、速率常数,R、C为常数,T为温度)。
a
在催化剂作用下,测得Rlnk与温度( )的关系如图1所示。催化效率较高的是 (填“Catl”或“Cat2”),在Cat2催化剂作用下。活化能E 为
a
(4)在体积均为2L的甲、乙两恒容密闭容器中分别通入 l mol N2和3mol H
2
,分别在不同条件下达到平
衡,测得 NH₃的物质的量与时间的关系如图2所示。
①相对甲,乙仅改变的一个条件是 ,正反应速率:a (填“>”、“<”或
“=”)b。
②在该条件下,乙的平衡常数为 (结果保留2位小数)。
7.(14分)(2023·广东湛江高二毕业班调研考试)2023年5月,中国神舟十六号载人飞船成功发射,三
位航天员景海鹏、朱杨柱、桂海潮在天宫空间站开启长达半年的太空生活。
(1)法国化学家Paul Sabatier提出并命名的“Sabatier反应”实现了CO 甲烷化,科技人员基于该反应设
2
计如图过程完成空间站中CO 与O 的循环,从而实现O 的再生。
2 2 2
①写出与CH 具有相同空间结构的一种微粒: 。
4
②在特定温度下,由稳定态单质生成1mol化合物的焓变叫做该物质在此温度下的标准摩尔生成焓。
表中为几种物质在298K的标准生成焓。
物质 CO(g) CH(g) HO(g) H(g)
2 4 2 2
标准摩尔生成焓/(kJ·mol-1) -393.51 -74.85 -241.82 0
则Sabatier反应CO(g)+4H (g) CH (g)+2 HO(g) ΔH kJ·mol-1。
2 2 4 2
③下列有关Sabatier反应说法正确的是 。
A.输送进入Sabatier反应器的是电解水装置的阴极产物
B.采用高压和合适催化剂均有利于提高Sabatier反应的转化率
C.恒温条件下,在刚性容器中发生Sabatier反应,气体密度不变时,说明反应达到平衡D.应该在Sabatier反应器的前端维持较高温度,后端维持较低温度
④一定条件下,CH 分解形成碳的反应历程如图所示,其中决定反应速率的是第 步反应。
4
(2)航天员呼吸产生的CO 还可以利用Bosch反应:CO(g)+2H (g) C(s)+ 2HO(g) 代替Sabatier
2 2 2 2
反应。在250℃时,向体积为2L恒容密闭容器中通入2molH 和1molCO 发生Bosch反应,测得容器内气
2 2
压变化如图所示。
①试解释容器内气压先增大后减小的原因: 。
②该温度下Bosch反应的K= (写出计算过程,K 为用气体的分压表示的平衡常数,分压=
p p
气体的体积分数×体系总压)。
③在上图基础上画出其他条件相同,向体系加入催化剂时其压强随时间的变化曲线。
8.(15分)研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C HN)。
2 8 2
已知:①C HN(l)+4O(g)===2CO (g)+N(g)+4HO(l) ΔH=-2 765.0 kJ·mol-1
2 8 2 2 2 2 2 1
②2O(g)+N(g)===N O(l) ΔH=-19.5 kJ·mol-1
2 2 2 4 2
③HO(g)===H O(l) ΔH=-44.0 kJ·mol-1
2 2 3
则C HN(l)+2NO(l)===3N (g)+2CO(g)+4HO(g)的ΔH为__________。
2 8 2 2 4 2 2 2
(2)碘蒸气存在能大幅度提高NO的分解速率,反应历程为
2
第一步:I(g)→2I(g)(快反应)
2
第二步:I(g)+NO(g)→N (g)+IO(g)(慢反应)
2 2
第三步:IO(g)+NO(g)→N (g)+O(g)+I(g)(快反应)
2 2 2
实验表明,含碘时 NO 分解速率方程 v=k·c(N O)·[c(I)]0.5(k 为速率常数)。下列表述正确的是
2 2 2
________(填字母)。
A.NO分解反应中,k值与碘蒸气浓度大小有关 B.v(第二步的逆反应)<v(第三步反应)
2C.IO为反应的催化剂 D.第二步活化能比第三步大
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和
NO 发生反应:2NO(g)+2CO(g)===N (g)+2CO(g) ΔH=-746.8 kJ·mol-1。实验测得:v =k
2 2 正
·p2(NO)·p2(CO),v =k ·p(N )·p2(CO)。其中k 、k 分别为正、逆反应速率常数,只与温度有关;p为
正 逆 逆 2 2 正 逆
气体分压(分压=物质的量分数×总压)。
①达到平衡后,仅升高温度,k 增大的倍数__________(填“大于”“小于”或“等于”)k 增大的倍
正 逆
数。
②一定温度下在刚性密闭容器中充入CO、NO和N 的物质的量之比为2∶2∶1,压强为p。达平衡时
2 0
压强为0.9p,则=__________。
0
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数K :
p
ⅰ.3N H(l)===4NH(g)+N(g) ΔH K
2 4 3 2 1 p1
ⅱ.4NH(g)===2N (g)+6H(g) ΔH K
3 2 2 2 p2
绘制pK -T和pK -T的线性关系如图所示(已知:pK =-lg K ):
p1 p2 p p
①由图可知,ΔH________(填“>”或“<”)0。
1
②反应3NH(l)===3N (g)+6H(g)的K=________(用K 、K 表示);该反应的ΔH________(填“>”
2 4 2 2 p1 p2
或“<”)0,写出推理过程:______________________________________________。