文档内容
专题 09 化学反应速率与化学平衡
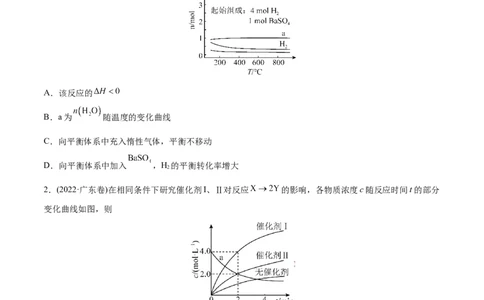
1.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,各
组分的物质的量(n)如图所示。下列说法正确的是
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
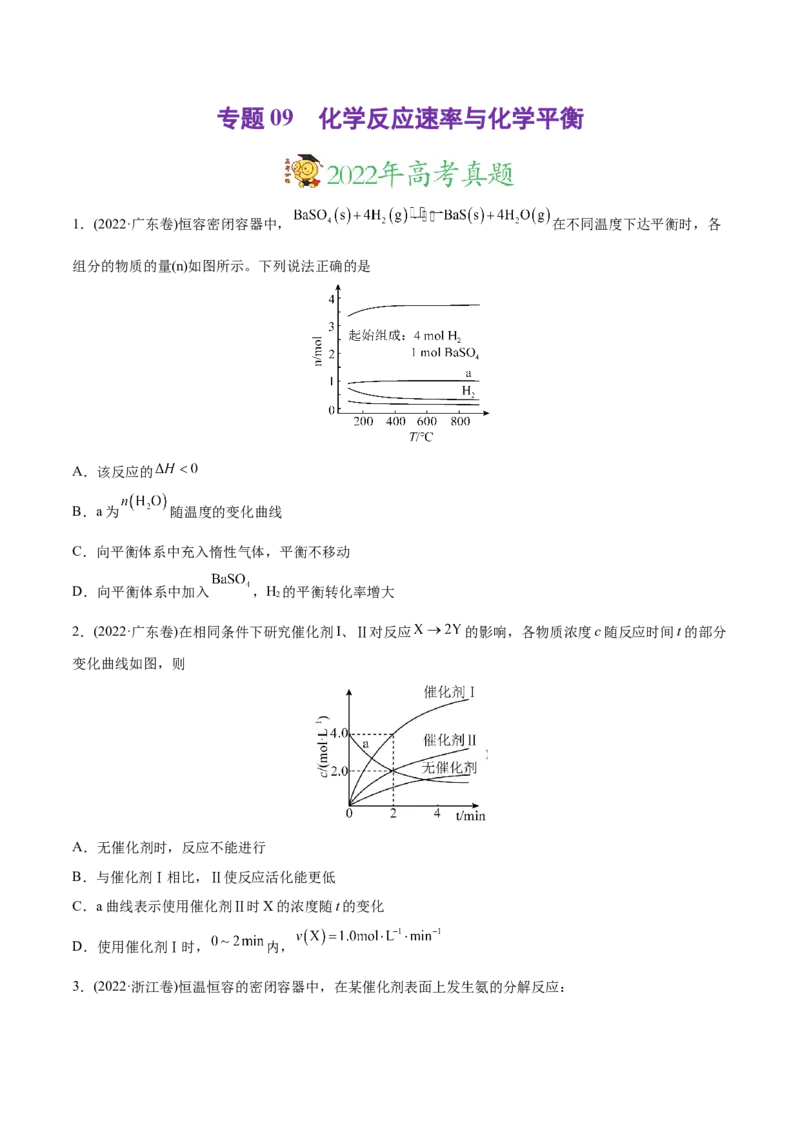
2.(2022·广东卷)在相同条件下研究催化剂I、Ⅱ对反应 的影响,各物质浓度c随反应时间t的部分
变化曲线如图,则
A.无催化剂时,反应不能进行
B.与催化剂Ⅰ相比,Ⅱ使反应活化能更低
C.a曲线表示使用催化剂Ⅱ时X的浓度随t的变化
D.使用催化剂Ⅰ时, 内,
3.(2022·浙江卷)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下
列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
4.(2022·浙江卷)关于反应 ,达到平衡后,下列说法不
正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明
上述反应存在限度
5.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
1.(2022·安徽·芜湖一中一模)北京时间10月6日晚,2021年诺贝尔化学奖授予 Benjamin List和David
W.C.MacMillan,以奖励他们“对于有机小分子不对称催化的重要贡献”。不对称催化剂具有选择性。下
列说法错误的是
A.催化剂不仅可以是金属催化剂和酶,也可以是有机小分子
B.不对称催化剂可以提高目标产物在最终产物中的比率
C.催化剂在反应前后的质量和性质不变
D.“不对称有机催化”对医药研究和绿色化学有极为重要的意义
2.(2022·安徽·淮北市教育科学研究所一模)向30mL1.0mol•L-1的HSO 和3mL30%的HO 的混合溶液中加
2 4 2 2
入经处理过的铁丝,铁丝表面产生气泡,随后消失,再产生气泡,再消失,周而往复,振荡周期为20s左
右,可维持数小时。一种可能的反应机理为:
(a)Fe+2H+=Fe2++H ↑
2
(b)2Fe2++H O+H O=Fe O+4H+
2 2 2 2 3
(c)Fe O+6H+=2Fe3++3H O
2 3 2
(d)2Fe3++H =2Fe2++2H+
2
下列说法错误的是
A.该振荡反应与H+浓度的变化有关 B.Fe O、Fe3+为中间产物
2 3
C.冰水浴比室温条件下的振荡周期要短 D.由该机理可知:产生的气体是H
2
3.(2022·内蒙古·包钢一中一模)一定温度下,在三个体积均为1L的恒容密闭容器中发生反应:2CHOH(g)
3
CHOCH (g)+HO(g)
3 3 2
容器编
温度(℃) 起始物质的量(mol) 平衡物质的量(mol)号 CHOH(g) CHOCH (g) HO(g)
3 3 3 2
① 387 0.20 0.080 0.080
② 387 0.40
③ 207 0.20 0.090 0.090
下列说法正确的是A.该反应的正反应为吸热反应
B.达到平衡时,容器①中的CHOH体积分数比容器②中的小
3
C.若容器①中反应达到平衡时增大压强,则各物质浓度保持增大
D.若起始向容器①中充入CHOH 0.10mol、CHOCH 0.10mol、HO 0.10mol,则反应将向逆反应方向进行
3 3 3 2
4.(2021·河南信阳·模拟预测)常压下羰基化法精炼镍的原理为 。 时,
该反应的平衡常数 。
已知: 的沸点为 ,固体杂质不参与反应。
第一阶段:将粗镍与 反应转化成气态 ;
第二阶段:将第一阶段反应后的气体分离出来,加热至 制得高纯镍。
下列判断正确的是
A. 是离子化合物
B.第一阶段,反应体系的温度应控制在 以上,以达到气化分离的目的
C.反应达到平衡状态以后,保持体积不变通入 ,平衡正向移动,反应的平衡常数增大
D.第二阶段,可以通过增大压强来提高 分解率
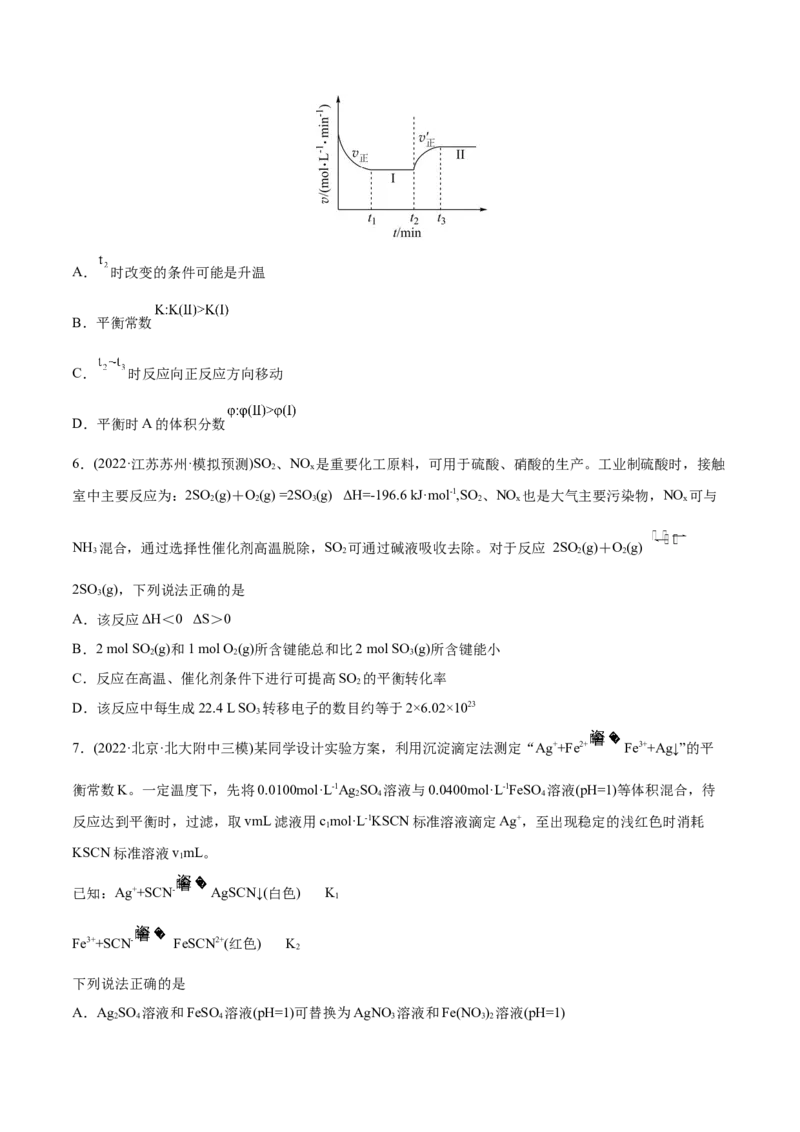
5.(2022·新疆乌鲁木齐·一模)已知: ,向一恒温恒容的密闭容器中充入
和 发生反应, 时达到平衡状态I。在 时改变某一条件, 时重新达到平衡状态II,正反应速率随
时间的变化如图所示。下列说法正确的是A. 时改变的条件可能是升温
B.平衡常数
C. 时反应向正反应方向移动
D.平衡时A的体积分数
6.(2022·江苏苏州·模拟预测)SO 、NO 是重要化工原料,可用于硫酸、硝酸的生产。工业制硫酸时,接触
2 x
室中主要反应为:2SO (g)+O(g) =2SO (g) ΔH=-196.6 kJ·mol-1,SO、NO 也是大气主要污染物,NO 可与
2 2 3 2 x x
NH 混合,通过选择性催化剂高温脱除,SO 可通过碱液吸收去除。对于反应 2SO (g)+O(g)
3 2 2 2
2SO (g),下列说法正确的是
3
A.该反应ΔH<0 ΔS>0
B.2 mol SO (g)和1 mol O (g)所含键能总和比2 mol SO (g)所含键能小
2 2 3
C.反应在高温、催化剂条件下进行可提高SO 的平衡转化率
2
D.该反应中每生成22.4 L SO 转移电子的数目约等于2×6.02×1023
3
7.(2022·北京·北大附中三模)某同学设计实验方案,利用沉淀滴定法测定“Ag++Fe2+ Fe3++Ag↓”的平
衡常数K。一定温度下,先将0.0100mol·L-1Ag SO 溶液与0.0400mol·L-1FeSO 溶液(pH=1)等体积混合,待
2 4 4
反应达到平衡时,过滤,取vmL滤液用cmol·L-1KSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗
1
KSCN标准溶液vmL。
1
已知:Ag++SCN- AgSCN↓(白色) K
1
Fe3++SCN- FeSCN2+(红色) K
2
下列说法正确的是
A.Ag SO 溶液和FeSO 溶液(pH=1)可替换为AgNO 溶液和Fe(NO ) 溶液(pH=1)
2 4 4 3 3 2B.K>>K ,Fe3+是滴定终点的指示剂
1 2
C.若不过滤,直接用浊液做滴定实验测定c(Ag+),则所测K值偏大
D.若改为测定滤液中c(Fe3+),选择合适的滴定方法直接滴定滤液,也能达到目的
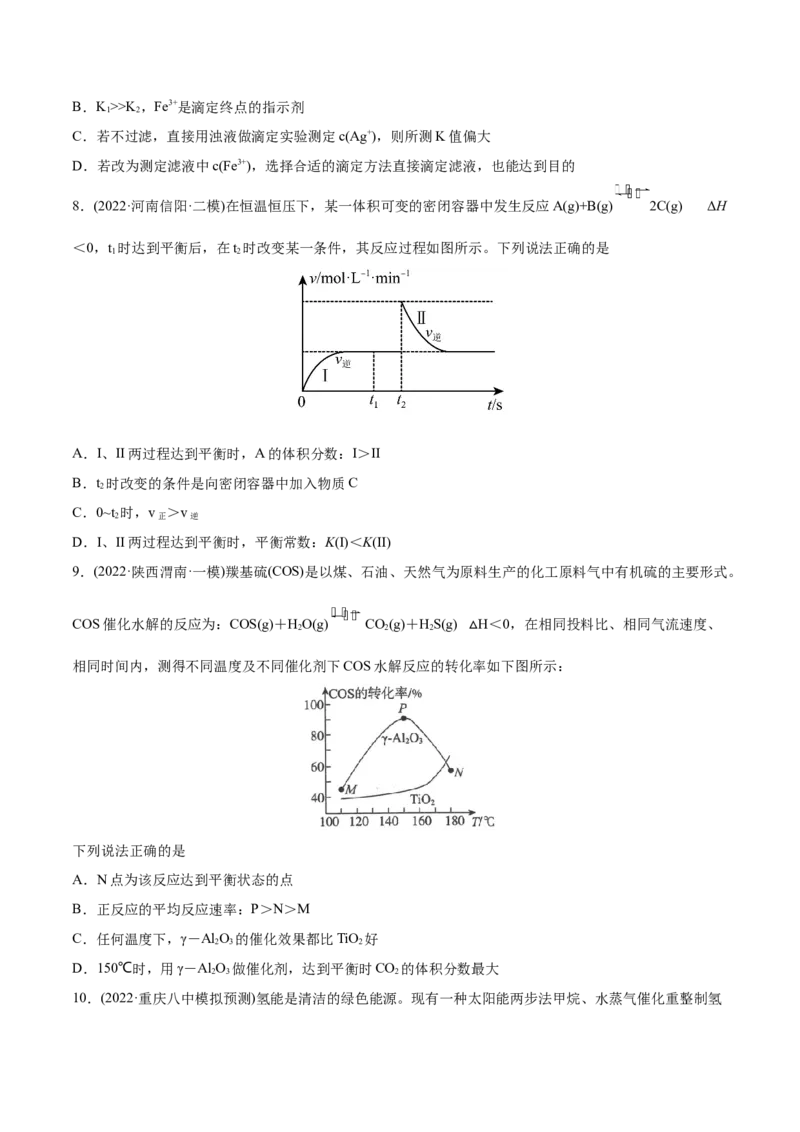
8.(2022·河南信阳·二模)在恒温恒压下,某一体积可变的密闭容器中发生反应A(g)+B(g) 2C(g) ΔH
<0,t 时达到平衡后,在t 时改变某一条件,其反应过程如图所示。下列说法正确的是
1 2
A.I、II两过程达到平衡时,A的体积分数:I>II
B.t 时改变的条件是向密闭容器中加入物质C
2
C.0~t 时,v >v
2 正 逆
D.I、II两过程达到平衡时,平衡常数:K(I)<K(II)
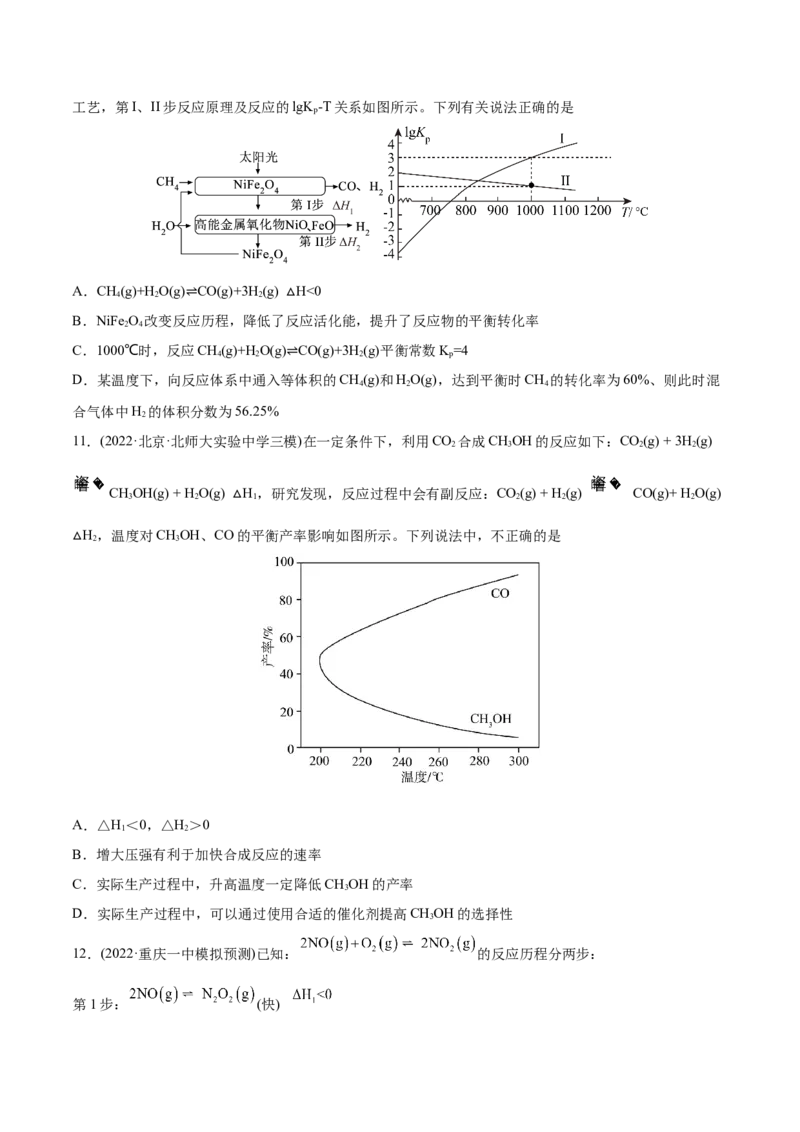
9.(2022·陕西渭南·一模)羰基硫(COS)是以煤、石油、天然气为原料生产的化工原料气中有机硫的主要形式。
COS催化水解的反应为:COS(g)+HO(g) CO(g)+HS(g) H<0,在相同投料比、相同气流速度、
2 2 2
△
相同时间内,测得不同温度及不同催化剂下COS水解反应的转化率如下图所示:
下列说法正确的是
A.N点为该反应达到平衡状态的点
B.正反应的平均反应速率:P>N>M
C.任何温度下,γ-Al O 的催化效果都比TiO 好
2 3 2
D.150℃时,用γ-Al O 做催化剂,达到平衡时CO 的体积分数最大
2 3 2
10.(2022·重庆八中模拟预测)氢能是清洁的绿色能源。现有一种太阳能两步法甲烷、水蒸气催化重整制氢工艺,第I、II步反应原理及反应的lgK -T关系如图所示。下列有关说法正确的是
p
A.CH(g)+HO(g) CO(g)+3H(g) H<0
4 2 2
B.NiFe
2
O
4
改变反⇌应历程,降低了反△应活化能,提升了反应物的平衡转化率
C.1000℃时,反应CH(g)+HO(g) CO(g)+3H(g)平衡常数K=4
4 2 2 p
D.某温度下,向反应体系中通入等⇌体积的CH
4
(g)和H
2
O(g),达到平衡时CH
4
的转化率为60%、则此时混
合气体中H 的体积分数为56.25%
2
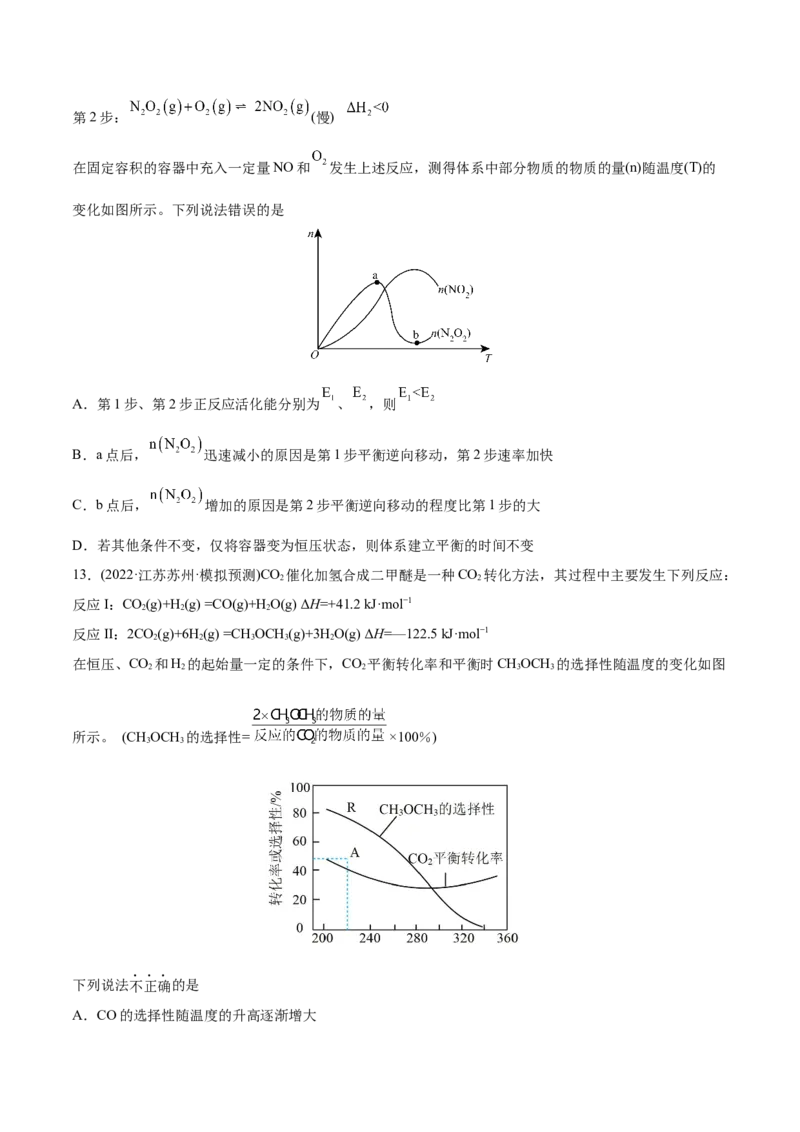
11.(2022·北京·北师大实验中学三模)在一定条件下,利用CO 合成CHOH的反应如下:CO(g) + 3H(g)
2 3 2 2
CHOH(g) + H O(g) H,研究发现,反应过程中会有副反应:CO(g) + H(g) CO(g)+ H O(g)
3 2 1 2 2 2
△
H,温度对CHOH、CO的平衡产率影响如图所示。下列说法中,不正确的是
2 3
△
A.△H<0,△H>0
1 2
B.增大压强有利于加快合成反应的速率
C.实际生产过程中,升高温度一定降低CHOH的产率
3
D.实际生产过程中,可以通过使用合适的催化剂提高CHOH的选择性
3
12.(2022·重庆一中模拟预测)已知: 的反应历程分两步:
第1步: (快)第2步: (慢)
在固定容积的容器中充入一定量NO和 发生上述反应,测得体系中部分物质的物质的量(n)随温度(T)的
变化如图所示。下列说法错误的是
A.第1步、第2步正反应活化能分别为 、 ,则
B.a点后, 迅速减小的原因是第1步平衡逆向移动,第2步速率加快
C.b点后, 增加的原因是第2步平衡逆向移动的程度比第1步的大
D.若其他条件不变,仅将容器变为恒压状态,则体系建立平衡的时间不变
13.(2022·江苏苏州·模拟预测)CO 催化加氢合成二甲醚是一种CO 转化方法,其过程中主要发生下列反应:
2 2
反应I:CO(g)+H(g) =CO(g)+H O(g) ΔH=+41.2 kJ·mol−1
2 2 2
反应II:2CO(g)+6H(g) =CH OCH (g)+3HO(g) ΔH=—122.5 kJ·mol−1
2 2 3 3 2
在恒压、CO 和H 的起始量一定的条件下,CO 平衡转化率和平衡时CHOCH 的选择性随温度的变化如图
2 2 2 3 3
所示。 (CHOCH 的选择性= ×100%)
3 3
下列说法不正确的是
A.CO的选择性随温度的升高逐渐增大B.反应2CO(g)+4H(g)=CH OCH (g)+HO(g) ΔH=—204.9 kJ·mol−1
2 3 3 2
C.在240~320℃范围内,温度升高,平衡时CHOCH 的物质的量先增大后减小
3 3
D.反应一段时间后,测得CHOCH 的选择性为48%(图中A点),增大压强可能将CHOCH 的选择性提升
3 3 3 3
到B点
14.(2022·江苏·扬州中学三模)液氨是一种很好的溶剂,液氨可以微弱的电离产生NH 和NH 。NH 中的
3
一个H原子若被-NH 取代可形成NH(联氨),若被-OH取代可形成NH OH(羟胺)。在有NH 存在时,
2 2 4 2
Cu(OH) 能溶于氨水形成[Cu(NH )]2+。NH 经过一定的转化可以形成N、NO、NO 、NO(无色)、HNO 等。
2 3 4 3 2 2 2 4 3
对于反应2NO (g) NO(g),下列说法正确的是
2 2 4
A.该反应的H >0
B.该反应的平衡常数表达式为K=
C.升高温度,该反应的正反应速率减小,逆反应速率增大
D.将反应器容积压缩为原来的一半,气体颜色比压缩前深
15.(2022·重庆市育才中学模拟预测)25℃时,恒容密闭容器中只含有X,发生反应: ,
X的起始压强为 ,X分解的速率方程为: ,其中k定温下为常数。生成的Y可快速建立平
衡: ,平衡常数 。下列说法正确的是
A.当X分解的速率 时,W的压强为
B.若升高温度,Z和W的物质的量之比为 ,则
C.相同时间内,X的平均速率是Y的平均速率的2倍
D.若缩小体积,则单位时间内X的转化率减小
16.(2022·上海上海·二模)有研究认为,强碱性环境下反应:I-+ClO- IO-+Cl-可能分如下三步进行:
第一步:ClO-+H O HClO+OH- K=3.3×10-10
2 1
第二步:…… K=……
2第三步:HIO+OH- IO-+H O K=2.3×103
2 3
下列说法正确的是
A.第二步反应的平衡常数表达式为K=
2
B.由K值大小可以判断第三步反应比第一步快
C.升高温度会使K 变小、K 变大
1 3
D.OH-是该反应的催化剂
17.(2022·湖南·长郡中学模拟预测)在体积为2L的恒温密闭容器中充入 和 ,发生下
述反应: ,10min后达到平衡, 为0.4mol。下列说法正确的是
A.0~10min内,用 表示的平均反应速率为
B.当混合气体的密度不再改变时,可以表示反应达到平衡状态
C.若升高温度 ,反应的平衡常数减小,则平衡时 的物质的量变化
D.平衡后,如果此时移走 和 ,在相同温度下达到平衡时 的物质的量小于
0.2mol