文档内容
专题三 金属及其化合物 能力提升检测卷
(本卷共20小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 K 39
Ca 40 Mn 55 Fe 56 Ni 59 Cu 64
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.“嫦娥五号”中使用了大量合金。下列有关金属或合金的说法中不正确的是
A.生铁属于合金
B.一般合金的熔点比各成分金属的低
C.合金的化学性质与其成分金属的化学性质不同
D.改变原料的配比、生成合金的条件,可以得到具有不同性能的合金
2.生活中处处有化学,下列叙述正确的是
A.铅笔芯的成分为二氧化铅
B.青铜和黄铜是不同结构的单质铜
C.碳酸氢钠可做食品膨松剂
D.焰火中红色来源于钠盐灼烧
3.生活因化学更美好。以下生活用途和化学原理都正确且具有对应关系的是
选
生活用途 化学原理
项
A 维生素C帮助人体将 转化为易吸收的 维生素C具有还原性
B 葡萄酒中添加二氧化硫 二氧化硫具有漂白性
C 过氧化钠用作呼吸面具中的供氧剂 过氧化钠分解放出氧气
D 明矾可用作净水剂和消毒剂 铝离子水解生成氢氧化铝胶体
4.《天工开物》中“治铁"原典中记载:“凡治铁成器,取已炒熟铁为之……凡炉中炽铁用炭,煤炭
居十七,木炭居十三……即用煤炭也别有铁炭一种,取其火性内攻、焰不虚腾者,与炊炭同行而有分类
也……”。下列说法正确的是
A.熟铁是纯净的铁单质,生铁是铁和碳的混合物
B.治铁过程只涉及化合反应与置换反应,
C.铁炭和炊炭均为碳元素的同素异形体D.治铁用到的煤炭和木炭均可还原铁的氧化物
5.2022年春晚上,《只此青绿》惊艳了许多观众,生动还原了北宋名画——《千里江山图》。下列
说法合理的是
A.《千里江山图》中青色来自蓝铜矿颜料[ ]可表示为
B.《千里江山图》中绿色颜料铜绿的主要成分是氢氧化铜
C.《千里江山图》中的红色来自赭石(Fe O),其性质稳定,不易被空气氧化
2 3
D.《千里江山图》的画布材质为麦青色的蚕丝织品——绢,绢的主要成分是纤维素
6.关于北京冬奥会火炬,下列说法错误的是
A.外壳是碳纤维,属于有机高分子材料
B.氢气作燃料对环境友好无污染
C.点火段材料使用铝合金是因为其密度小、性质稳定
D.含钠元素的特殊配方使火焰呈黄色
7.下列说法正确的是
A.NaO在空气中加热可得固体NaO
2 2 2
B.Mg加入到过量FeCl 溶液中可得Fe
3
C.FeS 在沸腾炉中与O 反应主要生成SO
2 2 3
D.HO 溶液中加入少量MnO 粉末生成H 和O
2 2 2 2 2
8.硫酸铁溶液中加入少量Fe粉,溶液颜色变浅,要证明该过程发生了氧化还原反应,加入下列试剂
一定可行的是
A.KSCN溶液 B.酸性高锰酸钾溶液
C.NaOH溶液 D.铜粉
9.核潜艇上的核反应堆使用液态铝钠合金作载热介质。有关说法中正确的是
A.该合金的熔点介于钠、铝之间 B.铝钠合金的良好传热性与自由电子有关
C.钠或铝形成的氧化物均为碱性氧化物D.原子半径钠大于铝,金属键钠强于铝
10.下列离子方程式中,能正确表达反应颜色变化的是
A.将“84”消毒液和洁厕灵混用会产生黄绿色气体:ClO-+Cl-+H O=Cl ↑+2OH-
2 2B.向Mg(OH) 浊液中滴加足量FeCl 溶液出现红褐色沉淀:3Mg(OH) +2Fe3+=2Fe(OH) +3Mg2+
2 3 2 3
C.将SO 通入溴水中使其褪色:SO +2HO+Br =2H++SO +2HBr
2 2 2 2
D.NaO 在空气中放置后由淡黄色变为白色:2NaO=2Na O+O↑
2 2 2 2 2 2
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项
是符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只
选一个且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.某溶液含Na+、NH 、SO 、Cl-、Fe2+、Fe3+中的几种,且各离子浓度相同。为确定其组成,进行
实验:①取少量溶液,加入足量HNO 酸化的Ba(NO )(aq),产生白色沉淀,过滤;②向滤液中加入足量的
3 3 2
NaOH(aq),产生红褐色沉淀,微热,产生气体。关于原溶液的说法正确的是
A.肯定没有Fe3+ B.需通过焰色反应确定Na+是否存在
C.Fe2+、Fe3+都存在 D.存在NH 、SO 、Cl-、Fe2+
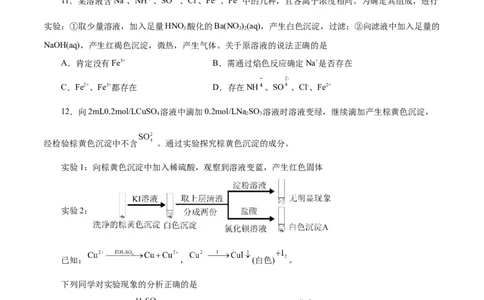
12.向2mL0.2mol/LCuSO 溶液中滴加0.2mol/LNa SO 溶液时溶液变绿,继续滴加产生棕黄色沉淀,
4 2 3
经检验棕黄色沉淀中不含 。通过实验探究棕黄色沉淀的成分。
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2:
已知: , (白色) 。
下列同学对实验现象的分析正确的是
A.实验1中加入稀 后溶液变蓝可证实棕黄色沉淀中含有
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有
C.实验2中加入淀粉溶液后无明显现象,说明不存在
D.在 的存在下, 与 发生了氧化还原反应,产生CuI沉淀和 ,说明棕黄色沉淀中含有和
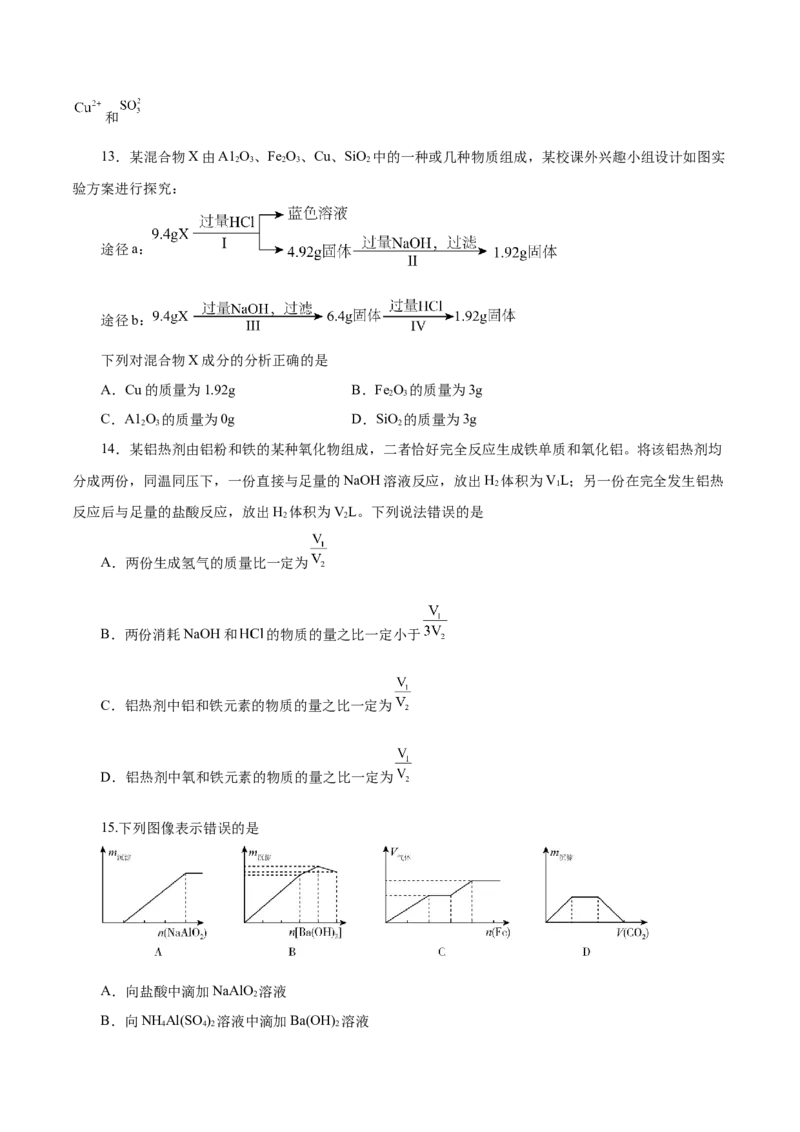
13.某混合物X由A1 O、Fe O、Cu、SiO 中的一种或几种物质组成,某校课外兴趣小组设计如图实
2 3 2 3 2
验方案进行探究:
途径a:
途径b:
下列对混合物X成分的分析正确的是
A.Cu的质量为1.92g B.Fe O 的质量为3g
2 3
C.A1 O 的质量为0g D.SiO 的质量为3g
2 3 2
14.某铝热剂由铝粉和铁的某种氧化物组成,二者恰好完全反应生成铁单质和氧化铝。将该铝热剂均
分成两份,同温同压下,一份直接与足量的NaOH溶液反应,放出H 体积为VL;另一份在完全发生铝热
2 1
反应后与足量的盐酸反应,放出H 体积为VL。下列说法错误的是
2 2
A.两份生成氢气的质量比一定为
B.两份消耗NaOH和 的物质的量之比一定小于
C.铝热剂中铝和铁元素的物质的量之比一定为
D.铝热剂中氧和铁元素的物质的量之比一定为
15.下列图像表示错误的是
A.向盐酸中滴加NaAlO 溶液
2
B.向NH Al(SO ) 溶液中滴加Ba(OH) 溶液
4 4 2 2C.向HSO 和HNO 物质的量2:1的混合稀酸溶液中逐渐加入 粉
2 4 3
D.向NaOH和Ca(OH) 物质的量2:1的混合溶液中通入CO
2 2
第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
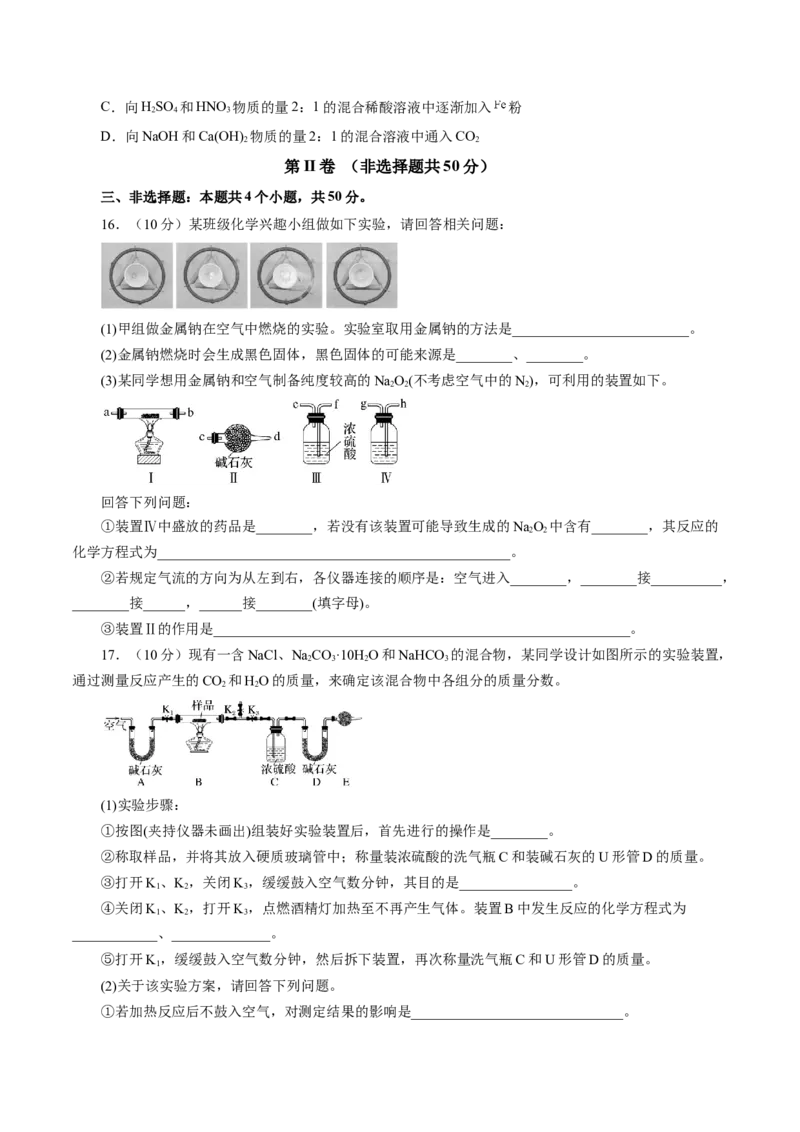
16.(10分)某班级化学兴趣小组做如下实验,请回答相关问题:
(1)甲组做金属钠在空气中燃烧的实验。实验室取用金属钠的方法是_________________________。
(2)金属钠燃烧时会生成黑色固体,黑色固体的可能来源是________、________。
(3)某同学想用金属钠和空气制备纯度较高的NaO(不考虑空气中的N),可利用的装置如下。
2 2 2
回答下列问题:
①装置Ⅳ中盛放的药品是________,若没有该装置可能导致生成的NaO 中含有________,其反应的
2 2
化学方程式为__________________________________________________。
②若规定气流的方向为从左到右,各仪器连接的顺序是:空气进入________,________接__________,
________接______,______接________(填字母)。
③装置Ⅱ的作用是___________________________________________________________。
17.(10分)现有一含NaCl、NaCO·10H O和NaHCO 的混合物,某同学设计如图所示的实验装置,
2 3 2 3
通过测量反应产生的CO 和HO的质量,来确定该混合物中各组分的质量分数。
2 2
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C和装碱石灰的U形管D的质量。
③打开K、K,关闭K,缓缓鼓入空气数分钟,其目的是________________。
1 2 3
④关闭K、K,打开K,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为
1 2 3
____________、______________。
⑤打开K,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C和U形管D的质量。
1
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是______________________________。②E处干燥管中盛放的药品是________,其作用是___________________________________,
如果实验中没有该装置,则会导致测得的NaHCO 的质量________(填“偏大”“偏小”或“无影
3
响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m g、m g,则混合物中NaCO·10H O的
1 2 2 3 2
质量分数为____________(用含w、m、m 的代数式表示)。
1 2
18.(15分)为探究Fe2+与SCN-能否形成配位化合物,某研究性学习小组进行如图实验:
探究Ⅰ
(1)配制FeSO 溶液应使用________的蒸馏水。
4
(2)已知溶液颜色越深,色度越大。测得实验i、ii、iii色度数据如表:
实验 i ii iii
色度 0.075 0.049 0.015
实验i的作用是________,甲同学推测实验iii色度比实验ii小的原因可能有:①Mg2+和Fe2+对配合物
解离影响不同;②______________________________________________。
探究Ⅱ
(3)X为________,实验iv的红色比实验v深的原因为________。
(4)在探究Ⅰ的基础上进行探究Ⅱ的目的为__________________________________。
(5)分析可利用KSCN溶液检测Fe2+、Fe3+混合溶液中Fe3+的原因:________。
19.(15分)磷酸铁(FePO )常用作电极材料。以硫铁矿(主要成分是FeS,含少量Al O、SiO 和
4 2 2 3 2
Fe O)为原料制备磷酸铁的流程如下:
3 4已知几种金属离子沉淀的pH如下表所示:
金属氢氧化物 Fe(OH) Fe(OH) Al(OH)
3 2 3
开始沉淀的pH 2.3 7.5 4.0
完全沉淀的pH 4.1 9.7 5.2
请回答下列问题:
(1)滤渣3的主要成分是________(写出化学式)。
(2)用FeS还原Fe3+的目的是__________________________________________________,
加入FeO的作用是________________________________________(用离子方程式表示)。
(3)试剂R宜选择________(填字母)。
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)检验“氧化”之后溶液是否含Fe2+的操作是_________________________________。