文档内容
专题讲座(七)晶胞的分析与计算
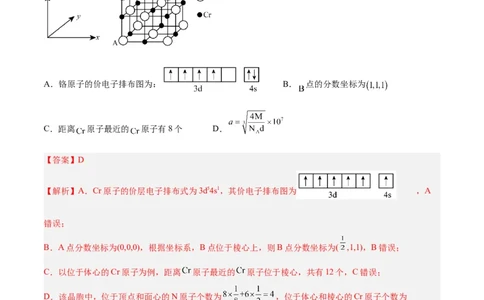
1.氮化铬的晶胞结构如图所示, 点分数坐标为 。氮化铬的晶体密度为 ,摩尔质量为
,晶胞参数为 , 代表阿伏加德罗常数的值。下列说法正确的是
A.铬原子的价电子排布图为: B. 点的分数坐标为
C.距离 原子最近的 原子有8个 D.
【答案】D
【解析】A.Cr原子的价层电子排布式为3d54s1,其价电子排布图为 ,A
错误;
B.A点分数坐标为(0,0,0),根据坐标系,B点位于棱心上,则B点分数坐标为( ,1,1),B错误;
C.以位于体心的Cr原子为例,距离 原子最近的 原子位于棱心,共有12个,C错误;
D.该晶胞中,位于顶点和面心的N原子个数为 ,位于体心和棱心的Cr原子个数为
,则 ,解得 nm,D正确;
故选D。
2. 晶体是制备氟代硼铍酸钾晶体的原料之一,其晶胞结构与 类似,下列说法中不正确的是A.Be原子的配位数是12
B.若原子a、b的坐标分别为 、 ,则原子c的坐标为
C.沿晶胞面对角线投影,所得的投影结果是
D.设O与Be的最近距离为 ,用 表示阿伏加德罗常数的值,则 晶体的密度为
【答案】A
【解析】A.由晶胞结构可知Be位于O原子构成的四面体的体心,Be原子的配位数是4,A错误;
B.由 的晶胞结构可知,每个Be处于晶胞体对角线的 处,结合原子a、b的坐标可知原子c的坐标
为 ,B正确;
C.沿面对角线进行投影,可知所得的投影结果是 ,C正确;
D.若O与Be的最近距离为 ,则题中a、c之间的距离为 ,又因为a、c之间的距离为晶胞体对角线长的 ,则晶胞体对角线长为 ,故晶胞棱长为 ,晶胞内Be的个数为4,O的个数为
,则根据晶胞质量=晶胞密度×晶胞体积可得,晶胞密度为 ,D正
确;
故选:A。
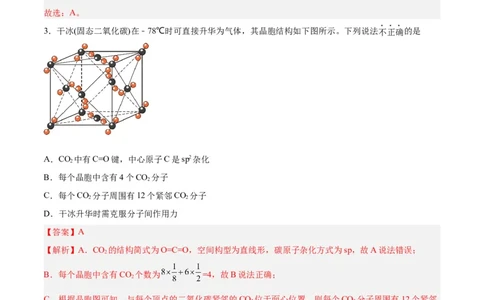
3.干冰(固态二氧化碳)在﹣78℃时可直接升华为气体,其晶胞结构如下图所示。下列说法不正确的是
A.CO 中有C=O键,中心原子C是sp2杂化
2
B.每个晶胞中含有4个CO 分子
2
C.每个CO 分子周围有12个紧邻CO 分子
2 2
D.干冰升华时需克服分子间作用力
【答案】A
【解析】A.CO 的结构简式为O=C=O,空间构型为直线形,碳原子杂化方式为sp,故A说法错误;
2
B.每个晶胞中含有CO 个数为 =4,故B说法正确;
2
C.根据晶胞图可知,与每个顶点的二氧化碳紧邻的CO 位于面心位置,则每个CO 分子周围有12个紧邻
2 2
的CO 分子,故C说法正确;
2
D.干冰属于分子晶体,因此干冰升华时需要克服分子间作用了,故D说法正确;
答案为A。
4.A、B为原子序数依次增大的短周期主族元素,基态原子的最外层均有2个未成对电子,A、B形成的
二元化合物在自然界中普遍存在,并有多种结构,如图是其中一种结构的晶胞示意图。下列说法正确的是A.该二元化合物是分子晶体
B.每个晶胞拥有A原子的数目为6个
C.该二元化合物A、B两原子的杂化方式不同
D.该二元化合物中只有B原子满足8电子稳定结构
【答案】B
【分析】周期表中基态原子的最外层均有2个未成对电子的元素在第IVA族和第VIA族,短周期中符合此
条件的有碳、硅、氧、硫四种元素,由图中看出,一个A周围有2个B,一个B原子周围有四个A,AB
原子个数比应该是2:1,可以形成CO,CS,SiO 等物质,又知A、B原子序数依次增大,只有A是O元
2 2 2
素,B是Si元素符合,形成的化合物是SiO。
2
【解析】A.SiO 是原子晶体,故A错误;
2
B.由图可知晶胞中B原子(即Si原子)所在位置有4个在棱上,2个在面上,1个在晶胞内该晶胞中含有
Si原子个数为 +2 +1=3,按照Si与O原子1:2,所以含有6个氧原子,故B正确;
C.SiO 中Si原子和O原子都是sp3杂化,杂化方式相同,故C错误;
2
D.硅最外层四个电子,一个硅与周围4个氧原子形成共价键,O原子最外层有6个电子,与2个硅形成共
价键,因此Si原子和O原子都满足8电子稳定结构,故D错误;
答案选B。
5.NaCl广泛应用于食品、氯碱工业等领域,其晶胞如下图所示,下列说法不正确的是A.a表示的是 ,b表示的是
B.每个晶胞中含有4个 和4个
C.NaCl由固态变成气态,需要吸收能量破坏离子键
D.基态 与 最外层电子排布符合 ,二者位于周期表的p区
【答案】D
【解析】A.同主族元素,从上到下离子半径依次增大,电子层结构相同的离子,核电荷数越大,离子半
径越大,则氯离子的离子半径大于钠离子,所以晶胞中大球a表示的是氯离子,小球b表示的是钠离子,
故A正确;
B.由晶胞结构可知,晶胞中位于顶点和面心的氯离子个数为8× +6× =4,位于棱上和体心的钠离子个
数为4× +1=4,故B正确;
C.氯化钠是含有离子键的离子化合物,由固态变成气态时需要吸收能量破坏离子键,故C正确;
D.钠元素的原子序数为11,基态原子的价电子排布式为3s1,则钠元素位于元素周期表的s区,故D错
误;
故选D。
6.双钙钛矿型晶体的一种典型结构单元如图所示,真实的晶体中存在5%的氧原子缺陷,能让 在其中
传导,可用作固体电解质材料。已知La为+3价,Ba为+2价。以下说法错误的是
A.该晶体的一个完整晶胞中含有1个Co原子
B.晶体中与La距离最近的Ba的数目为6
C.+3价Co与+4价Co的原子个数比为4∶1
D.忽略氧原子缺陷,每个Co原子都处于氧原子围成的正八面体空隙的中心
【答案】A【解析】A. 该晶体的一个完整晶胞由8个图示结构单元组成,该晶体的一个完整晶胞中含有8个Co原
子,故A错误;
B. 根据图示,晶体中与La距离最近的Ba的数目为6,故B正确;
C. 根据均摊原则,La数为 、Ba数为 、Co数为1、O数为 ,所以化学式为
LaBaCo O,真实的晶体中存在5%的氧原子缺陷,+3价Co的个数为x,根据化合价代数和等于
2 6
0,+3+2+3x+4(2-x)-2×6×95%=0,x=1.6,所以+3价Co与+4价Co的原子个数比为4∶1,故C正确;
D. 忽略氧原子缺陷,根据图示,每个Co原子都处于氧原子围成的正八面体空隙的中心,故D正确;
故选A。
7.某无机物常应用于电子陶瓷工业,其晶胞结构如图所示。设晶胞参数为anm。下列说法错误的是
A.Ti4+处于O2-形成的八面体的体心位置 B.Ba2+与O2-最近距离是
C.该晶胞的密度是 D.将部分Ba2+换成Sr2+,则晶胞参数发生改变
【答案】C
【解析】A.晶胞中O2-位于面心,Ti4+位于体心,Ti4+处于O2-形成的八面体的体心位置,故A正确;
B.根据立体几何知识,2个Ba2+与1个O2-构成了一个等腰直角三角形,直角边长为 ,Ba2+与O2-最近距
离即斜边长为 ,故B正确;
C.Ba2+位于顶角,晶胞中Ba原子数目为 ,晶胞中O2-位于面心,O原子数目为 ,Ti4+位于体
心,数目为1,该晶胞化学式为BaTiO ,晶胞的质量为m= ,晶胞参数为anm,晶胞体积为
3V=(a×10-7)3cm3,该晶胞的密度是 ,故C错误;
D.Ba2+与Sr2+的离子半径不同,棱长也不同,则晶胞参数发生改变,故D正确;
故选:C。
8.X为一种由汞(Hg)、锗(Ge)、锑(Sb)形成的可作潜在拓扑绝缘体材料的新物质,其晶胞如图所示(底面为
正方形)。下列说法错误的是
A.X的化学式为
B.与Hg距离最近的Sb的数目为4
C.若晶胞中原子1的坐标为 ,则原子2的坐标为
D.设X的最简式的分子量为 ,则X晶体的密度为
【答案】C
【解析】A.X中含Hg个数为 ,Ge个数为 ,Sb个数为8,则X的化学式
为 ,故A正确;
B.以右侧面的Hg分析,与Hg距离最近的Sb的数目为4,故B正确;
C.若晶胞中原子1的坐标为 ,则原子2在上面那个立方体的体对角线的四分之一处,其z坐标为,则其坐标为 ,故C错误;
D.设X的最简式的分子量为 ,则X晶体的密度为 ,故D正
确。
综上所述,答案为C。
9.金刚石的晶胞如图1所示,图1中原子坐标参数A为 ,B为 ,C为 。在立方晶
胞中,与晶胞体对角线垂直的面,在晶体学中称为 晶面,如图2所示。下列说法错误的是
A.金刚石是由碳元素组成的
B.图1中原子坐标参数D为
C.若图1金刚石的晶胞参数为apm,则其晶胞中两个碳原子之间的最短距离为 cm
D.图2晶胞中可以称为 晶面的面共有8个
【答案】C
【解析】A.金刚石是由碳元素组成的单质,A正确;
B.D与周围4个原子形成正四面体结构,D处于前面、下面和左面的1/4,D原子的坐标参数为
,B正确;C.金刚石晶胞中两个碳原子之间的最短距离是体对角线的 ,为 cm,C错误;
D.图2晶胞中共有8个顶点,4条体对角线,由(1,1,1) 晶面定义可知,晶胞中可以称为 晶面的面共
有8个,D正确;
故选C。
10.一种化合物的结构如图所示,Q、X、Y、Z、W为相邻两个短周期主族元素,原子序数依次增大,W
元素的最外层电子数等于其电子总数的三分之一。下列说法正确的是
A.通常所用的农药中含有Z、W等元素
B.氢化物的沸点一定是Y>Z>X
C.由Q、Y、W形成的正盐只有一种
D.Q的单质在空气中燃烧的产物具有强氧化性
【答案】A
【分析】从结构图可知,Y共用2对电子,达到稳定结构,Y最外层有6个电子,X共用4对电子达到稳
定结构,则X最外层有4个电子,Z共用1对电子,则Z最外层有7个电子,W得一个电子后形成6个共
价键,W元素的最外层电子数等于其电子总数的三分之一,则W最外层有5个电子,又因为Q、X、Y、
Z、W为相邻两个短周期主族元素,原子序数依次增大,故Q为Li,X为C,Y为O,Z为F,W为P。
【解析】A.通常所用的农药中含有F、P等元素,A正确;
B.未说明是最简单氢化物,无法比较沸点高低,B错误;
C.由Li、P、O形成的正盐有 、 等,C错误;
D.Li在空气中燃烧生成 ,其不具有强氧化性,D错误;
故选A。
11.钾元素与氧元素形成的某些化合物可以作为宇宙飞船的供氧剂,其中一种化合物的晶胞在XY平面、
XZ平面、YZ平面上的投影如图所示,其晶胞边长为anm, 为阿伏伽德罗常数的值下列说法正确的是
A.晶胞的化学式为
B.晶胞中存在的微粒间作用力只有离子键
C.距离最近的K原子之间的距离为anm
D.晶胞的密度为
【答案】D
【解析】A.根据晶胞的投影图可以知道,K原子在晶胞的顶点和体心,一个晶胞含有K原子
,O原子有两个在晶胞内,八个在棱上,一个晶胞中含有O原子 ,则晶胞的化学式为 ,故
A错误;
B.晶胞的化学式为 ,则晶胞中存在的微粒间作用力有离子键和共价键,故B错误;
C.K原子在晶胞的顶点和体心,则距离最近的K原子之间的距离为体对角线的一半即 anm,故C错
误;
D.根据前面分析该晶胞中含有2个 ,则晶胞的密度为 ,故D正确。
综上所述,答案为D。
12. 是锂离子电池正极材料,晶体中 围绕 形成八面体,八面体共棱形成层状空间结构,与
层交替排列。在充放电过程中, (Ⅲ)与 (Ⅳ)相互转化, 在层间脱出或嵌入,晶胞组成变化如
图所示。下列说法正确的是A. 中
B.每个 晶胞中 与Co(Ⅳ)个数比为
C.每个 晶胞转化为 晶胞转移的电子数为4
D.相同质量的 分别转化为 与 转移电子数之比为
【答案】B
【解析】A.由图可知, 中 的个数为2+8 =3, 中 的个数为1+8 =2,则
,x= ,故A错误;
B.由A可知 中 ,设每个 晶胞中Co(Ⅳ)的个数为a, (Ⅲ)的个数为b,根据
化合价代数和为零可知, +4a+3b=2×2,a+b=1,解得a= ,b= , 与Co(Ⅳ)个数比为 ,故B正
确;
C. 中 的个数为1+8 =2, 中 的个数为1+4 = ,每个 晶胞转化
为 晶胞过程中失去 个 ,转移的电子数为 ,故C错误;
D.每个 晶胞转化为 转移的电子数为 , 中 的个数为2+8 =3,每个晶胞转化为 过程中得到1个 ,转移1个电子,则相同物质的量的 分别转化
为 与 转移电子数之比为 ,故D错误;
故选B。
13.某卤化物可用于制作激光基质材料,其立方晶胞结构如图所示,已知:晶胞参数为 , 为阿伏
加德罗常数的值。下列有关该晶体的说法正确的是
A.化学式为 B.K的配位数为6
C.若K位于晶胞的体心,则F位于面心 D.密度为
【答案】A
【解析】A. 晶胞中,钾原子位于顶点,个数为 ,镁原子位于体心,个数为1,氟原子位于
面心,个数为 ,则晶胞中K、Mg、F的原子个数比为1:1:3,化学式为 ,A项正确;
B.与K等距且最近的F位于面心,共有12个,所以K的配位数为12,B项错误;
C.晶体中若K位于晶胞的体心,则F位于棱心,Mg位于顶点,C项错误;
D.该晶体的密度 ,D项错误;
故选A。
14.氧化锌(ZnO)的透明度高,具有优异的常温发光性能。氧化锌的两种晶胞结构如图所示。下列说法错
误的是A.甲、乙两种晶体类型的晶胞内 数目之比为2∶1
B.甲中 位于 形成的四面体空隙中,空隙填充率为50%
C.乙的晶胞沿z轴的二维投影图如图丙所示
D.两种晶胞中 的配位数均为4
【答案】C
【解析】A.甲类型的晶胞中有4个Zn2+位于晶胞内,则甲晶胞有4个Zn2+;乙晶胞有4个Zn2+位于晶胞棱
上,1个Zn2+位于晶胞内,则乙晶胞共 个Zn2+,甲、乙两种晶体类型的晶胞内Zn2+数目之比为
2 : 1,故A正确;
B.甲晶胞中O2-形成8个空隙,Zn2+占据4个空隙,则空隙填充率为50%,故B正确;
C.乙的晶胞沿z轴的二维投影图如图 ,故C错误;
D.O2-的配位数即为晶胞中距离O2-最近的离子个数,观察甲乙两晶胞,可知距离O2-最近的离子个数均为4
个Zn2+,则两种晶胞中O2-的配位数均为4,故D正确;
故选C。
15.具有光催化活性的TiO 可通过氮掺杂生成TiO N 后,在光照下的输出稳定性更好,其晶胞结构如
2 2-a b
图,已知原子1、原子2的分数坐标为(0,0, )和(1,0,0),设阿伏加德罗常数的值为N ,下列说法正
A
确的是A.氮掺杂生成的TiO N 中,a= ,b=
2-a b
B.原子3的分数坐标为(1,0, )
C.TiO 晶体中,Ti的配位数为8
2
D.TiO 的密度为 g·cm-3
2
【答案】A
【解析】A.由TiO N 晶体结构可知,氮掺杂反应后有3个氧空穴,O原子6个在棱上、6个在后面,1
2-a b
个在体内,O原子个数为 ,N原子1个在棱上、1个在面,N原子个数为
,Ti原子8个在顶点、4个在面心,1个在体内,Ti原子个数为 ,
, , ,A正确;
B.原子1、2的坐标分别为 ,由TiO2的晶胞结构可知,原子3的坐标为 ,B错
误;
C.钛离子形成体心四方点阵,氧离子形成八面体,八面体嵌入体心四方点阵中,每个钛离子周围有6个
氧离子,Ti的配位数为8,C错误;
D. Ti原子在晶胞的8个顶点、4个面心和1个在体内,Ti原子的个数为 ,O原子在8个
棱上、8个面上,2个在体内,O原子个数为 ,则1mol晶胞的质量 ,一个晶胞的质量为 ,体积为 ,则TiO2的密度为
,D错误;
故答案为:A。
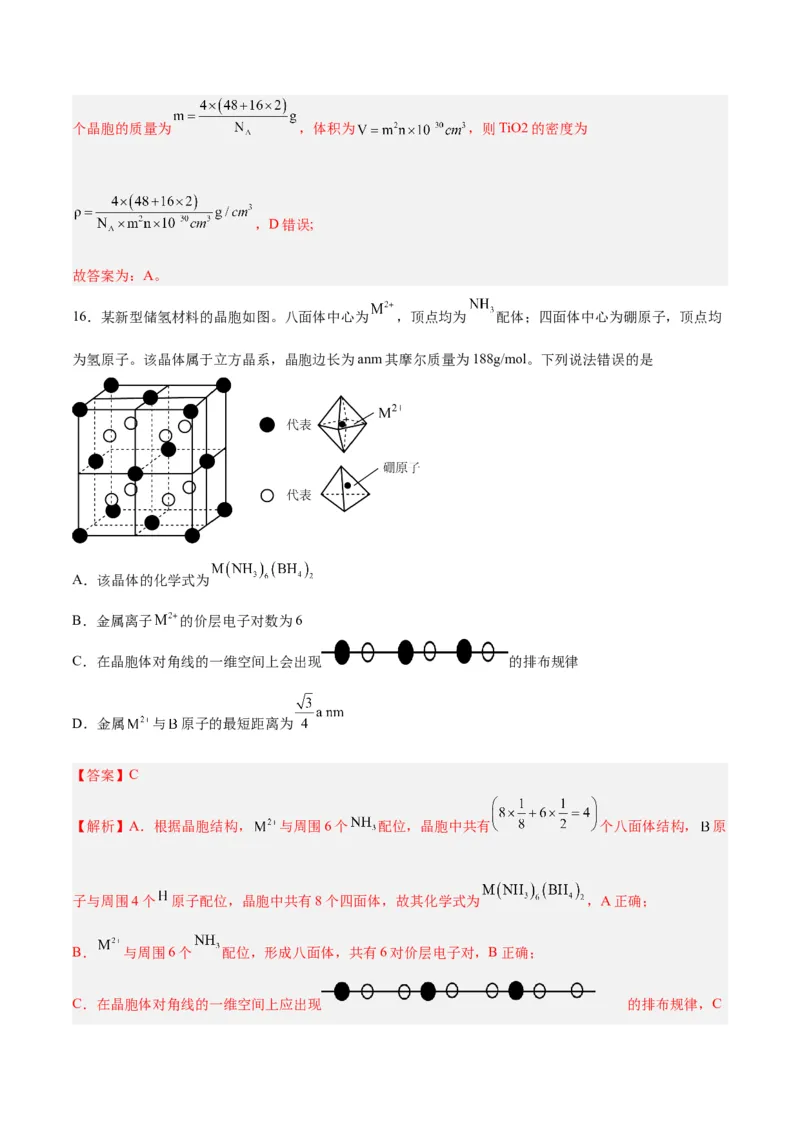
16.某新型储氢材料的晶胞如图。八面体中心为 ,顶点均为 配体;四面体中心为硼原子,顶点均
为氢原子。该晶体属于立方晶系,晶胞边长为anm其摩尔质量为188g/mol。下列说法错误的是
A.该晶体的化学式为
B.金属离子 的价层电子对数为6
C.在晶胞体对角线的一维空间上会出现 的排布规律
D.金属 与 原子的最短距离为
【答案】C
【解析】A.根据晶胞结构, 与周围6个 配位,晶胞中共有 个八面体结构, 原
子与周围4个 原子配位,晶胞中共有8个四面体,故其化学式为 ,A正确;
B. 与周围6个 配位,形成八面体,共有6对价层电子对,B正确;
C.在晶胞体对角线的一维空间上应出现 的排布规律,C错误;
D.如图 ,pb长度即为金属 与 原子的最短距离, ,
, ,则 ,D正确。
故选C。
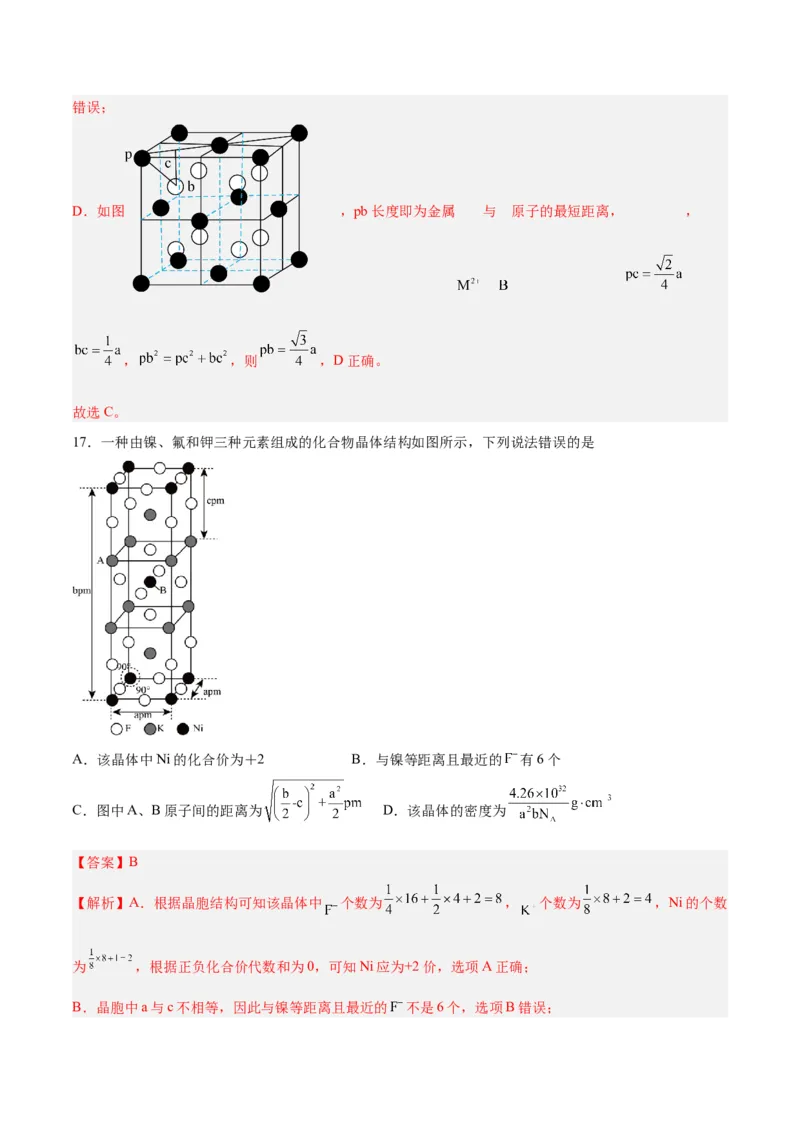
17.一种由镍、氟和钾三种元素组成的化合物晶体结构如图所示,下列说法错误的是
A.该晶体中Ni的化合价为+2 B.与镍等距离且最近的 有6个
C.图中A、B原子间的距离为 D.该晶体的密度为
【答案】B
【解析】A.根据晶胞结构可知该晶体中 个数为 , 个数为 ,Ni的个数
为 ,根据正负化合价代数和为0,可知Ni应为+2价,选项A正确;
B.晶胞中a与c不相等,因此与镍等距离且最近的 不是6个,选项B错误;C.图中A位于棱边 处,B原子位于中心,二者之间的距离为 pm,选项C正确;
D.该晶胞的化学式为 ,晶胞质量为426/ ,晶胞体积为 ,因此该晶体的密度为
,选项D正确;
答案选B。
18.氟元素可形成多种有工业价值和科研价值的化合物,如OF 、NF 、XeF 等。其中XeF 的四方晶胞结
2 3 2 2
构如图所示,图中M点原子坐标参数为( , , ),Xe和F的最短距离为bnm、下列说法错误的是
A. OF 分子中键角小于 分子中的
2
B. 中Xe的杂化方式为sp
C.基态N、F原子核外电子均有5种空间运动状态
D.Q点原子坐标参数为 [ ]
【答案】B
【解析】A.OF 中 原子有2对孤电子对,NF 中 原子有1对孤电子对,孤电子对对成键电子对的排斥
2 3
力大于成键电子对对成键电子对的排斥力,故OF 分子中键角小于NF 分子中的,A正确;
2 3
B.XeF 中Xe的价层电子对数目为5,不可能为sp杂化,B错误;
2
C.基态N、F原子核外电子均占据5个原子轨道,故均有5种空间运动状态,C正确;D.由信息,Q点原子坐标参数为 ,D正确;
故答案为:B。
19.某铁氮化合物晶体的晶胞结构如图所示。若晶胞中距离最近的两个铁原子距离为apm,阿伏加德罗常
数的值为N ,则下列说法不正确的是
A
A.若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为棱心、面心和体心
B.该化合物化学式为Fe N
4
C.N原子的分数坐标为( , , )
D.该晶体的密度为 g/cm3
【答案】A
【解析】A.由题干晶胞示意图可知,若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为棱心和体心,A
错误;
B.由题干晶胞示意图可知,一个晶胞中含有Fe个数为: =4,N原子个数为1,故该化合物化
学式为Fe N,B正确;
4
C.由题干晶胞示意图可知,N原子位于体心上,故N原子的分数坐标为( , , ),C正确;
D.由B项分析可知,一个晶胞中含有Fe个数为: =4,N原子个数为1,设晶胞的边长为
dpm,若晶胞中距离最近的两个铁原子距离为apm,即有 ,解得d= ,则该晶体的密度为= g/cm3,D正确;
故答案为:A。
20.黄铁矿是自然界中常见的金属矿物,主要成分为 。工业上常煅烧其生成含铁矿渣和含硫气体。含
硫气体可用来提取硫和制造硫酸,制硫酸时的尾气常用氨水吸收;含铁矿渣与硫酸反应后再加入
溶液,可制备 。常温下可用铁质容器贮存浓硫酸。 的晶胞如下图所示。
下列化学反应表示正确的是
A.煅烧黄铁矿:
B. 气体与 气体混合:
C.氨水吸收过量 :
D. 溶液与 溶液混合的离子方程式:
【答案】B
【解析】A.黄铁矿“煅烧”时反应的化学方程式为 ,不是生成三氧化
硫,故A错误;
B. 气体与 气体混合发生的反应为 ,故B正确;
C.用氨水吸收少量SO 生成亚硫酸铵,离子方程式为:2NH ·H O+SO =2NH +SO +H O,亚硫酸铵要拆
2 3 2 2 2
开,故C错误;D. 属于弱酸的酸式酸根离子,部分发生电离,不能将其拆开,故D错误;
故答案选B。