文档内容
绝密★启用前
2025 年高考考前信息必刷卷 03(河北专用)
化 学
考情速递
高考·新动向:
突出关键能力考查,激发学生从事科学研究、探索未知的兴趣,助力拔尖创新人才的选拔培养,充分
发挥高考育人功能和积极导向作用。试题突出化学的育人价值,凸显化学实验学科特色,侧重于逻辑分析
能力的应用,试题素材选取范围广,内容富有时代气息,试题内容综合性强,突出科学探究及科学研究思
维方法。
高考·新考法:
第5题,以反应历程为载体,考查反应热、杂化方式、反应速率的影响因素等。第9题,以酸碱中和
溶液中的分布分数图像为载体,考查溶液的酸碱性、分布系数与pH的关系、平衡常数等。
命题·大预测:
化学考试中获得高分还体现在规范答题、避免非智力因素失误上。如化学用语使用不规范;不注意有
效数字处理,热化学方程式漏写状态;多元弱酸根离子的水解反应不分步写;有机物的结构简式氢原子写
多或写少;酯化反应漏写水等。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39 Ti 48
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.文物是一个国家悠久历史最生动的体现。下列文物材质的主要成分属于天然高分子材料的是A.鎏金舞马衔杯纹银壶 B.云龙纹瓷瓶 C.三彩载乐骆驼俑 D.鹭鸟纹彩色蜡染褶裙
2.下列化学用语表示正确的是
A.Cl 分子中σ键的形成:
2
B.基态Fe2+的价层电子轨道表示式为:
C.NaCl溶液中的水合离子:
D.氯化铵的电子式:
3.设 为阿伏加德罗常数的值。下列说法正确的是
A.3.2g 中 的数目为0.1
B.4.6g乙醇完全氧化生成乙醛,转移电子数为0.2
C.常温常压下,124g 中所含P—P的数目为4
D.1mol 中σ键的个数为10
4.下列离子方程式书写正确的是
A.少量的 通入亚硫酸氢钠溶液中:
B.向“84”消毒液中通入少量的 气体:
C.向饱和碳酸钠溶液中通入足量 :
D.用惰性电极电解氯化镁溶液:
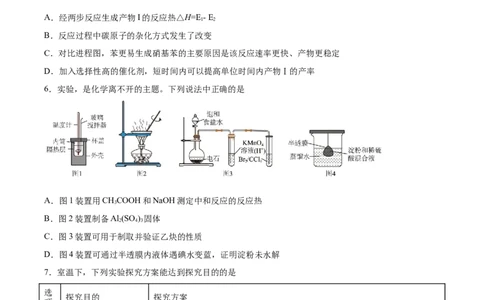
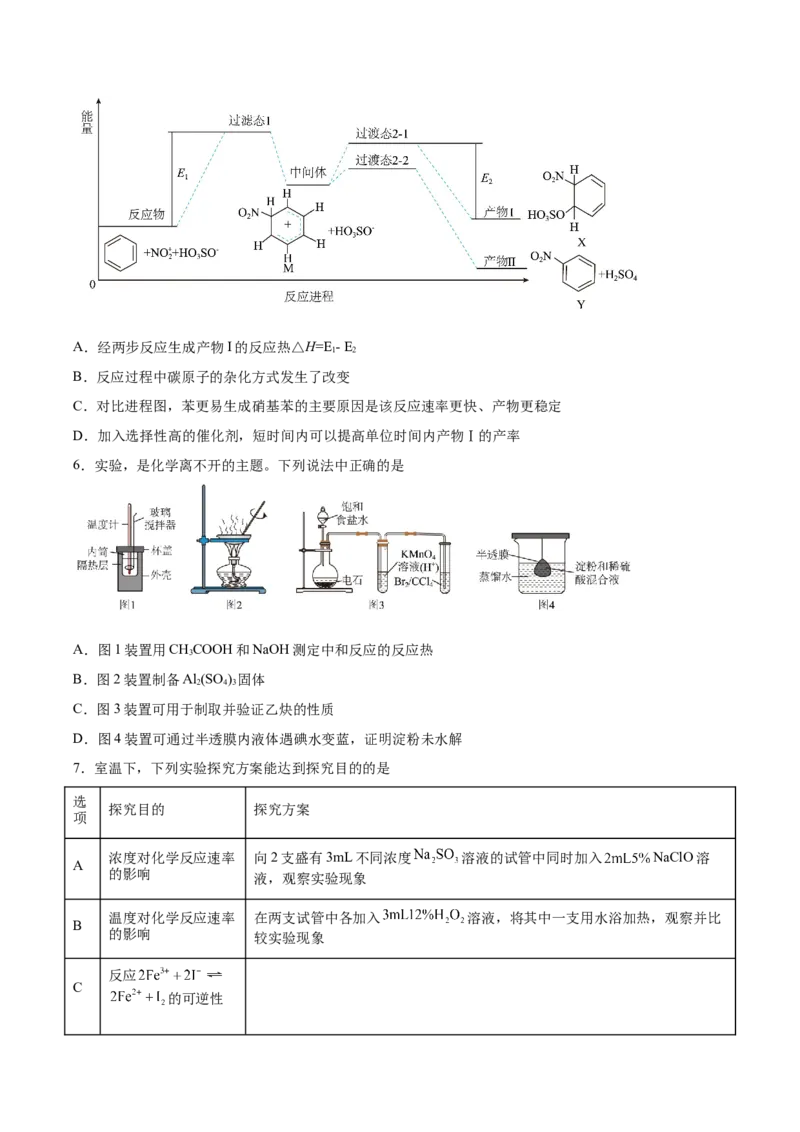
5.苯在浓HNO 和浓HSO 作用下,反应过程中能量变化示意图如下。下列说法不正确的是
3 2 4A.经两步反应生成产物I的反应热△H=E- E
1 2
B.反应过程中碳原子的杂化方式发生了改变
C.对比进程图,苯更易生成硝基苯的主要原因是该反应速率更快、产物更稳定
D.加入选择性高的催化剂,短时间内可以提高单位时间内产物Ⅰ的产率
6.实验,是化学离不开的主题。下列说法中正确的是
A.图1装置用CHCOOH和NaOH测定中和反应的反应热
3
B.图2装置制备Al (SO ) 固体
2 4 3
C.图3装置可用于制取并验证乙炔的性质
D.图4装置可通过半透膜内液体遇碘水变蓝,证明淀粉未水解
7.室温下,下列实验探究方案能达到探究目的的是
选
探究目的 探究方案
项
浓度对化学反应速率 向2支盛有3mL不同浓度 溶液的试管中同时加入 NaClO溶
A
的影响
液,观察实验现象
温度对化学反应速率 在两支试管中各加入 溶液,将其中一支用水浴加热,观察并比
B
的影响 较实验现象
反应
C
的可逆性向 溶液中滴加 溶液,振荡,用苯多次萃
取后,取水层分装在两支试管,向其中一支滴加几滴KSCN溶液,对比两试
管中溶液的颜色
探究固体表面积对反 称取相同质量的大理石和纯碱,加入盛有浓度、体积均相同的盐酸中的小烧
D
应速率的影响 杯中,观察实验现象
8.对下列事实解释错误的是
事实 解释
A 在水中的溶解度:O>O O 是极性分子,O 是非极性分子,HO是极性溶剂
3 2 3 2 2
B 熔点:SiO>CO SiO 的相对分子质量大于CO,分子间作用力强于CO
2 2 2 2 2
C 酸性:FCH COOH>ClCH COOH F的电负性强于Cl,FCH COOH中O-H键的极性更强
2 2 2
D 硬度:金刚石 碳化硅 C-C键的键长较短,键能较大
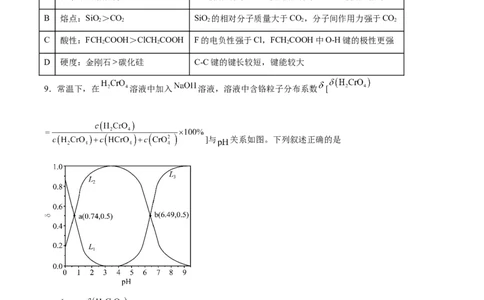
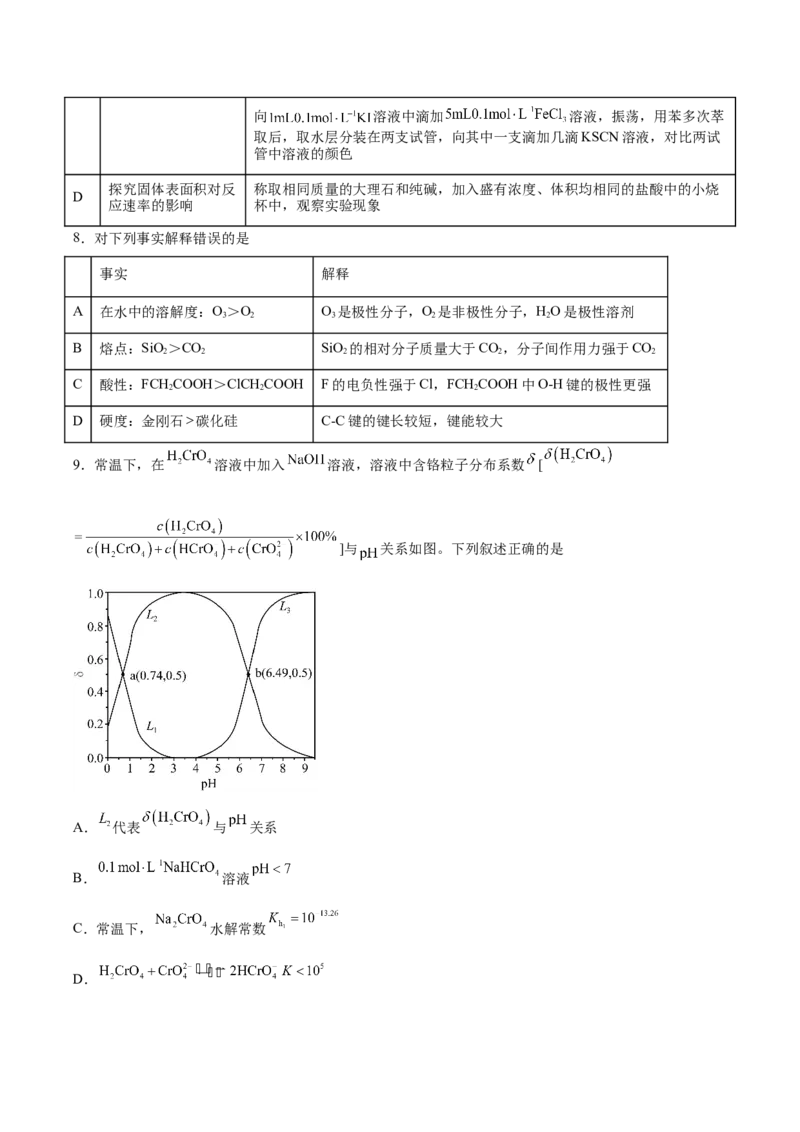
9.常温下,在 溶液中加入 溶液,溶液中含铬粒子分布系数 [
]与 关系如图。下列叙述正确的是
A. 代表 与 关系
B. 溶液
C.常温下, 水解常数
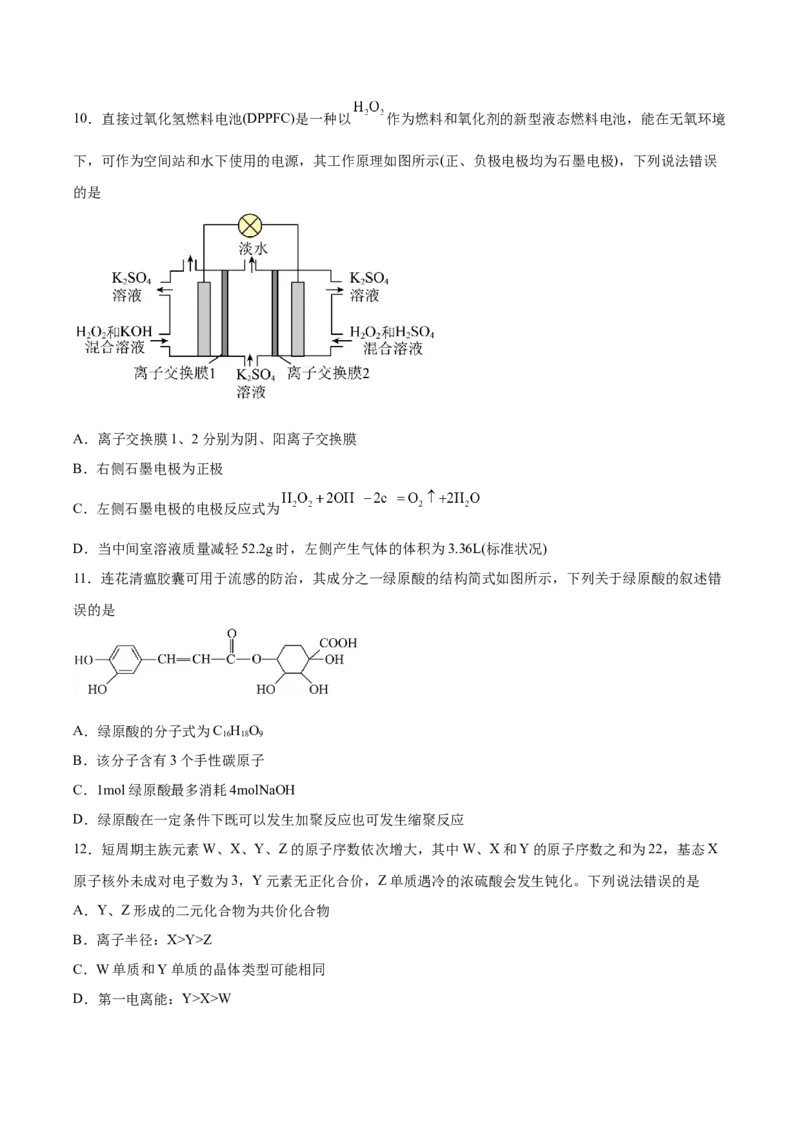
D.10.直接过氧化氢燃料电池(DPPFC)是一种以 作为燃料和氧化剂的新型液态燃料电池,能在无氧环境
下,可作为空间站和水下使用的电源,其工作原理如图所示(正、负极电极均为石墨电极),下列说法错误
的是
A.离子交换膜1、2分别为阴、阳离子交换膜
B.右侧石墨电极为正极
C.左侧石墨电极的电极反应式为
D.当中间室溶液质量减轻52.2g时,左侧产生气体的体积为3.36L(标准状况)
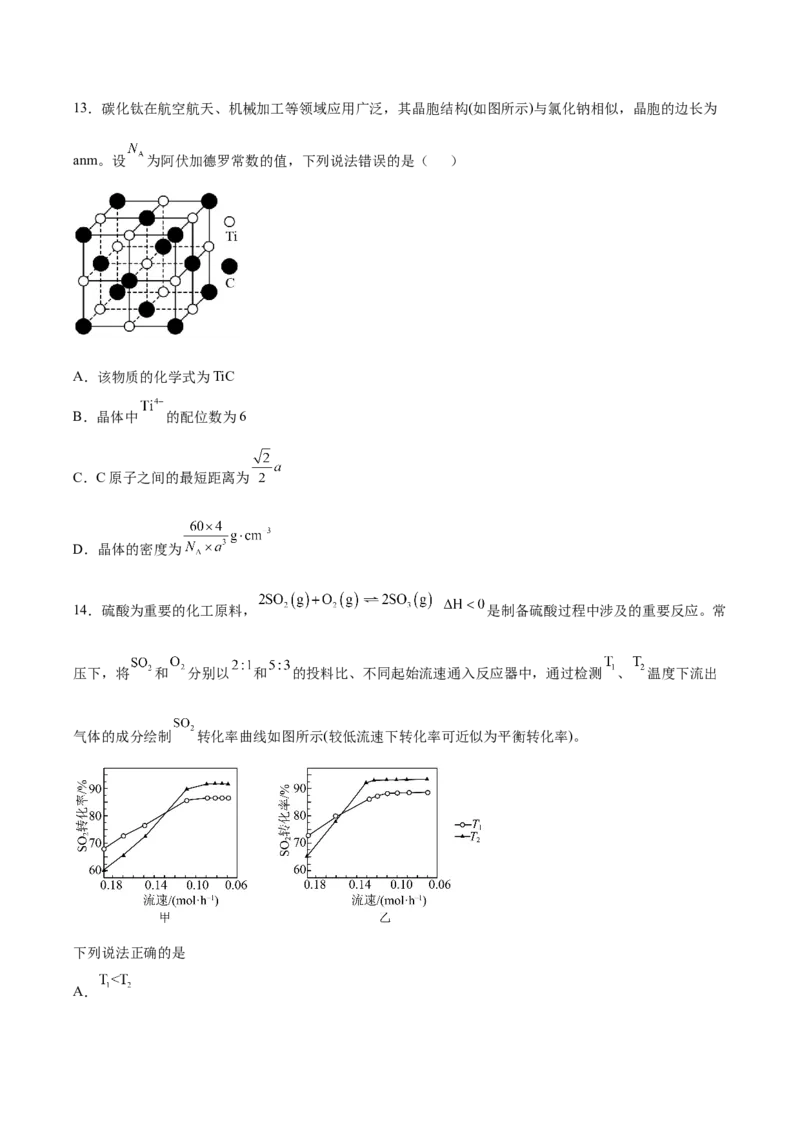
11.连花清瘟胶囊可用于流感的防治,其成分之一绿原酸的结构简式如图所示,下列关于绿原酸的叙述错
误的是
A.绿原酸的分子式为C H O
16 18 9
B.该分子含有3个手性碳原子
C.1mol绿原酸最多消耗4molNaOH
D.绿原酸在一定条件下既可以发生加聚反应也可发生缩聚反应
12.短周期主族元素W、X、Y、Z的原子序数依次增大,其中W、X和Y的原子序数之和为22,基态X
原子核外未成对电子数为3,Y元素无正化合价,Z单质遇冷的浓硫酸会发生钝化。下列说法错误的是
A.Y、Z形成的二元化合物为共价化合物
B.离子半径:X>Y>Z
C.W单质和Y单质的晶体类型可能相同
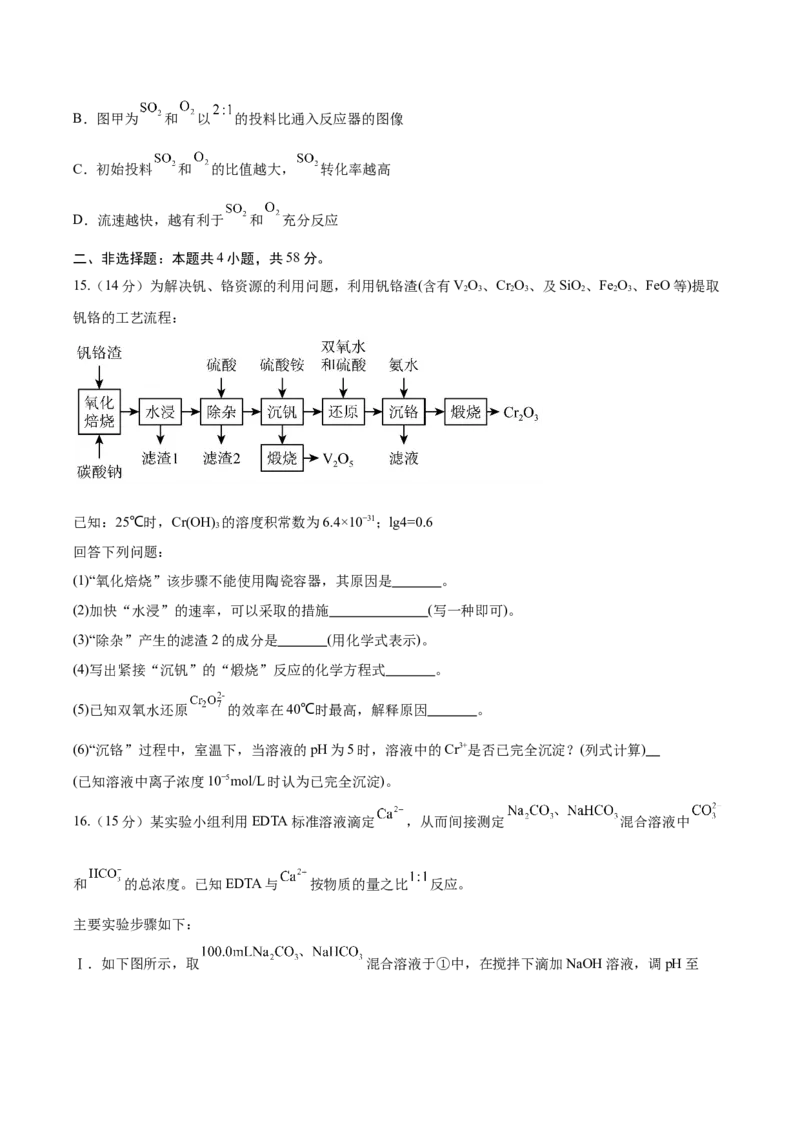
D.第一电离能:Y>X>W13.碳化钛在航空航天、机械加工等领域应用广泛,其晶胞结构(如图所示)与氯化钠相似,晶胞的边长为
anm。设 为阿伏加德罗常数的值,下列说法错误的是( )
A.该物质的化学式为TiC
B.晶体中 的配位数为6
C.C原子之间的最短距离为
D.晶体的密度为
14.硫酸为重要的化工原料, 是制备硫酸过程中涉及的重要反应。常
压下,将 和 分别以 和 的投料比、不同起始流速通入反应器中,通过检测 、 温度下流出
气体的成分绘制 转化率曲线如图所示(较低流速下转化率可近似为平衡转化率)。
下列说法正确的是
A.B.图甲为 和 以 的投料比通入反应器的图像
C.初始投料 和 的比值越大, 转化率越高
D.流速越快,越有利于 和 充分反应
二、非选择题:本题共4小题,共58分。
15.(14分)为解决钒、铬资源的利用问题,利用钒铬渣(含有VO、Cr O、及SiO、Fe O、FeO等)提取
2 3 2 3 2 2 3
钒铬的工艺流程:
已知:25℃时,Cr(OH) 的溶度积常数为6.4×10−31;lg4=0.6
3
回答下列问题:
(1)“氧化焙烧”该步骤不能使用陶瓷容器,其原因是 。
(2)加快“水浸”的速率,可以采取的措施 (写一种即可)。
(3)“除杂”产生的滤渣2的成分是 (用化学式表示)。
(4)写出紧接“沉钒”的“煅烧”反应的化学方程式 。
(5)已知双氧水还原 的效率在40℃时最高,解释原因 。
(6)“沉铬”过程中,室温下,当溶液的pH为5时,溶液中的Cr3+是否已完全沉淀?(列式计算)
(已知溶液中离子浓度10−5mol/L时认为已完全沉淀)。
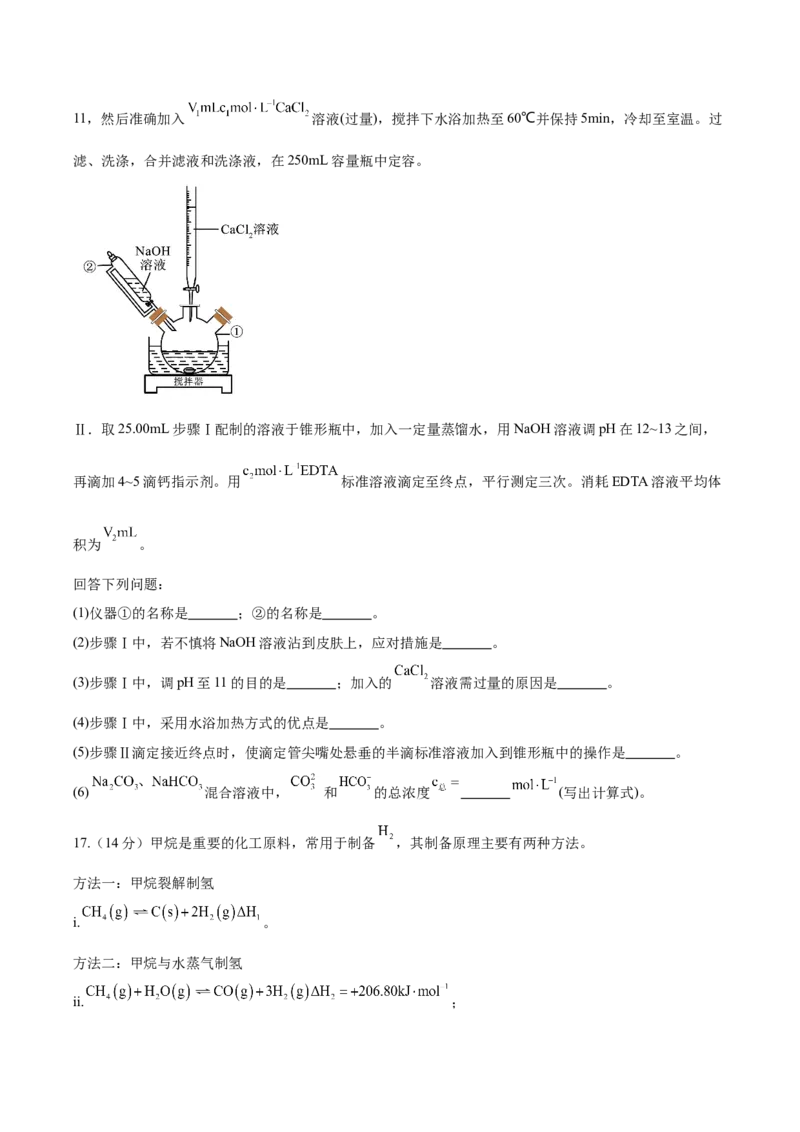
16.(15分)某实验小组利用EDTA标准溶液滴定 ,从而间接测定 混合溶液中
和 的总浓度。已知EDTA与 按物质的量之比 反应。
主要实验步骤如下:
Ⅰ.如下图所示,取 混合溶液于①中,在搅拌下滴加NaOH溶液,调pH至11,然后准确加入 溶液(过量),搅拌下水浴加热至60℃并保持5min,冷却至室温。过
滤、洗涤,合并滤液和洗涤液,在250mL容量瓶中定容。
Ⅱ.取25.00mL步骤Ⅰ配制的溶液于锥形瓶中,加入一定量蒸馏水,用NaOH溶液调pH在12~13之间,
再滴加4~5滴钙指示剂。用 标准溶液滴定至终点,平行测定三次。消耗EDTA溶液平均体
积为 。
回答下列问题:
(1)仪器①的名称是 ;②的名称是 。
(2)步骤Ⅰ中,若不慎将NaOH溶液沾到皮肤上,应对措施是 。
(3)步骤Ⅰ中,调pH至11的目的是 ;加入的 溶液需过量的原因是 。
(4)步骤Ⅰ中,采用水浴加热方式的优点是 。
(5)步骤Ⅱ滴定接近终点时,使滴定管尖嘴处悬垂的半滴标准溶液加入到锥形瓶中的操作是 。
(6) 混合溶液中, 和 的总浓度 (写出计算式)。
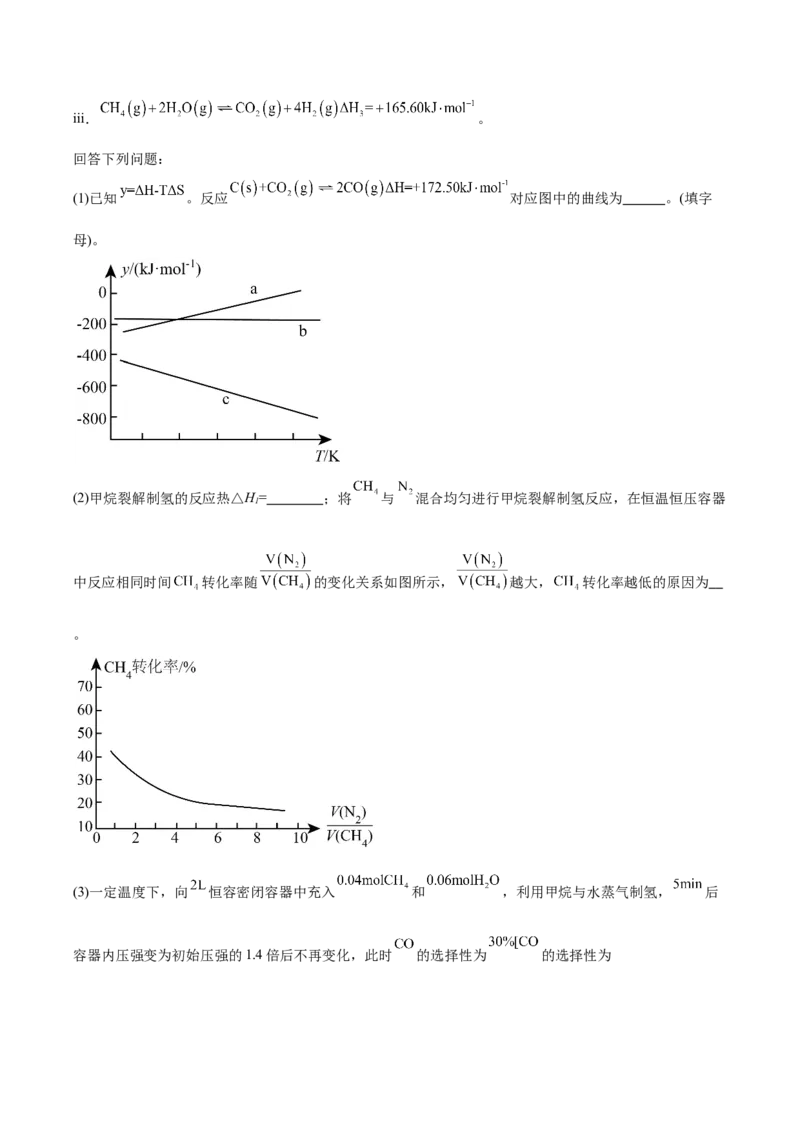
17.(14分)甲烷是重要的化工原料,常用于制备 ,其制备原理主要有两种方法。
方法一:甲烷裂解制氢
i. 。
方法二:甲烷与水蒸气制氢
ii. ;iii. 。
回答下列问题:
(1)已知 。反应 对应图中的曲线为 。(填字
母)。
(2)甲烷裂解制氢的反应热△H= ;将 与 混合均匀进行甲烷裂解制氢反应,在恒温恒压容器
1
中反应相同时间 转化率随 的变化关系如图所示, 越大, 转化率越低的原因为
。
(3)一定温度下,向 恒容密闭容器中充入 和 ,利用甲烷与水蒸气制氢, 后
容器内压强变为初始压强的1.4倍后不再变化,此时 的选择性为 的选择性为]。
① 的平衡转化率为 。
② 内, 的消耗速率为v(H O)= 。
2
③该温度下,反应iii的平衡常数 (列出计算式即可)。
④能影响 的平衡选择性的条件为 。(任写两种)。
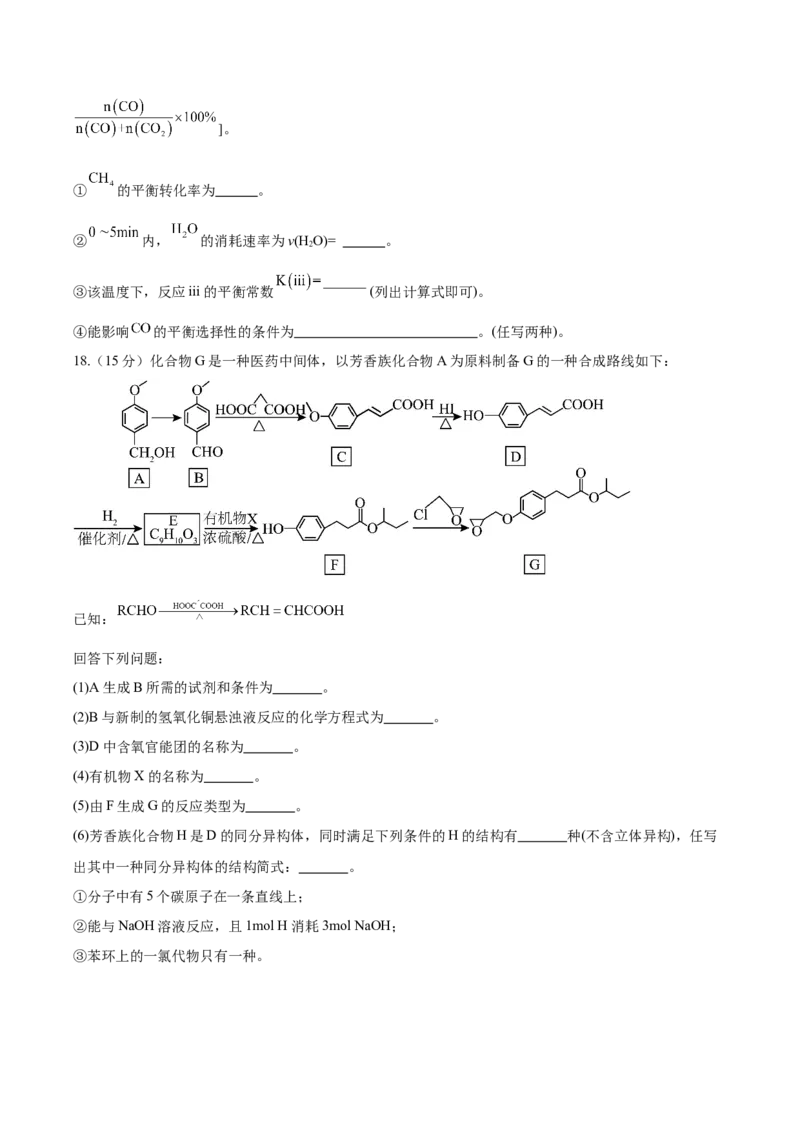
18.(15分)化合物G是一种医药中间体,以芳香族化合物A为原料制备G的一种合成路线如下:
已知:
回答下列问题:
(1)A生成B所需的试剂和条件为 。
(2)B与新制的氢氧化铜悬浊液反应的化学方程式为 。
(3)D中含氧官能团的名称为 。
(4)有机物X的名称为 。
(5)由F生成G的反应类型为 。
(6)芳香族化合物H是D的同分异构体,同时满足下列条件的H的结构有 种(不含立体异构),任写
出其中一种同分异构体的结构简式: 。
①分子中有5个碳原子在一条直线上;
②能与NaOH溶液反应,且1mol H消耗3mol NaOH;
③苯环上的一氯代物只有一种。