文档内容
绝密★启用前
2025 年高考考前信息必刷卷 05(上海专用)
化 学
考情速递
高考·新动向:上海高考化学试题独树一帜,题目以课题形式出现,有助于引导高中化学教学方式的转
变。上海高考化学中设置一些与实际教学内容相联系但形式为课题研究的题目,促使教师在教学中更
加注重将知识与实际的课题研究相融合,培养学生解决复杂问题的能力,也让学生适应这种在课题情
境下运用知识的考查方式。
高考·新考法:上海高考化学试卷设置了五道主题式综合题,这可以看作是一种课题形式的体现。每道
大题依据其内在的逻辑关联分设选择、填空、简答、计算等题型,形式新颖。这些主题式综合题多角
度、多层次考查学生化学学科核心素养发展水平。
高考·新情景:创设真实情境是上海高考化学命题的一大特点,这与课题形式出题相契合。比如以医药
健康中的降血糖药物瑞格列奈的合成情境出题,这类似于一个药物合成课题。学生要在这个情境下分
析合成过程中的化学物质转化、反应条件、反应类型等化学知识,从原料出发,经过多步反应得到目
标产物,如同在研究一个具体的化学课题。这种情境化的课题形式命题有助于考查学生将化学知识应
用于实际情境的能力,以及在复杂情境下分析和解决问题的能力。
命题·大预测:预测在2025年的高考试题中仍会继续延续课题出题方式,更贴近工业生产。以课题形式
出现的题目要求考生具备综合运用化学知识的能力。例如在一道关于环境污染治理的课题形式题目中,
考生可能需要运用化学平衡、氧化还原反应、离子反应等多方面知识来提出治理方案。这需要考生将
所学的各个知识点串联起来,从整体上分析和解决问题,而不是孤立地看待每个知识点,这是应对课
题形式题目的关键能力之一。
(试卷满分100分,考试时间60分钟)
1.本考试分设试卷和答题纸。答题前,务必在答题纸上填写学校、姓名、座位号,并将核对后的条
形码贴在指定位置上。作答必须涂或写在答题纸上,在试卷上作答一律不得分。
2.选择类试题中,标注“不定项”的试题,每小题有1~2个符合条件的选项;标注“双选”的试题,
每小题有两个符合条件的选项;标注“单选”的试题,每小题只有一个符合条件的选项。
3.可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 P-31
Cl-35.5 Ca-40 Mn-55 Cr-52 Fe-56 Cu-64 Xe-131
一、独特的氟元素(本题共21分)
1.氟在周期表中的位置是 ,是 区元素,核外有 种能量不同的电子。
2.下列关于氟元素的性质说法正确的是 。
A.原子半径最小 B.原子第一电离能最大C.元素的电负性最强 D.最高正化合价为+7
3.有关18F、19F说法正确的是 。
A.不同种核素 B.19F比18F多一个电子
C.18F、19F 化学性质不同 D.通过化学变化,可将18F转为19F
2 2
4.液态HF中存在:3HF HF -+X,则其中X为 ,HF -的结构为:[F-H…F]-,则HF
2 2
与F-间以 相连接。
5.一种稀有气体化合物可表示为Xe+[PtF]-,下列说法正确的是 (不定项),其外界的价电子
6
排布式是 ( 双选)。
A.中心离子为Pt5+ B.配体为F原子 C.含2种化学键 D. 含7N 个σ键
A
6.Xe与F 反应生成XeF 、XeF 和XeF 三种气体,产物的物质的量之比为1:6:3,写出有关化学反
2 2 4 6
应方程式 ;一定条件下,在50L容器中通入1 mol Xe和9 molF ,反应10
2
min后,剩余8.9 mol气体,则v(XeF )= 。
4
7.XeF 的空间结构与CF 不同,则XeF 空间结构为 ;它能与全氟丙烯反应:
4 4 4
XeF +2CF CF=CF =2CF CFCF+Xe,该反应中,部分碳原子由 杂化转变为 杂化。
4 3 2 3 2 3
【答案】1.第二周期ⅦA族(2分) p(1分) 3(1分)
2.C(2分)
3.A(2分)
4.HF-(1分) 氢键(1分)
2
5.AC(2分) 5s25p5(2分)
6.10Xe+22F =XeF +6XeF +3XeF (2分) 6.0×10-4mol·L-1·min-1 (2分)
2 2 4 6
7.平面正四边形(1分) sp2(1分) sp3(1分)
【解析】1.氟是9号元素,在周期表中的位置是第二周期ⅦA族,电子排布式为1s22s22p5,是p区元
素,含有3个能级,核外有3种能量不同的电子。
2.A项,同一周期主族元素从左至右,原子序数递增、原子半径递减,氟原子在本周期主族元素中
半径最小,但氢原子半径小于氟原子半径,故A错误;B项,同一周期主族元素从左至右,第一电离能有
增大的趋势,氟原子在本周期主族元素中第一电离能最大,但氦原子的第一电离能大于氟原子,故B错误;
C项,据同一周期主族元素从左至右电负性增强、同一主族从上至下电负性减弱可知,氟元素的电负性最
强,故C正确;D项,氟元素无正化合价,故D错误;故选C。
3.A项,18F与19F质子数相同、中子数不同,因此两者是不同种核素,A正确;B项,18F与19F互为
同位素,质子数和电子数均相同,19F比18F多一个中子,B错误;C项,18F、19F 为同种物质,化学性质
2 2
相同,C错误;D项,同位素之间的转化为物理变化,D错误;故选A。4.液态HF中存在:3HF HF -+X,根据元素守恒、电荷守恒,X为HF-,HF -的结构为:[F-
2 2 2
H…F]-,则HF与F-间以氢键相连接。
5.A项,[PtF]-中心离子为Pt5+,A正确;B项,[PtF]-配体为F离子,B错误;C项,Xe+[PtF]-含有
6 6 6
离子键和极性共价键,C正确;D项,1molXe+[PtF]-含6N 个Pt-Fσ键,D错误;故选AC;Xe是第五周期
6 A
0族元素,则Xe+的价电子排布式是5s25p5。
6.Xe与F 反应生成XeF 、XeF 和XeF 三种气体,产物的物质的量之比为1:6:3,根据元素守恒得
2 2 4 6
反应方程式:10Xe+22F =XeF +6XeF +3XeF ;
2 2 4 6
x=0.3,则 。
7.CF 中,C的价层电子对数为4+ =4+0=4,不含孤电子对,其空间构型为正四面体形,XeF
4 4
的空间结构与CF 不同,则XeF 中,Xe的价层电子对数为4+ =4+2=6,含两个孤电子对,其空间结
4 4
构为平面正四边形;全氟丙烯中单键碳杂化方式为sp3,双键碳杂化方式为sp2,全氟丙烷中只有单键碳,
碳原子杂化方式全是sp3,部分碳原子的杂化方式由sp2杂化转变为sp3杂化。
二、肼(本题共18分)
肼(N H)是强还原剂;在碱性溶液中能将银、镍等金属离子还原成金属;还可用作喷气式发动机燃料、
2 4
火箭燃料、显影剂、抗氧剂、还原剂等,亦能使锅炉内壁的铁锈变成磁性氧化铁层,可减缓锅炉锈蚀,是
一种重要的工业用品。请回答下列问题。
1.肼分子中,N原子的杂化方式为
2.与NH 类似,肼溶于水后,可以形成一种二元弱碱,请写出这种二元弱碱与足量酸反应后形成的
3
正离子的化学式 ,肼(N H)有较强的还原性,与NO 等可组成火箭推进剂。
2 4 2 4
3.已知:Ⅰ. kJ·mol-1
Ⅱ. kJ·mol-1
Ⅲ. kJ·mol-1火箭发射时NH 与NO 反应生成N 和HO(g),该反应的热化学方程式是 。
2 4 2 4 2 2
4.肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
ⅰ.NH +NaClO=NH Cl+NaOH(快)
3 2
ⅱ. (慢)
已知电负性N>Cl,下列说法正确的是 。
A.反应ⅰ中NaClO做氧化剂
B.适当提高反应ⅰ温度,可显著提高相同时间内NH·H O的产量
2 4 2
C.采用3.0 MPa压强可以增大NH 的溶解度,提高反应ⅱ中NH Cl的利用率
3 2
采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。
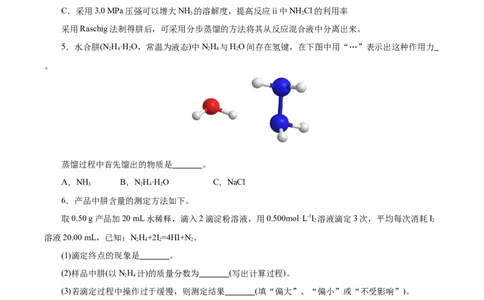
5.水合肼(N H·H O,常温为液态)中NH 与HO间存在氢键,在下图中用“…”表示出这种作用力
2 4 2 2 4 2
。
蒸馏过程中首先馏出的物质是 。
A.NH B.NH·H O C.NaCl
3 2 4 2
6.产品中肼含量的测定方法如下。
取0.50 g产品加20 mL水稀释,滴入2滴淀粉溶液,用0.500mol·L-1I 溶液滴定3次,平均每次消耗I
2 2
溶液20.00 mL,已知:NH+2I =4HI+N 。
2 4 2 2
(1)滴定终点的现象是 。
(2)样品中肼(以NH 计)的质量分数为 (写出计算过程)。
2 4
(3)若滴定过程中操作过于缓慢,则测定结果 (填“偏大”、“偏小”或“不受影响”)。
【答案】1.sp3(2分)
2.NH2+(2分)
2 6
3.2NH(g)+NO(g)=3N(g)+4HO(g) ΔH=-947.5kJ·mol−1 (2分)
2 4 2 4 2 2
4.C(2分)5. (2分) A(2分)
6.(1)溶液由无色变为蓝色,半分钟内溶液不再变为无色(2分)
(2)32%(2分) (3)偏小(2分)
【解析】1.根据 ,N原子形成3个σ键,含1对孤电子对,杂化轨道数为4,杂
化类型为sp3杂化;
2.肼溶于水后,可以形成一种二元弱碱电离出的阳离子为NH2+,即与足量酸反应后形成的正离子的
2 6
化学式:NH2+;
2 6
3.根据盖斯定律:II×2-III×2-I得:2NH(g)+NO(g)=3N(g)+4HO(g) ΔH=-947.5kJ·mol−1。
2 4 2 4 2 2
4.A项,由于电负性N>Cl,在反应i.NH +NaClO=NH Cl+NaOH(快)中,N为-3价,Cl为+1价,H
3 2
为+1价,Na为+1价,各种元素都化合价不变,所以该反应为非氧化还原反应,NaClO不是作氧化剂,A
错误;B项,适当提高反应温度,可以加快反应速率,但温度过高,反应ⅱ的化学平衡又逆向移动,导致
NH·H O的产量会降低,B错误;C项,采用3.0 MPa压强可以增大NH 的溶解度,使反应ⅱ的化学平衡
2 4 2 3
正向移动,从而可提高反应ⅱ中NH Cl的利用率,C正确;故选C;
2
5.水合肼(N H·H O,常温为液态)中,NH 与HO间存在氢键是:NH 中N原子与HO分子中的H
2 4 2 2 4 2 2 4 2
原子形成氢键;NH 中H原子与HO分子中的O原子形成氢键,在如图中用“…”表示出这种作用力为:
2 4 2
;NH·H O中NH 和HO的氢键大于NH 分子间的氢键,使得
2 4 2 2 4 2 3
NH·H O沸点比NH 高,NH·H O在常温下为液态,NH 为气态;而NaCl为离子化合物,其沸点在三种
2 4 2 3 2 4 2 3
物质中最高,故蒸馏过程中首先蒸馏出的物质是沸点低的NH ,故选A;
3
6.(1)滴定时发生反应:NH+2I =4HI+N ,用淀粉溶液作指示剂,根据反应消耗I 标准溶液体积判断
2 4 2 2 2产品中肼含量时,随着I 标准溶液的滴入,溶液中NH 不断消耗,当其消耗完全,滴入的标准溶液中的I
2 2 4 2
遇淀粉,溶液会变为蓝色,故滴入最后半滴I 标准溶液时,溶液由无色变为蓝色,半分钟内不再变为无色,
2
说明滴定达到终点,停止滴定。故滴定终点现象是:溶液由无色变为蓝色,半分钟内不再变为无色;(2)根
据反应NH+2I =4HI+N 可得关系式NH ~2I ,滴定时反应消耗I 的物质的量是n(I)=0.500 mol/L×0.0200
2 4 2 2 2 4 2 2 2
L=0.0100 mol,则样品中NH 的物质的量是n(N H)= n(I)=5.00×10-3 mol,故样品中肼的质量分数为
2 4 2 4 2
×100%=32%;(3)肼(N H)有较强的还原性,若滴定过程中操作过于缓慢,溶液中肼
2 4
易被空气中氧气氧化,导致消耗的I 标准溶液体积偏小,则根据I 标准溶液体积计算的肼的含量就会偏低,
2 2
最终使测定结果会偏小。
三、工业制硫酸(本题共22分)
硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催化氧化,现在某温度下,
2
在体积为5 L的密闭容器内发生如下反应:2SO (g)+O(g) 2SO (g) ΔH=−198 kJ·mol-1。
2 2 3
1.下列现象的成因与二氧化硫排放相关的是___________。
A.温室效应 B.酸雨 C.雾霾 D.臭氧层空洞
2.该反应自发进行的条件是___________。
A.高温自发 B.低温自发 C.总是自发 D.总是不自发
3.能判断该反应一定处于平衡状态的标志是___________。(不定项)
A.υ (O )=2υ (SO ) B.混合气体的密度保持不变
正 2 逆 2
C.混合气体平均摩尔质量保持不变 D.SO 和O 的转化率恰好相等
2 2
4.反应20 min后气体总物质的量减少了10 mol,则SO 的平均反应速率为 。
2
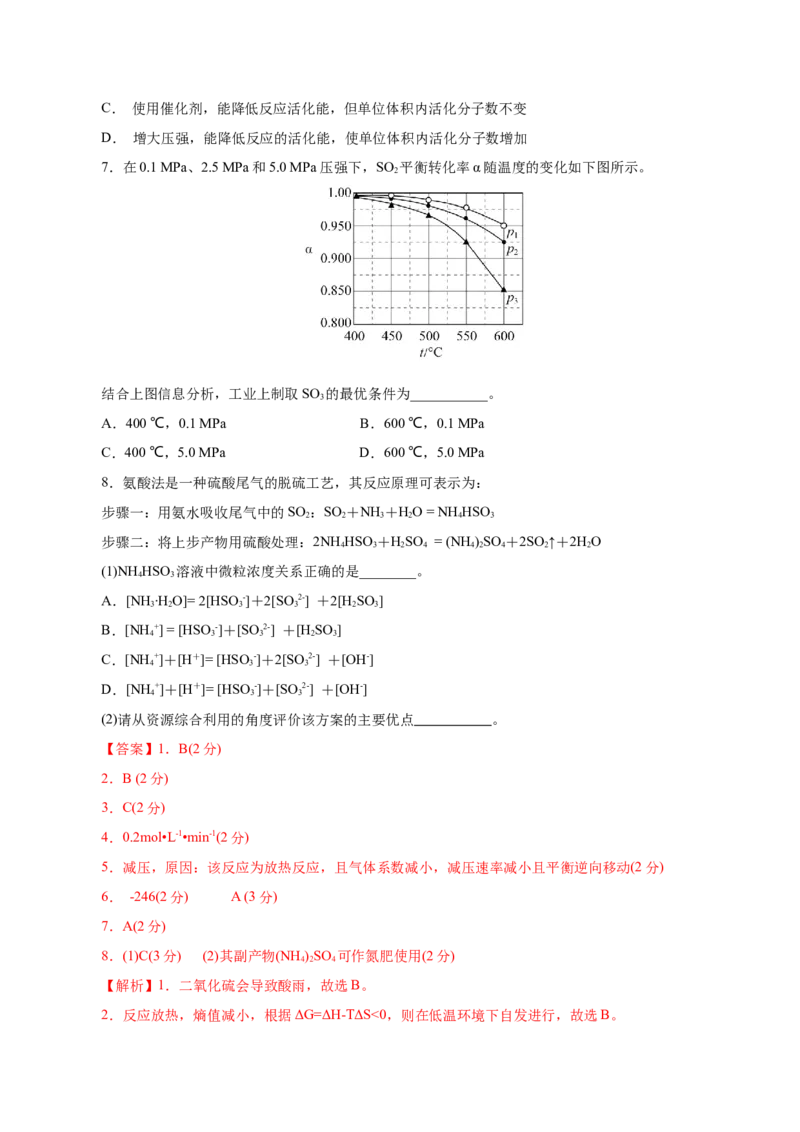
5.若在某一时刻,v =v =v,若改变某一条件,使该时刻v ”、“<”或
3 2 3 3
“=”),其原因是 。
4.从反应后的混合液中分离获取NaHCO 固体的方法为___________。
3
A.过滤 B.重结晶 C.萃取 D.蒸馏
5.分离获得的NaHCO 固体需在阴凉、干燥处自然晾干。该过程不采用加热烘干的原因是:
3
。
6.滴定法测定碳酸氢钠样品的纯度(杂质为碳酸钠):称量8.254 g碳酸氢钠样品配制成250 mL溶液,
取25.00 mL于锥形瓶中,加入甲基橙作指示剂,用0.5000 mol/L标准盐酸溶液滴定,重复操作3次,平均
消耗盐酸19.80 mL。(1)实验所需的定量仪器有电子天平、 。
(2)到达滴定终点的现象为 。
(3)通过计算判断该产品的纯度级别 (写出计算过程)
纯度级别 优级纯 分析纯 化学纯
质量分数
≥99.0% ≥98.5% ≥97.0%
ω(NaHCO )
3
【答案】1.C(2分)
2.2OH-+CO =CO 2-+H O(2分)
2 3 2
3.>(2分) Q点时溶质恰好完全转化为NaHCO ,此时溶液的pH>7,溶液呈碱性,说明HCO -水
3 3
解生成HCO 的程度大于电离产生CO2-的程度(2分)
2 3 3
4.A(2分)
5.2NaHCO NaCO+CO↑+HO(2分)
3 2 3 2 2
6.(1)250mL容量瓶、酸式滴定管、碱式滴定管(3分)
(2)溶液由黄色变为橙色且半分钟不变色(2分) (3)分析纯(2分)
【解析】氢氧化钠溶液中通入CO,CO 先与NaOH反应生成NaCO,M点之前,溶液的碱性较强,
2 2 2 3
M点溶质为NaCO 和未完全反应的NaOH;继续通入CO,到N点完全生成NaCO;继续通入CO,Q
2 3 2 2 3 2
点时溶质恰好完全转化为NaHCO 。
3
1.强电解质是在水溶液中完全发生电离的电解质,醋酸是弱酸,属于弱电解质,自来水是混合物,不
属于电解质,葡萄糖是非电解质,小苏打为NaHCO ,是在水溶液中完全发生电离的电解质,属于强电解
3
质,故选C。
2.6分钟(M点之前)时,溶液的碱性较强,说明此时CO 先与NaOH反应生成NaCO,离子方程式为:
2 2 3
2OH-+CO =CO 2-+H O。
2 3 2
3.Q点时溶质恰好完全转化为NaHCO ,此时溶液的pH>7,溶液呈碱性,说明HCO -水解生成HCO
3 3 2 3
的程度大于电离产生CO2-的程度,此时溶液中[H CO]>[ CO 2-]。
3 2 3 3
4.从反应后的混合液中分离获取NaHCO 固体可以采用过滤的方法,故选A。
3
5.分离获得的NaHCO 固体需在阴凉、干燥处自然晾干,不采用加热烘干的原因是NaHCO 受热会发
3 3
生分解:2NaHCO NaCO+CO↑+HO。
3 2 3 2 2
6.(1)该实验需要配置250mL NaHCO 溶液,取25.00 mL于锥形瓶中后用0.5000 mol/L标准盐酸溶液
3
滴定该NaHCO 溶液,所需的定量仪器有电子天平、250mL容量瓶、酸式滴定管、碱式滴定管;(2)碳酸氢
3
钠溶液显碱性,滴定前加入甲基橙溶液显黄色,到达滴定终点后溶液为橙色,故当滴定至溶液由黄色变为
橙色且半分钟不变色为滴定终点;(3)碳酸氢钠样品中含有碳酸钠,滴定过程中发生反应:NaHCO +HCl=NaCl+H O+CO↑、NaCO+2HCl=2NaCl+H O+CO↑,用0.5000 mol/L标准盐酸溶液滴定
3 2 2 2 3 2 2
25.00 mL溶液,重复操作3次,平均消耗盐酸19.80 mL,n(HCl)=0.0198L×0.5000 mol/L=0.0099mol,设
n(NaHCO )=xmol,n(Na CO)=ymol,则x+2y=0.0099mol,84x+106y= ,解得x=0.0097,
3 2 3
y=0.0001,则该产品的纯度为 ,纯度级别为分析纯。