文档内容
热点强化 22 氧化还原滴定
1.原理
以氧化剂或还原剂为滴定剂,直接滴定一些具有还原性或氧化性的物质,或者间接滴定本身
并没有还原性或氧化性但能与某些还原剂或氧化剂反应的物质。
2.试剂
(1)常见用于滴定的氧化剂:KMnO 、KCr O、I 等。
4 2 2 7 2
(2)常见用于滴定的还原剂:亚铁盐、草酸、维生素C等。
3.指示剂
(1)氧化还原指示剂。
(2)专用指示剂,如淀粉可用作碘量法的指示剂。
(3)自身指示剂,如KMnO 溶液可自身指示滴定终点。
4
4.氧化还原反应滴定计算注意事项
(1)通过原子守恒或得失电子守恒快速建立待测物和滴定试剂之间的定量关系。
(2)在代入数据计算时要留意所取待测物和滴定试剂物理量的不同,不同物理量之间的计算
要留意单位之间的换算,如mL与L,g、kg与mg等。
(3)结果表达要关注待测物给定的量与滴定时实际取用的量是否一致,如给定待测物是1 L或
500 mL,滴定时取用了其中的100 mL或25 mL,后续数据的处理和最终结果的表达要与给
定的量保持一致。
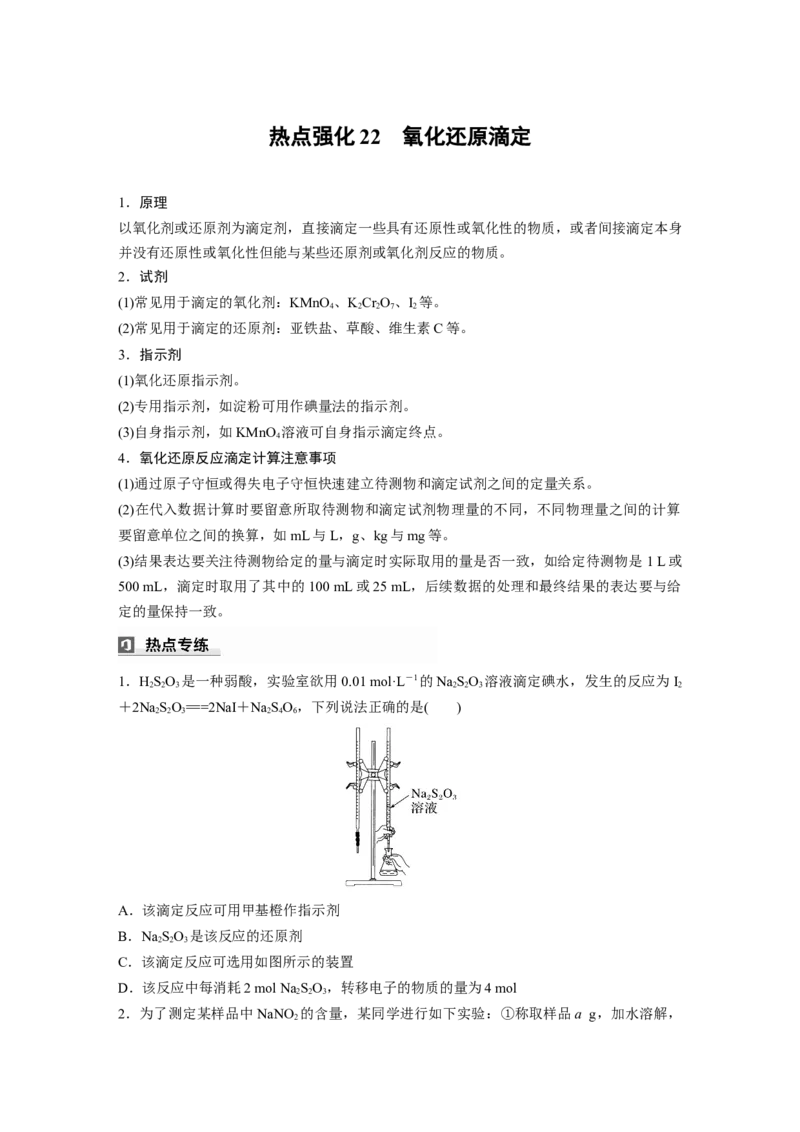
1.HSO 是一种弱酸,实验室欲用0.01 mol·L-1的NaSO 溶液滴定碘水,发生的反应为I
2 2 3 2 2 3 2
+2NaSO===2NaI+NaSO,下列说法正确的是( )
2 2 3 2 4 6
A.该滴定反应可用甲基橙作指示剂
B.NaSO 是该反应的还原剂
2 2 3
C.该滴定反应可选用如图所示的装置
D.该反应中每消耗2 mol Na SO,转移电子的物质的量为4 mol
2 2 3
2.为了测定某样品中NaNO 的含量,某同学进行如下实验:①称取样品a g,加水溶解,
2配制成100 mL溶液。②取25.00 mL溶液于锥形瓶中,用0.020 0 mol·L-1 KMnO 标准溶液
4
(酸
性)进行滴定,滴定结束后消耗KMnO 溶液 V mL。
4
(1)滴定过程中发生反应的离子方程式是____________________________________________
______________________________________________________________________________;
测得该样品中NaNO 的质量分数为_______________________________________________。
2
(2)若滴定过程中刚出现颜色变化就停止滴定,则测定结果____________(填“偏大”“偏
小”或“无影响”)。
3.烟道气中的NO 是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。
x
将V L气样通入适量酸化的HO 溶液中,使NO 完全被氧化为NO,加水稀释至100.00
2 2 x
mL。量取20.00 mL该溶液,加入V mL c mol·L-1 FeSO 标准溶液(过量),充分反应后,
1 1 4
用c mol·L-1 KCr O 标准溶液滴定剩余的Fe2+,终点时消耗KCr O 溶液V mL。
2 2 2 7 2 2 7 2
回答下列问题:
(1)滴定过程中发生下列反应:
3Fe2++NO+4H+===NO↑+3Fe3++2HO、Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2 2
则气样中NO 折合成NO 的含量为____________________ mg·m-3。
x 2
(2)若FeSO 标准溶液部分变质,会使测定结果__________(填“偏高”“偏低”或“无影
4
响”)。