文档内容
第 43 讲 电解原理应用新拓展
[复习目标] 1.深化对电解原理及规律的理解,提升应用电解原理综合分析解决实际问题的
能力。2.熟知电解原理创新试题的呈现方式及问题设置,总结解答此类问题的一般方法及规
律。
1.电解原理常见的考查点
电解原理及应用是高考高频考点,该类试题往往与生产、生活及新科技等相联系,以装置图
或流程图为载体呈现,题材广、信息新,题目具有一定难度。主要考查阴、阳极的判断、电
极反应式及电解反应方程式的书写、溶液离子浓度变化及有关计算等。
2.“5点”突破电解综合应用题
(1)分清阴、阳极,与电源正极相连的为阳极,与电源负极相连的为阴极,两极反应为“阳
氧阴还”。
(2)剖析离子移向,阳离子移向阴极,阴离子移向阳极。(注意离子交换膜会限制某些离子的
移动方向)
(3)注意放电顺序,正确判断放电的微粒或物质。
(4)注意介质,正确判断反应产物,酸性介质不出现OH-,碱性介质不出现H+;不能想当然
地认为金属作阳极,电极产物为金属阳离子。
(5)注意得失电子守恒和电荷守恒,正确书写电极反应式。
类型一 电解与物质制备
1.(2023·浙江1月选考,11)在熔融盐体系中,通过电解TiO 和SiO 获得电池材料(TiSi),
2 2
电解装置如图,下列说法正确的是( )
A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:8H++TiO+SiO+8e-===TiSi+4HO
2 2 2
C.该体系中,石墨优先于Cl-参与反应
D.电解时,阳离子向石墨电极移动
答案 C
解析 由图可知,石墨优先于Cl-参与反应,在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,与电源正极相连,则电极 A作阴极,TiO 和SiO 得到电子产生
2 2
电池材料(TiSi),电极反应为TiO+SiO+8e-===TiSi+4O2-。
2 2
2.(2022·重庆,12)硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电
解槽中水溶液的主要成分及反应过程如图所示。
下列说法错误的是( )
A.惰性电极2为阳极
B.反应前后WO、WO数量不变
C.消耗1 mol氧气,可得到1 mol硝酮
D.外电路通过1 mol电子,可得到1 mol水
答案 C
解析 惰性电极2,Br-被氧化为Br ,为阳极,故A正确;WO、WO循环反应,反应前后
2
WO、WO数量不变,故B正确;总反应为氧气把二丁基-N-羟基胺氧化为硝酮,1 mol二丁
基-N-羟基胺失去2 mol H原子生成1 mol硝酮,氧气最终生成水,根据氧原子守恒,消耗1
mol氧气,可得到2 mol硝酮,故C错误;外电路通过1 mol电子时生成0.5 mol H O ,HO
2 2 2 2
最终生成水,根据氧原子守恒,可得到1 mol水,故D正确。
3.(2022·湖北,14)含磷有机物应用广泛。电解法可实现由白磷直接制备 Li[P(CN)],过程
2
如图所示(Me为甲基)。下列说法正确的是( )
A.生成1 mol Li[P(CN) ],理论上外电路需要转移2 mol电子
2
B.阴极上的电极反应为:P+8CN--4e-===4[P(CN) ]-
4 2
C.在电解过程中CN-向铂电极移动
D.电解产生的H 中的氢元素来自于LiOH
2
答案 D
解析 石墨电极为阳极,对应的电极反应式为P +8CN--4e-===4[P(CN) ]-,则生成1 mol
4 2
Li[P(CN)],理论上外电路需要转移1 mol电子,A错误;阴极上发生还原反应,应该得电
2
子,电极反应式为2HCN+2e-===H↑+2CN-,B错误;石墨电极为阳极,铂电极为阴极,
2CN-应该向阳极移动,即移向石墨电极,C错误;由所给图示可知HCN在阴极放电,产生
CN-和H ,而HCN中的H来自于LiOH,则电解产生的H 中的氢元素来自于LiOH,D正
2 2
确。
类型二 电解与分离、提纯
4.我国科学家以石墨烯壳层封装钴镍纳米粒子的“铠甲”催化剂作电极,实现了合成气中
HS杂质的高效去除,其工作原理如图所示。下列说法错误的是( )
2
A.x为电源负极,阴极区溶液的pH增大
B.为同时实现氢气和硫粉的分离与回收,隔膜为阳离子交换膜
C.阳极的电极反应式为HS-2e-===S↓+2H+
2
D.通电一段时间后,阴极区的溶液可以补充到阳极区,实现电解液的再生
答案 C
解析 据图可知与电源y连接的电极上HS发生氧化反应转化为S,所以y为电源正极,x
2
为电源负极,阴极发生还原反应,电极反应式为 2HO+2e-===2OH-+H↑,所以阴极区
2 2
溶液的pH增大,A正确;阳极发生氧化反应,电极反应式为 HS+2CO-2e-===S↓+
2
2HCO,C 错误;通电一段时间后,阴极区得到氢氧化钠溶液,阳极区得到 NaHCO ,
3
NaHCO 溶液与NaOH溶液反应生成NaCO ,所以将阴极区溶液补充到阳极区可实现电解
3 2 3
液的再生,D正确。
5.电解法常用于分离提纯物质,某混合物浆液含 Al(OH) 、MnO 和少量NaCrO 。考虑到
3 2 2 4
胶体的吸附作用使NaCrO 不易完全被水浸出,某研究小组利用设计的电解分离装置(如图),
2 4
使浆液分离成固体混合物和含铬元素溶液进行回收利用(已知:2CrO+2H+Cr O+
2
HO),下列说法不正确的是( )
2
A.阴极室生成的物质为NaOH和H
2
B.阳极发生的电极反应是2HO-4e-===4H++O↑
2 2
C.a离子交换膜为阳离子交换膜D.当外电路中转移2 mol电子时,阳极室可生成1 mol Cr O
2
答案 D
解析 电解时,阳极上水中的氢氧根离子放电:2HO-4e-===O↑+4H+,故CrO通过阴
2 2
(b)离子交换膜向阳极移动,因2CrO+2H+Cr O+HO为可逆反应,故外电路中转移 2
2 2
mol 电子时,阳极室生成的 Cr O 小于 1 mol;阴极上水中的氢离子放电:2HO+2e-
2 2
===H↑+2OH-,混合物浆液中的Na+通过阳(a)离子交换膜进入阴极,故阴极反应生成 H
2 2
和NaOH。
类型三 电解与“三废”治理
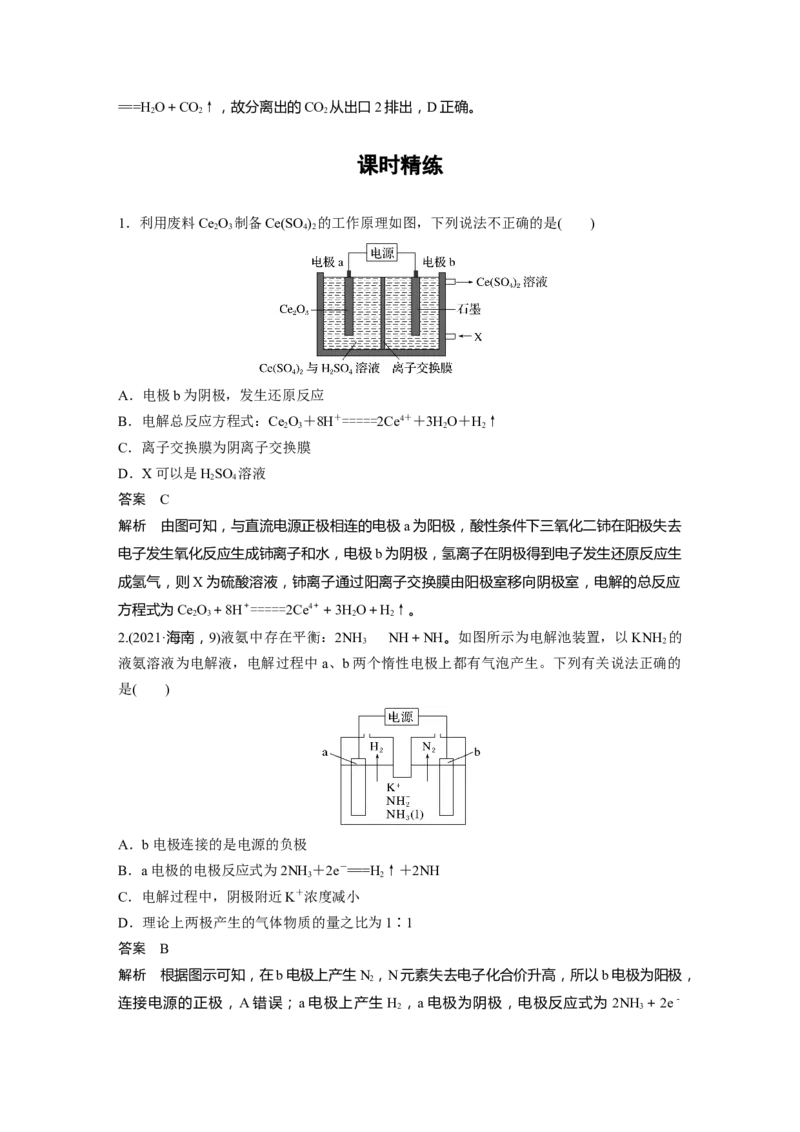
6.(2021·辽宁,13)利用 (Q)与 (QH )电解转化法从烟
2
气中分离CO 的原理如图。已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的
2
是( )
A.a为电源负极
B.溶液中Q的物质的量保持不变
C.CO 在M极被还原
2
D.分离出的CO 从出口2排出
2
答案 C
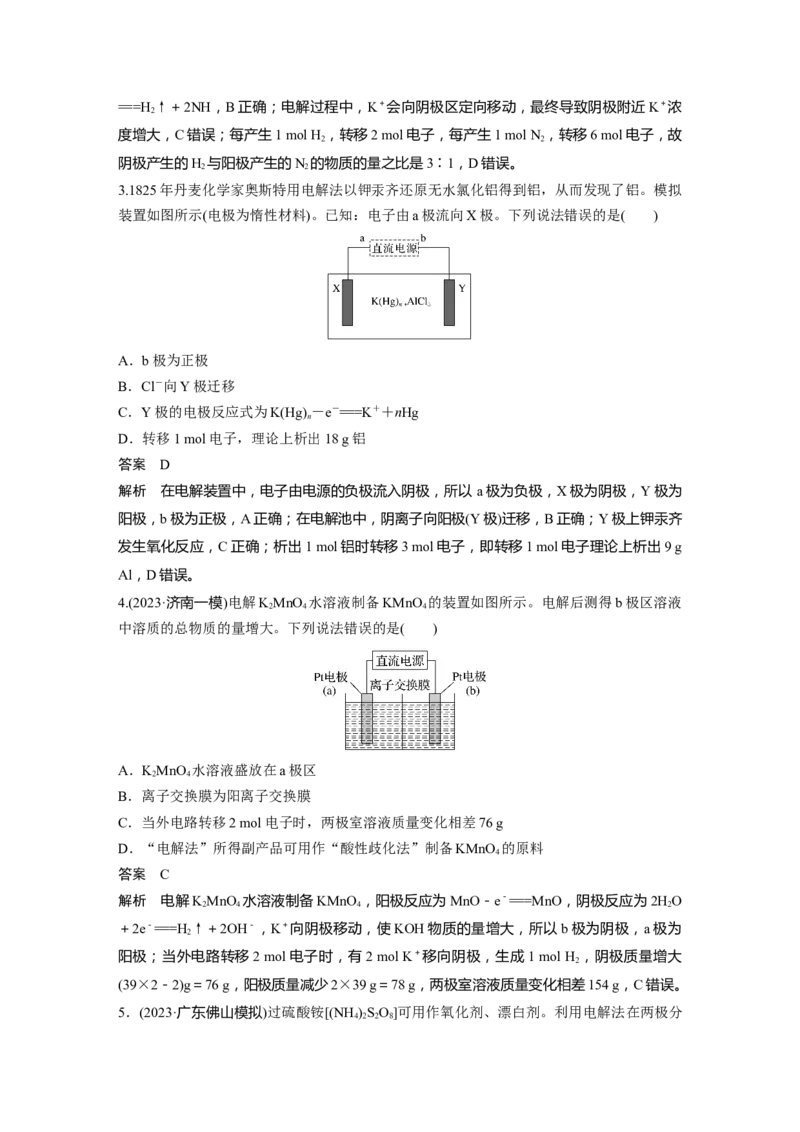
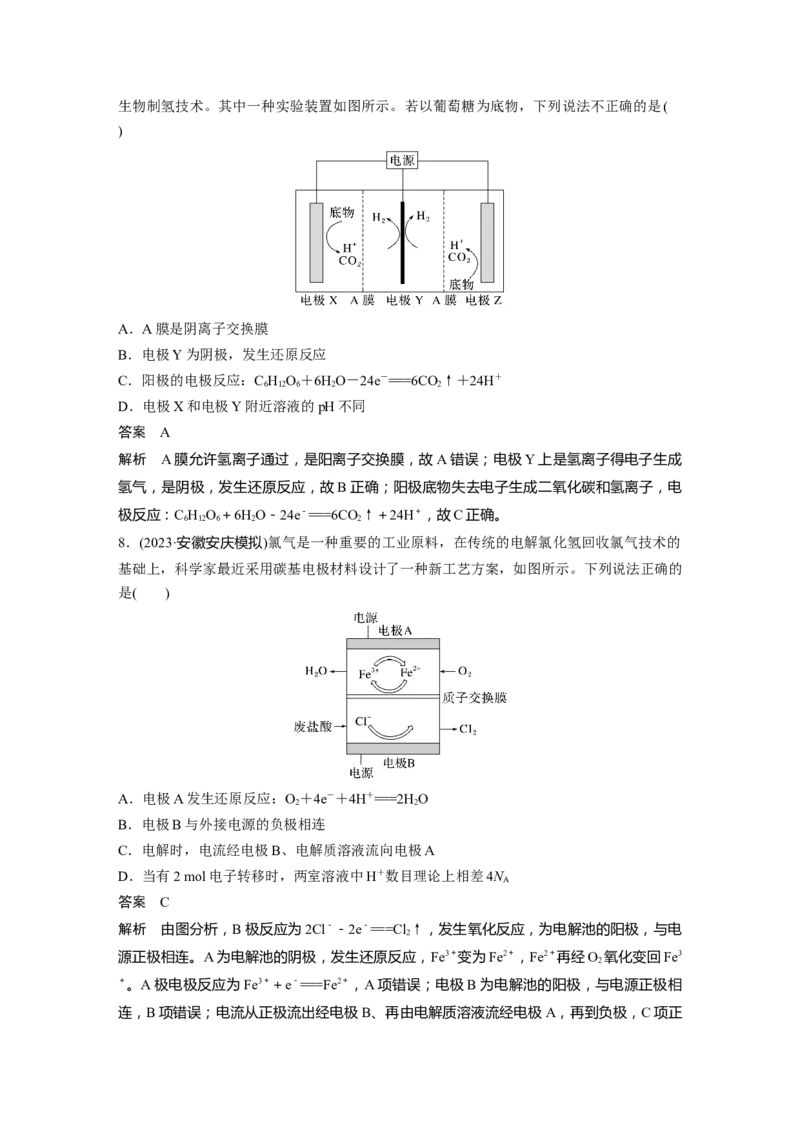
解析 由题干信息可知,M极发生的是由 (Q)转化为
(QH )的还原反应,故 M 极为阴极,电极反应式为 +2HO+2e-===
2 2
+2OH-,故与M极相连的a电极为负极,N极为阳极,电极反应式
为 -2e-=== +2H+,b极为电源正极,据此分析解题。
由分析可知,溶液中Q的物质的量保持不变,B正确;CO 在M极发生的反应为CO+OH-
2 2
===HCO,C错误;在M极上生成的HCO,向阳极移动,N极上发生的反应为HCO+H+===HO+CO↑,故分离出的CO 从出口2排出,D正确。
2 2 2
课时精练
1.利用废料Ce O 制备Ce(SO) 的工作原理如图,下列说法不正确的是( )
2 3 4 2
A.电极b为阴极,发生还原反应
B.电解总反应方程式:Ce O+8H+=====2Ce4++3HO+H↑
2 3 2 2
C.离子交换膜为阴离子交换膜
D.X可以是HSO 溶液
2 4
答案 C
解析 由图可知,与直流电源正极相连的电极a为阳极,酸性条件下三氧化二铈在阳极失去
电子发生氧化反应生成铈离子和水,电极b为阴极,氢离子在阴极得到电子发生还原反应生
成氢气,则X为硫酸溶液,铈离子通过阳离子交换膜由阳极室移向阴极室,电解的总反应
方程式为Ce O+8H+=====2Ce4++3HO+H↑。
2 3 2 2
2.(2021·海南,9)液氨中存在平衡:2NH NH+NH。如图所示为电解池装置,以KNH 的
3 2
液氨溶液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的
是( )
A.b电极连接的是电源的负极
B.a电极的电极反应式为2NH +2e-===H↑+2NH
3 2
C.电解过程中,阴极附近K+浓度减小
D.理论上两极产生的气体物质的量之比为1∶1
答案 B
解析 根据图示可知,在b电极上产生N,N元素失去电子化合价升高,所以b电极为阳极,
2
连接电源的正极,A错误;a电极上产生 H ,a电极为阴极,电极反应式为 2NH +2e-
2 3===H↑+2NH,B正确;电解过程中,K+会向阴极区定向移动,最终导致阴极附近K+浓
2
度增大,C错误;每产生1 mol H ,转移2 mol电子,每产生1 mol N ,转移6 mol电子,故
2 2
阴极产生的H 与阳极产生的N 的物质的量之比是3∶1,D错误。
2 2
3.1825年丹麦化学家奥斯特用电解法以钾汞齐还原无水氯化铝得到铝,从而发现了铝。模拟
装置如图所示(电极为惰性材料)。已知:电子由a极流向X极。下列说法错误的是( )
A.b极为正极
B.Cl-向Y极迁移
C.Y极的电极反应式为K(Hg) -e-===K++nHg
n
D.转移1 mol电子,理论上析出18 g铝
答案 D
解析 在电解装置中,电子由电源的负极流入阴极,所以 a极为负极,X极为阴极,Y极为
阳极,b极为正极,A正确;在电解池中,阴离子向阳极(Y极)迁移,B正确;Y极上钾汞齐
发生氧化反应,C正确;析出1 mol铝时转移3 mol电子,即转移1 mol电子理论上析出9 g
Al,D错误。
4.(2023·济南一模)电解KMnO 水溶液制备KMnO 的装置如图所示。电解后测得b极区溶液
2 4 4
中溶质的总物质的量增大。下列说法错误的是( )
A.KMnO 水溶液盛放在a极区
2 4
B.离子交换膜为阳离子交换膜
C.当外电路转移2 mol电子时,两极室溶液质量变化相差76 g
D.“电解法”所得副产品可用作“酸性歧化法”制备KMnO 的原料
4
答案 C
解析 电解KMnO 水溶液制备KMnO ,阳极反应为MnO-e-===MnO,阴极反应为2HO
2 4 4 2
+2e-===H↑+2OH-,K+向阴极移动,使KOH物质的量增大,所以b极为阴极,a极为
2
阳极;当外电路转移2 mol电子时,有2 mol K+移向阴极,生成1 mol H ,阴极质量增大
2
(39×2-2)g=76 g,阳极质量减少2×39 g=78 g,两极室溶液质量变化相差154 g,C错误。
5.(2023·广东佛山模拟)过硫酸铵[(NH )SO]可用作氧化剂、漂白剂。利用电解法在两极分
4 2 2 8别生产过硫酸铵和过氧化氢的装置如图所示。下列说法错误的是( )
A.a为外接电源的负极
B.电解总反应:O+2H++2SO=====HO+SO
2 2 2 2
C.阴离子交换膜可用阳离子交换膜替代
D.电解池工作时,Ⅰ室溶液质量理论上逐渐减小
答案 C
解析 由(NH )SO →(NH )SO ,氧元素化合价升高被氧化,故右侧Pt电极为阳极,b为外
4 2 4 4 2 2 8
接电源正极,a为外接电源负极,左侧Pt电极为阴极。阴极氧气被还原,阳极硫酸根离子被
氧化,电解总反应正确,B正确;根据阳极产物可知,反应需要消耗硫酸根离子,阴离子交
换膜不可用阳离子交换膜替代,C错误;电解池工作时,Ⅰ室发生反应:O +2e-+2H+
2
===HO,同时SO移向阳极,故Ⅰ室溶液质量理论上逐渐减小,D正确。
2 2
6.(2023·杭州重点中学高三联考)科学家利用多晶铜高效催化电解CO 制乙烯,原理如图所
2
示。已知:电解前后电解液浓度几乎不变。下列说法正确的是( )
A.铂电极为阳极,产生的气体是O 和CO
2 2
B.多晶铜电极的电极反应式为2CO+12HCO+12e-===C H+12CO+4HO
2 2 4 2
C.通电过程中,溶液中HCO通过阴离子交换膜向右槽移动
D.当电路中通过0.6 mol电子时,理论上能产生C H 1.12 L
2 4
答案 A
解析 该电解池的总反应方程式为2CO +2HO===C H +3O ,多晶铜电极为阴极,该电极
2 2 2 4 2
的电极反应式为14CO +8HO+12e-===C H +12HCO,铂电极为阳极,该电极的反应式为
2 2 2 4
12HCO-12e-===12CO +3O +6HO。HCO在铂电极发生反应,并且电解前后电解液浓度
2 2 2
几乎不变,所以溶液中HCO通过阴离子交换膜向左槽移动,故C错误;由多晶铜电极电极
反应式分析可知,当电路中通过0.6 mol电子时,理论上能产生0.05 mol C H ,该题目没有
2 4
说明条件为标准状况,故D错误。
7.(2023·浙江省金、丽、衢十二校高三模拟)微生物电解池(MEC)是近年来快速发展的一种生物制氢技术。其中一种实验装置如图所示。若以葡萄糖为底物,下列说法不正确的是(
)
A.A膜是阴离子交换膜
B.电极Y为阴极,发生还原反应
C.阳极的电极反应:C H O+6HO-24e-===6CO↑+24H+
6 12 6 2 2
D.电极X和电极Y附近溶液的pH不同
答案 A
解析 A膜允许氢离子通过,是阳离子交换膜,故 A错误;电极Y上是氢离子得电子生成
氢气,是阴极,发生还原反应,故B正确;阳极底物失去电子生成二氧化碳和氢离子,电
极反应:C H O+6HO-24e-===6CO↑+24H+,故C正确。
6 12 6 2 2
8.(2023·安徽安庆模拟)氯气是一种重要的工业原料,在传统的电解氯化氢回收氯气技术的
基础上,科学家最近采用碳基电极材料设计了一种新工艺方案,如图所示。下列说法正确的
是( )
A.电极A发生还原反应:O+4e-+4H+===2HO
2 2
B.电极B与外接电源的负极相连
C.电解时,电流经电极B、电解质溶液流向电极A
D.当有2 mol电子转移时,两室溶液中H+数目理论上相差4N
A
答案 C
解析 由图分析,B极反应为2Cl--2e-===Cl↑,发生氧化反应,为电解池的阳极,与电
2
源正极相连。A为电解池的阴极,发生还原反应,Fe3+变为Fe2+,Fe2+再经O 氧化变回Fe3
2
+。A极电极反应为Fe3++e-===Fe2+,A项错误;电极B为电解池的阳极,与电源正极相
连,B项错误;电流从正极流出经电极B、再由电解质溶液流经电极A,再到负极,C项正确;A极区发生的反应为4Fe2++O +4H+===2HO+4Fe3+,该反应中每转移2 mol电子需
2 2
要消耗2 mol H+。同时,电解池工作时,每转移2 mol电子,有2 mol H+从B极经质子交换
膜流向A极,即A极H+没有发生变化。而B极由于H+移走而减少了2 mol,所以两极H+
数目相差2N ,D项错误。
A
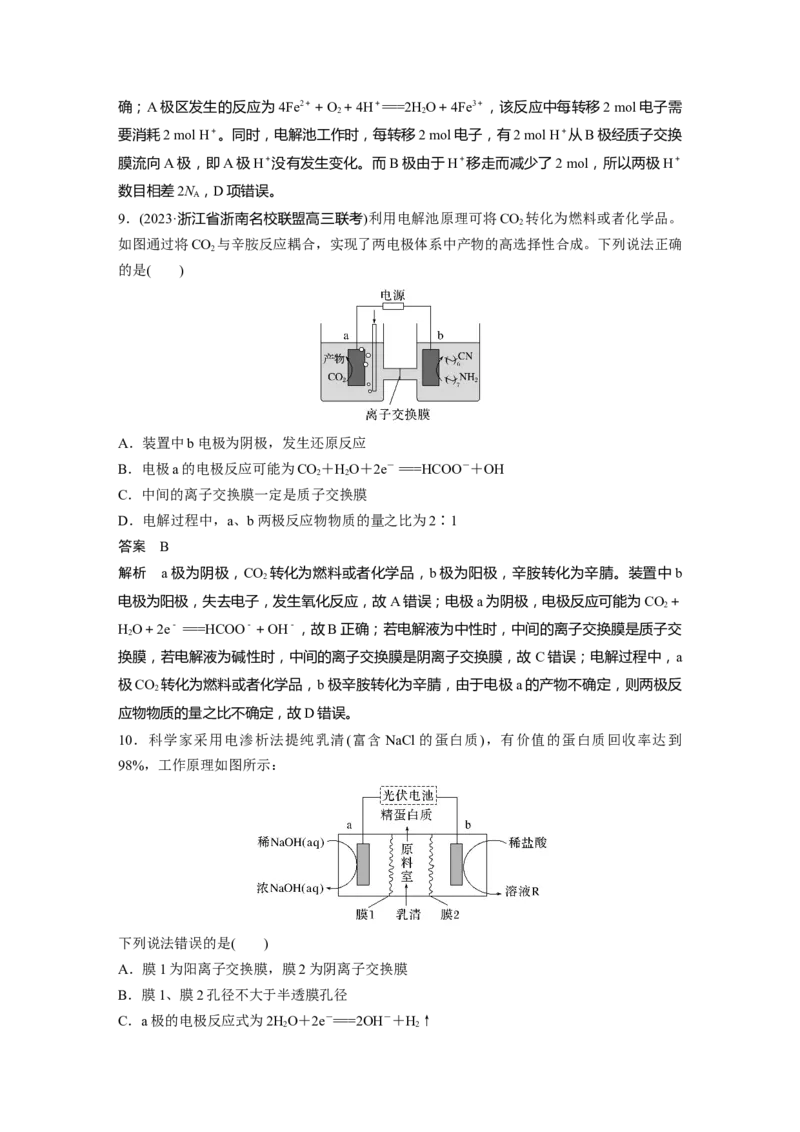
9.(2023·浙江省浙南名校联盟高三联考)利用电解池原理可将CO 转化为燃料或者化学品。
2
如图通过将CO 与辛胺反应耦合,实现了两电极体系中产物的高选择性合成。下列说法正确
2
的是( )
A.装置中b电极为阴极,发生还原反应
B.电极a的电极反应可能为CO+HO+2e- ===HCOO-+OH
2 2
C.中间的离子交换膜一定是质子交换膜
D.电解过程中,a、b两极反应物物质的量之比为2∶1
答案 B
解析 a极为阴极,CO 转化为燃料或者化学品,b极为阳极,辛胺转化为辛腈。装置中b
2
电极为阳极,失去电子,发生氧化反应,故A错误;电极a为阴极,电极反应可能为CO+
2
HO+2e- ===HCOO-+OH-,故B正确;若电解液为中性时,中间的离子交换膜是质子交
2
换膜,若电解液为碱性时,中间的离子交换膜是阴离子交换膜,故 C错误;电解过程中,a
极CO 转化为燃料或者化学品,b极辛胺转化为辛腈,由于电极a的产物不确定,则两极反
2
应物物质的量之比不确定,故D错误。
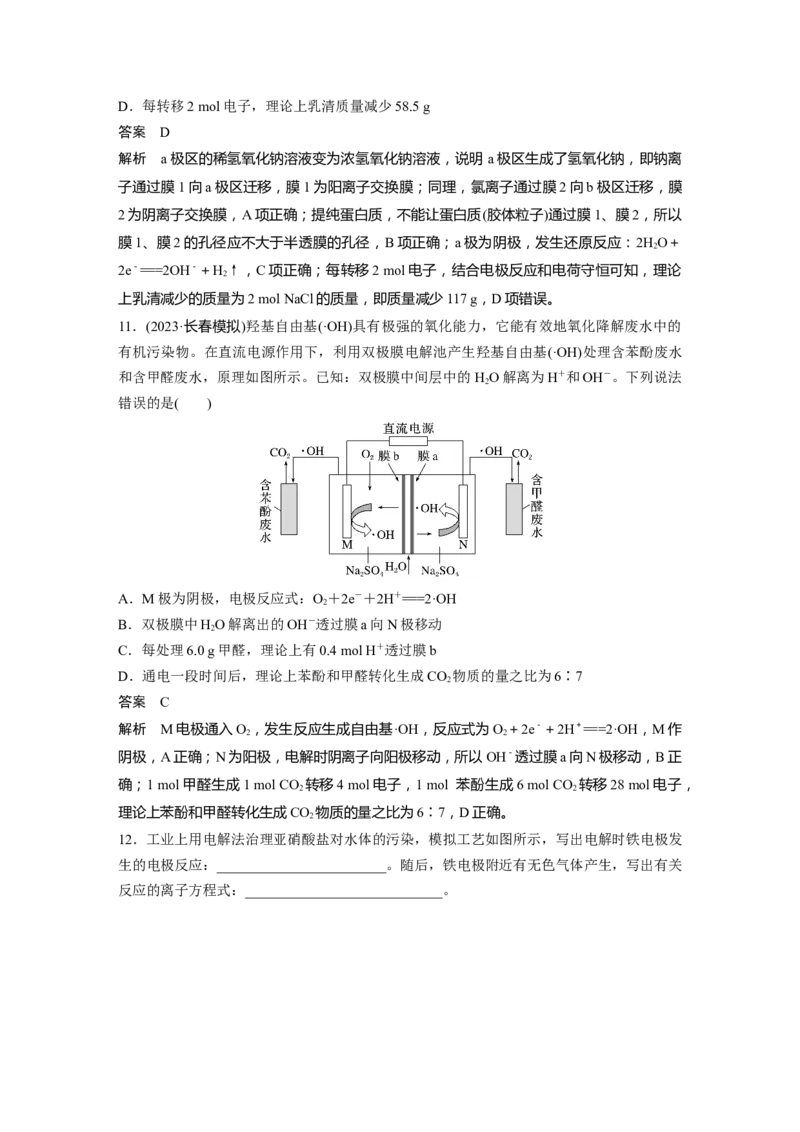
10.科学家采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质回收率达到
98%,工作原理如图所示:
下列说法错误的是( )
A.膜1为阳离子交换膜,膜2为阴离子交换膜
B.膜1、膜2孔径不大于半透膜孔径
C.a极的电极反应式为2HO+2e-===2OH-+H↑
2 2D.每转移2 mol电子,理论上乳清质量减少58.5 g
答案 D
解析 a极区的稀氢氧化钠溶液变为浓氢氧化钠溶液,说明 a极区生成了氢氧化钠,即钠离
子通过膜1向a极区迁移,膜1为阳离子交换膜;同理,氯离子通过膜2向b极区迁移,膜
2为阴离子交换膜,A项正确;提纯蛋白质,不能让蛋白质(胶体粒子)通过膜1、膜2,所以
膜1、膜2的孔径应不大于半透膜的孔径,B项正确;a极为阴极,发生还原反应:2HO+
2
2e-===2OH-+H↑,C项正确;每转移2 mol电子,结合电极反应和电荷守恒可知,理论
2
上乳清减少的质量为2 mol NaCl的质量,即质量减少117 g,D项错误。
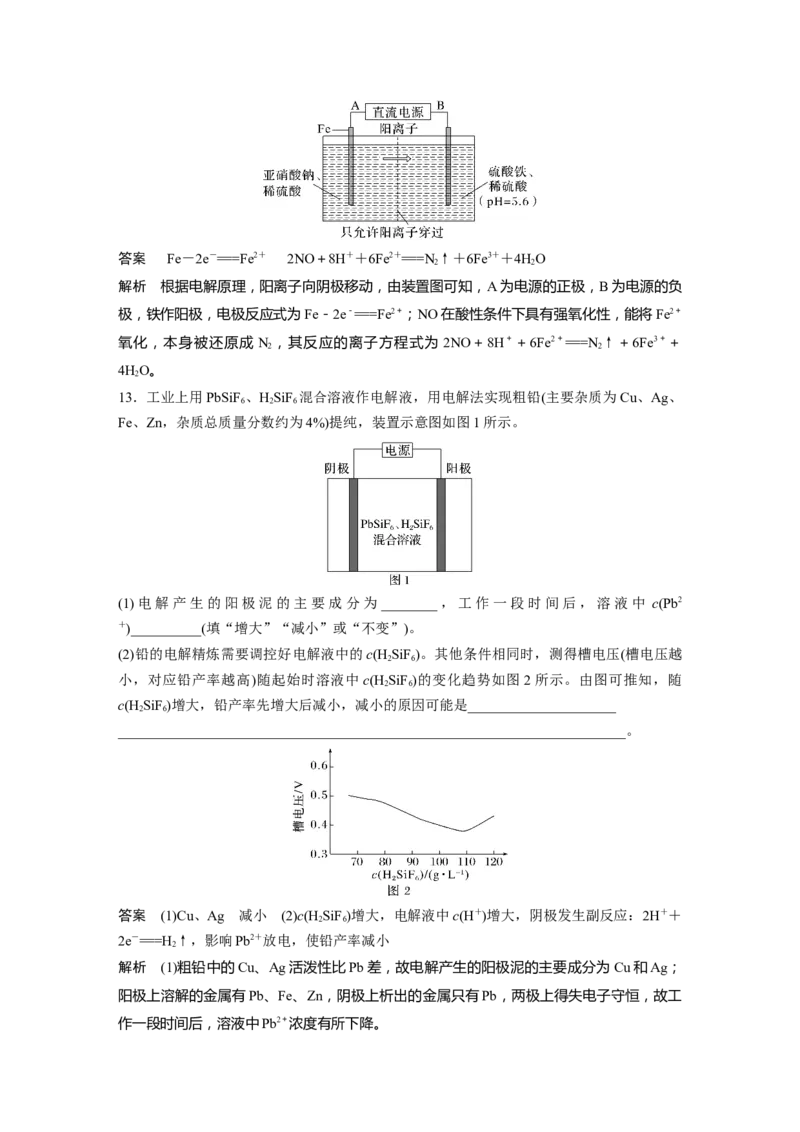
11.(2023·长春模拟)羟基自由基(·OH)具有极强的氧化能力,它能有效地氧化降解废水中的
有机污染物。在直流电源作用下,利用双极膜电解池产生羟基自由基(·OH)处理含苯酚废水
和含甲醛废水,原理如图所示。已知:双极膜中间层中的 HO解离为H+和OH-。下列说法
2
错误的是( )
A.M极为阴极,电极反应式:O+2e-+2H+===2·OH
2
B.双极膜中HO解离出的OH-透过膜a向N极移动
2
C.每处理6.0 g甲醛,理论上有0.4 mol H+透过膜b
D.通电一段时间后,理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7
2
答案 C
解析 M电极通入O ,发生反应生成自由基·OH,反应式为O +2e-+2H+===2·OH,M作
2 2
阴极,A正确;N为阳极,电解时阴离子向阳极移动,所以OH-透过膜a向N极移动,B正
确;1 mol甲醛生成1 mol CO 转移4 mol电子,1 mol 苯酚生成6 mol CO 转移28 mol电子,
2 2
理论上苯酚和甲醛转化生成CO 物质的量之比为6∶7,D正确。
2
12.工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图所示,写出电解时铁电极发
生的电极反应:________________________。随后,铁电极附近有无色气体产生,写出有关
反应的离子方程式:____________________________。答案 Fe-2e-===Fe2+ 2NO+8H++6Fe2+===N↑+6Fe3++4HO
2 2
解析 根据电解原理,阳离子向阴极移动,由装置图可知,A为电源的正极,B为电源的负
极,铁作阳极,电极反应式为Fe-2e-===Fe2+;NO在酸性条件下具有强氧化性,能将Fe2+
氧化,本身被还原成 N ,其反应的离子方程式为 2NO+8H++6Fe2+===N↑+6Fe3++
2 2
4HO。
2
13.工业上用PbSiF 、HSiF 混合溶液作电解液,用电解法实现粗铅(主要杂质为Cu、Ag、
6 2 6
Fe、Zn,杂质总质量分数约为4%)提纯,装置示意图如图1所示。
(1)电解产生的阳极泥的主要成分为 ________,工作一段时间后,溶液中 c(Pb2
+)__________(填“增大”“减小”或“不变”)。
(2)铅的电解精炼需要调控好电解液中的c(H SiF)。其他条件相同时,测得槽电压(槽电压越
2 6
小,对应铅产率越高)随起始时溶液中c(H SiF)的变化趋势如图2所示。由图可推知,随
2 6
c(H SiF)增大,铅产率先增大后减小,减小的原因可能是_____________________
2 6
________________________________________________________________________。
答案 (1)Cu、Ag 减小 (2)c(H SiF)增大,电解液中c(H+)增大,阴极发生副反应:2H++
2 6
2e-===H↑,影响Pb2+放电,使铅产率减小
2
解析 (1)粗铅中的Cu、Ag活泼性比Pb差,故电解产生的阳极泥的主要成分为Cu和Ag;
阳极上溶解的金属有Pb、Fe、Zn,阴极上析出的金属只有Pb,两极上得失电子守恒,故工
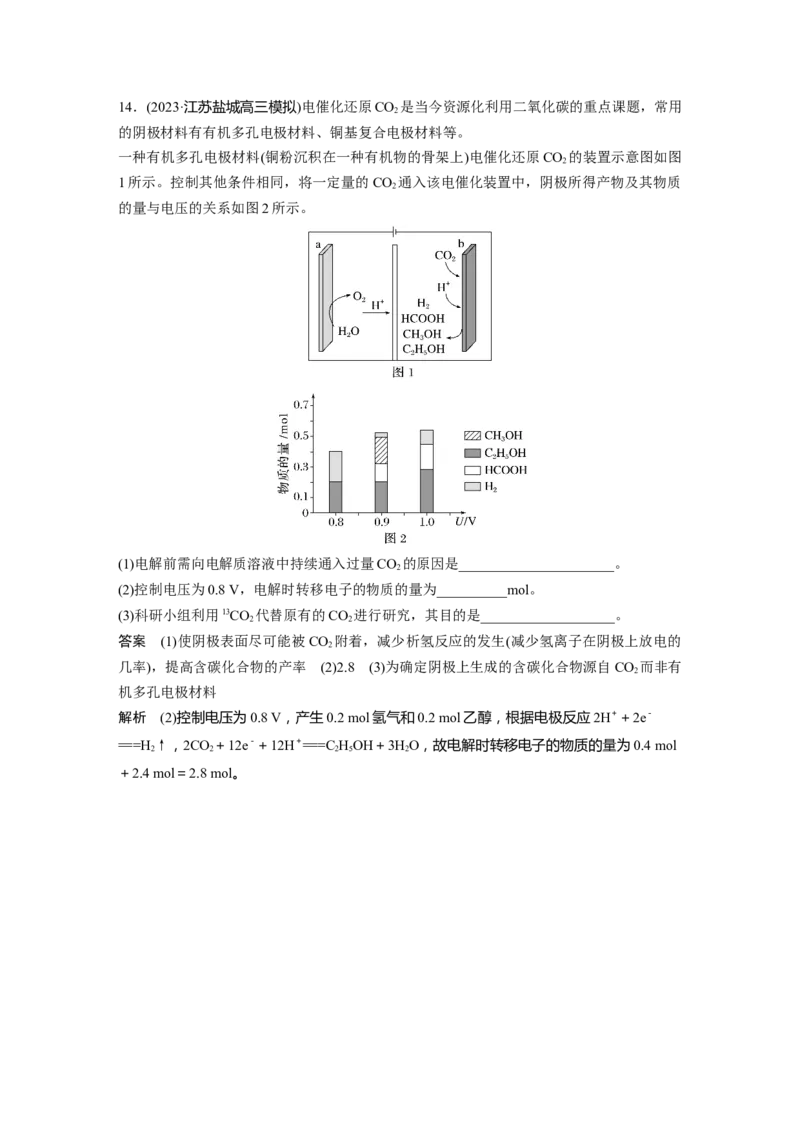
作一段时间后,溶液中Pb2+浓度有所下降。14.(2023·江苏盐城高三模拟)电催化还原CO 是当今资源化利用二氧化碳的重点课题,常用
2
的阴极材料有有机多孔电极材料、铜基复合电极材料等。
一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO 的装置示意图如图
2
1所示。控制其他条件相同,将一定量的CO 通入该电催化装置中,阴极所得产物及其物质
2
的量与电压的关系如图2所示。
(1)电解前需向电解质溶液中持续通入过量CO 的原因是______________________。
2
(2)控制电压为0.8 V,电解时转移电子的物质的量为__________mol。
(3)科研小组利用13CO 代替原有的CO 进行研究,其目的是___________________。
2 2
答案 (1)使阴极表面尽可能被CO 附着,减少析氢反应的发生(减少氢离子在阴极上放电的
2
几率),提高含碳化合物的产率 (2)2.8 (3)为确定阴极上生成的含碳化合物源自CO 而非有
2
机多孔电极材料
解析 (2)控制电压为0.8 V,产生0.2 mol氢气和0.2 mol乙醇,根据电极反应2H++2e-
===H↑,2CO+12e-+12H+===C HOH+3HO,故电解时转移电子的物质的量为0.4 mol
2 2 2 5 2
+2.4 mol=2.8 mol。