文档内容
微题型 02 晶体结构及相关计算
目录
.....................................................................................................................................1
【考向一】晶胞的结构与类型判断..................................................................................................................1
【考向二】晶体中微粒数或化学式的计算......................................................................................................5
【考向三】晶胞中的原子坐标..........................................................................................................................7
【考向四】晶体密度的相关计算......................................................................................................................8
【考向五】晶胞利用率的计算..........................................................................................................................9
【考向六】晶胞中特定位置微粒间距的计算..................................................................................................9
【考向七】晶胞中投影问题............................................................................................................................12
【考向八】晶胞中的配位数............................................................................................................................14
...................................................................................................................................16
【考向一】晶胞的结构与类型判断
【典例1】(2023上·江苏·高三校联考阶段练习)高纯度的铁可以使用氢还原高纯度的氧化铁或直接用五
羰基合铁 (熔点为 ,沸点为 )热分解制得。实验室可用赤血盐( )溶液检验
,黄血盐( )溶液检验 。下列有关铁及其化合物的说法正确的是
A. 元素位于周期表的第ⅧB族
B.赤血盐中铁元素核外有5个未成对电子
C. 晶体是离子晶体
D.若黄血盐受热分解产物之一的晶胞结构上图所示,则其化学式为
一、晶胞1.定义:晶胞是描述晶体结构的_基本单元__。
2.晶体与晶胞的关系:数量巨大的晶胞“_无隙并置__”构成晶体。
①相邻晶胞之间没有任何间隙。
②所有晶胞都是平行排列、取向相同。
二、晶体结构的堆积模型
1.晶体结构的密堆积的原理
金属原子、离子或分子在没有其他因素(如氢键)影响时,在空间的排列大都服从紧密堆积原理。这是因为
金属键、离子键和分子间作用力均没有_方向性__,因此都趋向于使原子、离子或分子吸引尽可能多的其
他原子、离子或分子分布于周围,并以密堆积的方式_降低__体系的能量,使晶体变得比较稳定。
2.等径圆球的密堆积(金属晶体)
①三维空间模型
A.非密置层在三维空间堆积
a.简单立方堆积
相邻非密置层原子的原子核在_同一直线上__的堆积,空间利用率太低,只有金属_钋__(Po)采用这种堆积
方式。
b.体心立方堆积
将上层金属原子填入下层金属原子形成的凹穴中,并使非密置层的原子稍稍分离,每层均照此堆积。这种
堆积方式所得的晶胞是一个含有两个原子的立方体,一个原子在立方体的_顶角__,另一个原子在立方体
的_体心__,其空间利用率比简单立方堆积_高__,碱金属属于这种堆积方式。
B.密置层在三维空间堆积
a.六方最密堆积
按ABABAB……的方式堆积,称为_A 型最密堆积__
3
b.面心立方最密堆积
按ABCABCABC……的方式堆积,称为_A 型最密堆积__。
1②常见的堆积模型
三种典型结构型式 面心立方最密堆积(A ) 体心立方堆积(A ) 六方最密堆积(A )
1 2 3
常见金属 Cu、Au、Ag Na、K、Fe Mg、Zn、Ti
结构示意图
晶胞
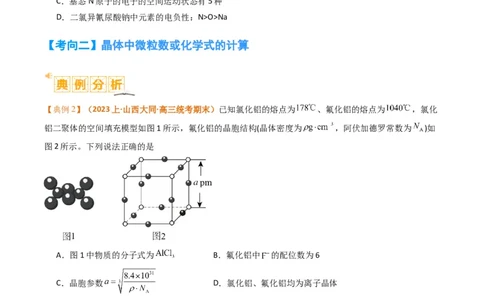
配位数 _12__ _8__ _12__
空间利用率 _74%__ 68% 74%
每个晶胞所含原子数 _4__ _2__ _2__
三、非等径圆球的密堆积(离子晶体)
①由于阴、阳离子的半径不同,因此离子晶体为_不等径圆球__的密堆积,可以将这种堆积方式看成是大
球先按一定的方式做_等径圆球__的密堆积,小球再填充在大球所形成的_空隙__中。
②在一些离子晶体中,阴离子半径较大,应先将阴离子看成是_等径圆球__进行密堆积,而阳离子有序地
填在阴离子所形成的空隙中。例如,NaCl晶体中的Cl-按_A 型__方式进行最密堆积,Na+填在Cl-所形成的
1
空隙中;ZnS晶体中S2-按_A 型__方式进行最密堆积,Zn2+填入S2-所形成的空隙中。
1
【变式1-1】(2023上·山西·高三校联考阶段练习)黄铜矿是工业炼铜的原料,含有的主要元素是硫、铁、
铜。下列有关说法正确的是
A.基态硫原子中核外电子有9种空间运动状态
B.硫元素最简单氢化物的分子的VSEPR构型是V形
C.铁元素在元素周期表的ds区
D.CuCl熔点为426℃,熔融时几乎不导电,容易形成二聚体,说明CuCl是原子晶体
【变式1-2】(2023上·江苏·高三校联考开学考试)我国疾控中心利用尿素( )制备出了两种低温消毒剂:三聚氰酸( )和二氯异氰尿酸钠( )。已知:尿素分
子中所有原子共平面。下列说法错误的是
A.尿素分子中键角 与键角 基本相等
B.三聚氰酸晶体属于分子晶体
C.基态N原子的电子的空间运动状态有5种
D.二氯异氰尿酸钠中元素的电负性:N>O>Na
【考向二】晶体中微粒数或化学式的计算
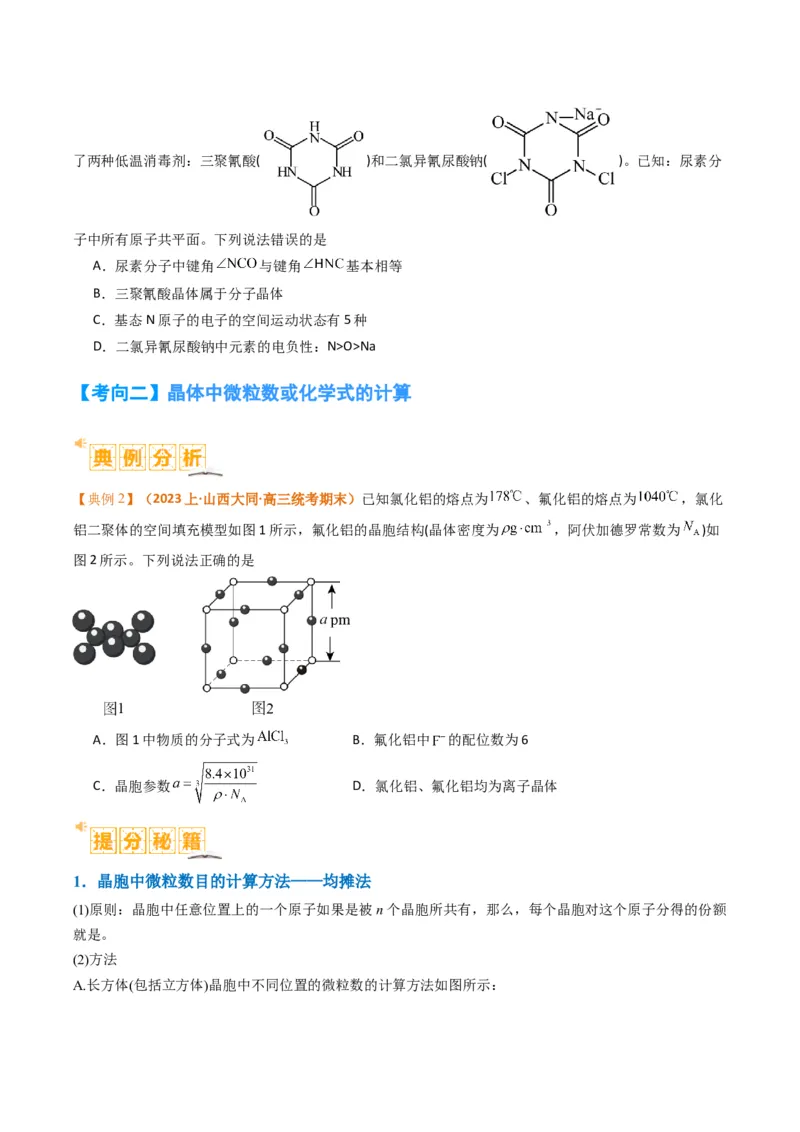
【典例2】(2023上·山西大同·高三统考期末)已知氯化铝的熔点为 、氟化铝的熔点为 ,氯化
铝二聚体的空间填充模型如图1所示,氟化铝的晶胞结构(晶体密度为 ,阿伏加德罗常数为 )如
图2所示。下列说法正确的是
A.图1中物质的分子式为 B.氟化铝中 的配位数为6
C.晶胞参数 D.氯化铝、氟化铝均为离子晶体
1.晶胞中微粒数目的计算方法——均摊法
(1)原则:晶胞中任意位置上的一个原子如果是被n个晶胞所共有,那么,每个晶胞对这个原子分得的份额
就是。
(2)方法
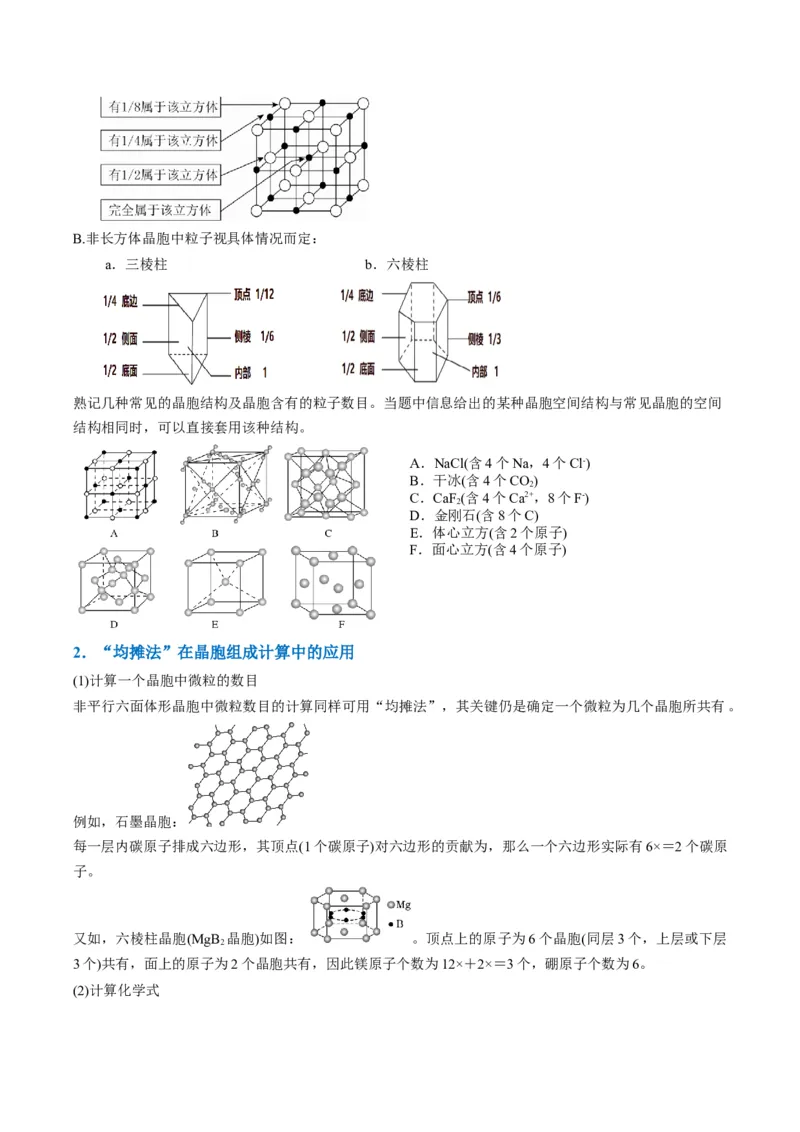
A.长方体(包括立方体)晶胞中不同位置的微粒数的计算方法如图所示:B.非长方体晶胞中粒子视具体情况而定:
a.三棱柱 b.六棱柱
熟记几种常见的晶胞结构及晶胞含有的粒子数目。当题中信息给出的某种晶胞空间结构与常见晶胞的空间
结构相同时,可以直接套用该种结构。
A.NaCl(含4个Na,4个Cl-)
B.干冰(含4个CO)
2
C.CaF (含4个Ca2+,8个F-)
2
D.金刚石(含8个C)
E.体心立方(含2个原子)
F.面心立方(含4个原子)
2.“均摊法”在晶胞组成计算中的应用
(1)计算一个晶胞中微粒的数目
非平行六面体形晶胞中微粒数目的计算同样可用“均摊法”,其关键仍是确定一个微粒为几个晶胞所共有。
例如,石墨晶胞:
每一层内碳原子排成六边形,其顶点(1个碳原子)对六边形的贡献为,那么一个六边形实际有6×=2个碳原
子。
又如,六棱柱晶胞(MgB 晶胞)如图: 。顶点上的原子为6个晶胞(同层3个,上层或下层
2
3个)共有,面上的原子为2个晶胞共有,因此镁原子个数为12×+2×=3个,硼原子个数为6。
(2)计算化学式(3)①单位换算:1 nm=10-7 cm、1 pm=10-10 cm
②金属晶体中体心立方、面心立方堆积中的几组公式(设棱长为a)
a.面对角线长:a b.体对角线长:a c.体心立方堆积:4r=a(r为原子半径)
d.面心立方堆积:4r=a(r为原子半径)
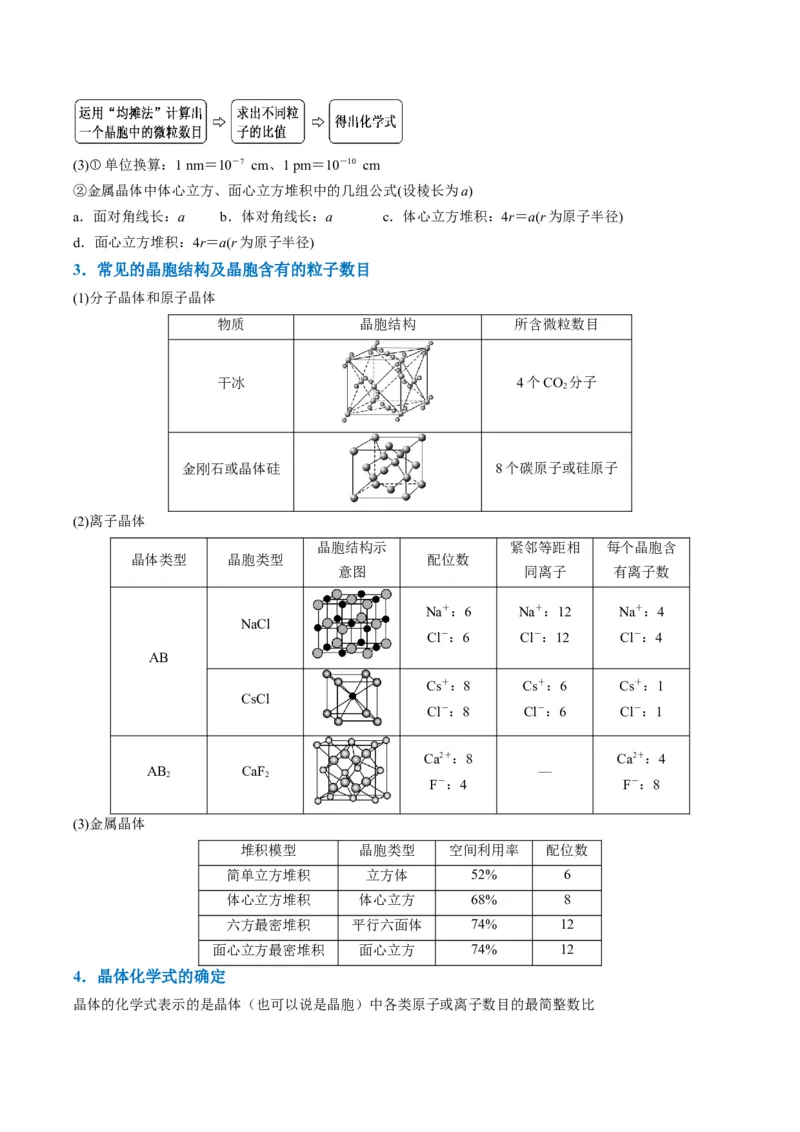
3.常见的晶胞结构及晶胞含有的粒子数目
(1)分子晶体和原子晶体
物质 晶胞结构 所含微粒数目
干冰 4个CO 分子
2
金刚石或晶体硅 8个碳原子或硅原子
(2)离子晶体
晶胞结构示 紧邻等距相 每个晶胞含
晶体类型 晶胞类型 配位数
意图 同离子 有离子数
Na+:6 Na+:12 Na+:4
NaCl
Cl-:6 Cl-:12 Cl-:4
AB
Cs+:8 Cs+:6 Cs+:1
CsCl
Cl-:8 Cl-:6 Cl-:1
Ca2+:8 Ca2+:4
AB CaF —
2 2
F-:4 F-:8
(3)金属晶体
堆积模型 晶胞类型 空间利用率 配位数
简单立方堆积 立方体 52% 6
体心立方堆积 体心立方 68% 8
六方最密堆积 平行六面体 74% 12
面心立方最密堆积 面心立方 74% 12
4.晶体化学式的确定
晶体的化学式表示的是晶体(也可以说是晶胞)中各类原子或离子数目的最简整数比团簇分子或纳米颗粒与晶胞不同,这两类物质是独立的分子,所有原子均为该分子所有。与晶体中多个晶
胞共用原子不相同
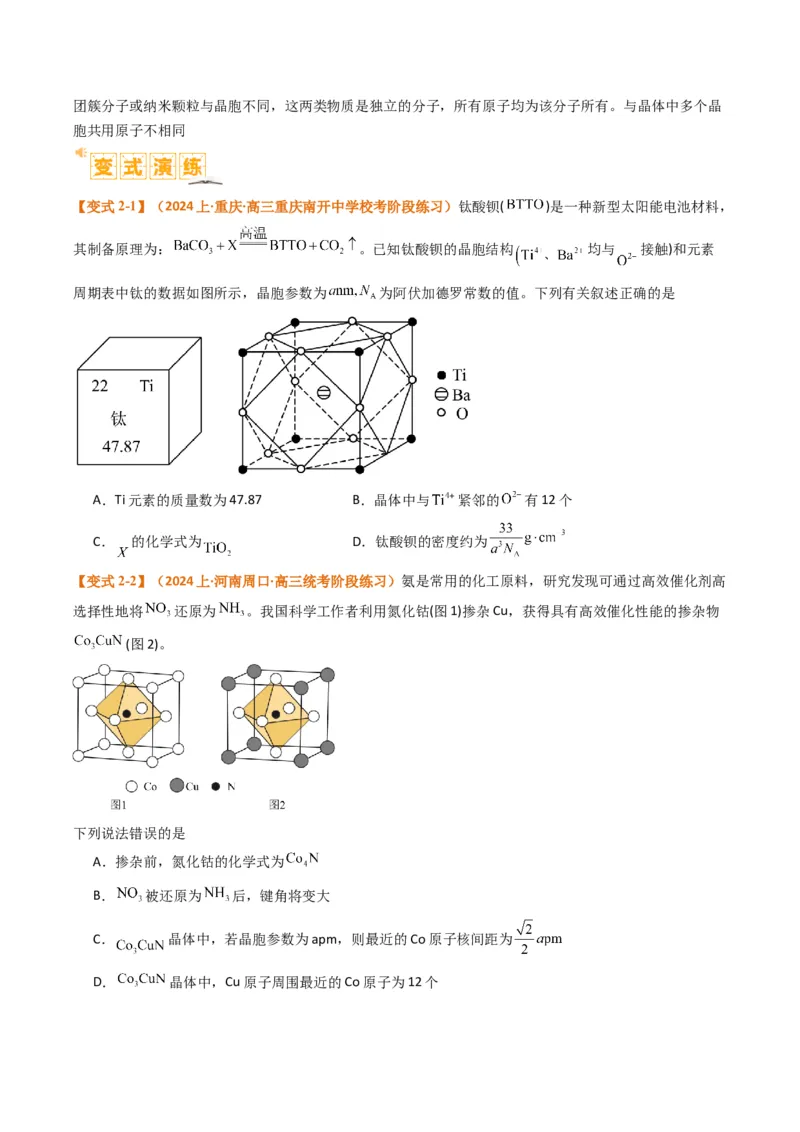
【变式2-1】(2024上·重庆·高三重庆南开中学校考阶段练习)钛酸钡( )是一种新型太阳能电池材料,
其制备原理为: 。已知钛酸钡的晶胞结构 均与 接触)和元素
周期表中钛的数据如图所示,晶胞参数为 为阿伏加德罗常数的值。下列有关叙述正确的是
A.Ti元素的质量数为47.87 B.晶体中与 紧邻的 有12个
C. 的化学式为 D.钛酸钡的密度约为
【变式2-2】(2024上·河南周口·高三统考阶段练习)氨是常用的化工原料,研究发现可通过高效催化剂高
选择性地将 还原为 。我国科学工作者利用氮化钴(图1)掺杂Cu,获得具有高效催化性能的掺杂物
(图2)。
下列说法错误的是
A.掺杂前,氮化钴的化学式为
B. 被还原为 后,键角将变大
C. 晶体中,若晶胞参数为apm,则最近的Co原子核间距为
D. 晶体中,Cu原子周围最近的Co原子为12个【考向三】晶胞中的原子坐标
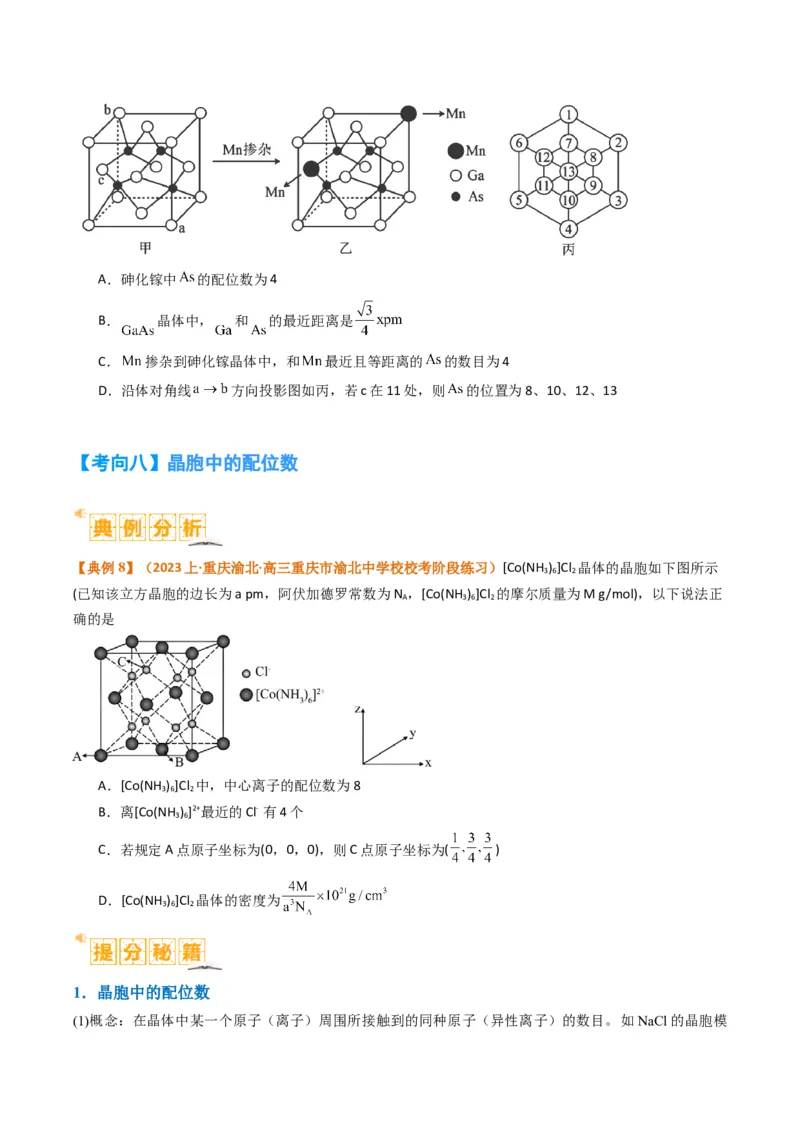
【典例3】(2023上·黑龙江·高三牡丹江一中校考期末)砷化镉晶胞结构如图,图1中“①”和“②”位是
“真空”,晶胞参数为apm,建立如图2,①号位的坐标为( , , )。已知:砷化镉的摩尔质量为
Mg·mol-1,N 为阿伏加德罗常数的值,下列说法错误的是
A
A.砷化镉中Cd与As原子个数比为3:2
B.两个Cd原子间最短距离为0.5a pm
C.③号位原子坐标参数为( ,1, )
D.该晶胞的密度为N (a×10—10)3g·cm-3
A
1.原子分数坐标
原子分数坐标概念:原子分数坐标参数表示晶胞内部各原子的相对位置。
2.原子分数坐标的确定方法
(1)依据已知原子的分数坐标确定坐标系取向和坐标原点。
(2)一般以坐标轴所在立体图形的棱长为1个单位(长、宽、高可以不同,但都为1个单位)。
(3)从原子所在位置分别向x、y、z轴作垂线,所得坐标轴上的截距即为该原子的分数坐标。
以立方体的三个棱延长线构建坐标轴,以晶胞边长为1个单位长度,O为坐标原点,其分数坐标规定为
(0,0,0)、A的坐标为(1,0,0)、B的坐标为(1,1,0)、C的坐标为(1,1,1)。
3.常见坐标系的构建
(1)立方晶胞坐标系建立方法
“立方晶胞”x轴、y轴、z轴均以晶胞参数长度为1个单位。① 简单立方晶胞
1点坐标(0,0,0);2点坐标(0,1,0);3点坐标(1,1,0);4点坐标(1,0,0);5点坐标(0,0,1);6点
坐标(0,1,1);7点坐标(1,1,1);8点坐标(1,0,1)。
②体心立方晶胞如图 体心坐标为( , , )
③面心立方晶胞如图 面心坐标为1/2
1点坐标(0,1/2,1/2);2点坐标(1/2,1/2,1);
3点坐标(1/2,1,1/2);4点坐标(1,1/2,1/2);
5点坐标(1/2,0,1/2);6点坐标(1/2,1/2,0)。
④金刚石体内心坐标:1/4或3/4
左上、左下、右上、右下的坐标为:(1/4,3/4,3/4)、(1/4,1/4,1/4)、(3/4,1/4,3/4)、(3/4,3/4,1/4)
⑤棱心坐标:有一个1/2,其余为0或1
1点坐标(1/2,0,1);2点坐标(0,1/2,1);3点坐标 (1/2,1,1);4 点
坐标(1,1/2,1);5点坐标(1/2,0,0);6点坐标(0,1/2,0);7点坐标(1/2,1,0);8点坐标(1,1/2,0)
(2)拉长的晶胞坐标系建立方法
“拉长的晶胞”x轴:a pm为1个单位,y轴:a pm为1个单位,z轴:2a pm为1个单位。
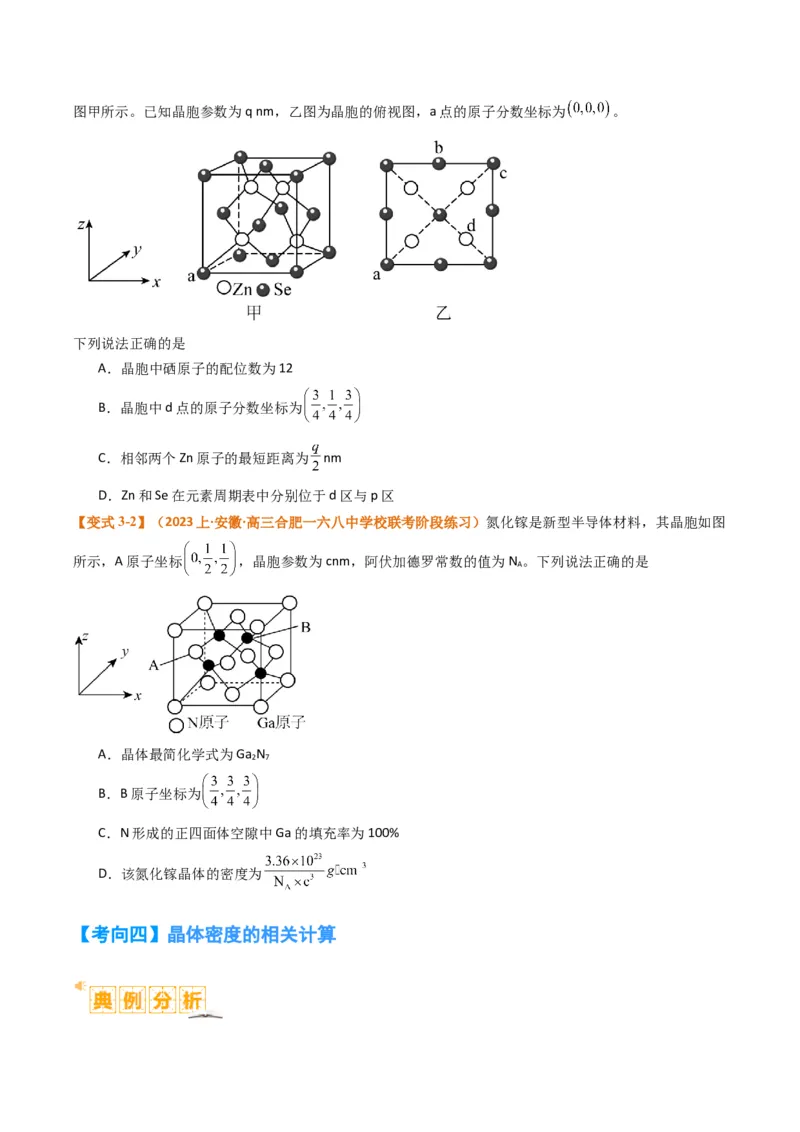
【变式3-1】(2023上·河南濮阳·高三濮阳一高校考期中)硒化锌是一种重要的半导体材料,其晶胞结构如图甲所示。已知晶胞参数为q nm,乙图为晶胞的俯视图,a点的原子分数坐标为 。
下列说法正确的是
A.晶胞中硒原子的配位数为12
B.晶胞中d点的原子分数坐标为
C.相邻两个Zn原子的最短距离为 nm
D.Zn和Se在元素周期表中分别位于d区与p区
【变式3-2】(2023上·安徽·高三合肥一六八中学校联考阶段练习)氮化镓是新型半导体材料,其晶胞如图
所示,A原子坐标 ,晶胞参数为cnm,阿伏加德罗常数的值为N 。下列说法正确的是
A
A.晶体最简化学式为Ga N
2 7
B.B原子坐标为
C.N形成的正四面体空隙中Ga的填充率为100%
D.该氮化镓晶体的密度为
【考向四】晶体密度的相关计算【典例4】(2024上·辽宁锦州·高三统考期末)一种由Mn、Se组成的化合物立方晶胞结构如图所示。已知
化合物的摩尔质量为 ,晶胞参数为anm,阿伏加德罗常数的值为 。下列说法错误的是
A.该化合物的化学式可表示为MnSe B.与Se原子距离最近的Se原子有12个
C.Mn、Se原子的最近距离是 D.晶胞密度为
1.晶体密度的计算
(1)计算晶胞的质量,进而计算晶体的密度
计算公式:ρ=。
式中N与晶胞的组成有关,M为晶体的摩尔质量,N 为阿伏加德罗常数的值,V为晶胞的体积,其单位为
A
cm3,ρ为晶体的密度,其单位为g·cm-3。
【变式4-1】(2023上·贵州贵阳·高三贵阳一中校考阶段练习)钙钛矿电池是第三代非硅薄膜太阳能电池的
代表,具有较高的能量转化效率。如图是一种边长为 的钙钛矿的正方体晶胞结构,其中 原子占据
正方体中心,O原子位于每条棱的中点。其中以原子1为原点,原子2的坐标为 。下列有关说法错
误的是
A.原子3的坐标为 B. 原子与 原子最近距离为
C.距离 原子最近的O原子有6个 D.该晶胞密度约为【变式4-2】(2023上·重庆·高三重庆八中校考阶段练习)一种新型超导材料由Li、Fe、Se组成,晶胞如图
所示(Fe原子均位于面上)。晶胞棱边夹角均为90°,X的坐标为(0,1, ),Y的坐标为( , , ),设N
A
为阿伏加德罗常数的值(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原
子分数坐标)。下列说法正确的是
A.可通过红外光谱和质谱测定原子坐标
B.坐标为( ,1, )的原子是Li原子
C.Se原子X与Se原子Y之间的距离为
D.该晶体的密度为
【考向五】晶胞利用率的计算
【典例5】(2023·全国·模拟预测)钠元素和硒元素可组成一种对蛋白质的合成和糖代谢有保护作用的无机
化合物,其晶胞结构如图所示。已知 和 的半径分别为a nm和b nm,晶胞参数为c nm。下列有关
说法错误的是A.该晶体的化学式为
B.与 距离最近且相等的 数目为8
C.该晶胞的空间利用率为
D. 位于由 构成的四面体空隙中, 位于由 构成的六面体空隙中
空间利用率(η)
(1)概念:指构成晶体的原子、离子或分子总体积在整个晶体空间中所占有的体积百分比。
(2)金属晶体空间利用率
空间利用率=×100%,球体积为金属原子的总体积。
(3)空间利用率的计算
①简单立方堆积
设原子半径为R,由于原子在晶胞棱的方向上相切,可以计算出晶胞参数:a=b=c=2R,α=β=γ=90°。
每个晶胞中包含一个原子。
η=×100%=×100%≈52.36%。
②体心立方堆积
设原子半径为R,由于原子在晶胞体对角线方向上相切,可以计算出晶胞参数:a=b=c=R,α=β=γ=
90°。每个晶胞中包含两个原子。
η=×100%=×100%≈68.02%。
③面心立方最密堆积设原子半径为R,由于原子在晶胞面对角线方向上相切,可以计算出晶胞参数:a=b=c=2R,α=β=γ=
90°。每个晶胞中包含四个原子。
η=×100%=×100%≈74.05%。
④六方最密堆积
设原子半径为R,根据原子在晶胞中的相切关系,可以计算出晶胞参数:a=b=2R,c=a≈1.633a,α=β=
90°,γ=120°。每个晶胞中包含两个原子。
η=×100%=×100%≈74.05%。
⑤金刚石型堆积
设原子半径为R,由于原子在晶胞体对角线方向上相切(相邻两个碳原子之间的距离为
晶胞体对角线的四分之一),可以计算出晶胞参数:a=b=c=R,α=β=γ=90°。每个
晶胞中包含八个原子。
η=×100%=×100%≈34.01%。
【变式5-1】(2023·湖北武汉·华中师大一附中)金刚石和C 都是由碳元素组成的重要单质,金刚石和C
60 60
分子及它们的晶胞如图所示(已知 ≈1.732、π≈3.14):
下列说法正确的是
A.每个金刚石晶胞中含有4个碳原子
B.每个C 分子含有90个σ键
60
C.金刚石和C 晶胞中微粒间的作用力均只有共价键
60
D.每个金刚石晶胞原子的空间利用率为74.05%
【变式5-2】(2023下·浙江金华)已知空间利用率是指构成晶体的原子、离子或分子在整个晶体空间中所
占有的体积百分比。下列有关说法不正确的是A.铜碘杂化团簇分子结构如图1所示,分子间通过范德华力聚集在一起
B. 晶体的晶胞如图2所示,标记为X的 的分子坐标为
C.H原子的电子云如图3所示,H原子核外大多数电子在原子核附近运动
D.金属Cu为面心立方晶胞(如图4所示),其空间利用率约为74%
【考向六】晶胞中特定位置微粒间距的计算
【典例6】(2024上·湖南长沙·高三长沙一中校考阶段练习) 是目前储氢密度最高的材料之一,其
晶胞结构如图所示,晶胞边长为apm。Mg原子占据Fe形成的所有四面体空隙,储氢后, 分子占据Fe
形成的八面体空隙,化学式为 。下列说法正确的是
A. 晶胞中,存在的化学键类型为金属键和离子键
B.氢气储满后晶体的化学式为
C.氢气储满后, 和 的最短距离为
D.晶胞中Fe与Mg的配位数均为4
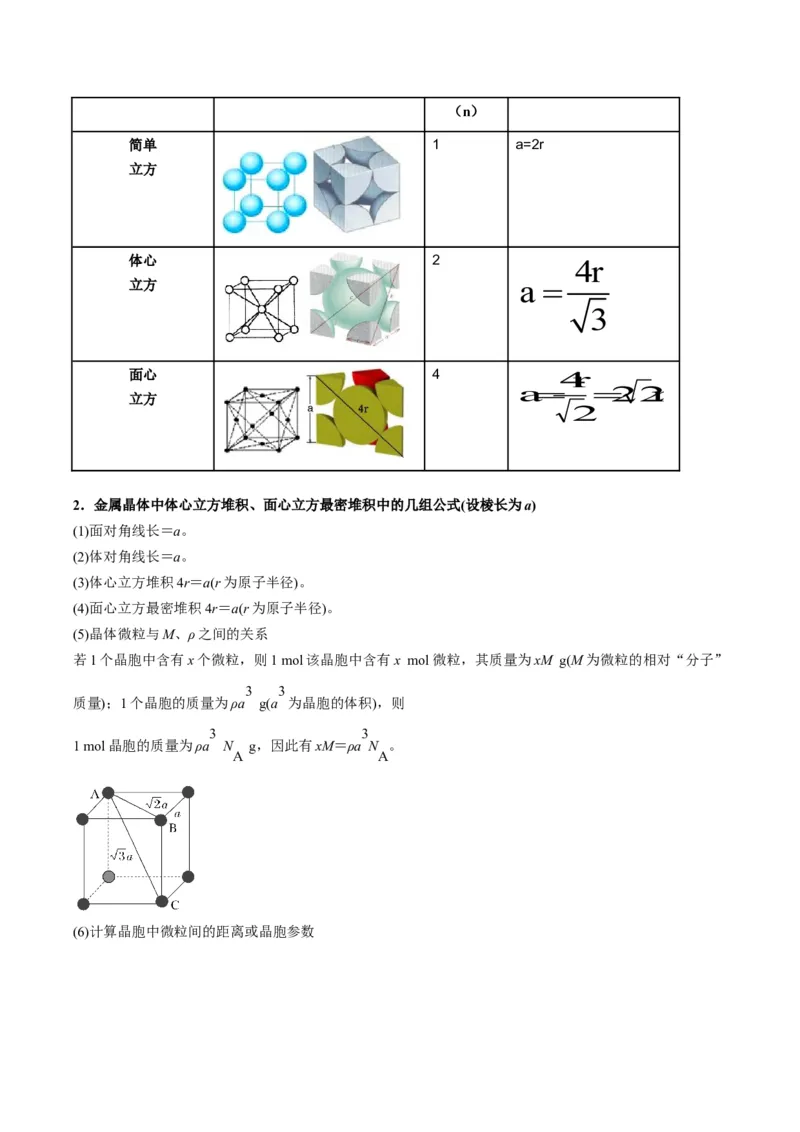
1.常见晶胞所含微粒的数目(n),晶胞边长(a)与原子半径(r)的关系
晶胞 模型 a与r的关系(n)
简单 1 a=2r
立方
体心 2 4r
立方 a
3
面心 4 4r
a 22r
立方
2
2.金属晶体中体心立方堆积、面心立方最密堆积中的几组公式(设棱长为a)
(1)面对角线长=a。
(2)体对角线长=a。
(3)体心立方堆积4r=a(r为原子半径)。
(4)面心立方最密堆积4r=a(r为原子半径)。
(5)晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol该晶胞中含有x mol微粒,其质量为xM g(M为微粒的相对“分子”
3 3
质量);1个晶胞的质量为ρa g(a 为晶胞的体积),则
3 3
1 mol晶胞的质量为ρa N g,因此有xM=ρa N 。
A A
(6)计算晶胞中微粒间的距离或晶胞参数立方晶胞参数a=。
-7 -10
(7)长度算关系式:1 nm=1×10 cm;1 pm=1×10 cm
【变式6-1】(2023上·重庆北碚)有一种有超导性的硼镁化合物,晶体结构属于立方晶系。其晶体结构、
晶胞沿 轴的投影图如图所示,关于其晶体下列说法正确的
A.该化合物的化学式为 B.一个晶胞中含有2个
C. 最近距离为 D.与 距离最近且相等的 有8个
【变式6-2】(2023上·江苏无锡)砷化硼的晶胞结构如图所示,晶胞的边长为apm,下列说法中正确的是
A.砷化硼的化学式为B As
2
B.砷化硼晶胞中,As的配位数是4
C.砷化硼晶胞中,B原子之间的最短距离为
D.与B原子最近且距离相等的B原子有6个
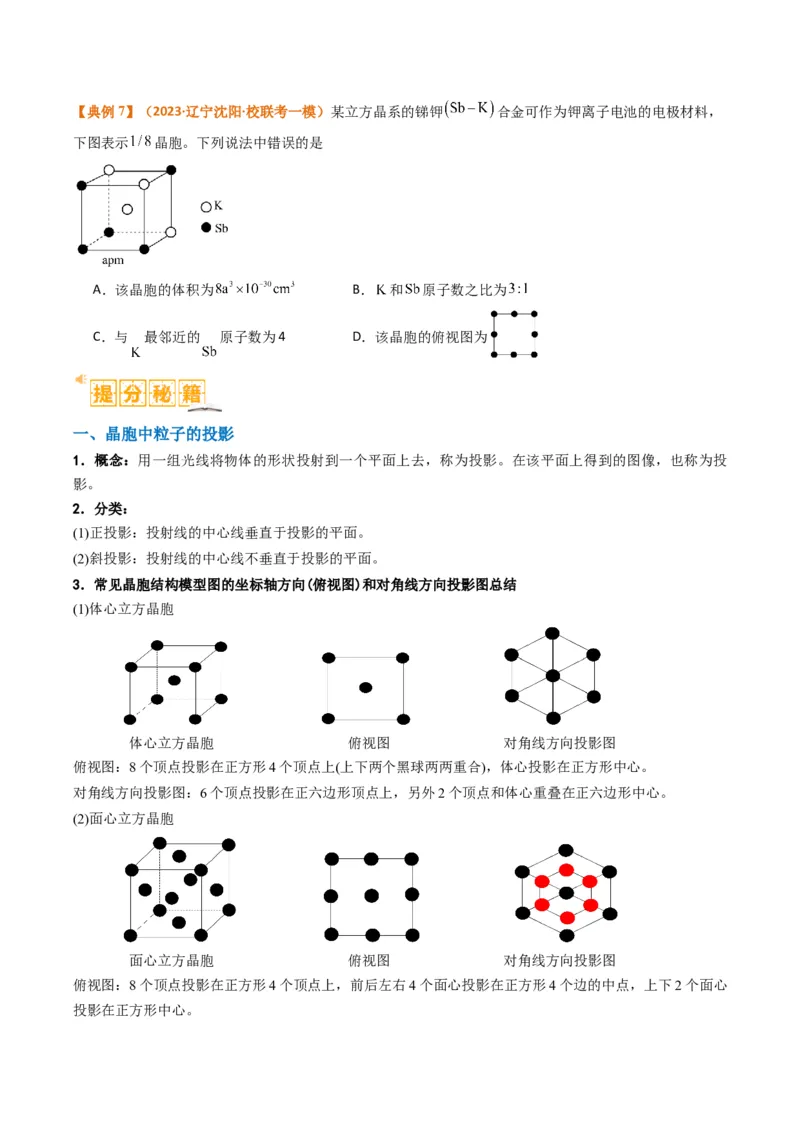
【考向七】晶胞中投影问题【典例7】(2023·辽宁沈阳·校联考一模)某立方晶系的锑钾 合金可作为钾离子电池的电极材料,
下图表示 晶胞。下列说法中错误的是
A.该晶胞的体积为 B. 和 原子数之比为
C.与 最邻近的 原子数为4 D.该晶胞的俯视图为
一、晶胞中粒子的投影
1.概念:用一组光线将物体的形状投射到一个平面上去,称为投影。在该平面上得到的图像,也称为投
影。
2.分类:
(1)正投影:投射线的中心线垂直于投影的平面。
(2)斜投影:投射线的中心线不垂直于投影的平面。
3.常见晶胞结构模型图的坐标轴方向(俯视图)和对角线方向投影图总结
(1)体心立方晶胞
体心立方晶胞 俯视图 对角线方向投影图
俯视图:8个顶点投影在正方形4个顶点上(上下两个黑球两两重合),体心投影在正方形中心。
对角线方向投影图:6个顶点投影在正六边形顶点上,另外2个顶点和体心重叠在正六边形中心。
(2)面心立方晶胞
面心立方晶胞 俯视图 对角线方向投影图
俯视图:8个顶点投影在正方形4个顶点上,前后左右4个面心投影在正方形4个边的中点,上下2个面心
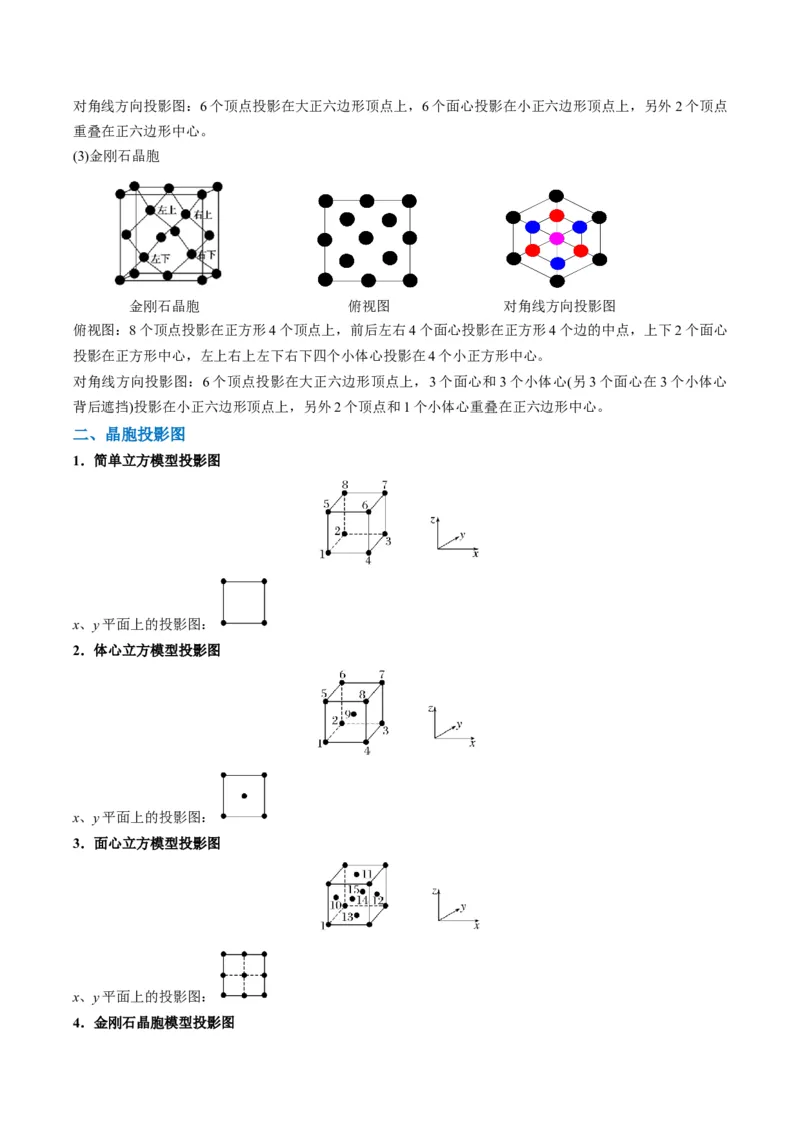
投影在正方形中心。对角线方向投影图:6个顶点投影在大正六边形顶点上,6个面心投影在小正六边形顶点上,另外2个顶点
重叠在正六边形中心。
(3)金刚石晶胞
金刚石晶胞 俯视图 对角线方向投影图
俯视图:8个顶点投影在正方形4个顶点上,前后左右4个面心投影在正方形4个边的中点,上下2个面心
投影在正方形中心,左上右上左下右下四个小体心投影在4个小正方形中心。
对角线方向投影图:6个顶点投影在大正六边形顶点上,3个面心和3个小体心(另3个面心在3个小体心
背后遮挡)投影在小正六边形顶点上,另外2个顶点和1个小体心重叠在正六边形中心。
二、晶胞投影图
1.简单立方模型投影图
x、y平面上的投影图:
2.体心立方模型投影图
x、y平面上的投影图:
3.面心立方模型投影图
x、y平面上的投影图:
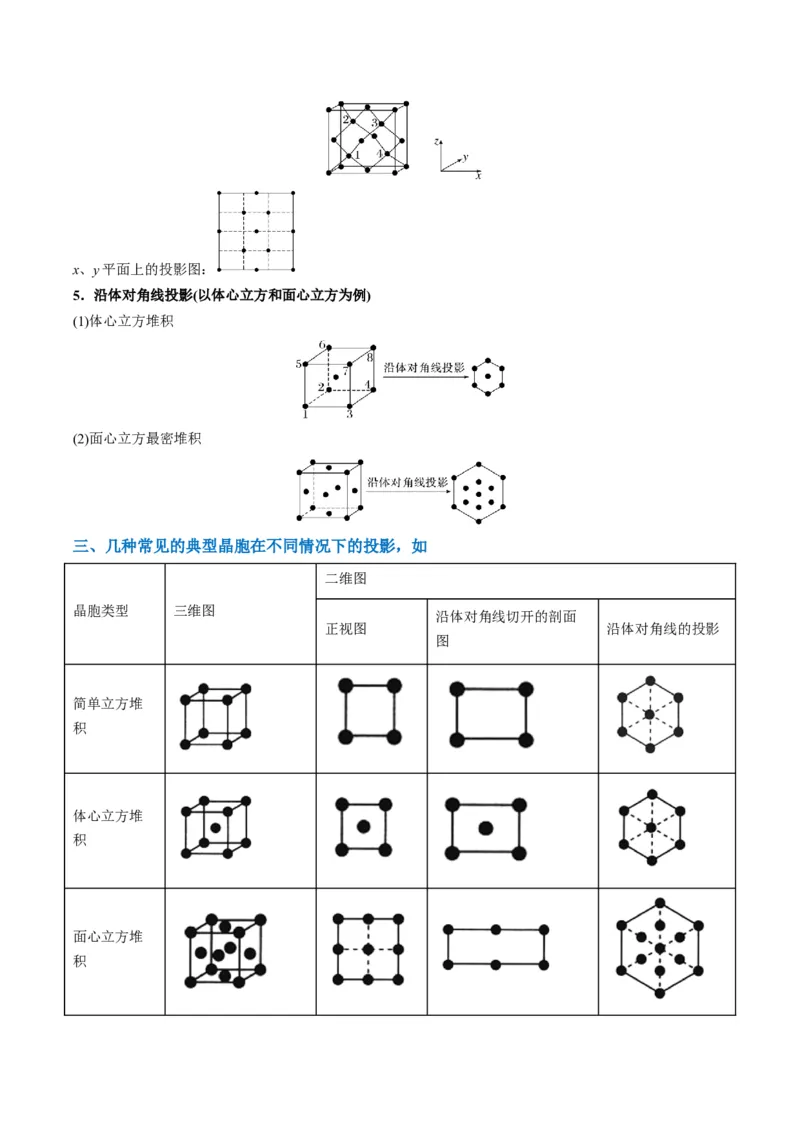
4.金刚石晶胞模型投影图x、y平面上的投影图:
5.沿体对角线投影(以体心立方和面心立方为例)
(1)体心立方堆积
(2)面心立方最密堆积
三、几种常见的典型晶胞在不同情况下的投影,如
二维图
晶胞类型 三维图
沿体对角线切开的剖面
正视图 沿体对角线的投影
图
简单立方堆
积
体心立方堆
积
面心立方堆
积晶胞
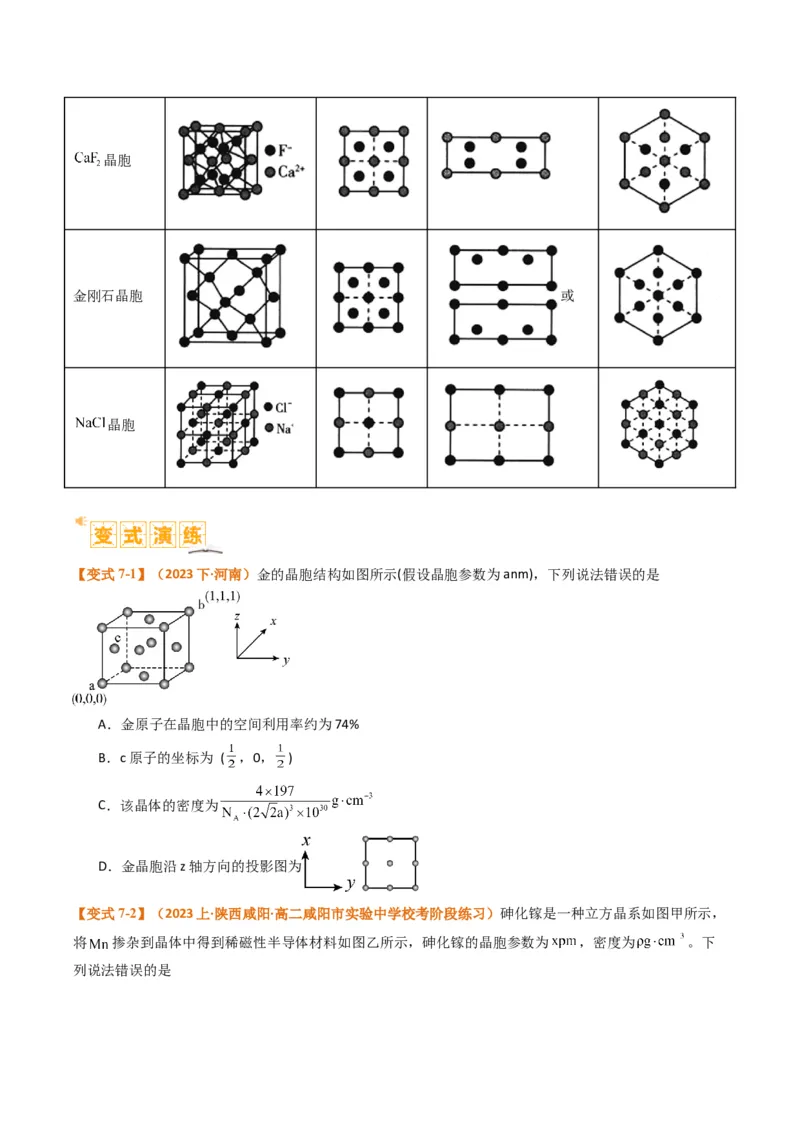
金刚石晶胞 或
晶胞
【变式7-1】(2023下·河南)金的晶胞结构如图所示(假设晶胞参数为anm),下列说法错误的是
A.金原子在晶胞中的空间利用率约为74%
B.c原子的坐标为 ( ,0, )
C.该晶体的密度为
D.金晶胞沿z轴方向的投影图为
【变式7-2】(2023上·陕西咸阳·高二咸阳市实验中学校考阶段练习)砷化镓是一种立方晶系如图甲所示,
将 掺杂到晶体中得到稀磁性半导体材料如图乙所示,砷化镓的晶胞参数为 ,密度为 。下
列说法错误的是A.砷化镓中 的配位数为4
B. 晶体中, 和 的最近距离是
C. 掺杂到砷化镓晶体中,和 最近且等距离的 的数目为4
D.沿体对角线 方向投影图如丙,若c在11处,则 的位置为8、10、12、13
【考向八】晶胞中的配位数
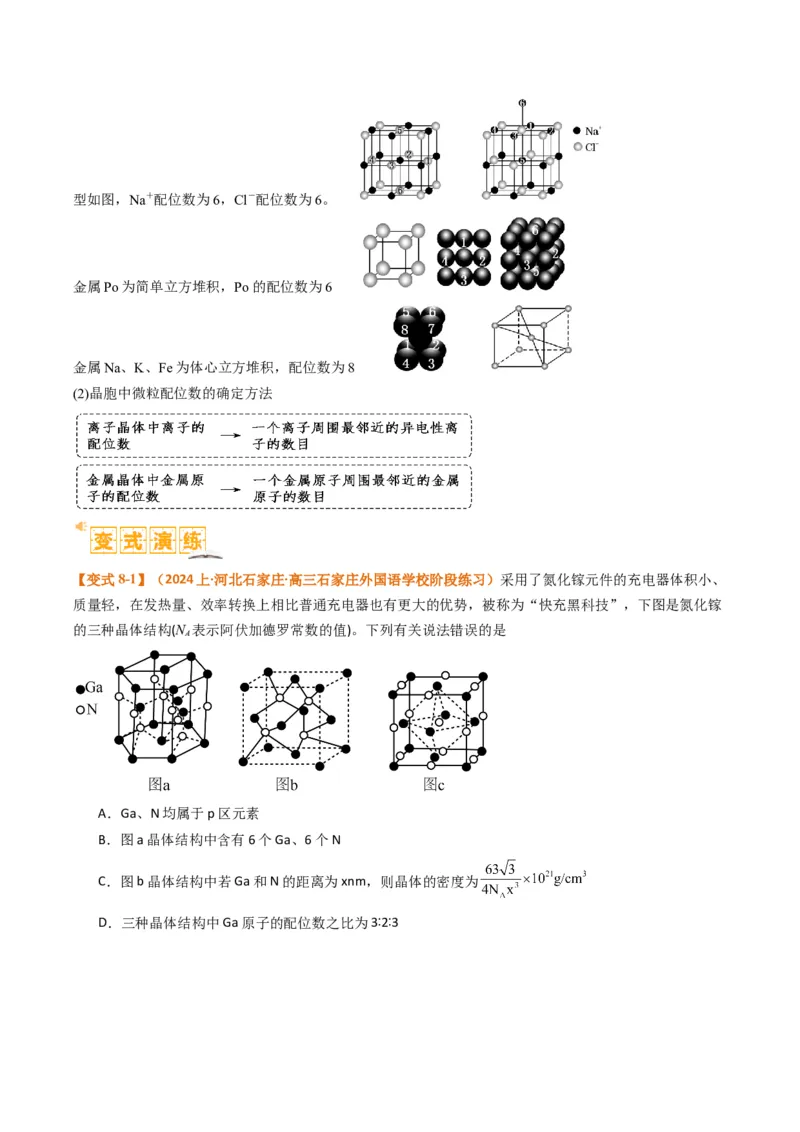
【典例8】(2023上·重庆渝北·高三重庆市渝北中学校校考阶段练习)[Co(NH ) ]Cl 晶体的晶胞如下图所示
3 6 2
(已知该立方晶胞的边长为a pm,阿伏加德罗常数为N ,[Co(NH ) ]Cl 的摩尔质量为M g/mol),以下说法正
A 3 6 2
确的是
A.[Co(NH ) ]Cl 中,中心离子的配位数为8
3 6 2
B.离[Co(NH ) ]2+最近的Cl- 有4个
3 6
C.若规定A点原子坐标为(0,0,0),则C点原子坐标为( )
D.[Co(NH ) ]Cl 晶体的密度为
3 6 2
1.晶胞中的配位数
(1)概念:在晶体中某一个原子(离子)周围所接触到的同种原子(异性离子)的数目。如NaCl的晶胞模型如图,Na+配位数为6,Cl-配位数为6。
金属Po为简单立方堆积,Po的配位数为6
金属Na、K、Fe为体心立方堆积,配位数为8
(2)晶胞中微粒配位数的确定方法
【变式8-1】(2024上·河北石家庄·高三石家庄外国语学校阶段练习)采用了氮化镓元件的充电器体积小、
质量轻,在发热量、效率转换上相比普通充电器也有更大的优势,被称为“快充黑科技”,下图是氮化镓
的三种晶体结构(N 表示阿伏加德罗常数的值)。下列有关说法错误的是
A
A.Ga、N均属于p区元素
B.图a晶体结构中含有6个Ga、6个N
C.图b晶体结构中若Ga和N的距离为xnm,则晶体的密度为
D.三种晶体结构中Ga原子的配位数之比为3∶2∶3【变式8-2】(2023上·湖南长沙·高三长郡中学校考阶段练习)硅与镁能够形成二元半导体材料,其晶胞如
图所示,已知晶胞参数为r nm。阿伏加德罗常数值为N ,下列说法正确的是
A
A.镁原子位于硅原子所构成的正八面体空隙中,空隙填充率为100%
B.晶体中硅原子的配位数为4
C.该晶体中两个硅原子间的最短距离为 nm
D.晶体的密度为 g/cm3
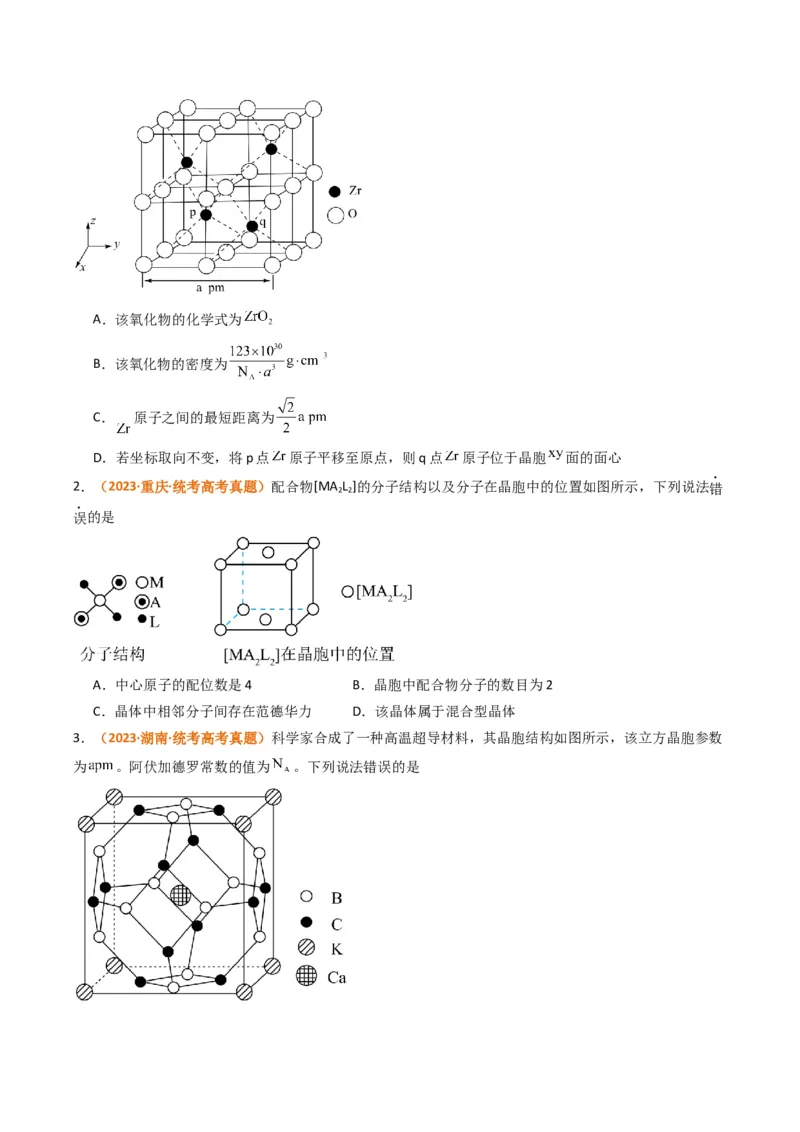
1.(2023·河北·统考高考真题)锆 是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物
晶体的立方晶胞, 为阿伏加德罗常数的值。下列说法错误的是A.该氧化物的化学式为
B.该氧化物的密度为
C. 原子之间的最短距离为
D.若坐标取向不变,将p点 原子平移至原点,则q点 原子位于晶胞 面的面心
2.(2023·重庆·统考高考真题)配合物[MA L ]的分子结构以及分子在晶胞中的位置如图所示,下列说法错
2 2
误的是
A.中心原子的配位数是4 B.晶胞中配合物分子的数目为2
C.晶体中相邻分子间存在范德华力 D.该晶体属于混合型晶体
3.(2023·湖南·统考高考真题)科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数
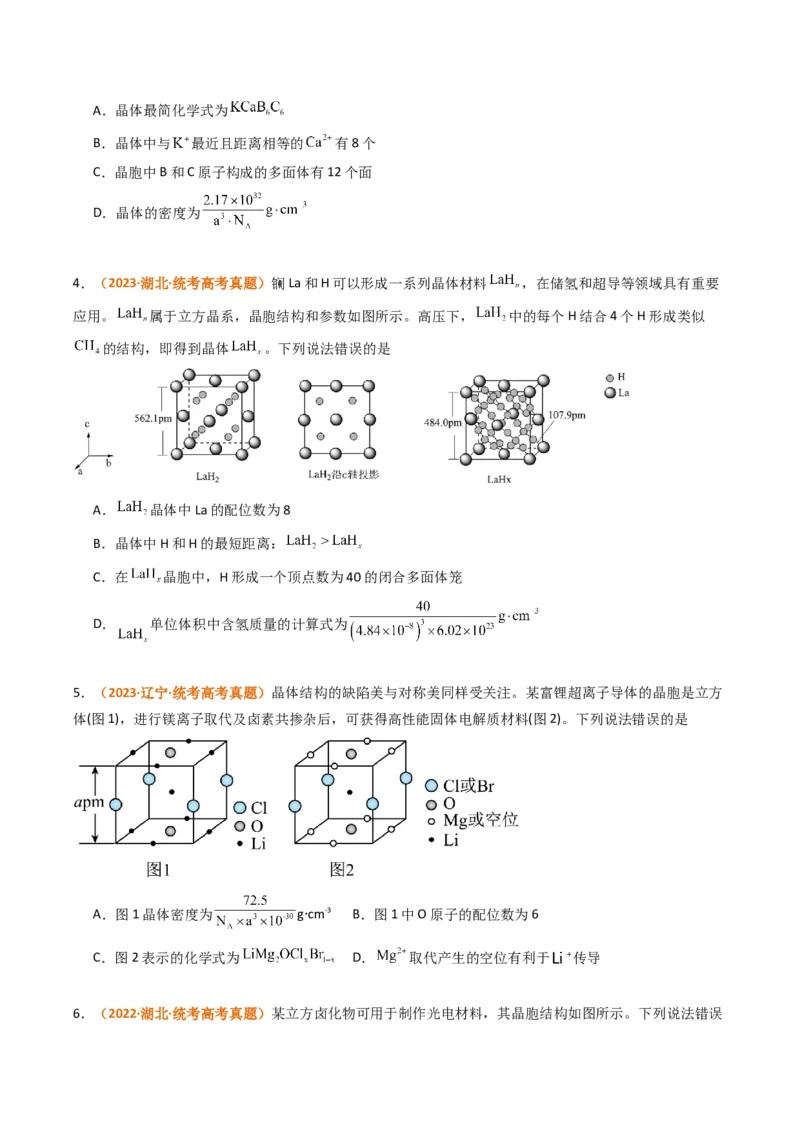
为 。阿伏加德罗常数的值为 。下列说法错误的是A.晶体最简化学式为
B.晶体中与 最近且距离相等的 有8个
C.晶胞中B和C原子构成的多面体有12个面
D.晶体的密度为
4.(2023·湖北·统考高考真题)镧La和H可以形成一系列晶体材料 ,在储氢和超导等领域具有重要
应用。 属于立方晶系,晶胞结构和参数如图所示。高压下, 中的每个H结合4个H形成类似
的结构,即得到晶体 。下列说法错误的是
A. 晶体中La的配位数为8
B.晶体中H和H的最短距离:
C.在 晶胞中,H形成一个顶点数为40的闭合多面体笼
D. 单位体积中含氢质量的计算式为
5.(2023·辽宁·统考高考真题)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方
体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 gcm-3 B.图1中O原子的配位数为6
∙
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
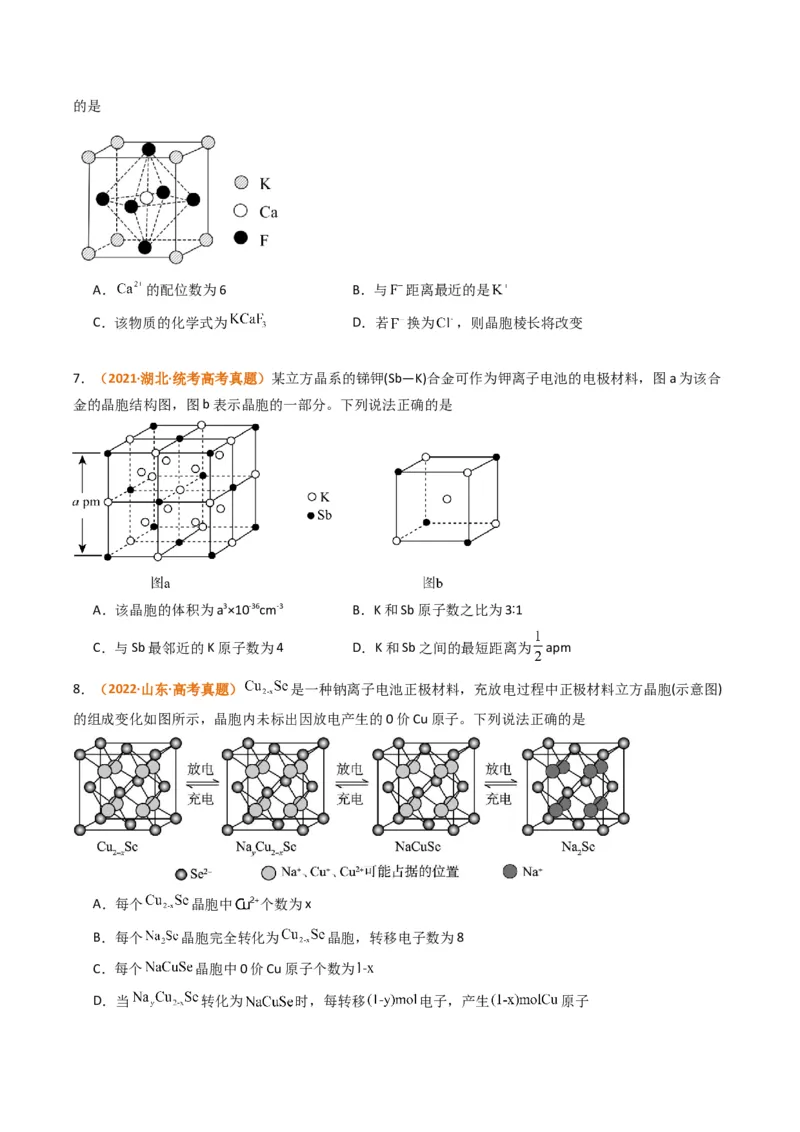
6.(2022·湖北·统考高考真题)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是
A. 的配位数为6 B.与 距离最近的是
C.该物质的化学式为 D.若 换为 ,则晶胞棱长将改变
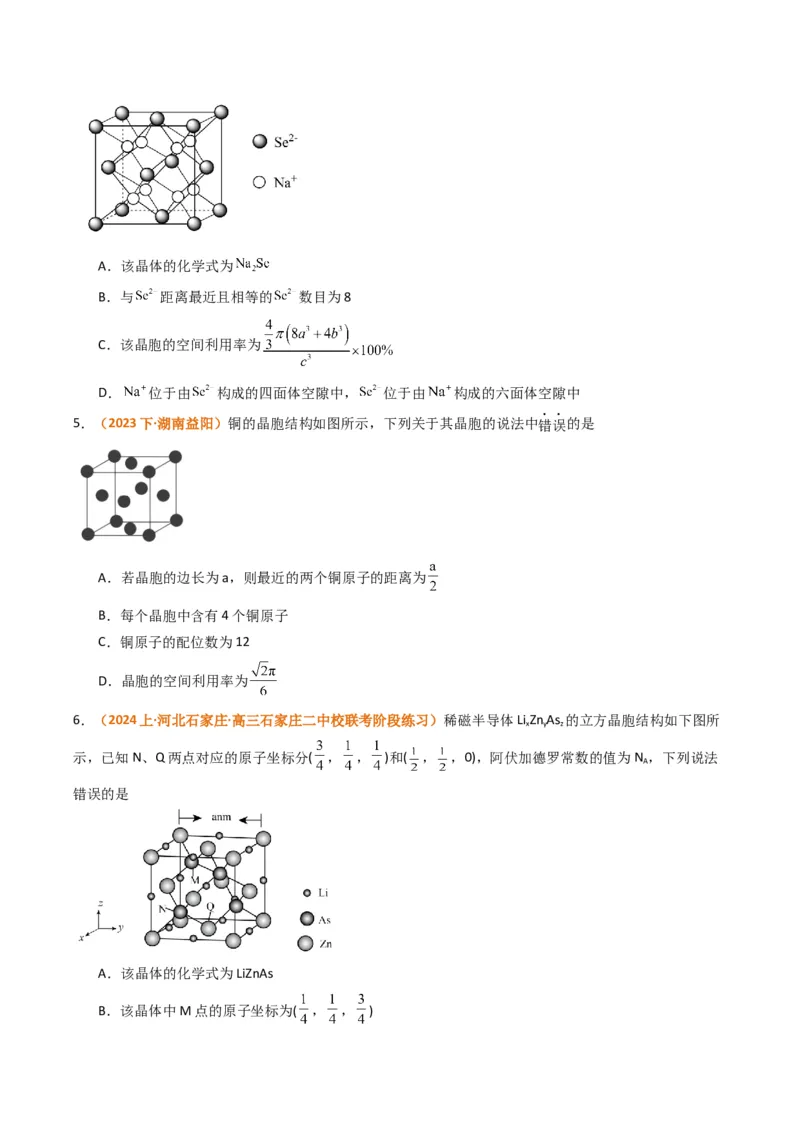
7.(2021·湖北·统考高考真题)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合
金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是
A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
8.(2022·山东·高考真题) 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)
的组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是
A.每个 晶胞中 个数为x
B.每个 晶胞完全转化为 晶胞,转移电子数为8
C.每个 晶胞中0价Cu原子个数为
D.当 转化为 时,每转移 电子,产生 原子1.(2023·云南·高三云南师大附中校考专题练习)金属钛具有耐压、耐腐蚀性质,可以通过反应
制取少量金属钛。下列有关说法正确的是
A.钠原子的结构示意图: B. 的电子式:
C.Ti晶体为金属晶体 D.质子数为22、中子数为30钛原子:
2.(2023·全国·高三专题练习)X、Y、Z、Q、W是原子序数依次增大的前四周期元素,X、Z的基态原子
2p能级上各有两个未成对电子,Y与Q同主族,W原子N能层只有一个电子,其余能层全充满。下列说法
错误的是
A.电负性为Z>Y>X
B.原子半径为r(Q)>r(Y)>r(Z)
C.X与Z可以形成含极性键的极性分子
D.W与Z形成的化合物晶胞如图,其化学式为WZ
3.(2024上·黑龙江齐齐哈尔·高三齐齐哈尔市第八中学校校考阶段练习)一种铜的溴化物晶胞结构如图所
示。下列说法正确的是
A.该化合物的化学式为CuBr
2
B.铜原子的配位数为12
C.与每个Br紧邻的Br有6个
D.由图中P点和Q点原子的分数坐标,可确定R点原子的分数坐标为( , , )
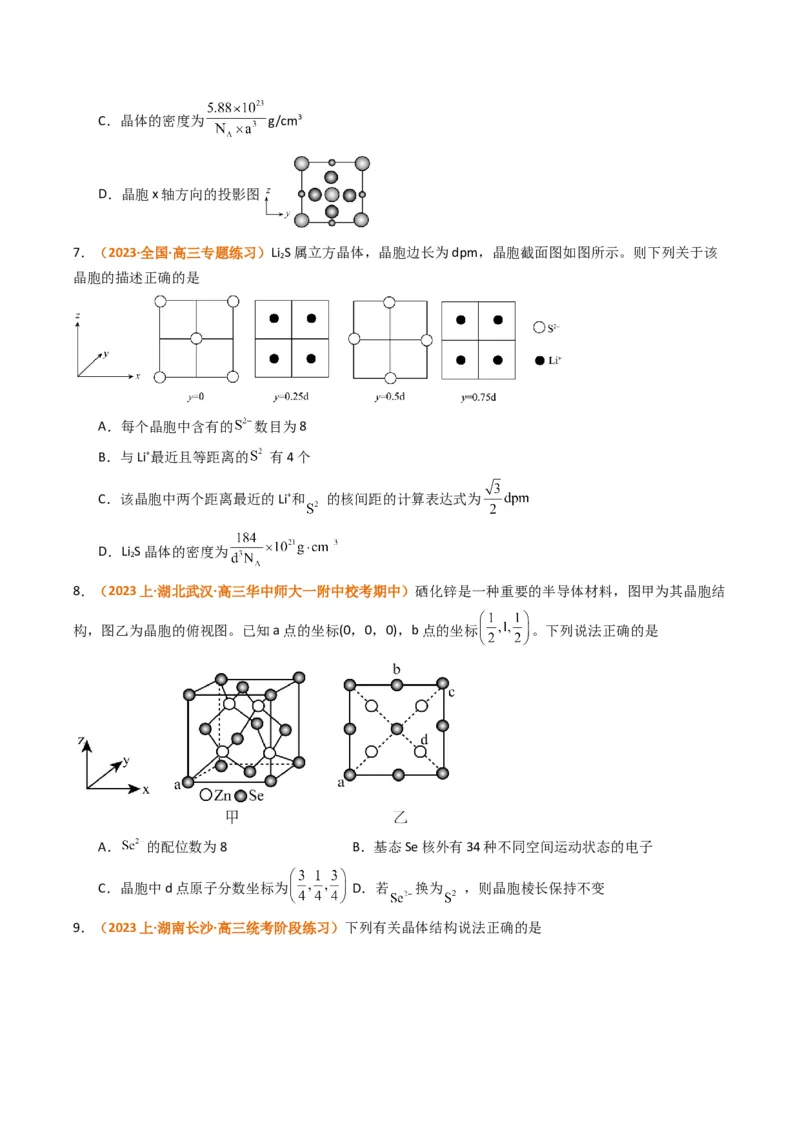
4.(2023下·安徽阜阳)钠元素和硒元素可组成一种对蛋白质的合成和糖代谢有保护作用的无机化合物,
其晶胞结构如图所示。已知 和 的半径分别为anm和bnm,晶胞参数为cnm。下列有关说法错误的
是A.该晶体的化学式为
B.与 距离最近且相等的 数目为8
C.该晶胞的空间利用率为
D. 位于由 构成的四面体空隙中, 位于由 构成的六面体空隙中
5.(2023下·湖南益阳)铜的晶胞结构如图所示,下列关于其晶胞的说法中错误的是
A.若晶胞的边长为a,则最近的两个铜原子的距离为
B.每个晶胞中含有4个铜原子
C.铜原子的配位数为12
D.晶胞的空间利用率为
6.(2024上·河北石家庄·高三石家庄二中校联考阶段练习)稀磁半导体LiZnAs 的立方晶胞结构如下图所
x y z
示,已知N、Q两点对应的原子坐标分( , , )和( , ,0),阿伏加德罗常数的值为N ,下列说法
A
错误的是
A.该晶体的化学式为LiZnAs
B.该晶体中M点的原子坐标为( , , )C.晶体的密度为 g/cm3
D.晶胞x轴方向的投影图
7.(2023·全国·高三专题练习)Li S属立方晶体,晶胞边长为dpm,晶胞截面图如图所示。则下列关于该
2
晶胞的描述正确的是
A.每个晶胞中含有的 数目为8
B.与Li+最近且等距离的 有4个
C.该晶胞中两个距离最近的Li+和 的核间距的计算表达式为
D.Li S晶体的密度为
2
8.(2023上·湖北武汉·高三华中师大一附中校考期中)硒化锌是一种重要的半导体材料,图甲为其晶胞结
构,图乙为晶胞的俯视图。已知a点的坐标(0,0,0),b点的坐标 。下列说法正确的是
A. 的配位数为8 B.基态Se核外有34种不同空间运动状态的电子
C.晶胞中d点原子分数坐标为 D.若 换为 ,则晶胞棱长保持不变
9.(2023上·湖南长沙·高三统考阶段练习)下列有关晶体结构说法正确的是A.在NaCl晶胞中,与 最邻近且等距离的 有6个
B.在干冰晶体中,每个晶胞拥有6个 分子
C. 晶胞中 的配位数为4
D.该气态团簇分子的化学式为
10.(2023上·江西南昌·高三校联考期中)半导体材料硒化锌的晶胞如图所示。通过晶体衍射测得晶胞中,
面心上硒与顶点硒之间距离为anm,代表阿伏加德罗常数的值。以晶胞参数为单位长度建立坐标系,可以
表示晶胞中各原子的位置,称为原子坐标。在ZnSe晶胞坐标系中,A点硒原子坐标为 ,B点锌原
子坐标为 。下列说法不正确的是
A.Se原子的配位数为4
B.C的原子坐标参数为( , , )
C.硒化锌晶体密度为
D.已知SeO 的熔点为165℃,在126℃时升华,则SeO 晶体类型与ZnSe晶体不同
3 3