文档内容
第二章 化学物质及其变化
第04讲 离子反应 离子方程式(精练)
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2021·上海黄浦区·高三二模)下表中物质的分类完全正确的是( )
选项 A B C D
强电解质
弱电解质 HClO
非电解质 Al
A.A B.B C.C D.D
【答案】A
【解析】A. 在水中能完全电离,所以是强电解质, 在水中能部分电离,所以是弱电解质,
自身不能电离,是非电解质,故A正确;B. 在水中能完全电离,所以是强电解质,溶于水的
碳酸钙能完全电离,所以属于强电解质,金属Al不是化合物,既不是电解质也不是非电解质,故B错误;
C.溶于水的 能完全电离,所以 是强电解质,HClO在水中能部分电离,所以是弱电解质,
部分电离,是弱电解质,故C错误;D. 在水中能完全电离,所以是强电解质,
在水中能完全电离,所以是强电解质, 在水溶液中不能发生电离,所以是非电解
质,故D错误;故答案选A。
2.(2021·上海崇明区·高三一模)如下说法正确的一组是
①难溶于水的盐(CaCO、BaSO 等)都是弱电解质
3 4
②醋酸铵是弱电解质
③弱酸、弱碱和水都是弱电解质
④强酸溶液的导电性一定强于弱酸溶液的导电性
⑤电解质溶液能导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电A.①③⑤⑥ B.②④⑤⑥ C.③⑤ D.③⑥
【答案】C
【解析】①电解质的强弱与水溶性无关,虽然CaCO、BaSO 等难溶,但溶于水的部分完全电离,为强电解
3 4
质,故①错误;②醋酸铵属于盐,在水溶液中完全电离,为强电解质,故②错误;③弱电解质包括弱酸、
弱碱和少部分盐以及水,故③正确;④溶液的导电性与溶液中的离子浓度和离子所带电荷多少有关,与是
否为强酸或弱酸无关,若强酸的浓度很小,其导电性不一定大于浓度大的弱酸溶液,故④错误;⑤电解质
在水溶液中可以电离出自由移动的离子,从而可以导电,故⑤正确;⑥熔融的电解质不一定能导电,如
HCl为电解质,但熔融时不能产生离子,不能导电,故⑥错误;综上所述答案为正确的有③⑤,故答案为
C。
3.(2020·北京昌平区·高三二模)下列化学用语表述不正确的是( )
A.电解CuCl 溶液:Cu2++2Cl- Cu+Cl↑
2 2
B.NaCl的形成过程:
C.HCl在水中电离:HCl=H++Cl-
D.NHCl在水中发生水解:NH++HO NH·HO+H+
4 4 2 3 2
【答案】B
【解析】A.电解CuCl 溶液阳极反应为:2Cl--2e-= Cl↑,阴极反应为:Cu2++2e-=Cu,总反应为:Cu2+
2 2
+2Cl- Cu+Cl↑,A正确;B.NaCl是离子化合物,书写电子式时需写成 ,形成过程为:
2
,B错误;C.HCl是强电解质,在水中完全电离,HCl=H++Cl-,C正确;D.
NHCl是强酸弱碱盐,NH+在水中能发生水解,使溶液显酸性:NH++HO NH·HO+H+,D正确;故选B。
4 4 4 2 3 2
4.(2021·北京顺义区·高三二模)下列离子方程式正确的是
A.用小苏打治疗胃酸过多:HCO +H+=CO↑+HO
2 2
B.稀HNO 和铜反应:Cu+2NO +4H+=Cu2++2NO↑+2HO
3 2 2
C.钠和水反应:Na+HO=Na++OH-+H↑
2 2
D.用醋酸除去水垢:2H++CaCO=Ca2++CO↑+HO
3 2 2
【答案】A
【解析】A.小苏打为NaHCO,胃酸主要为HCl,因此用小苏打治疗胃酸过多发生的反应为:HCO
3+H+=CO↑+HO,A正确;B.稀HNO 和铜反应生成NO,而不是NO,B错误;C.钠和水反应生成NaOH和H,
2 2 3 2 2
反应的离子方程式为:2Na+2HO=2Na++2OH-+H↑,C错误;D.醋酸是弱酸,在离子方程式中不拆写,D错
2 2
误;答案选A。
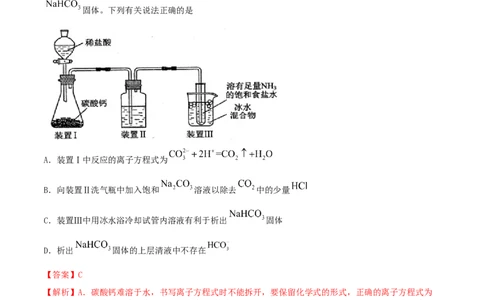
5.(2021·江苏高三二模)侯氏制碱法制取 的原理为
。实验室用如题图所示的装置模拟侯氏制碱法制取少量
固体。下列有关说法正确的是
A.装置Ⅰ中反应的离子方程式为
B.向装置Ⅱ洗气瓶中加入饱和 溶液以除去 中的少量
C.装置Ⅲ中用冰水浴冷却试管内溶液有利于析出 固体
D.析出 固体的上层清液中不存在
【答案】C
【解析】A.碳酸钙难溶于水,书写离子方程式时不能拆开,要保留化学式的形式,正确的离子方程式为
,故A错误;B.饱和 溶液也能吸收 ,所以除去 中
的少量 要用饱和 溶液,故B错误;C.为降低碳酸氢钠的溶解度,装置Ⅲ中用冰水浴充分冷
却试管内溶液,使 固体析出,故C正确;D.析出 固体后的溶液为混有氯化铵的饱和溶液,上层清液中还存在 ,故D错误;答案选C。
6.(2021·天津武清区·高三一模)下列离子方程式书写正确的是
A. 与 溶液反应:
B. 溶液呈碱性:
C.向 溶液中加入铜粉:
D. 与足量稀硝酸反应:
【答案】A
【解析】A. 与 和水反应生成氢气和偏铝酸钠,离子方程式为:
,A正确;B. 溶液中的S2-水解使溶液显碱性,多元弱酸的
酸根的水解是分步的,故水解的离子方程式为: , ,
B错误;C.向 溶液中加入铜粉,Fe3+和Cu反应生成Fe2+和Cu2+,离子方程式为:
,C错误;D. 会被稀硝酸氧化成Fe3+,同时生成NO气体,离子方程
式为: ,D错误;故选A。
7.(2021·广东深圳市·高三一模)能正确表示下列变化的离子方程式是
A.NaHCO 的水解反应:HCO +HO CO +HO+
3 2 3
B.用FeCl 溶液蚀刻铜印刷电路板:Fe3++Cu=Fe2++Cu2+
3
C.向NaAlO 溶液中通入过量的CO:AlO +CO+2HO=Al(OH)↓+HCO
2 2 2 2 3
D.向Ca(ClO) 溶液中通入SO:SO+HO+Ca2++2ClO- =CaSO↓+2HClO
2 2 2 2 3
【答案】C
【解析】A. NaHCO 的水解反应生成碳酸和氢氧化钠:HCO +HO HCO +OH-,原方程式为电离方程式,
3 2 2 3故A错误;B. 用FeCl 溶液蚀刻铜印刷电路板:2Fe3++Cu=2Fe2++Cu2+,原方程式电子得失不守恒,故B错
3
误;C. 向NaAlO 溶液中通入过量的CO 生成氢氧化铝沉淀和碳酸氢钠:AlO +CO+2HO=Al(OH)↓+HCO
2 2 2 2 3
,故C正确;D. Ca(ClO) 溶液具有强氧化性,能将SO 氧化,向Ca(ClO) 溶液中通入SO 生成硫酸钙和盐
2 2 2 2
酸:SO+HO+Ca2++ClO- =CaSO↓+2H++Cl-,故D错误;故选C。
2 2 4
8.(2021·山东济南市·高三一模)重质二氧化锰具有优良的电化学性能,广泛应用于各类化学电源中。
以硫酸锰为原料制备重质二氧化锰的工艺流程如下:
下列说法错误的是
A.“沉锰”的主要反应为
B.“焙烧”过程在敞开、低压容器中进行效率更高
C.用少量氨水吸收“焙烧”产生的气体,所得溶液可用于“沉锰”
D.工艺中的硫酸表现酸性,髙锰酸钾做氧化剂
【答案】A
【解析】A. 如果是 ,氢离子还会与 反应,
,正确的离子方程式为 ,故A错误;
B. 敞开、低压容器中有利于二氧化碳的释放,有利于反应正向进行,效率更高,故B正确;C. “焙
烧”产生的气体为二氧化碳,用少量氨水吸收二氧化碳生成碳酸氢铵,可用于“沉锰” ,故C正确;D.
酸性髙锰酸钾具有强氧化性,做氧化剂,硫酸提供酸性环境,有利于物质稳定存在,故D正确;故选A。
9.(2021·山东济宁市·高三一模)以黄铁矿的烧渣(主要成分为 、 、 等)为原料制取新
型高效的无机高分子絮凝剂—聚合硫酸铁 (其中 )的工艺流程如图:已知:为防止 水解,原料中的 必须先还原为 。
下列有关说法错误的是
A.“取样分析”目的是可以用来确定氧化 所需 的量
B.为促进水解反应,应在高温条件下进行
C.氧化反应的离子方程式为
D.水解时溶液的pH偏小或偏大都会影响聚合硫酸铁的产率
【答案】B
【解析】A.因为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+,所以
确定下一步还原所需铁的量,然后Fe2+再被氧化Fe3+,需要确定氧化Fe2+所需NaClO 的量,A正确;B.该
3
流程中要得到 ,若温度过高,则将转化为Fe(OH) 沉淀,使得产物不纯,故应该
3
控制反应温度,B错误;C.从流程中可知,进入氧化反应的是Fe2+,即NaClO 将Fe2+氧化为Fe3+,故氧化
3
反应的离子方程式为 ,C正确;D.水解时溶液的pH偏小将使
大部分Fe3+不能水解仍然以Fe3+存在,而pH偏大将生成Fe(OH) 沉淀,故都会影响聚合硫酸铁的产率,D正
3
确;故答案为:B。
10.(2021·山西吕梁市·高三一模)下列说法对应的离子方程式合理的是
A.泡沫灭火器的工作原理:2Al3++3CO +3HO=2Al(OH)↓+3CO↑
2 3 2
B.侯氏制碱法中NaHCO 的制备:NH+CO+HO=HCO +NH
3 3 2 2
C.草酸使酸性KMnO 溶液褪色:5HCO+2MnO +6H+=2Mn2++10CO↑+8HO
4 2 2 4 2 2
D.双氧水中加入稀硫酸和KI溶液:2I-+HO+2H+=I+O↑+2HO
2 2 2 2 2【答案】C
【解析】A.泡沫灭火器是用硫酸铝和碳酸氢钠溶液反应,故其工作原理为:Al3++3HCO =Al(OH)↓+
3
3CO↑,A不合题意;B.侯氏制碱法中生成的NaHCO 为沉淀,故其制备原理为:Na++NH+CO+
2 3 3 2
HO=NaHCO↓+NH ,B不合题意;C.草酸使酸性KMnO 溶液褪色:5HCO+2MnO +6H+=2Mn2++10CO↑
2 3 4 2 2 4 2
+8HO,C符合题意;D.双氧水中加入稀硫酸和KI溶液:2I-+HO+2H+=I+2HO,D不合题意;故答案
2 2 2 2 2
为:C。
11 .(2020·邹城市兖矿第一中学高三月考)下列离子方程式书写不正确的是
A.A1C1 溶液与烧碱溶液反应,当n(OH-) :n(A13+)=7 : 2 时,2A13++7OH-==A1(OH)↓+ AlO-+2HO
3 3 2 2
B.当向饱和NaCO 溶液中通入过量CO 时,CO2-+CO + HO==2HCO-
2 3 2 3 2 2 3
C.CuCl 溶液与 NaHS 溶液反应,当n(CuCl):n(NaHS) = l : 2 时,Cu2++2HS-==CuS↓十HS↑
2 2 2
D.Fe 与稀硝酸反应,当 n(Fe) : n(HNO)=l : 2 时,3Fe+2NO-+8H+==3Fe2+ +2NO↑+4HO
3 3 2
【答案】B
【解析】A.AlCl 溶液与氢氧化钠反应,按照1:3反应生成氢氧化铝沉淀,按照1:4反应生成偏铝酸钠,
3
当n(OH-):n(Al3+)=7:2时,反应生成氢氧化铝和偏铝酸钠的混合物,离子方程式:2Al3++7OH-
=Al(OH)↓+AlO-+2HO,故A正确;B.二者反应生成碳酸氢钠,碳酸氢钠溶解性小于碳酸钠,所以会有晶
3 2 2
体析出,离子方程式为2Na++CO2-+CO+HO=2NaHCO↓,故B错误;C.CuCl 溶液与NaHS溶液反应,当
3 2 2 3 2
n(CuCl):n(NaHS)=1:2时,离子方程式:Cu2++2HS-=CuS↓+HS↑,故C正确;D.Fe与稀硝酸反应,当
2 2
n(Fe):n(HNO)=1:2时,反应生成硝酸亚铁,离子方程式:3Fe+2NO-+8H+=3Fe2++2NO↑+4HO,故D正确;
3 3 2
故选B。
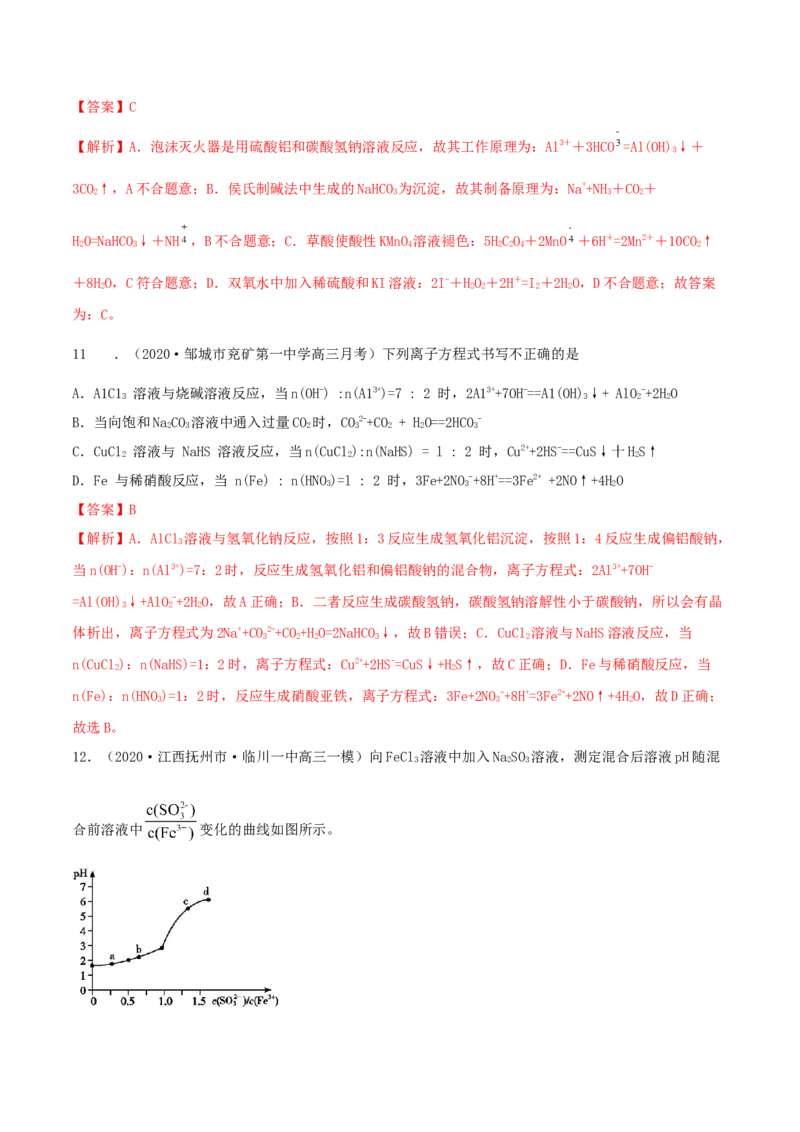
12.(2020·江西抚州市·临川一中高三一模)向FeCl 溶液中加入NaSO 溶液,测定混合后溶液pH随混
3 2 3
合前溶液中 变化的曲线如图所示。实验发现:
ⅰ.a 点溶液澄清透明,向其中滴加 NaOH 溶液后,立即产生灰白色沉淀,滴入 KSCN 溶液显红色;ⅱ.c
点和 d 点溶液中产生红褐色沉淀,无气体逸出;取其上层清液滴加NaOH溶液后无明显现象,滴加 KSCN
溶液显红色。
下列分析合理的是
A.检验a点溶液中反应生成的阴离子所需试剂为:稀硝酸和BaCl 溶液
2
B.c点和d点出现上述现象的主要原因是Fe3+和 发生双水解反应
C.b点较a点溶液pH升高的主要原因:2Fe3++ +HO = 2Fe2++ +2H+
2
D.向d点上层清液中滴加 NaOH溶液无明显现象,证明溶液中无Fe3+
【答案】B
【解析】i.a点溶液透明澄清,向其中滴加NaOH溶液后,立即产生灰白色沉淀,说明溶液中有Fe2+,滴
入KSCN溶液显红色,说明溶液中含Fe3+,发生的离子反应是2Fe3++SO +HO═2Fe2++SO +2H+;ii.c点
2
和d点溶液中产生红褐色沉淀,无气体逸出,发生的反应为2Fe3++3SO +6HO 2Fe(OH)+3HSO,取其
2 3 2 3
上层清液滴加NaOH溶液后无明显现象,滴加KSCN溶液显红色,说明含Fe3+。
A.检验a点溶液中反应生成的阴离子所需试剂为:稀盐酸和BaCl 溶液,硝酸也能将SO 氧化,故A错误;
2
B.c点和d点溶液中产生红褐色沉淀,无气体逸出,故发生的反应为2Fe3++3SO +6HO
2
2Fe(OH)+3HSO,故B正确;C.若2Fe3++SO2-+HO═2Fe2++SO2-+2H+发生此反应,酸性加强,pH减小,
3 2 3 3 2 4
故C错误;D.d点发生的反应为2Fe3++3SO +6HO 2Fe(OH)+3HSO,这是一个可逆反应,反应物不能
2 3 2 3
完全转化为生成物,故滴加KSCN溶液,溶液变红;滴加NaOH溶液,平衡向逆反应方向进行,故红色沉淀
减少,即红色减弱,故D错误;故选B。
二、主观题(共3小题,共40分)
13.(2020·青铜峡市高级中学高三开学考试)(8分)正确书写下列离子反应方程式
(1)将少量NaHSO 溶液滴加到Ba(OH) 溶液中,当恰好完全沉淀时,反应的离子方程式为____。
4 2
(2)在酸性条件下,向含铬废水中加入FeSO,可将 还原为Cr3+,该过程的离子反应方程式为_。
4(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为____。
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO,自身被还原成Cl-,该过程的离子反应方程式为_。
2
【答案】(1)Ba2++H++OH-+ =BaSO↓+HO
4 2
(2) +6Fe2++14H+=2Cr3++6Fe3++7HO
2
(3)ClO-+2I-+HO=I+Cl-+2OH-
2 2
(4)HO+ClO-+Mn2+=MnO+2H++Cl-
2 2
【解析】(1)将少量NaHSO 溶液滴加到Ba(OH) 溶液中,当恰好完全沉淀时生成硫酸钡、氢氧化钠和水,反
4 2
应的离子方程式为Ba2++H++OH-+ =BaSO↓+HO。
4 2
(2)在酸性条件下,向含铬废水中加入FeSO,可将 还原为Cr3+,其中亚铁离子被氧化为铁离子,则
4
该过程的离子反应方程式为 +6Fe2++14H+=2Cr3++6Fe3++7HO。
2
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,碘离子被氧化为单质碘,
反应的离子方程式为ClO-+2I-+HO=I+Cl-+2OH-。
2 2
(4)已知酸性环境下,ClO-可将Mn2+氧化成MnO,自身被还原成Cl-,根据电子得失守恒可知该过程的离子
2
反应方程式为HO+ClO-+Mn2+=MnO+2H++Cl-。
2 2
14.(2020·天津耀华中学高三调研)(18分)请按要求书写下列离子方程式:
(1)复分解离子反应中,量变引起的变化。
①将NaHSO 溶液滴入Ba(OH) 溶液中,当溶液恰好呈中性时,反应的离子方程式为
4 2
______________________________________________________________________________。
②向Ba(HCO ) 溶液中滴入NaHSO 溶液,至沉淀完全,写出反应的离子方程式:
3 2 4
_____________________________________________________________________________。
在上述溶液中继续滴入NaHSO 溶液,此时离子方程式为____________________。
4
③0.2 mol·L-1的NH Al(SO ) 溶液与0.3 mol·L-1的Ba(OH) 溶液等体积混合:
4 4 2 2
____________________________________________________________________________。
(2)氧化还原反应中,反应物及量的变化。向含有a mol FeBr 的溶液中,通入x mol Cl ,若x=a
2 2
________________________________________________________________________,
若x=4a_________________________________________________________________。
(3)特殊条件下离子方程式的书写①在碱性条件下,Cl 可将废水中的CN-氧化为无毒的CO、N,该过程反应的离子方程式为
2 2 2
_______________________________________________________________________________。
②在酸性条件下,向含铬废水中加入FeSO ,可将Cr O还原为Cr3+,该过程的离子反应方程式为
4 2
_____________________________________________________________________。
③在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为
________________________________________________________________________。
【答案】(1)①2H++SO+Ba2++2OH-===BaSO ↓+2HO
4 2
②Ba2++SO+H++HCO===BaSO ↓+HO+CO↑ HCO+H+===CO ↑+HO
4 2 2 2 2
③2Al3++3SO+3Ba2++6OH-===2Al(OH) ↓+3BaSO↓
3 4
(2)2Fe2++2Br-+2Cl===Br +2Fe3++4Cl- 2Fe2++4Br-+3Cl===2Br +2Fe3++6Cl-
2 2 2 2
(3)①5Cl+2CN-+8OH-===2CO +N+10Cl-+4HO
2 2 2 2
②Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
③ClO-+2I-+HO===I +Cl-+2OH-
2 2
【解析】(1)①当溶液呈中性时,n(H+)=n(OH-),可假设Ba(OH) 为1 mol,即Ba2+为1 mol,OH-为2
2
mol,需要2 mol NaHSO ,反应的离子方程式为2H++SO+Ba2++2OH-===BaSO ↓+2HO;②向
4 4 2
Ba(HCO ) 溶液中滴入NaHSO 溶液,至沉淀完全,n(Ba2+)=n(SO),发生反应的离子方程式为Ba2++SO+
3 2 4
H++HCO===BaSO ↓+HO+CO↑,此时HCO过量,继续加入NaHSO 溶液,HCO与H+反应,反应的离
4 2 2 4
子方程式为HCO+H+===CO ↑+HO;③NH Al(SO ) 与Ba(OH) 按照2∶3的物质的量之比反应生成氢氧化
2 2 4 4 2 2
铝、硫酸钡和硫酸铵,离子方程式:2Al3++3SO+3Ba2++6OH-===2Al(OH) ↓+3BaSO↓。
3 4
(2)向含有a mol FeBr 的溶液中,通入x mol Cl ,若x=a,亚铁离子全部被氧化,溴离子一半被氧化,则
2 2
反应的离子方程式为2Fe2++2Br-+2Cl===Br +2Fe3++4Cl-;若x=4a,亚铁离子和溴离子全部被氧化,
2 2
反应的离子方程式为2Fe2++4Br-+3Cl===2Br +2Fe3++6Cl-。
2 2
(3)特殊条件下离子反应方程式的书写①在碱性条件下,Cl 可将废水中的CN-氧化为无毒的CO、N,自
2 2 2
身被还原为Cl-,根据电子守恒、电荷守恒及原子守恒可知发生反应的离子方程式为5Cl+2CN-+8OH-
2
===2CO +N+10Cl-+4HO;②二价铁离子有还原性,Cr O有强氧化性,二者能发生氧化还原反应,二
2 2 2 2
价铁离子被氧化成三价铁离子,Cr O被还原为Cr3+,反应方程式:Cr O+6Fe2++14H+===2Cr3++6Fe3++
2 2
7HO;③次氯酸钠具有强氧化性,可氧化I-生成单质I,I 遇淀粉变蓝,反应的离子方程式为ClO-+2I-+
2 2 2
HO===I+Cl-+2OH-。
2 2
15.(14分)以硅藻土为载体的五氧化二钒(V O)是接触法生产硫酸的催化剂。从废矾催化剂中回收 VO
2 5 2 5
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
物质 VO VO KSO SiO Fe O Al O
2 5 2 4 2 4 2 2 3 2 3质量分数/% 2.2~2.9 2.8~3.1 22~28 60~65 1~2 <1
以下是一种废钒催化剂回收工艺路线:
回答下列问题:
(1)已知“酸浸”时,VO 转化为VO,请写出该反应的离子方程式_________,同时将VO 转成VO2+,反
2 5 2 4
应的离子方程式为_____,“废渣1”的主要成分是____。
(2)工艺中“氧化”步骤使VO2+变为VO反应的离子方程式为__________,欲使3 mol的VO2+变为VO+,则需
2
要氧化剂KClO 至少为_____mol。
3
(3)工艺中“中和”步骤生成“废渣2”的离子方程式为____________________________。
(4)“离子交换”和“洗脱”可简单表示为4ROH+VOR VO +4OH-(ROH为强碱性阴离子交换树
4 4 4 12
脂)。为了提高洗脱效率,淋洗液应该呈__________性(填“酸”“碱”或“中”)。
【答案】(每空2分)(1)V O+2H+===2VO+HO VO+4H+===2VO2++2HO SiO;
2 5 2 2 4 2 2
(2)6VO2++ClO+3HO===6VO+Cl-+6H+ 0.5
2
(3)Fe3++3OH-===Fe(OH) ↓、Al3++3OH-===Al(OH) ↓
3 3
(4)碱
【解析】从废钒催化剂中回收VO,由流程可知,“酸浸”时VO 转化为VO +,VO 转成VO2+.氧化铁、
2 5 2 5 2 2 4
氧化铝均转化为金属阳离子,只有SiO 不溶,则过滤得到的滤渣1为SiO,然后加氧化剂KClO,将
2 2 3
VO2+变为VO +,再加KOH时,铁离子、铝离子转化为Fe(OH)、Al(OH) 沉淀,同时中和硫酸,过
2 3 3
滤得到的滤渣2为Fe(OH)、Al(OH),“离子交换”和“洗脱”可简单表示为:4ROH+V O 4-
3 3 4 12
R VO +4OH-,由ROH为强碱性阴离子交换树脂可知,碱性条件下利用反应正向移动,流出
4 4 12
液中主要为硫酸钾,“沉钒”得到偏钒酸铵(NH VO )沉淀,“煅烧”时分解生成VO。
4 3 2 5
(1)“酸浸”时VO 转化为VO+,反应的离子方程式为VO+2H+=2VO++HO,VO 转成VO2+,反应的离子方
2 5 2 2 5 2 2 2 4
程式为VO+4H+===2VO2++2HO,由上述分析可知滤渣1为SiO,故答案为VO+2H+=2VO++HO;VO+4H+
2 4 2 2 2 5 2 2 2 4
===2VO2++2HO;SiO;
2 2
(2)“氧化”中欲使3 mol的VO2+变为VO+,离子方程式为6VO2++ClO+3HO===6VO+Cl-+6H+;“氧
2 2
化”中欲使3 mol的VO2+变为VO+,由电子守恒可知,则需要氧化剂KClO 至少为 =0.5mol。
2 3
(3)由上述流出分析可知滤渣2为Fe(OH)、Al(OH),发生的离子方程式分别为Fe3++3OH-
3 3===Fe(OH) ↓、Al3++3OH-===Al(OH) ↓;
3 3
(4)利用强碱性阴离子交换树脂可“离子交换”和“洗脱”,则应选择碱性条件下使用,且OH-浓度大反应逆
向移动提高洗脱效率,故答案为碱;